Linus Pauling
Linus Carl Pauling, nado en Portland (Oregón) o 28 de febreiro de 1901 e finado en Big Sur (California) o 19 de agosto de 1994 foi un químico e físico estadounidense. El mesmo chamábase cristalógrafo, biólogo molecular e investigador médico. Foi un dos primeiros químicos cuánticos, e recibiu o Premio Nobel de Química en 1954, polo seu traballo no que describía a natureza dos enlaces químicos. Así mesmo, e en plena guerra fría, recibiu o Premio Nobel da Paz en 1962, pola súa oposición ás probas nucleares terrestres.
Traxectoria[editar | editar a fonte]
Mocidade[editar | editar a fonte]

Linus Pauling naceu en Portland, (Oregón), o 28 de febreiro de 1901, fillo de Herman Henry William Pauling (1876-1910), estadounidense de ascendencia alemá, e de Lucy Isabelle Darling (1881-1926). O seu pai era farmacéutico que, sen ter éxito comercial, fixo á súa familia percorrer diferentes lugares do estado. Cando morreu, en 1910, Lucy Isabelle tivo que criar soa a Lunis e as súas dúas irmás, Pauline (1901-2003) e Frances Lucille (1904 - ?). A familia reinstalouse en Portland.
Na súa infancia, Linus foi un lector voraz, tanto que o seu pai chegou a escribir a un xornal local, pedindo suxestións de libros para mantelo ocupado. Un dos seus amigos, Lloyd Jeffress, tiña un pequeno laboratorio químico na súa habitación; e os experimentos creados neste laboratorio espertaron o interese de Pauling por ser un enxeñeiro químico.
No bacharelato, Pauling continuaba cos experimentos de química, pedindo prestada a maioría dos materiais e os equipos nunha acerera abandonada preto do lugar onde o seu avó traballaba como velador. As malas cualificacións que Pauling obtivo en historia dos Estados Unidos, impedíronlle graduarse do bacharelato. A escola deulle a súa diploma corenta e cinco anos máis tarde, despois de gañar os seus dous premios Nobel[1].
Estudos[editar | editar a fonte]

En 1917, Pauling ingresou na Universidade Agrícola de Oregón, en Corvallis ("OAC", chamada actualmente Universidade Estatal de Oregón). Paralelamente aos seus estudos, Linus Pauling tivo que traballar a tempo completo, debido ás súas necesidades financeiras. Entre os empregos que tivo, atópanse o de repartidor de leite, proxeccionista nun cine, e obreiro nun estaleiro. Ao comezo do seu segundo ano de estudos, Pauling propúxose buscar emprego en Portland para poder manter á súa nai, pero na Universidade propuxéronlle aceptar unha cátedra de química analítica cuantitativa (un curso que el mesmo acababa de tomar), que lle permitise ao mesmo tempo continuar os seus estudos.
No transcurso dos seus dous últimos anos na OAC, Pauling coñeceu os traballos de Lewis e Langmuir sobre a configuración electrónica dos átomos; así como da forma en que estes enlazábanse para formar moléculas. Neste momento, decidiu seguir unha carreira na investigación, concentrándose na comprensión da relación da estrutura atómica da materia, coas súas propiedades físicas e químicas; o cal levaríao a converterse nun dos pioneiros da química cuántica. Na OAC, tivo a oportunidade de realizar as súas primeiras investigacións con respecto ao efecto que un campo magnético ten sobre a orientación dun cristal de ferro.
Pauling graduouse como bachaler en Ciencias, en 1922, no área de enxeñaría de procesos. Inmediatamente, buscou continuar os seus estudos, cun posgraduado no Instituto Tecnolóxico de California (Caltech) en Pasadena. Buscando o doutoramento, Pauling traballou investigando a utilización da difracción dos raios X, na determinación da estrutura dos cristais. Durante os seus tres anos en Caltech, Puling publicou sete artigos sobre a estrutura cristalina dos minerales. O primeiro deles foi publicado na revista Journal of the American Chemical Society, e trataba a estrutura da molibdenita, MoS2. Linus Pauling recibiu o doutoramento en 1925, summa cum laude.
O 17 de xuño de 1923, Pauling casou con Ava Hellen Miller, con quen tivo tres fillos e unha filla. A parella coñeceuse na OAC, cando Pauling cursaba o último ano de estudos. Miller foi alumna de Pauling no curso "Química para estudantes de Economía Doméstica"[2], pola Universidade Estatal de Oregón.
Comezos da súa carreira científica[editar | editar a fonte]
Posteriormente a terminar os seus estudos de doutoramento, Pauling recibiu unha bolsa de estudos da Fundación Guggenheim, que lle permitiu viaxar a Europa para estudar baixo a dirección de Arnold Sommerfeld en Múnic, Niels Bohr en Copenhague e Erwin Schrödinger en Zürich. Durante a súa estancia na OAC, Pauling habíase familiarizado co traballo dos tres científicos, pioneiros da química cuántica. Ademais, en Europa, tivo a oportunidade de presenciar un dos primeiros estudos sobre enlácelos da molécula de hidróxeno, baseado en química cuántica. A investigación foi realizada por Walter Heitler e Fritz London. Pauling consagrou os seus anos en Europa a esta área, e decidiu facela a materia principal das súas investigacións futuras. Cando Pauling volveu aos Estados Unidos en 1927, obtivo unha posición de Profesor asistente de química teórica en Caltech.
Os primeiros cinco anos da carreira de Pauling transcorreron en Caltech e foron moi produtivos, aplicando a mecánica cuántica ao estudo de átomos e moléculas; en seguimiento aos seus estudos de cristais utilizando a difracción dos raios X. Nese período, Pauling publicou ao redor de cincuenta artigos, e creou as cinco Regras de Pauling, desenvolvidas para determinar a estrutura molecular dos cristais complexos. En 1929, foi nomeado Profesor asociado, e ao ano seguinte recibiu o título de Profesor.
En 1930, Pauling tivo unha estancia de verán en Europa, na cal traballou no instituto de Arnold Sommerfeld. Durante esta estancia, Pauling viu a posibilidade de utilizar aos electróns para os estudos de difracción, da mesma xeito en que usara os raios X anteriormente. Ao seu regreso, construíu un aparello de difracción electrónica, auxiliado polo seu estudante L. Ou. Brockway. O aparello foi utilizado para estudar a estrutura molecular dun gran número de substancias químicas. En 1931, Pauling recibiu o Premio Langmuir, outorgado pola American Chemical Society, polo traballo científico máis significativo, realizado por un investigador menor de 30 anos.
En 1932, Pauling concibiu a noción de electronegatividade. Utilizando diversas propiedades das moléculas, especialmente a súa momento dipolar e a enerxía necesaria para romper enlaces, estableceu a escala de Pauling, útil para a predición da natureza de enlaces químicos. A escala asigna un valor de electronegatividade á maioría dos elementos químicos. Este valor, é unha medida da forza con que os átomos dunha molécula atráense entre si. Ese mesmo ano, Pauling publicou o que é considerado o seu artigo máis importante, no cal desenvolve o novel concepto de hibridación dos orbitais atómicos, e realiza unha análise do carácter tetravalente do carbono.
En Caltech, Pauling desenvolveu unha forte amizade con Robert Oppenheimer, quen traballaba na Universidade de California, Berkeley, e ía regularmente a Caltech como investigador e mestre. Entre os dous, Oppenheimer e Pauling planearon traballar xuntos na investigación de enlaces químicos. Oppenheimer efectuaría os cálculos matemáticos, e Pauling interpretaría os resultados. Con todo, os plans non callaron por completo, pois Pauling comezou a sospeitar que o seu amigo estábase aproximando demasiado á súa esposa Ava Helen. Nunha ocasión que Pauling estaba ausente traballando, Oppenheimer invitou a Ava Helen a atoparse en México. Ela rexeitou a invitación de inmediato, e avisou ao seu marido. Este incidente, e a indolencia con que Ava Helen o tomou, provocaron que Pauling dese fin á relación co científico de Berkeley, creando unha fría tensión que durou polo resto das súas vidas. Aínda que máis tarde Oppenheimer propuxo a Pauling ser o xefe de química do Proxecto Manhattan, Pauling rexeitou a proposta, argumentando que el era pacifista.
A natureza do enlace químico[editar | editar a fonte]
Ao comezo da década de 1930, Pauling comezou a publicar as súas investigacións sobre a natureza do enlace químico, o cal levou ao seu famoso libro de texto The Nature of the Chemical Bond, publicado en 1939. Este libro é considerado un dos máis importantes traballos de química xamais publicados. Pódese ter unha idea da súa influencia con só recordar que nos primeiros trinta anos logo da súa primeira edición, o libro foi citado máis de 16.000 veces por outros autores. Isto convérteo na investigación máis citada como referencia no mundo científico. As investigacións nesta área valéronlle a Pauling o Premio Nobel de Química en 1954 "polas súas investigacións sobre a natureza do enlace químico e as súas aplicacións á determinación da estrutura das substancias complexas".
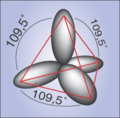
Como parte das súas investigacións sobre a natureza do enlace químico, Pauling creou o concepto de hibridación dos orbitais atómicos. Mentres que os electróns son descritos utilizando os orbitais, s, p etcétera, Pauling observou que para describir o enlace nas moléculas, é preferible construír funcións que son unha mestura destes orbitais. Por exemplo, os orbitais 2s e 2p dun átomo de carbono, pódense combinar para formar catro orbitais equivalentes, chamados orbitais híbridos sp3. Estes orbitais híbridos poden describir mellor a existencia de compostos como o metano, de geometría tetraédrica. Así mesmo, o orbital 2s pode combinarse con dous orbitais 2p, formando tres orbitais equivalentes, chamados orbitais híbridos sp2, mentres que o terceiro orbital 2p non se hibrida. Esta estrutura permite describir aos compostos insaturados, como o etileno.
Outro dos terreos nos que Pauling estaba interesado, era a comprensión da relación entre os enlaces iónicos, nos cales os electróns son transferidos dun átomo a outro; e os enlaces covalentes, nos cales ambos átomos aportan electróns. Pauling demostrou que estes dous tipos de enlaces, son en realidade casos extremos, e que a maioría de enlácelos son en realidade unha mestura de enlace iónico con covalente. É neste terreo que a noción de electronegatividade é máis útil, pois a diferenza entre as electronegatividades dos átomos participantes nun enlace resulta ser a medida máis adecuada para predicir o grao de ionicidade dun enlace.
O terceiro tema que Pauling traballou, aínda no terreo dos enlaces químicos, foi a comprensión e descrición da estrutura dos compostos aromáticos; especialmente o benceno (C6H6), o composto máis simple dos aromáticos.

A estrutura do benceno sempre fora motivo de controversia entre os científicos, pois non quedaba clara o xeito na que seis átomos de carbono e seis de hidróxeno podían enlazarse satisfacendo todo o seu potencial de enlace. Ata ese momento, a mellor descrición sobre devandita estrutura, era a formulada polo químico alemán Friedrich Kekulé. Nela, Kekulé describía a esta estrutura como a transición rápida entre dúas estruturas onde se alternaban de posición enlácelos simples e dobres. Pauling propuxo unha estrutura intermedia, baseada na mecánica cuántica, que considera unha superposición das dúas estruturas de Kekulé. Máis adiante, este fenómeno recibiu o nome de resonancia.
En certo xeito, a resonancia é análoga ao fenómeno de hibridación dos orbitais atómicos, xa que consiste na combinación de varias estruturas electrónicas: nela, os orbitais de diferentes átomos de carbono combínanse para formar os orbitais& moleculares.
Investigacións en bioloxía molecular[editar | editar a fonte]
A mediados da década de 1930, Pauling interesouse por unha nova discilpina científica. A comezos da súa carreira, el manifestara unha falta de interese polo estudo das moléculas biolóxicas. Con todo, en Caltech tivo oportunidade de tratar con biólogos de renome, como Thomas Hunt Morgan, Theodosius Dobzhansky, Calvin Bridges e Alfred Sturtevant. Pauling cambiou de opinión e comezou entón a estudar estas moléculas con interese, e grazas a unha bolsa de estudos da Fundación Rockefeller. Os seus primeiros traballos no tema, foron sobre a estrutura da hemoglobina. Chegou a poñer de manifesto que a estrutura da hemoglobina cambia dependendo de que a molécula capte ou perda un átomo de osíxeno. A raíz deste resultado, Linus Pauling decidiu estudar de forma máis precisa a estrutura das proteínas, utilizando a difracción de raios X. Con todo, a estrutura proteínica resultou ser moito máis difícil de determinar usando esta técnica, que a dos cristais minerais estudados anteriormente. Nesta década, o cristalógrafo británico William Astbury foi quen obtivo os mellores resultados usando raios X, pero cando Pauling intentou reinterpretar as súas observacións con axuda da mecánica cuántica en 1937, non o puido conseguir.
Foron necesarios once anos para que Pauling comprendese a orixe do problema. A súa análise matemática era correcto, pero os resultados de Astbury foron obtidos dun modo tal que as proteínas estaban inclinadas, respecto das posicións esperadas. Para explicar esta discrepancia, Pauling propuxo un modelo molecular da hemoglobina, no cal os átomos estaban posicionados en hélice, e aplicou esta idea ás proteínas en xeral.
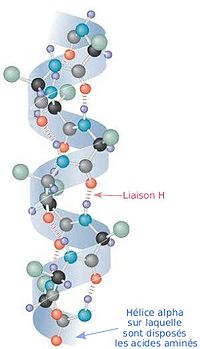
En 1951, baseados nas estruturas dos aminoácidos e dos péptidos e considerando a natureza planar do enlace peptídico; Pauling e os seus colegas propuxeron que a estrutura secundaria das proteínas estaba baseada na hélice alfa e a folla beta. Esta conclusión ejemplifica a capacidade de Pauling para pensar de xeito non convencional, pois o razoamento central da proposta radica en que unha volta da hélice pode conter un número non enteiro de aminoácidos.
A continuación, Pauling suxeriu unha estrutura helicoidal para o ácido desoxirribonucleico (ADN), aínda que o seu modelo tiña algúns erros, incluíndo o propoñer grupos neutros de fosfato, idea que estaba en conflito coa natureza aceda, e non neutra, do ADN Descrición.. Sir Lawrence Bragg decepcionárase cando soubo que Pauling gañara a carreira para descubrir a hélice alfa. O equipo de Bragg pois o seu equipo cometera un erro fundamental, ao non considerar a natureza planar do enlace peptídico. Cando nos Laboratorios Cavendish sóubose que Pauling traballaba cos modelos moleculares da estrutura do ADN, autorizouse a James Watson e Francis Crick para propoñer un modelo estrutural da molécula de ADN, utilizando material non publicado, dos investigadores Maurice Wilkins e Rosalind Elsie Franklin de King's College. En 1953, Watson e Crick propuxeron unha estrutura correcta para a dobre hélice do ADN, o que lles valería o Premio Nobel de Fisioloxía ou Medicina en 1962. Un dos obstáculos que Pauling enfrontou durante a súa investigación, foi a imposibilidad de consultar as fotografías, de alta calidade, de difracción do ADN que Franklin tomara. Cando Pauling íaas a ver durante un congreso en Inglaterra, o seu pasaporte foi retido polo Departamento de Estado dos Estados Unidos, que sospeitaba que Pauling tiña simpatías polo comunismo Este evento marcou o inicio de éraa coñecida como Maccarthismo nos Estados Unidos.. Watson e Crick tiveron acceso a estas fotografías grazas a que Wilkins mostroullas sen permiso da autora.
Neste período, Pauling tamén estudou as reaccións enzimáticas. Atópase entre os primeiros científicos que demostraron que os enzimas actúan estabilizando os estados de transición das reaccións químicas, o cal é fundamental para o entendemento dos seus mecanismos de acción. Pauling está tamén entre os primeiros que propuxeron que os anticorpos enlázanse aos antíxenos grazas a unha compatibilidade das súas estruturas. No mesmo orde de ideas, escribiu un artigo, xunto co físico convertido en biólogo Max Delbrück, onde suxire que a replicación do ADN é debida á compatibilidade, e non á similitude, como fora suxerido por outros científicos. O modelo de Watson e Crick viría corroborar esta idea. Por outra banda, Pauling contribuíu tamén, xunto con outros investigadores, á fabricación de anticorpos artificiais, e á dun substituto do plasma sanguíneo.
Activismo político[editar | editar a fonte]
Pauling non era un activista ata a segunda guerra mundial. Durante a guerra, contribuíu á posta a piques de explosivos e de combustible para mísiles. Do mesmo xeito, puxo a punto un detector de nivel de osíxeno para os submarinos. Ao comezo do proxecto Manhattan, que levaría á fabricación da primeira bomba atómica, Pauling recibiu unha oferta de Robert Oppenheimer, para encabezar ao departamento de química do proxecto. Pauling rexeitou a proposta. A raíz das súas contribucións durante a guerra, o Goberno dos Estados Unidos concedeulle a Medalla Presidencial ao Mérito, en 1948, a cal recibiu de mans do presidente Harry Truman. Con todo, marcado pola guerra en xeral, e os bombardeos de Hiroshima e Nagasaki, Pauling cambiou de posición e identificouse co activismo pacifista.
En 1946, uniuse ao Comité de Urxencia de Científicos Atómicos (ECAS, polas súas siglas en inglés) que Albert Einstein e Leó Szilárd fundaran dous anos antes. O comité tiña o fin de advertir á opinión pública dos perigos asociados ao desenvolvemento das armas nucleares. O activismo de Pauling provocou que o seu pasaporte fose confiscado en 1952, cando saía para un congreso en Londres. O pasaporte foi restaurado en 1954, pouco antes de partir a Estocolmo, a recibir o Premio Nobel. Ao ano seguinte, Linus Pauling asinou o Manifesto Russell-Einstein, unindo o seu nome ao de Bertrand Russell, Albert Einstein, e outros oito científicos e intelectuais, apelando á procura de solucións pacíficas durante a guerra fría.
Dous anos despois, Pauling redactou unha petición xunto co biólogo Barry Commoner, quen estudara a presenza de estroncio-90 radioactivo nos dentes de leite dos nenos estadounidenses; concluíndo que as probas nucleares na atmosfera teñen riscos para a saúde pública, en forma de precipitación radioactiva. Tamén participou nun debate público co físico atómico Edward Teller, sobre os riscos reais de mutaciones xenéticas provocadas por estas precipitacións.
En 1958, Pauling e a súa esposa presentaron ante a Organización de Nacións Unidas unha carta asinada por máis de 11.000 científicos, pedindo a suspensión das probas nucleares. A presión da opinión pública conduciu a unha moratoria nas probas na superficie, seguida pola firma do tratado de Prohibición Parcial de Probas Nucleares (PTBT, en inglés), asinado por 113 países, o 5 de agosto de 1963. Entre os firmantes, estaban John F. Kennedy polos Estados Unidos, e Nikita Khrushchev, pola Unión Soviética. O tratado entrou en vigor en outubro dese ano, e entón Pauling recibiu o Premio Nobel da Paz correspondente a 1962 (o premio fora reservado para que a data de entrega, coincidise coa de entrada en vigor do tratado). O premio foi outorgado a "Linus Pauling, quen desde 1946 ha avogado incesantemente, non soamente contra as probas nucleares, nin soamente contra a proliferación das armas nucleares, nin soamente contra o seu uso; senón en contra de calquera forma de resolver os conflitos internacionais pola via bélica." Cando se anunciou o premio, o Departamento de Química de Caltech non se molestou en felicitar a Pauling, xa que estaba incómodo coas actividades políticas do profesor. O Departamento de Bioloxía, ofreceu unha pequena festa, demostrando así a súa simpatía polo seu traballo nas mutaciones inducidas pola radiación. A desaprobación institucional sobre o activismo de Pauling, motivou que este renunciase ao seu posto en Caltech, en 1964. Entón, traballou na Universidade de California, San Diego, de 1967 a 1969; e na Universidade Stanford, de 1969 a 1973.
Moitos dos detractores de Pauling apreciaban o seu traballo científico, pero estaban en desacordo coa súa posición política; e representábaselle como un inxenuo portavoz do comunismo soviético. En 1955, Pauling foi citado a comparecer fronte ao subcomité de Seguridade Interior do Senado, que lle describiu como "a personalidade científica número un de todas as actividades importantes da ofensiva pacifista-comunista que hai neste país". Pauling regresou fronte a este subcomité varias veces máis, en especial cando enviou a súa petición contra as probas nucleares. A revista Life describiu ao Premio Nobel da Paz que Pauling recibiu como "un estraño insulto de Noruega". En 1970, Pauling recibiu o Premio Lenin da Paz, outorgado pola URSS.
Ata a fin da súa vida, Pauling valeuse da súa notoriedade como personalidade pública, para protestar contra os conflitos armados, incluíndo a guerra de Vietnam, e ata un "chamado pola paz en Croacia", en 1991. Do mesmo xeito, foi un feroz crítico do intervencionismo estadounidense en América Latina, especialmente en Nicaragua.
Recoñecemento[editar | editar a fonte]
Pauling é unha das poucas persoas que recibiron o Premio Nobel en máis dunha ocasión, xunto con Marie Curie (física e química), John Bardeen (física) e Frederick Sanger (química). Pauling é a única persoa que gañou dúas veces o premio Nobel, de xeito individual, pois tamén recibiu o Premio Nobel da Paz en 1962, pola súa campaña contra as probas nucleares terrestres Nobel Laureates Facts. Pauling fixo contribucións importantes á definición da estrutura dos cristais é das proteínas, e foi un dos fundadores da bioloxía molecular. É recoñecido como un científico moi versátil, debido ás súas contribucións en diversos campos, incluíndo a química inorgánica e orgánica, metalurxia, inmunoloxía, anestesioloxía, psicoloxía, decaimiento radioactivo e outros. Adicionalmente, Pauling abogou polo consumo de grandes doses de vitamina C, algo que agora considérase fóra da ortodoxia médica.
En 1931, Pauling publicou a súa obra, The Nature of the Chemical Bond ("A natureza do enlace químico"), na cal desenvolveu o concepto de hibridación dos orbitais atómicos. Tanto os seus traballos sobre os substitutos do plasma sanguíneo (con Harvey Itano), durante a segunda guerra mundial, como as súas investigacións na anemia falciforme (ou drepanocitosis, que cualificou co revolucionario termo de "enfermidade molecular"), influíron en gran medida á investigación en bioloxía da segunda metade do século XX. Notoriamente, Pauling descubriu a estrutura da hélice alfa (a forma de enrollamiento secundario das proteínas), o que o levou a achegarse ao descubrimento da dobre hélice do ácido desoxirribonucleico (ADN); pouco antes de que Watson e Crick fixesen o descubrimento en 1953. De feito, propuxo unha estrutura en forma de triplo hélice, a cal, estudando ao ADN por radiocristalografía podería levar á elaboración dun modelo en forma de dobre hélice.
Outros traballos[editar | editar a fonte]
Automóbil eléctrico[editar | editar a fonte]

A finais da década de 1950, Pauling comezou a interesarse no problema da contaminación do aire; particularmente polo fenómeno do smog que vira nos Ánxeles. Nesta época, a maioría dos científicos pensaban que o smog debíase ás emisións de refinarías e industrias químicas. Grazas aos traballos de Pauling, Arie Haagen-Smit e outros investigadores de Caltech, demostrouse que o principal responsable do smog son as emisións dos automóbiles. Pouco logo deste descubrimento, Pauling comezou a traballar no desenvolvemento dun automóbil eléctrico que fose funciional e barato. Para isto, uniu os seus esforzos cos enxeñeiros da empresa Eureka Williams, para o desenvolvemento do primeiro auto eléctrico de velocidade controlable, o Henney Kilowatt. Tras traballar no sistema de propulsión, Pauling demostrou que os acumuladores clásicos non poden entregar unha potencia suficiente para facer os motores eléctricos comparables aos motores de combustión interna. Tamén previu que o Henney Kilowatt sería pouco popular, pola baixa velocidade que alcanzaba, e a súa pouca autonomía. Acudiu con Eureka Williams para pedirlles que detivesen o proxecto ata que se desenvolvese unha batería máis potente, antes de comercializar o auto. A empresa preferiu facer o lanzamento, o que conduciu a un fracaso comercial.
Notas[editar | editar a fonte]
- ↑ Biografía de Linus Pauling Arquivado 21 de xuño de 2006 en Wayback Machine., en Nobelprize.org (en inglés)
- ↑ Cronoloxía da vida de Pauling
Véxase tamén[editar | editar a fonte]
| Commons ten máis contidos multimedia sobre: Linus Pauling |
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Linus Paper
- Biografía de la Academia Nacional de Ciencias
- Entrevista oral de Caltech
- Escaneos de 46 dos cadernos de Pauling, de 1922 a 1994
- El Lado Oscuro del Legado de Pauling
- The Pauling Catalogue
- Páxina web do Instituto Nobel, Premio Nobel de Química 1954 (en inglés)
- Biografía na páxina do Instituto Nobel (en inglés)
| Predecesor: Hermann Staudinger |
Premio Nobel de Química 1954 |
Sucesor: Vincent du Vigneaud |
- Premio Nobel de Química
- Premio Nobel da Paz
- Químicos dos Estados Unidos de América
- Presidentes da American Chemical Society
- Esperantistas
- Medalla Davy
- Nados en 1901
- Finados en 1994
- Nados en Portland, Oregón
- Doutores honoris causa pola Universidade Autónoma de Madrid
- Alumnos da Universidade Estatal de Oregón
- Alumnos do Instituto Tecnolóxico de California
- Premios Nobel dos Estados Unidos de América
- Premio Lenin da Paz



