Penicilina
| Penicilina | |
|---|---|
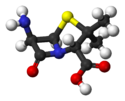
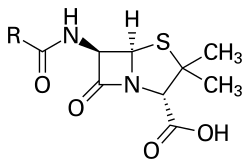 Estrutura central da penicilina, onde "R" é o grupo variable | |
 Estrutura da penicilina G en 3D. | |
| Datos clínicos | |
| AHFS/Drugs.com | Información detallada ó consumidor de Micromedex |
| Categoría no embarazo | |
| Rutas de administración | Intravenosa, intramuscular, subministración oral |
| Código ATC | |
| Datos farmacocinéticos | |
| Biodispoñibilidade | 60-75 % (humanos); 30 % (animais) |
| Unión a proteína plasmática | 50-80 %, principalmente albumina |
| Metabolismo | fígado |
| Semivida | entre 0.5 e 56 horas |
| Excreción | Renal |
| Identificadores | |
| Número CAS | |
| ChemSpider |
|
| Datos químicos e físicos | |
| Fórmula | C9H11N2O4S |
| |
Se cre que pode requirir tratamento, por favor, consúltello ao médico. | |
As penicilinas son antibióticos do grupo dos betalactámicos empregados profusamente no tratamento de infeccións provocadas por bacterias sensibles. A maioría das penicilinas son derivados do ácido 6-aminopenicilánico, diferindo entre si segundo a substitución na cadea lateral do seu grupo amino.[2] A bencilpenicilina ou penicilina G foi o primeiro antibiótico empregado amplamente en medicina; o seu descubrimento foi atribuído a Alexander Fleming en 1928,[3] quen xunto cos científicos Ernst Boris Chain e Howard Walter Florey -que crearon un método para producir en masa o fármaco- obtivo o Premio Nobel de Medicina en 1945.
Non se coñece por completo o mecanismo de acción das penicilinas, aínda que a súa analoxía á D-alanil-D-alanina terminal, situada na cadea lateral peptídica da subunidade do peptidoglicano (constituínte principal da parede bacteriana), suxire que o seu carácter bactericida deriva da súa intervención como inhibidor do proceso de transpeptidación durante a síntese daquel. Deste xeito, a penicilina actúa debilitando a parede bacteriana e favorecendo a lise osmótica da bacteria durante o proceso de multiplicación.[4]
Existe unha gran diversidade de penicilinas. Algunhas especies de fungos do xénero Penicillium sintetizan de forma natural penicilinas, como o primeiro tipo illado, a penicilina G. Porén, debido á aparición de resistencias, desenvolvéronse outras familias seguindo basicamente dúas estratexias: a adición de precursores para a cadea lateral no medio de cultivo do fungo produtor, o que se traduce na produción de penicilinas biosintéticas; e a modificación química da penicilina obtida pola fermentación biotecnolóxica, o que dá lugar ás penicilinas semisintéticas.[5]
As penicilinas difiren entre si segundo o seu espectro de acción. Por exemplo, a bencilpenicilina é eficaz contra bacterias grampositivas como estreptococos e estafilococos, así como gonococos e meningococos, pero debe administrarse por vía parenteral (por inxección) debido á súa sensibilidade ao pH ácido do estómago. A fenoximetil penicilina é, en cambio, resistente a este pH e pode administrarse por vía oral. A ampicilina, ademais de manter esta resistencia, é eficaz contra bacterias gramnegativas como Haemophilus, Salmonella e Shigella.[4]
Aínda que as penicilinas son os antibióticos menos tóxicos, é común que produzan alerxias. Ata o 10% dos pacientes que reciben tratamentos de betalactámicos desenvólvenas.[6] Posto que un choque anafiláctico pode conducir á morte do paciente, é necesario interrogalo antes de iniciar o tratamento.
Ademais das súas propiedades antibacterianas, a penicilina é un efectivo antídoto contra os efectos do envelenamento por α-amanitina, un dos aminoácidos tóxicos dos fungos do xénero Amanita.[7]
Historia das penicilinas[editar | editar a fonte]
- Artigo principal: Historia da penicilina.
Aínda que xeralmente se lle atribúe o científico británico Alexander Fleming o descubrimento da penicilina, moitas épocas e culturas diferentes chegaron mediante a observación e a experiencia a coñecer e empregar as propiedades bactericidas dos mofos. Descubríronse precedentes na Grecia e India antigas, e nos exércitos de Ceilán do século II, estivo tamén presente nas culturas tradicionais de rexións tan distintas e distantes como Serbia, Rusia ou China, así como nos nativos de Norteamérica.[8][9] Adoitábase aplicar alimentos embalorecidos ou terra do chan que contivese fungos ás feridas de guerra. Desde o século VIII polo menos, os médicos árabes curaban infeccións untando as feridas cunha pasta branca que se formaba nos arneses de coiro que se utilizaban nos burros de carga. Ao longo do século XVII algúns farmacólogos e herboristas ingleses, como John Parkington, incluíron o tratamento con fungos nos rexistros de farmacia.[N 1]

A finais do século XIX, Henle (un dos grandes científicos da chamada "xeración intermedia") suscita no seu discípulo Robert Koch, na Universidade de Gotinga, o interese polos traballos de Agostino Bassi e Casimir Davaine, que o levaría a investigar os microorganismos como axentes causais das enfermidades. Isto conduciríao en 1876 a descubrir que Bacillus anthracis era o axente causal específico do carbuncho, na liña da teoría microbiana da enfermidade, e a enunciar os seus sonados postulados.[12] Máis tarde, Paul Ehrlich, que traballou con Koch en Berlín, desenvolveu o concepto de "Magischen Kuger" ou balas máxicas, denominando así aqueles compoñentes químicos que puidesen eliminar selectivamente os xermes. Finalmente, en 1909 conseguiu sintetizar un composto, o Nº 606, máis tarde coñecido como salvarsán, que se mostrou eficaz contra a sífilis.[13] Este descubrimento influíu posteriormente en Alexander Fleming, ata o punto de que existen caricaturas do novo Fleming caracterizado e alcumado como "recruta 606".[14]
Ao mesmo tempo ou pouco despois, coñecido o feito de que as bacterias podían provocar enfermidades, sucedéronse multitude de observacións, tanto in vivo coma in vitro, de que os mofos exercían unha acción bactericida. Por só citar algúns nomes, sirvan de exemplo os traballos de John Scott Burdon-Sanderson, Joseph Lister, William Roberts, John Tyndall, Louis Pasteur e Jules Francois Joubert, Carl Garré, Vincenzo Tiberio, Ernest Duchesne, Andre Gratia e Sara Dath.[15][16][17][18][19][20][21]
En marzo de 2000, médicos do hospital San Xoán de Deus de San Xosé (Costa Rica) publicaron os escritos do científico e médico costarriqueño Clodomiro Clorito Picado Twight (1887-1944). Na reportaxe explican as experiencias que adquiriu Picado entre 1915 e 1927 sobre a acción inhibitoria dos fungos do xénero Penicillium sobre o crecemento de estafilococos e estreptococos.[22] Aparentemente, Clorito Picado informou do seu descubrimento á Academia das Ciencias de París, pero non o patentou, a pesar de que a súa investigación fora iniciada uns poucos anos antes que a de Fleming.[23][24]
Alexander Fleming[editar | editar a fonte]
- Artigo principal: Alexander Fleming.

O descubrimento da penicilina foi presentado como un exemplo "icónico" de como procede o método científico a través da observación, e da habilidade singular de Alexander Fleming de interpretar un fenómeno casual.[25] O propio Fleming abona esta versión na súa conferencia de recepción do premio Nobel.[26] Con todo, algúns autores revisan esta historia oficial, e opinan que, sen restar méritos, está distorsionada por mitos, a necesidade de propaganda na segunda guerra mundial e tamén unha certa loita polo prestixio de institucións con influencias sobre áreas do poder e nos medios de comunicación.[27][28][29]
George Wong, ao considerar a versión dun descubrimento casual, fai notar os seguintes antecedentes:[30]
- Coñecía a case todos os autores mencionados no apartado anterior. O seu gran número é xa por si só indicador de que existía toda unha corrente que investigaba no campo con mutuo coñecemento de traballos. O propio Fleming admíteo na súa conferencia do Nobel.[26]
- Buscaba activamente unha substancia bactericida: Impresionado polos campos de guerra europeos na primeira guerra mundial e as baixas por infección nas feridas, ensaiou con salvarsán, descubriu a lisozima constatando que non afectaba a ningún dos organismos problemáticos da penicilina, e iso aínda en contra da liña marcada polo seu xefe, Almroth Wright, máis interesado na inmunización.[31]
O descubrimento da penicilina segundo Fleming ocorreu a mañá do venres 28 de setembro de 1928, cando estaba estudando cultivos bacterianos de Staphylococcus aureus no soto do laboratorio do Hospital St. Mary en Londres, situado na Á Clarence, agora parte do Imperial College.[32] Tras regresar dun mes de vacacións, observou que moitos cultivos estaban contaminados, e tirounos a unha bandexa de lysol. Afortunadamente recibiu unha visita dun antigo compañeiro, e ao ensinarlle o que estaba facendo con algunha das placas que aínda non foran lavadas, deuse conta de que nunha delas, ao redor do fungo contaminante, creouse un halo de transparencia, o que indicaba destrución celular. A observación inmediata é que se trataba dunha substancia difusible procedente do contaminante. Posteriormente illou e cultivou o fungo nunha placa na que dispuña radialmente varios microorganismos comprobando cales eran sensibles. A identificación do espécime como Penicillium notatum realizouna Charles Thom. Publicou o seu descubrimento sen que recibise demasiada atención e, segundo os compañeiros de Fleming, tampouco el mesmo se deu de conta inicialmente do potencial da substancia, senón progresivamente, en especial pola súa baixa estabilidade. No seu traballo obtén un filtrado libre de células que inxectou a coellos comprobando así que carecía de toxicidade. Tamén apreciou a súa utilidade para illar a bacteria Haemophilus influenzae a partir de esputos.[30][33]
Primeiras aplicacións en medicina e illamento[editar | editar a fonte]


Fleming, debido ao seu carácter tímido, non conseguía transmitir entusiasmo sobre o seu descubrimento, aínda que continuou durante moito tempo traballando nel, ata 1934 en que o abandonou para dedicarse ás sulfamidas.[30] A primeira demostración de que a penicilina era útil para a medicina levouna a cabo en 1930 o patólogo inglés Cecil George Paine, antigo alumno de Fleming, que intentou tratar a sicose, pero sen éxito, probablemente porque o medicamento non era administrado con suficiente profundidade. Con todo, logrou ter éxito aplicando o filtrado en neonatos para o tratamento da oftalmía neonatal, logrando a súa primeira cura o 25 de novembro de 1930, nun adulto e tres bebés.[34] Aínda que estes resultados non foron publicados, influíron en Howard Walter Florey, que foi compañeiro de Paine na Universidade de Sheffield.
Entre 1928 e 1938 Florey interesouse en primeiro lugar pola lisozima, e posteriormente polo segundo descubrimento de Fleming. A diferenza deste último, que case non contaba con persoal, formou un grande equipo con personalidades do talle de Chain, Leslie Falk, Norman Heatley e ata outros 22 colaboradores entre investigadores e técnicos con gran cantidade de medios na escola de patoloxía Sir William Dunn de Oxford, aínda que curiosamente, segundo Florey, non polo seu potencial farmacéutico, senón por un puro interese científico. A súa capacidade de procesado superaba os 500 litros de cultivo semanais.[30]

A purificación da penicilina produciuse en 1939, a cargo do bioquímico Heatley, utilizando grandes volumes de filtrado mediante un sistema a contracorrente e extracción por amil acetato. Edward Abraham terminou de eliminar o resto de impurezas por cromatografía en columna de alumina. Posteriormente probouse a substancia en ratos infectados con Streptococcus. O primeiro ser humano tratado con penicilina purificada foi o axente de policía Albert Alexander no Hospital John Radcliffe, o 12 de febreiro de 1941. O paciente faleceu porque non se lle puido administrar suficiente fármaco.[35]
As primeiras compañías en interesarse pola patente foron Glaxo e Kemball Bishop.
Desenvolvemento da produción industrial e outras penicilinas[editar | editar a fonte]
A partir das investigacións de Florey en 1939 e de Heatley en 1941, a produción industrial da penicilina en Europa viuse en apertos económicos debido ao comezo da Segunda guerra mundial. Os científicos británicos buscaron axuda nos Estados Unidos, especificamente nos laboratorios de Peoria (Illinois), onde os seus científicos estaban traballando en métodos de fermentación para acelerar o crecemento de cultivos de fungos. [36] Florey e Heatley partiron da Universidade de Oxford cunha pequena cantidade de penicilina cara aos Estados Unidos. Bombearon aire dentro de enormes cubas cheas de millo fermentado con outros ingredientes e aditivos chaves o que demostrou poder producir rapidamente grandes cantidades de penicilina en comparación cos antigos métodos de crecemento sobre superficies planas.[37] A cepa de Penicillium que tivo o mellor rendemento non foi a importada polos científicos británicos senón unha cepa que crecía sobre un melón nun dos mercados de Peoria, mellorando a cantidade de produción nas condicións inmersas da nova técnica do laboratorio estadounidense, aproximadamente 70-80 unidades de penicilina por mililitro de cultivo.[38]
O 26 de novembro de 1941, Heatley e Andrew J. Moyer, o experto do laboratorio en Peoria, lograron multiplicar por 10 a produción de penicilina. Co aumento da cantidade de penicilina tamén baixou o custo dunha dose. Desde o prezo incalculable en 1940, o prezo da penicilina baixou a 20 dólares norteamericanos por dose en xullo de 1943 e máis aínda a 0,55 dólares por dose en 1946. Como consecuencia, os laboratorios de Gran Bretaña en 1999 e de Peoria en 2001 foron designados como Monumento Químico Histórico Internacional (International Historic Chemical Landmark).[39][40]
Penicilinas sintéticas[editar | editar a fonte]

Unha das varias presentacións da penicilina producida de modo natural é a bencilpenicilina ou penicilina G, a única que se usa clinicamente. A ela asociáronse a procaína e a benzatina para prolongar a súa presenza no organismo, obténdose as respectivas suspensións de penicilina G + procaína e penicilina G benzatina, que só se poden administrar por vía intramuscular.[41][42]
Máis tarde, modificouse a molécula de penicilina G para elaborar penicilinas sintéticas, como a penicilina V, que se poden administrar por vía oral ao resistir a hidrólise ácida do estómago.[43] Con todo, o relativamente estreito espectro de acción da actividade da penicilina V fixo que se sintetizasen derivados con acción sobre unha máis ampla gama de axentes infecciosos. O primeiro paso foi o desenvolvemento da ampicilina, efectiva fronte a patóxenos grampositivos e gramnegativos, que ademais resultou considerablemente económica de adquirir.[44]Outro avance foi o desenvolvemento da flucloxacilina, usada contra bacterias produtoras de β-lactamase como os Staphylococcus.[45] Hoxe en día existen múltiples derivados sintéticos da penicilina, como a cloxacilina e a amoxicilina, que se administran por vía oral e das que existe un abuso de consumo pola sociedade en xeral para autotratamento de infeccións leves víricas que non precisan terapia antibiótica.[46][47][48] Esta situación provocou unha alta porcentaxe de resistencia bacteriana fronte ás penicilinas e levou á ineficacia dos betalactámicos nalgunhas infeccións graves.[49]
As penicilinas foron amplamente utilizadas no campo da veterinaria desde 1950, en que comezaron a engadirse como aditivos no penso, debido á súa efectividade reducindo a mortalidade e a morbilidade fronte a infeccións clínicas, así como o incremento da taxa de engorde.[50] De feito, a amoxicilina foi descrita en 1976 como unha penicilina para uso veterinario.[51] Suxeriuse a relación entre este uso e a selección de cepas resistentes con capacidade de infectar a humanos. Con todo, aínda que algúns antibióticos se aplican en ambos os campos, a maioría das resistencias en humanos desenvolvéronse por un mal uso en medicina.[52]
Estrutura química[editar | editar a fonte]
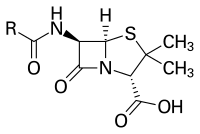
As penicilinas pertencen a unha familia de compostos químicos cunha estrutura química peculiar que lle confire unha actividade característica contra un grupo determinado de bacterias.[27] A pesar de que existen diferentes variantes, a estrutura química esencial da penicilina foi descuberta por Dorothy Crowfoot Hodgkin entre 1942 e 1945.[53] A maioría das penicilinas posúen como núcleo químico o anel 6-aminopenicilánico e difiren entre si segundo a cadea lateral ancorada ao seu grupo amino. Este núcleo 6-aminopenicilánico ou núcleo penam consta, á súa vez, dun anel tiazolidínico (un anel iminofenílico dos tiazoles) enlazado a un anel β-lactámico;[54] este último, aparentemente esencial para a actividade antimicrobiana do composto,[55] é hidrolizado mediante penicilinases (enzimas tipo β-lactamases) polas bacterias resistentes a penicilinas.[4]
Propiedades[editar | editar a fonte]
A penicilina natural ou penicilina G é cristalina, totalmente soluble en auga, solucións salinas e dextrosas isotónicas. O radical R, é o responsable da sensibilidade á hidrólise por parte das β-lactamases, do enlace a proteínas transportadoras e do vínculo coas proteínas bacterianas PBP que transportan a penicilina dentro da célula.[56] Ademais, asóciaselle á penicilina un dipéptido cisteína-valina, facendo que a penicilina teña a afinidade ideal polo encima bacteriano transpeptidase, o cal non se atopa no corpo humano e intervén na síntese do peptidoglicano.[57]
Existe unha analoxía estrutural entre a penicilina e o dipéptido D-alanil-D-alanina terminal asociado ás unidades de peptidoglicano que aparecen durante a formación da parede celular de certas bacterias (proceso de transpeptidación). O nucleófilo O(-) serina da transpeptidase ataca os grupos carbonilos dos ß-lactámicos, como a penicilina, por esa analoxía ao seu substrato D-Ala-D-Ala, o dipéptido antes mencionado. Dese xeito, uníndose covalentemente aos residuos de serina do sitio activo do encima en forma de complexo peniciloil, a penicilina inhibe a transpeptidase bacteriana.[56]
Alérxenos[editar | editar a fonte]
Os metabolitos que derivan da molécula intacta de penicilina actúan como haptenos e vólvense inmunitariamente activos a través da súa unión de tipo covalente, coas proteínas endóxenas no corpo, preferentemente por ataques aos grupos amino da lisina destas proteínas transportadoras, podendo inducir así unha reacción de hipersensibilidade.[55][58] O intermediario antixénico das penicilinas é o ácido peniciloíl que se forma ao abrirse o anel β-lactámico. O 95 % do medicamento unido aos tecidos aparece nesta forma. O devandito ácido, conxugado cun transportador proteico inmunoxénico é un dos axentes máis usados nas probas cutáneas para determinar se un paciente é alérxico á penicilina. Outros determinantes menos frecuentes, que inclúen o benzilpeniciloato e a amina-benzilpeniciloil son produtos que se forman in vivo e poden tamén atoparse nas solucións de penicilina preparadas para a súa administración comercial, que poden inducir unha reacción de hipersensibilidade.[55]
Clasificación[editar | editar a fonte]
| Naturais | Resistentes o ácido |
Antiestafilocócicas | Gramnegativas | ||
|---|---|---|---|---|---|
| Penicilina G (bencil) |
Penicilina V | Meticilina |
Isoxazolilopenicilinas: |
Temocilina | |
| Penicilina G Procaína |
Feneticilina | Nafcilina | |||
| Penicilina G benzatina |
Propicilina | ||||
| Aminopenicilinas | Antipseudomonas | Amidinopenicilinas | |||
| Amoxicilina | Ticarcilina | Mecilinam | |||
| Hetacilina | Apalcilina | Pivmecilinam | |||
| Espicilina | Ciclacilina | Azlocilina | Mezlocilina | ||
|
|

|

|
| |
|
Núcleo común |
Unha aminopenicilina | ||||
As penicilinas clasifícanse en dous grupos, naturais e semisintéticas, e en cada un deles hai compostos relativamente resistentes ao zume gástrico e polo tanto pódense administrar por vía oral, por exemplo, a penicilina V, a dicloxacilina e a amoxicilina.[43][47][60][61]
O termo penicilina úsase a miúdo, en sentido xenérico, para referirse a calquera das variantes que derivan da penicilina mesma.[62] As bencilpenicilinas teñen a maior actividade contra organismos grampositivos, cocos gramnegativos e organismos anaerobios que non producen β-lactamase.[63] Con todo, presentan unha baixa actividade contra bacilos gramnegativos.[63] A penicilamina, un metabolito da penicilina e análogo do aminoácido cisteína, é efectivo para o alivio da artrite reumatoide reducindo a velocidade de aparición de novos danos a articulacións, aínda que non se adoita receitar debido á súa elevada toxicidade.[64] Tamén existen no mercado penicilinas sintéticas, como a ticarcilina, a mezlocilina e a piperacilina.[65][66][67]
Penicilinas naturais e biosintéticas[editar | editar a fonte]
As penicilinas naturais son aquelas xeradas sen intervención biotecnolóxica. Entre elas destacan a bencilpenicilina, como produto final de interese terapéutico, e os intermediarios illables como a isopenicilina N ou a penicilina N.[68] As biosintéticas, en cambio, prodúcense mediante adición de determinados compostos no medio de cultivo do biorreactor empregado durante a súa produción, é dicir, sen que teña lugar un illamento e unha modificación química ex vivo.[69][70] Entre as biosintéticas destacan: a fenoximetilpenicilina, a alilmercaptometilpenicilina e, de novo, a bencilpenicilina (pois é posible inducir a súa síntese aplicando certos precursores no fermentador).[4][71][72]
Bencilpenicilina ou penicilina G[editar | editar a fonte]
- Artigo principal: Bencilpenicilina.

A bencilpenicilina, comunmente coñecida como penicilina G, é o estándar das penicilinas.[73] Polo xeral adminístrase por vía parenteral (intravenosa, intratecal ou intramuscular), porque tende a perder estabilidade co zume gástrico do estómago.[74] Debido a que se administra inxectada, libérase lentamente no corpo e así mantén o seu efecto durante moito tempo.[75]
As vantaxes da penicilina G son o seu baixo custo, a súa fácil administración, a súa excelente penetración nos tecidos e o seu índice terapéutico favorable. En contraste, as desvantaxes son a súa degradación polo ácido gástrico, a súa destrución polas β-lactamases bacterianas e a súa asociación co desenvolvemento de reacción adversa en cerca do 10% dos pacientes.[73][74]
As indicacións específicas da penicilina G inclúen: celulite, endocardite bacteriana, gonorrea, meninxite, pneumonía por aspiración, absceso pulmonar, pneumonía adquirida na comunidade, sífilis e sepse en nenos.[76]
Bencilpenicilina procaína[editar | editar a fonte]
A bencilpenicilina procaína (DCI), coñecida tamén como penicilina G procaína, é unha combinación da penicilina G cun anestésico local, a procaína.[77] Esta combinación ten como fin reducir a dor e a incomodidade asociada coa voluminosa inxección intramuscular de penicilina. Tras a administración dunha inxección intramuscular, o fármaco absórbese lentamente na circulación e hidrolízase a bencilpenicilina. Por iso, é administrada cando se desexa que as súas concentracións sexan baixas pero prolongadas. Este antibiótico é moi utilizado en veterinaria.[78]
A penicilina procaínica indícase para todas as infeccións locais graves por estreptococos, bacterias anaerobias, pneumococos e gonococos, sífilis, ántrax (como coadxuvante), otite media aguda purulenta, mastoidite aguda, amigdalite aguda por estreptococo hemolítico do grupo A, pneumonía pneumocócica, absceso peritonsilar e submandibular e gonorrea.[76] As indicacións específicas da bencilpenicilina procaína inclúen: sífilis,[N 2] infeccións do aparello respiratorio onde o paciente non cumpre o seu tratamento oral, celulite e erisipela.[76]
No pasado usábase para o tratamento da gonorrea xenitourinaria. Con todo, a bacteria Neisseria gonorrhoeae frecuentemente produce β-lactamases e chegou a desenvolver resistencia á penicilina, polo que se substituíu por ceftriaxone.[81][82] Tamén se usaba para o tratamento da pneumonía pneumocócica non complicada, pero a aparición do S. neumoniae penicilino-resistente nalgúns países limitou o seu uso.[83]
Bencilpenicilina benzatínica[editar | editar a fonte]
A bencilpenicilina benzatínica ou penicilina G benzatínica (DCI), é unha combinación con benzatina que se absorbe lentamente na circulación sanguínea logo dunha inxección intramuscular e logo hidrolízase a bencilpenicilina. É a primeira opción cando se require unha concentración baixa de bencilpenicilina, permitindo unha acción prolongada do antibiótico durante máis de 2-4 semanas por cada inxección.[84] A penicilina G benzatínica é administrada en casos de difteria, de infeccións do aparello respiratorio ou do aparello xenital e en certas infeccións producidas por gramnegativos, como a meninxite e a endocardite.[64] Pode causar urticaria, prurito e, moi de cando en cando, choque anafiláctico.[84]
As indicacións específicas da bencilpenicilina benzatínica inclúen: profilaxe da febre reumática e sífilis en fase temperá ou latente.[76]
Fenoximetilpenicilina ou penicilina V[editar | editar a fonte]
- Artigo principal: Fenoximetilpenicilina.
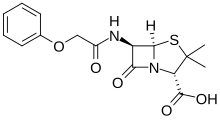
A fenoximetilpenicilina, comunmente chamada penicilina V, é a única penicilina activa por vía oral. Ten unha actividade menor que a bencilpenicilina, polo que se administra cando non se require alcanzar concentracións elevadas nos tecidos.[85]
Coa penicilina oral V, o espectro é practicamente igual ao da penicilina G: estreptococos, pneumococos e Neisseria, algúns anaerobios e estafilococos non produtores de penicilinase.[85] Non é inactivada polo zume gástrico, alcanzándose en pouco tempo concentracións adecuadas de penicilina en tecidos e plasma sanguíneo.[85] A absorción non está influída polas comidas, pero alcánzanse maiores concentracións plasmáticas cando se toma co estómago baleiro.[85] As indicacións específicas para a penicilina V inclúen: infeccións causadas por Streptococcus pyogenes (como a amigdalite, a farinxite e infeccións da pel), profilaxe da febre reumática e xenxivite moderada ou severa (xunto con metronidazol).[76]
A penicilina V é a primeira opción no tratamento de infeccións odontolóxicas. Ocasionalmente pode causar diarreas que non adoitan requirir suspensión da terapia. De cando en cando produce reaccións alérxicas severas e adoitan ser máis leves que con penicilina parenteral.[85]
Penicilinas semisintéticas[editar | editar a fonte]
As penicilinas semisintéticas son aquelas xeradas mediante o illamento dun intermediario estable durante unha produción microbiolóxica industrial (fermentación en biorreactores) continuada pola modificación química ou encimática do composto illado.[4] Divídense segundo a súa acción antibacteriana en cinco grupos: resistentes a β-lactamases, aminopenicilinas, antipseudomonas, amidinopenicilinas e resistentes a β-lactamases (gramnegativas).[86]
Resistentes a β-lactamases[editar | editar a fonte]

O seu uso é principalmente en infeccións por estafilococos produtores de β-lactamases, como o Staphylococcus aureus. Tamén presentan actividade, aínda que reducida, fronte a estreptococos, pero carecen dela fronte a enterococos.[87]
- A meticilina é unha penicilina de espectro reducido desenvolvida pola farmacéutica Beecham en 1959. Cando se desenvolveu, era especialmente activa contra grampositivos produtores de β-lactamases como Staphylococcus aureus, aínda que o desenvolvemento de resistencia por parte destes últimos (Staphylococcus aureus resistente á meticilina, SARM) impide actualmente o seu uso clínico.[88]
- Posteriormente apareceron a oxacilina e a nafcilina para uso parenteral, e dous fármacos para uso oral, a cloxacilina e a dicloxacilina.[89][90][91][92]
Aminopenicilinas[editar | editar a fonte]
O seu espectro de acción é moi grande, pero son sensibles ás β-lactamases. Adminístranse en casos de infeccións respiratorias das vías altas por estreptococos (sobre todo, S. pyogenes e S. pneumoniae) e por cepas de Haemophilus influenzae, infeccións urinarias por certas enterobacterias (como Escherichia coli e diversas infeccións xeradas por Enterococcus faecalis, Salmonella spp., Shigella spp. e Listeria monocytogenes.[93]
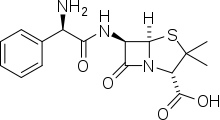
- A ampicilina é o epímero D(-) da aminopenicilina, un β-lactámico cun grupo fenil. Desenvolveuse nos laboratorios Beecham (actual GlaxoSmithKline) como resposta á necesidade de atopar derivados da penicilina de maior espectro, dada a aparición de cepas resistentes.[94] No ano 1959 descubriuse que o epímero D(-) da aminopenicilina cun grupo fenil era o máis activo dos derivados sintetizados.[95] Administrada oralmente, a ampicilina é absorbida, únese parcialmente a proteínas plasmáticas (15 a 25%) e é biodispoñible nun 40%.[96] Excrétase principalmente polo ril.[97]
- A pivampicilina é un éster metilado da ampicilina, administrada en forma de profármaco,[98] o cal potencia a biodispoñibilidade do medicamento, dada a súa maior liposolubilidade.[99] En medicina é indicado para o tratamento de pacientes, especialmente anciáns, con infeccións agudas das vías aéreas inferiores, como a pneumonía e a bronquite.[100]
- A amoxicilina é unha aminopenicilina de amplo espectro.[101] Como estratexia para potenciar a resistencia ás β-lactamases, preséntase acompañada de ácido clavulánico.[102] É indicada para o tratamento dun gran número de infeccións, incluíndo as do tracto respiratorio, dixestivo, genitourinario, sistema nervioso, así como en estomatoloxía e durante a erradicación de Helicobacter pylori en casos de úlcera péptica.[103]
Antipseudomónicas[editar | editar a fonte]
Estas penicilinas son de amplo espectro porque a súa cobertura de acción comprende grampositivos, gramnegativos e anaerobios. Dentro deste grupo existen dous subgrupos, as carboxipenicilinas e as ureidopenicilinas, atendendo á súa eficacia fronte a pseudomonas.[104]
Carboxipenicilinas[editar | editar a fonte]
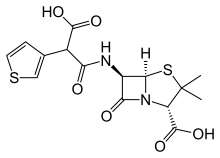
As carboxipenicilinas foron desenvolvidas para ampliar o espectro de bacterias gramnegativas cubertas por penicilinas, tales como infeccións nosocomiales causadas por Pseudomonas aeruginosa. Inicialmente produciuse a carbenicilina por substitución do grupo amino por un grupo carboxilo na ampicilina e posteriormente algunhas substitucións na carbenicilina permitiron desenvolver a ticarcilina.[105]
Presentan o mesmo espectro de acción que as aminopenicilinas, pero ampliado con Pseudomonas e B. fragilis.[87]
- A ticarcilina é unha carboxipenicilina empregada no tratamento de infeccións causadas por gramnegativos, especialmente de Pseudomonas aeruginosa, incluíndo casos de pneumonía, infeccións dos ósos, estómago, pel, articulacións, sangue, xinecolóxicas e das vías urinarias. A combinación dun aminoglicósido con carbenicilina ou ticarcilina foi utilizada no tratamento de infeccións severas por Pseudomonas. Como estratexia para potenciar a resistencia ás β-lactamases, preséntase acompañada de ácido clavulánico.[106]
- Hoxe en día, a carbenicilina non se fabrica en países como Estados Unidos e substituíuse o seu uso pola ticarcilina, a cal ten menos efectos adversos e é máis eficaz fronte a Pseudomonas aeruginosa.[107]
Ureidopenicilinas[editar | editar a fonte]
As ureidopenicilinas creáronse derivadas da molécula de ampicilina para ampliar aínda máis o espectro contra as bacterias gramnegativas e as Pseudomonas.[101] As ureidopenicilinas penetran ben nos tecidos e teñen excelentes concentracións tisulares, incluíndo o líquido cefalorraquídeo en pacientes con meninxes inflamadas, e niveis adecuados en óso para o tratamento de osteomielite. Do mesmo xeito que as carboxipenicilinas, están asociadas a hipopotasemia, hipernatremia e disfunción plaquetaria.[108] Neste grupo de penicilinas están a mezlocilina, azlocilina e a piperacilina.[101]
Amidinopenicilinas[editar | editar a fonte]
As amidinopenicilinas presentan grande eficacia fronte a gramnegativos, pero escasa ante cocos grampositivos, debido á súa estrutura química, a 6-amidinopenicilina.[109]
- O mecilinam actúa moi ben fronte a enterobacterias. A causa do seu éxito ante os gramnegativos débese á produción de esferoplastos pola súa afinidade á PBP2 e ó seu efecto sinérxico xunto a outros β-lactámicos.[109] Con todo, o mecilinam non pode actuar fronte a bacterias produtoras de β-lactamases nin ante Haemophilus influenzae, Pseudomonas aeruginosa nin B. fragilis. A súa utilización está indicada no caso de infeccións urinarias por enterobacterias, así como tamén na febre tifoide e a salmonelose septicémica.[109]
- O pivmecilinam é o éster do mecilinam e é indicada nos mesmos casos, aínda que presenta unha vantaxe en canto á administración, a diferenza da anterior amidinopenicilina, esta pódese administrar por vía oral, hidrolizándose despois a mecilinam.[110]
Resistentes a betalactamases de gramnegativos[editar | editar a fonte]
O representante do grupo é a temocilina, o cal só é útil fronte a enterobacterias, Haemophilus spp., e Neisseria gonorrhoeae. As bacterias grampositivas, anaerobias e Pseudomonas spp. son resistentes á súa acción.[111]
Mecanismo de acción[editar | editar a fonte]
A penicilina, como o resto dos β-lactámicos, exerce unha acción bactericida ao alterar a parede celular bacteriana, estrutura que non existe nas células humanas.[112] A parede bacteriana atópase por fóra da membrana plasmática e confire ás bacterias a resistencia necesaria para soportar, sen romper, a elevada presión osmótica que existe no seu interior. Ademais, a parede bacteriana é indispensable para:[4]
- A división celular bacteriana.[4]
- Os procesos de transporte de substancias aos que limita polas súas características de permeabilidade.[4]
- A capacidade patóxena e antixénica das bacterias, xa que conteñen endotoxinas bacterianas.[4]

Hai importantes diferenzas na estrutura da parede entre as bacterias grampositivas e gramnegativas, das que cabe destacar a maior complexidade e contido en lípidos nas gramnegativas.[4]
A acción da penicilina, e en xeral dos β-lactámicos, desenvólvese fundamentalmente na última fase da síntese do peptidoglicano da parede celular, uníndose a un enzima transpeptidase chamado proteína fixadora de penicilina,[113] responsable de producir unha serie de enlaces cruzados entre as cadeas de péptidos. A formación destes enlaces ou pontes é a que confire, precisamente, a maior rixidez á parede bacteriana. Polo tanto, os β-lactámicos como a penicilina inhiben a síntese do peptidoglicano indispensable na formación da parede celular bacteriana. As bacterias sen a súa parede celular estalan ou son máis facilmente fagocitadas polos granulocitos.[112]
Esta inhibición produce unha acumulación dos precursores do peptidoglicano, os cales producen unha activación de enzimas como hidrolases e autolisinas que dixiren, aínda máis, o remanente de peptidoglicano na bacteria. Ao perderen a súa parede celular como consecuencia da acción da penicilina, as bacterias grampositivas son denominadas protoplastos, mentres que as gramnegativas, que non chegan a perder toda a súa parede celular, reciben o nome de esferoplastos.[114]
A penicilina mostra un efecto sinérxico cos aminoglicósidos, posto que a inhibición da síntese do peptidoglicano permite que os aminoglicósidos penetren a parede celular con maior facilidade, permitindo así trastornos na síntese de proteínas dentro da célula bacteriana (feito que resulta nunha concentración menor de antibiótico que a requirida para eliminar o microorganismo susceptible).[115][116]
Uso en clínica[editar | editar a fonte]

Inicialmente, tras a comercialización da penicilina natural na década de 1940, a maioría das bacterias eran sensibles a ela.[118] Pero debido ao uso e abuso desta substancia moitas bacterias volvéronse resistentes, aínda que segue sendo activa nalgunhas cepas de Streptococcus sp, Staphylococcus sp, Neisseria sp, Clostridium sp, Listeria monocytogenes, Haemophilus sp, Bacteroides sp, Escherichia coli, Proteus mirabilis, Klebsiella e Enterobacter.[119]
A penicilina é indicada, por exemplo, en pacientes embarazadas, a termo ou non, como medida profiláctica cando se sospeita nelas un alto risco de infección polo estreptococo do grupo B.[120]
A penicilina V potásica indícase para tratar certas formas de pneumonía bacteriana, a escarlatina, e as infeccións en oídos, pel e garganta. Tamén se usa para previr a febre reumática recorrente e a corea infecciosa.[121] En forma inxectable, a penicilina V úsase en certas infeccións bacterianas dos ósos, estómago, articulacións, sangue, meninxite e das válvulas do corazón.[122]
O tratamento inicial dunha bacteriemia (presenza de bacterias en sangue que ocasiona febre alta, confusión, estupor e morte en apenas 12 horas), lévase a cabo coa administración de penicilinas semisintéticas como a nafcilina ou a metacilina intravenosas, se o paciente non é alérxico ou a infección é causada por bacterias sensibles.[123]
A borreliose, transmitida polas carrachas e que pode cursar sen tratamento durante varias semanas ou meses causando síntomas neurolóxicos ou cardíacos, é unha enfermidade que pode ser tratada con penicilina oral ou amoxicilina, especialmente en nenos. Nos estadios avanzados adóitase administrar penicilina intravenosa de 2 a 4 semanas.[124]
Os antibióticos de preferencia no tratamento do tétanos tamén son as penicilinas a altas doses.[123]
Aplicación veterinaria[editar | editar a fonte]
A penicilina G adminístrase en preparados inxectables para o tratamento de infeccións por organismos susceptibles en múltiples especies veterinarias, incluíndo cans, gatos, furóns domésticos, coellos, ourizos e aves. A penicilina G soa ou combinada usouse con éxito para tratar xatas con mastite.[125] Certas especies, incluíndo serpes, paxaros, tartarugas, coelliños de indias e chinchillas, mostraron sensibilidade á penicilina procaína.[126]
Implicacións clínicas[editar | editar a fonte]
A penicilina deu comezo á era dos antibióticos, traendo a cura de enfermidades comúns como a sífilis,[127] facendo que as intervencións cirúrxicas fosen menos arriscadas e que a medicina das infeccións fose máis confiable.[128] Antes da década de 1930, persoas adultas e nenos morrían en grandes cantidades por infeccións bacterianas como a pneumonía e a febre reumática, desde os máis pobres ata os máis ricos.[129][130] En 1924, o fillo do presidente estadounidense Calvin Coolidge, un mozo de 16 anos de idade, morreu por unha septicemia orixinada nunha ferida dun pé polas súas zapatillas de tenis.[27] Aínda que a prevención, as vacinas e outras medidas epidemiolóxicas trouxeron a erradicación de certas enfermidades, a penicilina por si soa salvou máis vidas desde a súa introdución no mercado que ningún outro medicamento.[131] Pero o mal uso da penicilina trouxo, á súa vez, resistencias en organismos que poden orixinar infeccións fulminantes como Staphylococcus e Clostridium. Fleming, durante o seu discurso de aceptación do premio Nobel polo seu descubrimento, dixo:
O tempo virá cando a penicilina poida ser comprada por calquera nas tendas. E logo está o perigo de que o home ignorante use a miúdo infradoses e, ao expor os seus microbios a cantidades non-letais do medicamento, os volva resistentes.Alexander Fleming.[131]
Farmacoloxía[editar | editar a fonte]
Dado que a maioría das penicilinas son destruídas polo zume gástrico, a absorción por vía oral non é boa e por iso deben ser administradas parenteralmente.[132] A penicilina absórbese rapidamente tanto coa administración intramuscular coma a subcutánea.[133] Os niveis sanguíneos posteriores á administración parenteral son elevados pero transitorios.[134] A toxicidade oral (LD50), é dicir, a dose letal no 50% dos animais de experimentación é aproximadamente 8 900 mg/kg.[135] Certas reaccións neurolóxicas obsérvanse, incluíndo convulsións, se a penicilina e outros β-lactámicos chegan a alcanzar concentracións moi elevadas no líquido cefalorraquídeo.[76]
A unión a proteínas séricas é variable nun rango que vai desde o 15% para a amoxicilina ata o 97% para a dicloxacilina.[136] A vida media sérica é curta, aproximadamente 30 minutos para penicilina G e 60 minutos para penicilinas de amplo espectro.[136]
A penicilina é eliminada polos riles, de modo que unha diminución ou inhibición da secreción tubular renal pode aumentar a concentración e o efecto terapéutico da penicilina. As doses deben ser reconsideradas en pacientes con insuficiencia renal ou que estean tomando outros medicamentos como o probenecid,[115][137] usado en pacientes que requiran concentracións particularmente elevadas de penicilina.[76]
As penicilinas non son metabolizadas ou só minimamente metabolizadas e son excretadas principalmente polos riles a través da filtración glomerular (10%) e a secreción tubular (90%).[138] O probenecid bloquea a excreción renal e así causa un aumento dos niveis séricos de penicilina.[115][139] Estes antibióticos (excepto as penicilinas penicilinase resistentes) poden ser eliminados do organismo por diálise peritoneal e hemodiálise. En pacientes con disfunción renal severa son necesarios axustes nas doses diarias para previr niveis excesivos e toxicidade consecuente.[140][141]
Unidades[editar | editar a fonte]
A acción da penicilina G definiuse inicialmente en unidades. Por exemplo, a penicilina G sódica cristalina contén aproximadamente 1 600 unidades/mg (1 unidade = 0.6 µg; 1 millón de unidades de penicilina = 0.6 g). As penicilinas semisintéticas prescríbense por peso no canto de facelo por unidades. A concentración inhibitoria mínima (CIM) de calquera penicilina (ou calquera outro antimicrobiano), polo xeral vén dada en gr/ml. A maioría das penicilinas dispénsanse en forma de sales de sodio ou potasio do ácido libre. A penicilina G potásica contén aproximadamente 1,7 mEq de K+ por cada millón de unidades de penicilina. Os sales de penicilina en forma cristalina seca consérvanse estables durante períodos longos de tempo, chegando a conservarse varios anos a 4 °C. As solucións preparadas perden a súa actividade con rapidez, unhas 24 horas a 20 °C, polo que cada solución debe ser preparada xusto antes da súa administración.[64]
Reaccións adversas[editar | editar a fonte]
Describíronse diversos tipos de reaccións, algunhas delas mortais, en persoas ás que se administrou penicilina. A penicilina e os seus derivados son as causas máis frecuentes de reaccións dependentes da inmunoglobulina E (IgE), aínda que poden tamén producirse inmunoglobulinas G e M.[115][142] As reaccións adversas á penicilina ocorren en ≤1% dos pacientes que toman o antibiótico. Aínda que a alerxia á penicilina é a forma máis frecuente de alerxia a medicamentos, menos do 20% das persoas que cren ser alérxicas sono verdadeiramente.[143] Entre as reaccións adversas máis comúns están:
- Reacción de hipersensibilidade ou alérxica: é o efecto adverso máis importante. Pode ser inmediata (2-30 minutos), acelerada (1-72 horas) ou tardía (máis de 72 horas). A gravidade é variable: desde simples erupcións cutáneas pasaxeiras (urticaria ou anxioedema), ata choque anafiláctico, o cal ocorre entre o 0,004% e o 0,04% dos casos e leva á morte no 10% desas situacións.[144][145]
- Trastornos gastrointestinais: o máis frecuente é a diarrea, xa que a penicilina elimina a flora intestinal. Pode tamén provocar náuseas e vómitos.[145]
- Infeccións adicionais, incluíndo candidíase.
Entre os efectos secundarios menos frecuentes, que se dan no 0,1-1% dos pacientes, están:
- Aumento reversible de encimas aminotransferases, que adoita pasar inadvertido.
- Trastornos hematolóxicos: anemia, neutropenia e trombocitopenia. A penicilina pode estimular a produción de anticorpos, principalmente IgG e IgM, os cales causan lesións nas células sanguíneas, ocasionando estes trastornos hematolóxicos.[115][146]
- Hipopotasemia: pouco frecuente.
- Nefrite intersticial.[147]
- Encefalopatía: que cursa con mioclonias, convulsións crónicas e tónico-clónicas de extremidades que poden acompañarse de somnolencia, estupor e coma. A encefalopatía é máis frecuente en pacientes con insuficiencia renal.[76]
A dor e a inflamación do sitio de inxección son tamén frecuentes nas penicilinas administradas por vía parenteral, como a benzilpenicilina. Ocasionalmente informouse que as penicilinas, así como outros fármacos, poden causar necrose epidérmica tóxica, pénfigo e eritema multiforme.
Os pacientes con fibrose quística teñen maior probabilidade de sufrir reaccións adversas á penicilina e os seus derivados.[148] A penicilina non causou defectos de nacemento polo que con frecuencia se receita a mulleres embarazadas. As penicilinas poden cruzar a barreira placentaria e só deben ser usadas no embarazo cando sexa absolutamente necesario e recomendado baixo supervisión médica. A penicilina pode tomarse durante a lactación, con todo, pequenas cantidades do antibiótico poden pasar ao leite materno e causar no lactante indixestión, diarrea ou reaccións alérxicas.[148]
Alerxia á penicilina[editar | editar a fonte]
As reaccións alérxicas a calquera dos antibióticos β-lactámicos poden darse en ata un 10% dos pacientes que reciben estes axentes.[6] Aceptouse no pasado que pode haber ata un 10% de sensibilidade cruzada entre os diferentes derivados da penicilina, é dicir, que un 10% de pacientes hipersensibles a un dos medicamentos, como as cefalosporinas e carbapenemas, tamén o será para os outros derivados da penicilina, por razón de que todas teñen un anel β-lactámico.[149][150] Con todo, achados recentes mostraron que non hai un aumento de alerxias cruzadas desde as cefalosporinas de segunda xeración ata as máis recentes.[151][152] Certas investigacións actuais demostraron que o principal factor na determinación de reaccións inmunitarias é a similitude que hai entre as cadeas laterais das cefalosporinas de primeira xeración e as penicilinas e non necesariamente entre a estrutura do β-lactámico común entre eles.[153] Nunha revisión de historias clínicas, atopouse que a alerxia á penicilina é máis frecuente nas mulleres que nos homes.[154][155]
A vía de administración máis frecuente coa cal aparecen estas reaccións alérxicas é a endovenosa, e raramente ocorre cando se administra por vía oral. Para desenvolver a reacción necesítase unha exposición inicial ao medicamento ou aos seus determinantes antixénicos, por exemplo, ao inxerir leite ou produtos de animais tratados con penicilina, a través do leite materno ou polo contacto co medicamento ao administralo ao individuo.[55]
A maioría dos pacientes expostos á penicilina desenvolven anticorpos fronte a este antibiótico e, con todo, non manifestan reaccións ao exporse novamente a ela.[115][142] Aqueles que desenvolven reaccións alérxicas asociadas á administración de penicilinas mostran síntomas que varían amplamente: anafilaxe, enfermidade do soro, anemia hemolítica, enfermidades renais, anxioedema, urticaria, vasculite entre outros, e poden chegar a ocasionar a morte.[55]
As probas cutáneas, como o Pre-pen e o Kremers-Urban, deseñáronse para pacientes nos que se sospeitan reaccións alérxicas á penicilina mediadas por IgE e que se anticipa o seu tratamento, como no caso de pacientes con endocardite ou mulleres embarazadas con sífilis. Cerca do 25% dos pacientes con antecedentes de alerxia á penicilina terán unha proba cutánea positiva, mentres que un 6% (do 3 ao 10%) con antecedentes negativos presenta unha resposta cutánea positiva.[115] Outras probas, como a radioalergoadsorción ou probas in vitro, non ofrecen vantaxes sobre as probas cutáneas correctamente realizadas.
Como é de esperar, un gran número de pacientes (dun 50 a un 100%) cunha proba cutánea positiva, producen reaccións alérxicas á penicilina de ser administrado o antibiótico, mentres que un 0,5% dos pacientes con probas cutáneas negativas reaccionan ao fármaco, a cal tende a ser unha reacción leve ou tardía, logo da administración de penicilina. Logo de varios anos, ata un 80% dos pacientes perde a sensibilidade anafiláctica e os anticorpos IgE.[115]
Interaccións medicamentosas[editar | editar a fonte]
A penicilina non debe ser tomada conxuntamente con outros antibióticos como o cloranfenicol, a eritromicina, a tetraciclina ou a neomicina, entre outros, porque se reduce a súa efectividade.[156] Sábese que a penicilina diminúe o efecto das pílulas anticonceptivas e que as reaccións secundarias ocorren con máis frecuencia ao combinar a penicilina cos beta bloqueantes. Tamén interfire coa absorción do atenolol, e a grandes doses, a penicilina potencia o efecto dos medicamentos anticoagulantes.
Non se recomenda tomar refrescos carbonatados ou certos mollos naturais, pois o ambiente ácido destas bebidas pode destruír o medicamento. Por iso, as penicilinas orais deben ser inxeridas en xaxún ou unhas 2 horas despois de comer. A amoxicilina pode ser administrada coa comida.
Resistencia á penicilina[editar | editar a fonte]
Cerca do 25% das cepas de Streptococcus pneumoniae illadas en pacientes con otite media son resistentes á penicilina e á amoxicilina, e comparten esa resistencia con cerca do 33% de cepas de Haemophilus influenzae nestes pacientes.[115] Segundo publicacións recentes, a porcentaxe de illamentos de S. pneumoniae con susceptibilidade a penicilina diminuída en Chile e España,[157] por exemplo, é de ao redor dun 30% nos pacientes menores de 5 anos.[158] Polo xeral, as infeccións causadas por estas cepas resistentes asócianse a limitacións terapéuticas e un desenlace desfavorable da infección.[159]
O uso, moitas veces indiscriminado, destes fármacos ante o temor dunha complicación e/ou risco de morte do paciente, case sempre sen o amparo do coñecemento do axente causal da infección e o seu comportamento ante o tratamento aplicado, provoca tal efecto sobre os microorganismos que os leva a desenvolver unha resistencia maior. Este serio problema induciu a varios países a aplicar políticas de uso racional dos antibióticos, baseadas no coñecemento dos parámetros farmacodinámicos e microbiolóxicos destes fármacos e apoiadas pola realización de probas de laboratorio que permitan unha verdadeira avaliación da infección e do tratamento que debe ser aplicado.[160]
Logo da aparición de serias resistencias á penicilina, desenvolvéronse derivados con maior espectro de acción, así como penicilinas resistentes á β-lactamase, como é o caso da flucloxacilina, a dicloxacilina e a meticilina. Con todo, estes fármacos son aínda ineficaces contra as cepas do estafilococo resistente á meticilina, aínda que existen outros fármacos eficaces para tratar a súa infección.[161]
En xeral, a resistencia a antibióticos β-lactámicos en calquera bacteria fundaméntase na interacción entre os factores seguintes:[162][163]
- Permeabilidade da parede bacteriana ao antibiótico.
- Presenza, espectro de acción e afinidade das proteínas de unión a penicilina ou PBPs (do inglés penicillin binding proteins).[164]
- Existencia e eficacia dos mecanismos de excreción do composto.
- Afinidade do antibiótico polo sitio activo da PBP.
Algúns destes factores están relacionados coa localización taxonómica do microorganismo: por exemplo, a estrutura da parede das bacterias gramnegativas dificulta a permeabilidade do antibiótico e, por iso, diminúe a súa eficacia.
Cabe destacar a existencia de encimas que hidrolizan elementos das penicilinas diminuíndo a súa actividade: son as chamadas β-lactamases. Nas bacterias gramnegativas, o encima atópase no periplasma, xusto entre as membranas interna e externa, mentres que as grampositivas segregan a β-lactamase ao medio que as rodea. O encima pode ser codificado por xenes do cromosoma bacteriano ou por plásmidos. Un dos xenes bacterianos asociado á produción de β-lactamases é o blaZ, o cal pode ser localizado nun plásmido. A expresión deste xene vén determinada por dous xenes reguladores blaR1 e blaI. Certas evidencias fan supor que a exposición á penicilina provoca que a bacteria active o xene blaR1, cuxo produto actúa como unha protease activando o xene blaI e permitindo a síntese do encima por blaZ.[165]
A β-lactamase ten maior afinidade polo antibiótico que o que este ten pola súa diana. Certos antibióticos, como a ceftriaxona e a cefatazidima, son estables en presenza de β-lactamases codificadas e producidas desde plásmidos. Con todo, as codificadas e producidas desde cromosomas, como no caso de Enterobacter, son encimas que hidrolizan practicamente a todas as penicilinas e cefalosporinas.[115]
Determinouse que a mala evolución de certas enfermidades causadas por organismos con susceptibilidade diminuída á penicilina, como a pneumonía pneumocócica invasiva en nenos, tende a ser independente da susceptibilidade á penicilina do microorganismo.[166] Con todo, como a resistencia á penicilina e outros antibióticos continúa en aumento, estimulouse o interese en novos medicamentos para propiedades bactericidas en contra de organismos resistentes, medicamentos como as quinolonas, cuxo branco son os encimas ADN xirase de bacterias gramnegativas e topoisomerase tipo IV de bacterias grampositivas.[167]
Produción biotecnolóxica[editar | editar a fonte]

A produción industrial de penicilina emerxeu e floreceu como industria por mor da segunda guerra mundial, en especial pola cantidade de empregos dispoñibles nos Estados Unidos. En xullo de 1943, presentouse un plan para distribuíla en masa ás tropas na fronte de batalla de Europa e, grazas a iso, producíronse 425 millóns de unidades. Por entón, o fungo facíase crecer sobre unha capa delgada de cultivo posto en bandexas ou botellas. Para mellorar os requirimentos de espazo e dos materiais desenvolveuse un novo método comercial de fermentación mergullada en caldeiros de 20 000 a máis de 100 000 litros de capacidade, facendo que se reducisen os prezos de custo e aumentase a produción. Como consecuencia, en 1945, producíronse máis de 646 miles de millóns de unidades.[168] Xa que logo, o que era un composto caro e difícil de illar é hoxe unha «mercadoría química», é dicir, un composto quimicamente puro que se compra e vende a grande escala nun mercado competitivo.[169]
O desenvolvemento biotecnolóxico de cepas superproductoras foi outro campo de investigación de grande interese. A cepa illada orixinalmente por Fleming producía ao redor de 2 u/mL (unidades internacionais por mL). Os procesos empregados a finais da década dos 80 xeraban 85 000 u/mL. O desenvolvemento das cepas baseouse en:[5][170]
- a análise de numerosos illados de especies e cepas distintas;
- a súa mutaxénese mediante raios X, metilbiscloroetilamina, nitrosoguanidina, radiación UV de onda curta e outros;
- a recombinación mediante ciclos parasexuais en P. chrysogenum;
- a fusión de protoplastos;
- técnicas moleculares de barallado de ADN, que permiten realizar evolución dirixida de fragmentos de ADN mediante PCR.
Biosíntese e semisíntese[editar | editar a fonte]

A estratexia de produción industrial de penicilina está ligada ao tipo de penicilina a sintetizar. Basicamente, esta variedade reside na substitución do grupo acilo da posición 6 no ácido 6-aminopenicilánico. Cando a fermentación[N 3] se produce sen engadir ningún precursor prodúcense as penicilinas naturais. De entre elas, só a penicilina G é útil terapeuticamente e xa que logo é o composto a purificar. Por outra banda, de engadir outros precursores para a cadea lateral, o control da reacción mellora e é posible producir o composto desexado cunha alta especificidade. Esta estratexia dá lugar ás penicilinas biosintéticas, como a penicilina V ou a penicilina O (en pequenas cantidades). A aproximación ao problema máis empregada pasa pola modificación química do composto obtido mediante fermentación. Deste xeito é posible obter unha gran diversidade de penicilinas semisintéticas.[5]
A xeración de penicilinas semisintéticas require a produción, mediante fermentación, de penicilina G (nalgúns casos penicilina V), composto que se converte en ácido 6-aminopenicilánico mediante unha transformación química, ou, máis frecuentemente, encimática. Este composto é logo modificado mediante o encima penicilina acilase de modo que se engada a cadea lateral desexada á posición 6, o que dá lugar á penicilina semisintética final. De feito, o 38% das penicilinas producidas comercialmente empréganse na medicina humana, o 12 % en veterinaria e o 43% como precursores para o deseño de penicilinas semisintéticas.[5]
Regulación da síntese[editar | editar a fonte]
O anel tiazolidínico da β-lactama xérase mediante a unión dos aminoácidos L-cisteína, L-valina e ácido α-aminoadípico. Este último, aminoácido non proteico, únese ao residuo de cisteína mediante unha síntese de péptido non ribosomal, a cuxo produto se fusiona unha valina mediante unha epimerización, reacción que dá lugar a un tripéptido. Este tripéptido cíclase mediante un proceso aínda non descrito dando lugar ao primeiro produto illable, a isopenicilina N. A acción da penicilina transacetilase, que substitúe a cadea de α-aminoadípico no C6 por unha molécula de ácido fenilacético activada, produce a bencilpenicilina.[171]
A produción de penicilina é unha área que require a colaboración de científicos e enxeñeiros para a efectiva produción de cantidades industriais do antibiótico. A penicilina é un metabolito secundario do fungo Penicillium, é dicir, o fungo non produce o antibiótico cando crece baixo condicións normais, só cando o seu crecemento se atopa inhibido por verse sometido a condicións de estrés. Outros factores inhiben a produción de penicilina, incluíndo a súa mesma ruta de produción. Por exemplo, a lisina inhibe a súa síntese debido a que inhibe a homocitrato sintase, encima implicado na síntese de ácido α-aminoadípico. Porén, a retroinhibición por lisina non parece ser un factor limitante na produción industrial do composto. Outros elementos reguladores son: a concentración de fosfato, de glicosa e de ión amonio.[5]
As células de Penicillium medran usando unha técnica coñecida como «fed-batch» (cultivo de lote nutrido), no que se ven continuamente suxeitas a condicións de estrés e, polo tanto, producen penicilina en abundancia. As fontes de carbono dispoñibles son tamén importantes porque a glicosa inhibe a penicilina mentres que a lactosa non. O valor do pH, os niveis de nitróxeno, fosfato e osíxeno son tamén críticos nos lotes de produción e deben controlarse automaticamente.
Notas[editar | editar a fonte]
- ↑ Para referencias xerais desta sección, consultar Historia da penicilina.
- ↑ En Estados Unidos, a presentación chamada Bicillin C-R, unha suspensión inxectable que contén 1,2 millóns de unidades de penicilina benzatina con 1,2 millóns de unidades de procaína por 4 mL, non se recomenda para o tratamento da sífilis porque é unha dose menor á recomendada para o tratamento eficaz de devandita infección. Cometéronse erros nese país polo similares que resultan os nomes Bicillin L-A e Bicillin C-R.[79] Como resultado, fixéronse cambios no empaquetado do Bicillin CR e CR 900/300 coa aclaratoria "Non apto para o tratamento da sífilis"[80]
- ↑ Entendendo fermentación non no sentido metabólico da palabra, senón no sentido biotecnolóxico de produción a grande escala nun biorreactor.[5]
- Referencias
- ↑ Walling, Anne D. (15 de setembro de 2006). "Tips from Other Journals – Antibiotic Use During Pregnancy and Lactation". American Family Physician. Consultado o 25 de setembro de 2015.
- ↑ Farreras, P.; Rozman, C. (1978). Medicina Interna (en castelán) 2 (9ª ed.). Barcelona: Marin S.A. pp. 760–763. ISBN 84-7102-980-4.
- ↑ "Discovery and Development of Penicillin". American Chemical Society. Consultado o 29 de novembro de 2017.
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 Prescott, L.M. (1999). McGraw-Hill Interamericana de España, S.A.U., ed. Microbiología. ISBN 84-486-0261-7.
- ↑ 5,0 5,1 5,2 5,3 5,4 5,5 Crueger, Wulf; Crueger, Anneliese (1989). Sinauer Associates, ed. A texbook of industrial microbiology (2 ed.). Sunderland. ISBN 0878931317.
- ↑ 6,0 6,1 Solensky R (2003). Clinical reviews in allergy & immunology, ed. Hypersensitivity reactions to beta-lactam antibiotics 24. pp. 201–20. PMID 12721392. doi:10.1385/CRIAI:24:3:201.
- ↑ Enjalbert F, Rapior S, Nouguier-Soulé J, Guillon S, Amouroux N, Cabot C (2002). Treatment of amatoxin poisoning: 20-year retrospective analysis. J Toxicol Clin Toxicol. 40. PMID 12475187.
- ↑ Sokoloff,, Boris (1945). Ziff-Davis, ed. The Story of Penicillin.
- ↑ Brown, Kevin (2004). Penicillin Man: Alexander Fleming and the Antibiotic Revolution. ISBN 0-7509-3152-3.
- ↑ Br Med J., ed. (1892). The Clarence Memorial Wing, St. Mary's Hospital (en inglés) 2. PMCID PMC2421595.
- ↑ Glynn, AA (2006). Journal of Antimicrobial Chemotherapy, ed. Museum review: Alexander Fleming Laboratory Museum. St Mary's Hospital, Praed Street, London W2 1NY, UK [Curator: Kevin Brown] (en inglés) 58. doi 10.1093/jac/dkl148.
- ↑ Volcy, Charles (2004). Unibiblos, ed. Lo malo y lo feo de los microbios, páx. 84. ISBN 958-701-400-6.
- ↑ Calvo, A (2006). Rev Esp Quimioterap, ed. Ehrlich y el concepto de "bala mágica" (PDF) 19.
- ↑ "People and discoveries:Alexander Fleming" (en inglés). Public Broadcasting Service. Consultado o 31 de agosto de 2010.
- ↑ Sherry F. Queener et al., Beta-lactam Antibiotics for Clinical Use, Informa Health Care, 1986, ISBN 0-8247-7386-1, 9780824773861, p. 4. Consultar: J. B. Sanderson. Appendix No 5. "Further report of researches concerning the intimate pathology of contagion. The origin and distribution of microzymes (bacteria) in water, and the circumstances which determine their existence in the tissue and liquids of the living body". 13th Report of the Medical Officer of the Privy Council [John Simon], with Appendix, 1870. Her Majesty's Stationary Office, Londre, 1871, pp. 56-66; reimpreso en Quarterly Journal of Microscopical Science, n. ser., XI, 1871, pp. 323-352, dispoñible na web do Journal of Cell Science.
- ↑ John Bankston (2004). Joseph Lister and the Story of Antiseptics (Uncharted, Unexplored, and Unexplained) (en inglés). Bear: Mitchell Lane Publishers. ISBN 1-58415-262-1.
- ↑ Power, D'Arcy (1901). Lee, Sidney, ed. Entrada "Roberts, William (1830-1899)" en Dictionary of National Biography. Londres: Smith, Elder & Co.
- ↑ Varios autores (1910-1911). Entrada «Tyndall, John». En Chisholm, Hugh. Encyclopædia Britannica.
- ↑ Debré, Patrice (2000). Louis Pasteur. JHU Press. ISBN 9780801865299.
- ↑ Gli antibiotici? Una scoperta italiana Arquivado 02 de febreiro de 2017 en Wayback Machine.(en italiano)
- ↑ "Antibióticos e inmunidad". Arquivado dende o orixinal o 21 de decembro de 2009. Consultado o 3 de agosto de 2011.
- ↑ Dr. Clodomiro Picado Twight Honored with WIPO medal (PDF). WIPO Magazine. p. 11. Consultado o 02-03-2008.
- ↑ "El descubridor de la penicilina era costarricense, según dos científicos. . Infomed 4 de agosto de 1999. Ano 6, Non. 150". Arquivado dende o orixinal o 24 de febreiro de 2009. Consultado o 30 de agosto de 2010.
- ↑ Jaramillo Antillón, Juan (2005). "El principio de la quimioterapia y los antibióticos". En Universidade de Costa Rica. Historia y filosofía de la Medicina (en castelán). ISBN 9977679851.
Tilio von Vulgo, Édgar Cabezas e María San Román afirman a intervención de Clorito Picado no descubrimento da penicilina (páxinas 160 e 161).
- ↑ López, MT, Gómez-Lus, ML (2006). Rev. Esp. Quimioterap., ed. "Las claves de una época: Wright y Fleming" (PDF) (en castelán). p. 6. Arquivado dende o orixinal (PDF) o 06 de abril de 2010. Consultado o 31 de agosto de 2010.(en castelán)
- ↑ 26,0 26,1 Alexander Fleming (11 de decembro). "Penicillin. Conferencia Nobel" (PDF) (en inglés). Arquivado dende o orixinal (PDF) o 15 de decembro de 2010. Consultado o 31 de agosto de 2010.(en inglés)
- ↑ 27,0 27,1 27,2 Bud, Robert (2007). Oxford University Press, ed. Penicillin: Triumph and Tragedy. Ver capítulo:The Brand in the Era of Propaganda. ISBN 0-19-925406-0.
- ↑ Clarke, Tom (2002). Penicillin paper restores Fleming's healthy reputation. Nature 419. doi 10.1038/419867b.
- ↑ Hantula, Richard (2002). Alexander Fleming. Gareth Stevens. ISBN 0-8368-5243-5.
- ↑ 30,0 30,1 30,2 30,3 Wong, G (2003). "Penicillin" (en inglés). Consultado o 31 de agosto de 2010.
- ↑ Alexander Fleming (1881–1955): Discoverer of penicillin(en inglés)
- ↑ Kendall F. Haven, Marvels of Science (Libraries Unlimited, 1994) p182
- ↑ Fleming, A. (1929). On the antibacterial action of cultures of a Penicillium, with special reference to their use in the isolation of B. influenzae Arquivado 10 de agosto de 2011 en Wayback Machine.. British Journal of Experimental Pathology. 10: 226-236.(en inglés)
- ↑ Wainwright, M & Swan, HT (1986). Medical History, ed. "Discovery of penicillin" (en inglés). Consultado o 1 de setembro de 2010.
- ↑ Wainwright M, M; Swan, HT (30 de xaneiro de 1986). American Chemical Society, ed. "C.G. Paine And The Earliest Surviving Clinical Records Of Penicillin Therapy" (en inglés).
- ↑ The Illinois Historic Preservation Agency. (07-04-2006). "Penicillin: "The Miracle Drug"" (PDF) (en inglés). Consultado o 1-09-2010.
- ↑ ""Penicillin: Opening the Era of Antibiotics"". National Center for Agricultural Utilization Research website. 07-04-2006. Arquivado dende o orixinal o 06-03-2016. Consultado o 19-06-2007.
- ↑ Universidade de Wisconsin-Madison (07-04-2006). ""Tom Volk's Fungus of the Month for November 2003"". National Center for Agricultural Utilization Research website (en inglés). Consultado o 1-09-2010.
- ↑ Royal Society of Chemistry. Discovery and Development of Penicillin Arquivado 04 de decembro de 2008 en Wayback Machine. (en inglés). 19 de novembro, 1999. The Alexander Fleming Laboratory Museum, Londres, RU. Consultado o 1-09-2010.
- ↑ Cote, Gregory. Carbohydrate Research at the USDA Laboratory in Peoria, Illinois (en inglés). Agricultural Research Service. Consultado o 1-09-2010.
- ↑ Inyección de penicilina G procaína(en castelán)
- ↑ Inyección de penicilina G benzatina(en castelán)
- ↑ 43,0 43,1 Penicilina V potásica oral(en castelán)
- ↑ Post penicillin antibiotics : from acceptance to resistance? : a Witness Seminar held at the Wellcome Institute for the History of Medicine, London, on 12 May 1998 (en inglés) 6. [London]: [Wellcome Trust]. [2000]. pp. 28–36. ISBN 9781841290126. OCLC 43549178.
- ↑ Bavestrello F, Luis; Cabello M, Angela; Casanova Z, Dunny (novembro de 2002). "Impacto de medidas regulatorias en la tendencia de consumo comunitario de antibióticos en Chile". Revista médica de Chile 130 (11): 1265–1272. ISSN 0034-9887. doi:10.4067/S0034-98872002001100009. Consultado o 18 de setembro de 2017.
- ↑ "Cloxacillin (Professional Patient Advice)". www.drugs.com. Arquivado dende o orixinal o 20 de decembro de 2016. Consultado o 10 de decembro de 2016.
- ↑ 47,0 47,1 "Amoxicillin". The American Society of Health-System Pharmacists. Arquivado dende o orixinal o 05 de setembro de 2015. Consultado o 1 de agosto de 2015.
- ↑ La amoxicilina, usos y abusos Arquivado 22 de xaneiro de 2018 en Wayback Machine.(en castelán)
- ↑ La OMS publica la lista de las bacterias para las que se necesitan urgentemente nuevos antibióticos(en castelán)
- ↑ Gersema LM, Helling DK. The use of subtherapeutic antibiotics in animal feed and its implications on human health. Drug Intell Clin Pharm. 1986 Mar;20(3):214-8. Consultado o 1-09-2010.
- ↑ Palmer GH, Buswell JF, Dowrick JS, Yeoman GH. (1976) Amoxycillin: a new veterinary penicillin. Vet Rec. 1976 Jul 31;99(5):84-5. Consultado o 1-09-2010.
- ↑ Phillips I, Casewell M, Cox T, De Groot B, Friis C, Jones R, Nightingale C, Preston R, Waddell J. Does the use of antibiotics in food animals pouse a risk to human health? A critical review of published data. J Antimicrob Chemother. 2004 Jan;53(1):28-52. Epub 2003 Dec 4. Consultado o 1-09-2010.
- ↑ Bentley, Ronald. The Molecular Structure of Penicillin Arquivado 08 de outubro de 2009 en Wayback Machine. (en inglés). J. Chem. Educ. 2004 81 1462. Consultado o 1-09-2010.
- ↑ Jeremy Berg e John Tymoczko. Figure 8.26. Structure of Penicillin. (descrición da imaxe en inglés). Biochemistry (5ª edición). National Center for Biotechnology Information. Consultado o 1-09-2010.
- ↑ 55,0 55,1 55,2 55,3 55,4 ALPIZAR OLIVARES, Yulién. A penicilina e os seus derivados como axentes desencadenamentos da resposta inmune. Rev Cubana Hematol Inmunol Hemoter [online]. 2000, vol. 16, no. 2 [citado 2008-11-08], pp. 99-104. Dispoñible en: [1]. ISSN 0864-0289.(en castelán)
- ↑ 56,0 56,1 G Zhao, WK Yeh, RH Carnahan, J Flokowitsch, TI Meier, WE Alborn Jr, GW Becker and SR Jaskunas. Biochemical characterization of penicillin-resistant and -sensitive penicillin-binding protein 2x transpeptidase activities of Streptococcus pneumoniae and mechanistic implications in bacterial resistance to beta-lactam antibiotics Arquivado 27 de febreiro de 2010 en Wayback Machine. (artigo completo dispoñible en inglés). J. Bacteriol., 08 1997, 4901-4908, Vol 179, No. 15. Consultado o 1 de setembro de 2010.
- ↑ Antonio Delgado Cirilo, Cristina Minguillón Llombart, Jesús Joglar Tamargo (2003). Introducción a la química terapéutica (en castelán). Ediciones Díaz de Santo. Consultado o 31 de xullo do 2020.
- ↑ John L. Ingraham, Catherine A. Ingraham, Joaquín J. Neto, Emilia (trad.) Quesada, Antonio Ventosa (1871). Reverté, ed. Introducción a la Microbiología. ISBN 84-291-1871-3.
- ↑ Tomado e adaptado de Farmacología humana. Autores: Jesús Flórez, Juan Antonio Armijo e África Mediavilla. Publicado por Elsevier España, 2004; páx. 1108. ISBN 84-458-1290-4.
- ↑ "Penicillins". poultrymed.com (en inglés). Consultado o 23 de xaneiro de 2018.
- ↑ "Dicloxacilina". medlineplus.gov (en castelán).
- ↑ Tomislav Meštrović. "Penicillin Variants". news-medical.net (en inglés). Consultado o 24-01-2018.
- ↑ 63,0 63,1 "Benzylpenicillin". drugbank.ca (en inglés). Consultado o 24-01-2018.
- ↑ 64,0 64,1 64,2 Katzung, Bertram G. (2007). "Chapter 43. Beta-Lactam Antibiotics & Other Inhibitors of Cell Wall Synthesis". En McGraw-Hill. Basic & Clinical Pharmacology (9 ed.). ISBN 0071451536.
- ↑ "Ticarcilina". iqb.es (en castelán). Consultado o 24-01-2018.
- ↑ "Mezlocilina". salud.es. Consultado o 24-01-2018.
- ↑ Tan JS, File TM (1995). "Antipseudomonal penicillins". Medical Clinics of North America (en inglés) 79 (4): 679–93. PMID 7791416.
- ↑ Santiago Gutiérrez; Javier Casqueiro; Juan Francisco Martín. "Los hongos como factorías celulares: biodiversidad de metabolitos secundarios" (PDF) (en castelán). Consultado o 24-01-2018.
- ↑ A. P. BallJ. A. GrayJ. McM. Murdoch. "The Natural Penicillins — Benzylpenicillin (Penicillin G) and Phenoxymethylpenicillin (Penicillin V)". Consultado o 24-01-2018.
- ↑ Alfonso R. Gennaro (2003). Remington Farmacia (en castelán). Ed. Médica Panamericana. p. 1804.
- ↑ "Fenoximetilpenicilina" (en castelán). Consultado o 24-01-2018.
- ↑ William Andrew Publishing (2013). "Pharmaceutical Manufacturing Encyclopedia, 3rd Edition" (en inglés). Elsevier. Consultado o 24-01-2018.
- ↑ 73,0 73,1 "Nuevos datos sobre la ruta biosintética por la que se produce penicilina G". dicyt.com (en castelán). Consultado o 24-01-2018.
- ↑ 74,0 74,1 Juan Manuel Sanchez Yanez (2011). Las Enfermedades Infecciosas En La Historia Humana (en castelán). librosenred. p. 243.
- ↑ Varios autores (2001). Diario de medicina (en castelán). Editorial Complutense.
- ↑ 76,0 76,1 76,2 76,3 76,4 76,5 76,6 76,7 Rossi S, editor, ed. (2006). Australian Medicines Handbook. Adelaida: Australian Medicines Handbook. ISBN 0-9757919-2-3.
- ↑ Residues of Some Veterinary Drugs in Animals and Foods: Monographs Prepared by the Fiftieth Meeting of the Joint FAO/WHO Expert Committee on Food Additives : Rome, 17-26 February 1998 (en inglés). Food & Agriculture Org. 1999. p. 96. ISBN 9789251042809. Arquivado dende o orixinal o 20 de decembro de 2016. Consultado o 24 de xaneiro de 2018.
- ↑ The European Agency for the Evaluation of Medicinal Products (1998). "Committee for veterinary medicinal products. Procaine summary report" (PDF) (en inglés). Arquivado dende o orixinal (PDF) o 25 de xaneiro de 2018. Consultado o 24 de xaneiro de 2018.
- ↑ MMWR Morb. Mortal. Wkly. Rep. (2005). Inadvertent use of Bicillin C-R to treat syphilis infection--Os Angeles, California, 1999-2004 54. pp. 217–9. PMID 15758893.
- ↑ United States Food & Drug Administration. "FDA Strengthens Labels of Two Specific Types of Antibiotics to Ensure Proper Use."
- ↑ "UK doctors advised gonorrhoea has turned drug resistant". BBC News. 10 de outubro de 2011.
- ↑ Gonococcal Infections in Adolescents and Adults
- ↑ Campbell, Jr., G. Douglas; Silberman, Ronald (1998-5). "Drug‐Resistant Streptococcus pneumoniae". Clinical Infectious Diseases (en inglés) 26 (5): 1188–1195. ISSN 1058-4838. doi:10.1086/520286.
- ↑ 84,0 84,1 "Penicilina G (Bencilpenicilina)" (PDF). pediamecum.es. Arquivado dende o orixinal (PDF) o 19-02-2018. Consultado o 25-01-2018.
- ↑ 85,0 85,1 85,2 85,3 85,4 "Penicilina V: Antimicrobianos" (en castelán). Consultado o 25-01-2018.
- ↑ Flórez, Jesús; Armijo, Juan Antonio; Mediavilla África (2004). "Antibióticos β-lactámicos". En Masson. Farmacología humana ((Cuarta edición) ed.). p. 1108. ISBN 8445812904.
- ↑ 87,0 87,1 Castells Molina, Silvia; Hernández Pérez, Margarita (2007). "Farmacología antiinfecciosa". En Elsevier España. Farmacología en enfermería (Segunda ed.). p. 396 e 397. ISBN 84-8174-993-1.
- ↑ Gurusamy, Kurinchi Selvan; Koti, Rahul; Toon, Clare D.; Wilson, Peter; Davidson, Brian R. (2013-08-20). "Antibiotic therapy for the treatment of methicillin-resistant Staphylococcus aureus (MRSA) infections in surgical wounds". The Cochrane Database of Systematic Reviews (8): CD009726. ISSN 1469-493X. PMID 23963687. doi:10.1002/14651858.CD009726.pub2.
- ↑ "Inyección de oxacilina" (en castelán). Consultado o 26-01-2018.
- ↑ "Inyección de nafcilina" (en castelán). Consultado o 26-01-2018.
- ↑ "Cloxacilina" (en castelán). Consultado o 26-01-2018.
- ↑ "Dicloxacilina" (en castelán). Consultado o 26-01-2018.
- ↑ "Clasificación dos antimicrobianos" (en castelán). Arquivado dende o orixinal o 29-10-2008. Consultado o 4-09-2010.
- ↑ "THE MEDICINE CHEST" (en inglés). Archived from the original on 12-02-2008. Consultado o 25-01-2018.
- ↑ World Health Organization, ed. (abril 2015). "WHO Model List of Essential Medicines (19th List)" (PDF). Arquivado dende o orixinal (PDF) o 13 de decembro de 2016. Consultado o 8 de decembro de 2016.
- ↑ "Ampicilina" (PDF) (en castelán). Arquivado dende o orixinal (PDF) o 27-01-2018. Consultado o 25-01-2018.
- ↑ Diccionario de especialidades farmaceúticas. 2007.
- ↑ Ensink, J. M.; Klein, W. R.; Mevius, D. J.; Klarenbeek, A.; Vulto, A. G. (1992-9). "Bioavailability of oral penicillins in the horse: a comparison of pivampicillin and amoxicillin". Journal of Veterinary Pharmacology and Therapeutics (en inglés) 15 (3): 221–230. ISSN 0140-7783. doi:10.1111/j.1365-2885.1992.tb01010.x. Arquivado dende o orixinal o 13 de setembro de 2019. Consultado o 29 de marzo de 2019.
- ↑ K. Roholt, B. Nielsen, and E. Kristensen. Clinical Pharmacology of Pivampicillin. Antimicrob Agents Chemother. 1974 November; 6(5): 563–571. PMCID: PMC444693 (Consultado o 4-09-2010)
- ↑ Admani AK, Somasundram U., Singh I. El Tratamiento de los Pacientes Ancianos con Infecciones Agudas de las Vías Aéreas Inferiores: Comparación entre Pivampicilina y Amoxicilina Arquivado 23 de setembro de 2009 en Wayback Machine. (en español). Current Medical Research and Opinion 9(8):536-541, Ref.:10, 1985/ (Consultado o 4-09-2010)
- ↑ 101,0 101,1 101,2 Raúl Romero Cabello (2007). Microbiologia y parasitologia humana / Microbiology and Human Parasitology: Bases etiologicas de las enfermedades infecciosas y parasitarias / Etiological Basis of Infectious and Parasitic Diseases (en castelán). Ed. Médica Panamericana.
- ↑ Josep Maria Gatell Artigas, Josep Mensa Pueyo (2008). Guía terapéutica antimicrobiana, 2008. Elsevier España.
- ↑ "Lansoprazol, claritromicina y amoxicilina". medlineplus.gov (en castelán). Consultado o 26-01-2018.
- ↑ "Clasificación das antipseudomonas" (en castelán). Arquivado dende o orixinal o 27-07-2010. Consultado o 4-09-2010.
- ↑ Gustavo A. Quintero, Julio Alberto Nieto, Carlos H. Lerma (2001). Infección en cirugía (en castelán). Ed. Médica Panamericana. p. 87.
- ↑ MedlinePlus (2003). "Inxección de Ticarcilina disódica". Enciclopedia médica en español (en castelán). Consultado o 23 de setembro de 2008.
- ↑ "Venda de carbenicilina". Arquivado dende o orixinal o 16-10-2008. Consultado o 4-11-2008.
- ↑ Christian C. Patrick (2001). Clinical Management of Infections in Immunocompromised Infants and Children (en inglés). Lippincott, Williams & Wilkens.
- ↑ 109,0 109,1 109,2 A. C. Gómez García, C. Pérez Giraldo, M. T. Blanco Roca, F. J. Morán Domínguez e C. Hurtado Manzano. "Penicilinas" (PDF) (en castelán). Arquivado dende o orixinal (PDF) o 06-02-2009. Consultado o 26-01-2018.
- ↑ "Diferencias entre mecilinam e pivmecilinam". Arquivado dende o orixinal o 24-10-2010. Consultado o 9-10-2010.
- ↑ "Tema 2. Degradación Microbiológica y Conservación de los Productos Farmacéuticos.". Consultado o 26-01-2018.
- ↑ 112,0 112,1 La Pared bacteriana (en castelán). Arquivado dende o orixinal o 31 de xaneiro de 2018. Consultado o 26 de xaneiro de 2018.
- ↑ E. Gordon, N. Mouz, E. Duée and O. Dideberg (2 de xuño de 2000). "The crystal structure of the penicillin-binding protein 2x from Streptococcus pneumoniae and its acyl-enzyme form: implication in drug resistance". Journal of Molecular Biology (en inglés) 299 (2): 477–485. Consultado o 10 de setembro de 2010.
- ↑ Universidade de Granada, ed. (2006). "Síntesis péptidoglucano" (en castelán).
- ↑ 115,00 115,01 115,02 115,03 115,04 115,05 115,06 115,07 115,08 115,09 Harrison Principios de Medicina Interna (2006). "Patogenia de las reacciones a fármacos". Harrison online en español (en castelán) (16a ed.). McGraw-Hill. Arquivado dende o orixinal o 08 de febreiro de 2012. Consultado o 25 de setembro de 2010.
- ↑ E. Gutschik, O. B. Jepsen e Ida Mortensen (1977). "Effect of Combinations of Penicillin and Aminoglycosides on Streptococcus faecalis: A Comparative Study of Seven Aminoglycoside Antibiotics" (en inglés). Consultado o 02-02-2018.
- ↑ National Library of Science U.S. National Library of Medicine
- ↑ Sir Frank Macfarlane Burnet, David O. White (1972). Natural History of Infectious Disease (en inglés). CUP Archive. Consultado o 26-01-2018.
- ↑ Helena Curtis, Adriana Schnek (2008). Curtis. Biología (en castelán). Ed. Médica Panamericana. Consultado o 26-01-2018.
- ↑ Sociedad Española de Obstetricia y Ginecología, Sociedad Española de Neonatología, Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica, Sociedad Española de Quimioterapia y Sociedad Española de Medicina Familiar y Comunitaria (2003). "Prevención de la infección perinatal por estreptococo del grupo B" (PDF) (en castelán). Consultado o 26-01-2018.
- ↑ Medlineplus (2003). "Penicilina V potásica oral". Enciclopedia médica en castelán (en castelán). Consultado o 12 de setembro.
- ↑ MedlinePlus (xaneiro de 2003). "Inxección de Penicilina G potásica ou sódica". Enciclopedia médica en castelán (en castelán). Consultado o 11 de setembro de 2010.
- ↑ 123,0 123,1 The PDR Family Guide to Prescription Drugs. Escrito por Medical Economics Data (Firm). Publicado por Crown Trade Paperbacks, 1996. ISBN 0-609-80068-X
- ↑ William N. Kelley (1993). Medicina interna (en castelán). Ed. Médica Panamericana. p. 1065. Consultado o 26-01-2018.
- ↑ Hirvonen J, Pyörälä S, Heinäsuo A, Jousimies-Somer H. Penicillin G and penicillin G-tinidazole treatment of experimentally induced summer mastitis--effect on elimination rates of bacteria and outcome of the disease (en inglés). Vet Microbiol. 1994 Dec;42(4):307-15. PMID 9133056 Consultado o 12 de setembro de 2010
- ↑ Patient information sheet. Penicillin G (en inglés). Consultado o 12 de setembro de 2010
- ↑ ETS online. Tratamiento de la sífilis (en castelán). Arquivado dende o orixinal o 29-01-2018. Consultado o 28-01-2018.
- ↑ Francine Jacobs (1985). Breakthrough: The True Story of Penicillin (en inglés). Dodd, Mead. (require rexistro (?)).
- ↑ T. Häusler, Thomas Häusler (2016). Viruses Vs. Superbugs: A Solution to the Antibiotics Crisis? (en inglés). Springer.
- ↑ John C. Burnham (2015). Health Care in America: A History (en inglés). JHU Press.
- ↑ 131,0 131,1 Tradución libre do Sunday Times. Setembro 2008. Penicillin overuse puts Fleming's legacy at risk (artigo completo en inglés). Consultado o 12 de setembro de 2010.
- ↑ Javier Ramos Jiménez (2012). Infectología clínica (en castelán). Editorial El Manual Moderno.
- ↑ Joseph Price Remington (1965). Farmacia práctica de Remington: tratado de fabricación, normalización y despacho (en castelán). UTHEA.
- ↑ Carol T. Walsh, Rochelle D. Schwartz-Bloom (2004). Pharmacology: Drug Actions and Reactions (en inglés). CRC Press.
- ↑ Ficha de datos de seguridade (marzo, 2006). Penicillin G, Potassium Arquivado 06 de setembro de 2008 en Wayback Machine. (artigo completo dispoñible en inglés). Último acceso 12 de setembro de 2010.
- ↑ 136,0 136,1 Eric M. Scholar, William B. Pratt (2000). The Antimicrobial Drugs (en inglés). Oxford University Press.
- ↑ J. José Ramón Azanza, Emilio García, B. Belén Sádaba, Andrea Manubens (2009). "Uso de antimicrobianos en pacientes con insuficiencia renal o hepática" (en castelán). Consultado o 02-02-2018.
- ↑ Vicente Ausina Ruiz, Santiago Moreno Guillén (2006). Tratado SEIMC de enfermedades infecciosas y microbiología clínica (en castelán). Ed. Médica Panamericana.
- ↑ Vidal Group (2015). "Mecanismo de acción Probenecid" (en castelán). Consultado o 02-02-2018.
- ↑ Gerald L. Mandell (1993). Principles and Practice of Infectious Diseases (en inglés). Elsevier Health Sciences.
- ↑ J.F. Maher (1989). Replacement of Renal Function by Dialysis: A Textbook of Dialysis (en inglés). Springer Science & Business Media.
- ↑ 142,0 142,1 "THE FACTS ABOUT PENICILLIN ALLERGY: A REVIEW" (en inglés). Consultado o 09-02-2018.
- ↑ Salkind AR, Cuddy PG, Foxworth JW (2001). "JAMA Is this patient allergic to penicillin? An evidence-based analysis of the likelihood of penicillin allergy". pp. 2498–2505. PMID 11368703. doi:10.1001/jama.285.19.2498.
- ↑ Richard A. Lehne, Laura Rosenthal (2014). Pharmacology for Nursing Care - E-Book (en inglés). Elsevier Health Sciences.
- ↑ 145,0 145,1 RS Satoskar, Nirmala Rege, SD Bhandarkar (2015). Pharmacology and Pharmacotherapeutics - E-Book (en inglés). Elsevier Health Sciences.
- ↑ Faustina Rubio Campal, Benjamín García Espinosa, Manuel Carrasco Carrasco (2004). Fundamentos y técnicas de análisis hematológicos y citológicos (en castelán). Editorial Paraninfo. Consultado o 09-02-2018.
- ↑ Clínica Mayo. "Alergia a la penicilina" (en castelán). Consultado o 09-02-2018.
- ↑ 148,0 148,1 Harold M. Silverman. The Pill Book (12th Edition). Publicado por Bantam. ISBN 0-553-58892-3.
- ↑ Dash CH (1975). J. Antimicrob. Chemother., ed. Penicillin allergy and the cephalosporins 1. pp. 107/18. PMID 1201975.
- ↑ Gruchalla RS, Pirmohamed M (2006). N. Engl. J. Med., ed. Clinical practice. Antibiotic allergy 354. pp. 601/9. PMID 16467547. doi:10.1056/NEJMcp043986.
- ↑ Pichichero ME (2006). The Journal of family practice, ed. "Cephalosporins can be prescribed safely for penicillin-allergic patients" (PDF). pp. 106/12. PMID 16451776. Arquivado dende o orixinal (PDF) o 18 de outubro de 2006. Consultado o 19 de setembro de 2010.
- ↑ Pichichero ME (2007). Diagn. Microbiol. Infect. Dis., ed. Use of selected cephalosporins in penicillin-allergic patients: a paradigm shift 57. pp. 13S/18S. PMID 17349459. doi:10.1016/j.diagmicrobio.2006.12.004.
- ↑ Antunez C, Branca-Lopez N, Torres MJ; et al. (2006). J. Allergy Clin. Immunol., ed. Immediate allergic reactions to cephalosporins: evaluation of cros-reactivity with a panel of penicillins and cephalosporins 117. pp. 404/10. PMID 16461141. doi:10.1016/j.jaci.2005.10.032.
- ↑ "La alergia a la penicilina es más frecuente en mujeres - Noticias médicas - IntraMed". www.intramed.net (en castelán). Consultado o 29 de marzo de 2019.
- ↑ Park, Miguel A.; Matesic, Damir; Markus, Patricia J.; Li, James T.-C. (2007-7). "Female sex as a risk factor for penicillin allergy". Annals of Allergy, Asthma & Immunology (en inglés) 99 (1): 54–58. doi:10.1016/S1081-1206(10)60621-7.
- ↑ Drugs.com Interactions between penicillin and Erythromycin, Interactions between penicillin and Tetracycline Interactions between penicillin and Chloramphenicol
- ↑ Calvo A, Amores R, Valero E, Fontes F, Gómez-Lus ML, Prieto J; (16 de decembro de 2003). Working Group for the Study of Cefpodoxime., ed. "Activity of oral antibiotics against respiratory tract pathogens in Spain.". Rev Esp Quimioter. 16(4): 436–43.
Citado 25 de setembro de 2010.
- ↑ CONTRERAS M, Lily, FICA C, Alberto, FIGUEROA C, Oscar et al. Resistencia de Streptococcus pneumoniæ a penicilina e a súa asociación con factores clínicos e epidemiolóxicos: Clinical and epidemiological aspects. Rev. méd. Chile. [online]. ene. 2002, vol.130, num.1 [citado o 08 de novembro de 2008], p.26-34. ISSN 0034-9887.
- ↑ Bardi, Leticia; Badolati, Adelina; Corso, Alejandra; Rossi, M. Alicia.Fracaso del tratamiento con penicilina en un caso de meningitis por Neisseria meningiditis (en español). Medicamento (B.Aires);54(5,pt.1):427-30, sept.-oct. 1994. Citado 8 de novembro, 2008.
- ↑ María Espino, María J. Couto, Mario Le, Natasha Páez e Elisa Meriño.Efecto sinérgico de penicilina G e Kanamicina en septicemia neonatal por estafilococo Arquivado 31 de xaneiro de 2012 en Wayback Machine. (en español). Rev Cubana Pediatr 1998; 67(3). Último acceso 7 de novembro, 2008.
- ↑ Gemmell CG, Edwards DEI, Fraise AP et al. (2006). "Guidelines for the prophylaxis and treatment of methicillin-resistant Staphylococcus aureus (MRSA) infections in the UK". J Antimicrob Chemother (57): 589–608.
- ↑ James, P. A., and D. S. Reeves. 1996. Bacterial resistance to cephalosporins as a function of outer membrane permeability and access to their target. J. Chemother. 8(Suppl. 2):37-47
- ↑ James, P. A.; Lewis, D. A.; Jordens, J. Z.; Cribb, J.; Dawson, S. J.; Murray, S. A. (1996). "The incidence and epidemiology of β-lactam resistance in Haemophilus influenzae". Journal of Antimicrobial Chemotherapy (en inglés) 37 (4): 737–746. ISSN 0305-7453. doi:10.1093/jac/37.4.737.
- ↑ GEHLREIN M. ; LEYING H. ; CULLMANN W. ; WENDT S. ; OPFERKUCH W. Imipenem resistance in Acinetobacter baumanii is due to altered penicillin-binding proteins Chemotherapy. 1991, vol. 37, no6, pp. 405-412.
- ↑ TIBAVIZCO, Diego, RODRIGUEZ, José Yesid, SILVA, Edwin et al. Enfoque terapéutico da bacteriemia por Staphylococcus aureus. Biomédica. [online]. Abril/Xuño 2007, vol.27, num.2 [citado 22 de decembro de 2008], p.294-307. ISSN 0120-4157.
- ↑ MC Pírez García e col. Pneumonía neumocócica invasiva en niños de 0 a 24 meses: influye la resistencia bacteriana en la evolución? Arquivado 10 de outubro de 2007 en Wayback Machine. (artigo completo dispoñible en español). Anais de Pediatría. Setembro 2008; Volume 69 - Número 03 p. 205 - 209. PMID 18775263. Último acceso 18 de setembro, 2008.
- ↑ Maninder K. Sohi, Dennis A. Veselkov, Ivan Laponogov, Xiao-Su Pan, L. Mark Fisher e Mark R. Sanderson. The Difficult Case of Crystallization and Structure Solution for the ParC55 Breakage-Reunion Domain of Topoisomerase IV from Streptococcus pneumoniae (artigo completo dispoñible en inglés). PLoS ONE. setembro 2008; 3(9): e3201. PMCID: PMC2527675. Último acceso 18 de setembro, 2008.
- ↑ Parascandola John (1980). "The History of Antibiotics: a Symposium". Publication Non 5.
- ↑ Allen I. Laskin, Geoffrey M. Gadd, Sima Sariaslani (2008) Advances in Applied Microbiology Academic Press. ISBN 0-444-53191-2, 9780444531919 (en inglés)
- ↑ Shu-Jen Chiang (2004). Strain improvement for fermentation and biocatalysis processes by genetic engineering technology Arquivado 13 de setembro de 2019 en Wayback Machine. Journal of Industrial Microbiology and Biotechnology. DOI 10.1007/s10295-004-0131-z (en inglés)
- ↑ S. C. Warren, G. G. F. Newton, and E. P. Abraham (1967). Use of α-aminoadipic acid for the biosynthesis of penicillin N and cephalosporin C by a Cephalosporium sp Biochem J. 103(3): 891-901.
Véxase tamén[editar | editar a fonte]
| Wikimedia Commons ten máis contidos multimedia na categoría: Penicilina |
Bibliografía[editar | editar a fonte]
- Bud, Robert (2007). Penicillin: Triumph and Tragedy (en inglés). Oxford University Press. ISBN 0-19-925406-0. Consultado o 5 de novembro do 2017.
- de la Bedoyere, Guy (2005). The Discovery of Penicillin (en inglés). Evans Brothers. ISBN 0-237-52739-1.
- Nicolaou, K.C.; Corey, E. J. (1996). Classics in Total Synthesis : Targets, Strategies, Methods (5. repr. ed.). Weinheim: VCH ISBN 3-527-29284-5
- Williams T. I. (1948). De l'opium à la pénicilline. Les plantes qui guérissent (traduit de l'anglais par Jean Le Pas). París: ed. Eyrolles. Collection Pointes de la science, no 4.
- Fromols J. (1947). Pénicilline. Précis de posologie américaine, Lille: Yves Demailly (en francés).
Outros artigos[editar | editar a fonte]
- Antibiótico
- Antibiótico beta-lactámico
- Patoxenicidade bacteriana
- Quimioterapia antimicrobiana
- Resistencia a antibióticos
Ligazóns externas[editar | editar a fonte]
- Historia «oficial» da penicilina (en francés)
- A penicilina I. Descubrimento dun antibiótico (en francés)
- Penicilina en The Periodic Table of Videos (Universidade de Nottingham)
- The Discovery of Penicillin, A government produced film about the discovery of Penicillin by Sir Alexander Fleming, and the continuing development of its use as an antibiotic by Howard Florey and Ernst Boris Chain no YouTube.

