Valina
| Valina | |
|---|---|

|

|
Valina | |
Outros nomes Ácido 2-amino-3-metilbutanoico | |
| Identificadores | |
| Número CAS | 516-06-3, 72-18-4 (isómero L), 640-68-6 (isómero D) |
| PubChem | 1182 |
| ChemSpider | 6050 |
| UNII | 4CA13A832H |
| Número CE | 208-220-0 |
| DrugBank | DB00161 |
| KEGG | D00039 |
| ChEBI | CHEBI:57762 |
| ChEMBL | CHEMBL43068 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades[2] | |
| Fórmula molecular | C5H11NO2 |
| Masa molar | 117,15 g mol−1 |
| Densidade | 1,316 g/cm3 |
| Punto de fusión | 298 °C (descomposición) |
| Solubilidade en auga | soluble |
| Acidez (pKa) | 2,32 (carboxilo), 9,62 (amino)[1] |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
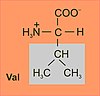
A valina (abreviadamente Val ou V)[3] é un α-aminoácido coa fórmula HO2CCH(NH2)CH(CH3)2. A L-valina é un dos 20 aminoácidos que forman parte das proteínas. Pola súa cadea lateral alifática clasifícase como aminoácido hidrófobo ou non polar. Xunto coa leucina e isoleucina, a valina é un aminoácido coa cadea lateral ramificada. Os seus codóns son GUU, GUC, GUA, e GUG. É un aminoácido esencial, xa que o noso metabolismo non o pode sintetizar e debemos tomalo na dieta.
O seu nome vénlle da planta valeriana (Valeriana officinalis).
Biosíntese[editar | editar a fonte]
Como a valina é un aminoácido esencial os alimentos da nosa dieta deben incluíla, normalmente como compoñente das súas proteínas. Abunda no queixo fresco, peixe, aves, cacahuetes, sementes de sésamo, e lentellas. As plantas poden sintetizala en varios pasos a partir do ácido pirúvico. A parte inicial desta vía metabólica tamén serve para producir leucina. O intermediato α-cetoisovalerato sofre unha aminación redutiva con glutamato. Entre os encimas implicados nesta biosíntese están:[4]
- Acetolactato sintase (tamén coñecido por acetohidroxiácido sintase).
- Acetohidroxiácido isomerorredutase.
- Dihidroxiácido deshidratase.
- Valina aminotransferase.
Síntese[editar | editar a fonte]
A valina racémica pode sintetizarse por brominación do ácido isovalérico seguida de aminación do α-bromo derivado[5]
- HO2CCH2CH(CH3)2 + Br2 → HO2CCHBrCH(CH3)2 + HBr
- HO2CCHBrCH(CH3)2 + 2 NH3 → HO2CCH(NH2)CH(CH3)2 + NH4Br
Degradación[editar | editar a fonte]
Na degradación oxidativa da valina orixínase succinil-CoA, polo que é un aminoácido glicoxénico.
Notas[editar | editar a fonte]
- ↑ Dawson, R.M.C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ Weast, Robert C., ed. (1981). CRC Handbook of Chemistry and Physics (62nd ed.). Boca Raton, FL: CRC Press. p. C-569. ISBN 0-8493-0462-8.
- ↑ IUPAC-IUB. Nomenclature and symbolism for amino acids and peptides (Recommendations 1983) [1].
- ↑ Lehninger (2000). Principles of Biochemistry (en inglés) (3ª ed.). ISBN 978-1572599314.
- ↑ Marvel C. S. (1940). "dl-Valine" 20: 106..
