Fibrose quística
Este artigo contén varias ligazóns externas e/ou bibliografía ao fin da páxina, mais poucas ou ningunha referencia no corpo do texto. Por favor, mellora o artigo introducindo notas ao pé, citando as fontes. Podes ver exemplos de como se fai nestes artigos. |
Este artigo ou sección precisa dunha revisión do formato que siga o libro de estilo da Galipedia. Mellore este artigo: sección véxase tamén - bibliografía, WP:LE#Intemporalidade da información Pode axudar a mellorar este artigo e outros en condicións semellantes. |

A fibrose quística[1][2][3], é unha das enfermidades xenéticas máis frecuentes na raza caucasiana cunha incidencia na poboación española, segundo recentes estudos de cribado neonatal, de aproximadamente 1/5.000 nados vivos. Ao presentar unha herdanza autosómica recesiva, calcúlase que un 4-5% da poboación xeral son portadores desta entidade na raza branca. É esta unha enfermidade das glándulas exócrinas que afecta a múltiples órganos e sistemas, debido á existencia de alteracións hidroelectrolíticas e das mucoproteínas a nivel glandular, orixinándose secrecións anómalas e espesas que producen obstrución e infección coas consecuentes manifestacións clínicas. A principal causa de morbilidade e mortalidade continúa sendo a afectación pulmonar, causante dun 95% dos falecementos.[4] Esta enfermidade foi orixinalmente denominada fibrose quística do páncreas, e tamén coñecida como mucoviscidose (do lat. muccus, 'moco', e viscos, 'pegañento'), é unha enfermidade frecuente que afecta o organismo en forma xeneralizada, causando morte prematura. A dificultade para respirar é o síntoma máis común, emerxente de infeccións pulmonares crónicas, as cales poden mostrarse resistentes ao tratamento con antibióticos e outros fármacos. A fibrose quística é un trastorno multisistémico que causa a formación e acumulación dun moco espeso e pegañento, afectando fundamentalmente a pulmóns, intestinos, páncreas e fígado. Así mesmo, caracterízase pola presenza dunha alta concentración de sal (NaCl) na suor, o que sentou as bases da proba estándar para este diagnóstico: o exame de electrólitos da suor. O mesmo avalía, entre outros ións, os niveis de cloruro excretados. Unha variedade de síntomas, incluíndo infeccións sinusais, diminución do crecemento, diarrea son o resultado dos efectos da fibrose quística sobre os distintos órganos.
Trátase dunha das enfermidades fatais máis comúns. A súa prevalencia é maior entre caucásicos; unha de cada 25 persoas de ascendencia europea é portadora asintomática dun xene para fibrose quística, sendo a enfermidade xenética heredable máis frecuente entre esta poboación. E aproximadamente unha de cada 25 persoas é portador san heterocigoto. Os afectados poden ser diagnosticados mediante probas xenéticas prenatais; tamén por screening neonatal ou, durante a infancia temperá, pola mencionada proba da suor. Non existe cura para a fibrose quística, con todo, hoxe en día existen tratamentos nos que se pode ter unha vida completamente normal alargando a mesma un 25%. A supervivencia media para estes pacientes estímase en 35 anos, alcanzando valores máis altos nalgúns países (57,8 en EE.UU.).[5][6] En casos severos, o empeoramento da enfermidade pode impor a necesidade dun transplante de pulmón.
A fibrose quística é causada por unha mutación nun xene chamado regulador da condutancia transmembrana da fibrose quística (CFTR, polas súas siglas en inglés). Este xene intervén na produción de suor, mollos gástricos e moco. Aínda que a maioría das persoas sas teñen dúas copias funcionais do xene, só unha é necesaria para impedir o desenvolvemento de fibrose quística. A fibrose quística desenvólvese cando ningún destes xenes opera normalmente. En consecuencia, considérase unha enfermidade autosómica recesiva. O nome fibrose quística refírese aos procesos característicos de cicatriz e formación de quistes dentro do páncreas, recoñecidos por primeira vez nos anos 1930.[7]
Síntomas e signos[editar | editar a fonte]
A sintomatoloxía da fibrose quística varía en función da idade do individuo, o grao en que ven afectados órganos específicos, a terapéutica instituída previamente, e os tipos de infeccións asociadas. Esta enfermidade compromete ao organismo na súa totalidade e amosa o seu impacto sobre o crecemento, a función respiratoria, a dixestión. O período neonatal caracterízase por un pobre aumento de peso e por obstrución intestinal producida por feces densas e voluminosas. Outros síntomas aparecen, máis tarde, durante a nenez e ao comezo da idade adulta. Estes inclúen retardo do crecemento, advenimiento da enfermidade pulmonar, e dificultades crecentes pola mala absorción de vitaminas e nutrientes no tracto gastrointestinal.
Á maioría dos nenos diagnostícaselles fibrose quística antes do primeiro ano de vida, cando a mucosidade pegañenta que afecta pulmóns e páncreas, comeza a mostrar o seu impacto. No tracto respiratorio, esas secrecións serven como caldo de cultivo para diversas bacterias responsables de infeccións crónicas, con deterioración progresiva e permanente do parénquima pulmonar. Conforme se agrava a condición respiratoria, os pacientes sofren hipertensión pulmonar. Por outra banda, no páncreas, o moco obstrúe o tránsito das encimas sintetizadas pola glándula e impide que cheguen até os intestinos para dixerir e absorber o alimento.
Enfermidade pulmonar e sinusal[editar | editar a fonte]

A enfermidade pulmonar resulta do bloqueo das vías aéreas máis pequenas co moco espeso característico da fibrose quística. A inflamación e a infección producen dano aos pulmóns e cambios estruturais que conducen a unha variedade de síntomas. Nas etapas iniciais, comunmente preséntanse tose incesante, produción copiosa de flegma, e unha diminución na capacidade aeróbica. Moitos destes síntomas ocorren cando certas bacterias (fundamentalmente, Pseudomonas aeruginosa) que normalmente viven no moco espeso, medran de xeito descontrolado e causan pneumonía. En estados avanzados da fibrose quística, os cambios na arquitectura do pulmón producen dificultades respiratorias crónicas.
Outros síntomas inclúen expectoración de sangue ou esputo sanguinolento, dilatación crónica dos bronquios ou bronquíolos (bronquiectasia), elevación da presión sanguínea no pulmón, insuficiencia cardíaca, sensación de non estar a recibir suficiente osíxeno ou dispnea, insuficiencia respiratoria e atelectasia; podería requirirse soporte ventilatorio.[8] Ademais das infeccións bacterianas máis comúns, as persoas con fibrose quística desenvolven con maior facilidade outros tipos de enfermidades respiratorias. Entre estas atópase a aspergilose broncopulmonar alérxica, caracterizada por unha resposta de hipersensibilidade ante un fungo ordinario do xénero Aspergillus (Aspergillus fumigatus), que agudiza os problemas respiratorios. Outro exemplo é a infección co complexo Mycobacterium avium (MAC), grupo de actinobacterias emparentadas con Mycobacterium tuberculose, que pode ocasionar danos maiores ao pulmón, e que non responde á terapéutica con antibióticos convencionais.
O moco nos seos paranasais é igualmente denso e pegañento, e tamén pode causar oclusión dos orificios por onde os seos habitualmente drenan, o cal fai que se acumulen secrecións que actúan como caldo de cultivo para os patóxenos antes mencionados. Nestes casos, pódense presentar dor facial, febre, secreción nasal profusa e cefaleas. Nas persoas con fibrose quística, a miúdo obsérvase crecemento sobreabundante de tecido nasal (pólipos), a consecuencia da inflamación por infección sinusal crónica. Estes pólipos poden agravar a obstrución das vías respiratorias superiores e intensificar as dificultades respiratorias.[9][10]
Enfermidade gastrointestinal, hepática e pancreática[editar | editar a fonte]
Con anterioridade á difusión das probas prenatal e neonatal para fibrose quística, era frecuente que a enfermidade se detectase ao constatar que o recentemente nacido non podía expulsar as súas primeiras feces (meconio). O meconio pode obstruír completamente os intestinos e causar graves trastornos. Esta condición, chamada íleo meconial, ocorre no 10% dos recentemente nacidos con fibrose quística.[11] Así mesmo, é tamén frecuente a asociación de fibrose quística con protrusión das membranas rectais internas (prolapso rectal), debida ao maior volume fecal, á malnutrición, e á elevación da presión intraabdominal por tose crónica.[12]
O moco glutinoso observado no pulmón ten o seu correlato nas secrecións espesas do páncreas, órgano responsable de prover mollos dixestivos que facilitan a descomposición química dos alimentos. Estas secrecións impiden o movemento das encimas pancreáticas cara ao intestino e producen dano irreversible no páncreas, a miúdo acompañado de dolorosa inflamación (pancreatitis).[13] A deficiencia de encimas dixestivas tradúcese nun impedimento para absorber os nutrientes, coa subseguinte excreción destes nas feces: este trastorno é coñecido como malabsorción. A malabsorción conduce á desnutrición e ao retardo no crecemento e desenvolvemento, ambos os debidos á baixa biodispoñibilidade calórica. As persoas con fibrose quística teñen, en particular, problemas para absorber as vitaminas A, D, E, e K. Ademais da afección pancreática, adoitan experimentar acidez crónica, xerostomía, obstrución intestinal por intususcepción, e estrinximento.[14] Os pacientes maiores desenvolven tamén a síndrome de obstrución intestinal distal causado polas feces glutinosas.[15]
Estas secrecións tamén poden causar problemas no fígado. A bile, producida por esta víscera para facilitar a dixestión, podería bloquear as vías biliares, danando os tecidos adxacentes. Co tempo, esta situación conduce á cirrose. Nese caso, resultan comprometidas funcións de primeira orde, tales como as implicadas na neutralización de toxinas, e na síntese de importantes proteínas (por exemplo, os factores de coagulación, responsables da coagulación sanguínea).[16]
Enfermidade endócrina e crecemento[editar | editar a fonte]
O páncreas contén os illotes de Langerhans, que son os responsables de producir insulina, unha hormona que axuda a regular os niveis de glicosa en sangue. Un dano no páncreas pode provocar a perda das células dos illotes e conducir á diabetes.[17] Por outra banda, a vitamina D suplementada pola alimentación está implicada na regulación do calcio e do fósforo. A baixa dispoñibilidade desta, por mor da malabsorción, conduce á osteoporose, aumentando o risco de sufrir fracturas.[18] Adicionalmente, as persoas con fibrose quística a miúdo presentan, en mans e pés, unha malformación denominada dedos en escarvadentes de tambor, a cal se debe aos efectos desta enfermidade crónica e á hipoxia nos seus ósos.
O retardo no crecemento é un selo distintivo desta enfermidade. Os nenos con fibrose quística non logran, polo xeral, gañar peso e altura en taxas comparables ás dos seus pares; a miúdo, só reciben diagnóstico apropiado unha vez que se investigan as causas deste fenómeno. Os determinantes do retardo no crecemento son multifactoriais e inclúen a infección pulmonar crónica, a malabsorción de nutrientes no tracto gastrointestinal, e o aumento da demanda metabólica asociado á afección crónica.
A fibrose quística pode diagnosticarse por exame de electrólitos da suor, ou proba xenética. Ao ano 2006, nos Estados Unidos, o dez por cento dos casos son detectados pouco despois do nacemento como parte dos programas de pescuda neonatal, que identifican niveis elevados na encima tripsina. Con todo, na maioría dos países estes exames non se realizan de xeito rutineiro. Por esta causa, é frecuente que os afectados só reciban diagnóstico apropiado unha vez que os síntomas forzan unha avaliación para esta enfermidade. A proba diagnóstica máis comunmente utilizada é o exame da suor, descrito por Lewis E. Gibson e Robert E. Cooke en 1959,[19] usando electroforese cuantitativa (iontoforese) cun fármaco estimulante da suoración (pilocarpina). Esta substancia, que posúe carga positiva, aplícase sobre un eléctrodo positivo (+), en contacto coa pel. Logo, mediante o paso de corrente eléctrica, a droga migra polo tegumento cara a outro eléctrodo de carga oposta (-), colocado a certa distancia, até atravesar a epiderme, producindo a estimulación das glándulas suoríparas e causando unha suoración controlada. As mostras de suor son logo colleitadas en papel de filtro ou nun tubo capilar e son analizadas, determinándose as concentracións de sodio e cloruro. As persoas con fibrose quística posúen niveis máis altos destes ións na suor. Unha vez que o exame da suor deu positivo, realízase un diagnóstico máis detallado e preciso, mediante a identificación das mutacións no xene CFTR.[20]
Existen diversas probas para identificar eventuais complicacións e controlar a evolución da enfermidade. As imaxes obtidas por raios X e TAC facilitan a detección de signos de lesión ou infección nos pulmóns. O cultivo de esputo, examinado por microscopio, prové información respecto de cales son as bacterias responsables, e permite escoller os antibióticos máis efectivos. As probas de función pulmonar miden as capacidades pulmonares, os volumes pulmonares e a rapidez con que estes poden ser mobilizados (fluxos aéreos). Por medio de tales exames, é posible determinar se é procedente un tratamento con antibióticos ou ben avaliar a resposta ao mesmo. Os análise de sangue poden identificar problemas hepáticos, deficiencias vitamínicas, e revelar a irrupción da diabetes. Os dispositivos DEXA ou DXA (do inglés para "absorciometría de raios X de enerxía dual"), utilízanse como proba para determinar a presenza de osteoporose. Por último, a cuantificación de elastase fecal, facilita a detección de insuficiencia de encimas dixestivas.
Fisiopatoloxía[editar | editar a fonte]
A proteína sintetizada a partir do xene CFTR únese á membrana externa das células nas glándulas suoríparas, pulmón, páncreas, e outros órganos afectados. A proteína atravesa esta membrana e actúa como unha canle iónico conectando a parte interna da célula (citoplasma) co fluído extracelular. Esta canle é maiormente responsable de controlar o paso de cloruro cara a (e desde) o medio interno. Cando a proteína CFTR non funciona correctamente, este movemento vese restrinxido, reténdose cloruro no espazo extracelular. Debido a que o cloruro ten carga eléctrica negativa, os ións con carga positiva tampouco poderán cruzar a membrana citoplasmática, por mor da atracción eléctrostática exercida polos ións cloruro. O sodio é o máis común entre os ións presentes fóra da célula, e a combinación de sodio e cloruro dá lugar ao cloruro de sodio, o cal se perde en grandes cantidades na suor dos individuos con fibrose quística. Esta perda de sal constitúe o argumento básico para explicar a eficacia do test da suor.[8]
O mecanismo polo cal esta disfunción celular produce as manifestacións clínicas antes descritas non se coñece con exactitude. Unha das teorías que tenta explicalo, suxire que a falla da proteína CFTR para transportar o cloruro, determina a acumulación de abundante moco nos pulmóns, creando un medio propicio (rico en nutrientes) para as bacterias, que logran así eludir ao sistema inmunitario. Tamén se postula que esta anomalía na proteína CFTR induce un aumento paradoxal na captura de sodio e cloruro, o que estimula a reabsorción de auga, e resulta na formación da mucosidade deshidratada e espesa. Outras teorías enfócanse no fenómeno do movemento de cloruro cara ao exterior da célula, que tamén provoca desecamento do moco e das secrecións pancreáticas e biliares. En xeral, estas hipóteses coinciden en atribuír os maiores trastornos á obstrución dos condutos máis delgados polas secrecións espesas e glutinosas nos distintos órganos afectados. Esta situación condiciona a infección crónica e promove a remodelación estrutural do pulmón, ademais de producir dano pancreático (mediado polas encimas dixestivas aglomeradas), e obstrución dos intestinos por grandes birlos fecais.[8]
O papel da infección crónica na enfermidade pulmonar[editar | editar a fonte]

Os pulmóns das persoas con fibrose quística son colonizados e infectados por bacterias desde idades temperás. Os microorganismos que se propagan nestes pacientes, prosperan no moco anómalo acumulado nas vías respiratorias máis estreitas. O moco glutinoso estimula o desenvolvemento de microambientes bacterianos (biofilms) que resultan difíciles de penetrar para as células inmunes e os antibióticos. Pola súa banda, os pulmóns responden o dano continuo, infrinxido polas secrecións espesas e as infeccións crónicas, remodelando gradualmente as vías respiratorias inferiores (bronquiectasia), o que volve á infección aínda máis difícil de erradicar.[21]
Co paso do tempo, cambian tanto o tipo de bacterias que afectan a estes pacientes, como as características específicas con que as mesmas preséntanse. Nunha primeira etapa, certas bacterias ordinarias como Staphylococcus aureus e Haemophilus influenzae colonizan e infectan os pulmóns. Máis tarde, con todo, prevalecen Pseudomonas aeruginosa (e, ás veces, o complexo Burkholderia cepacia, integrado por diferentes especies de Burkholderia). Unha vez diseminadas polas vías respiratorias, estas bacterias adáptanse ao medio e desenvolven resistencia aos antibióticos convencionais. Pseudomonas pode adquirir certas características especiais, dando lugar á formación de grandes colonias - estas cepas son coñecidas como Pseudomonas "mucoide" e son raras en persoas libres da enfermidade.[21]
Un dos modos en que a infección se propaga é por transmisión entre individuos con fibrose quística.[22] No pasado, era habitual que estes participasen, en forma conxunta, de campamentos estivais e outras actividades de esparexemento.[23][24] Os hospitais aloxaban aos pacientes con fibrose quística nunha área en común, e o equipamento de rigor (por exemplo, os nebulizadores)[25] non era esterilizado entre usos sucesivos.[26] Isto conduciu á transmisión de cepas bacterianas moi perigosas entre grupos de pacientes. Actualmente, a rutina en establecementos de atención sanitaria consiste en illar a estes pacientes uns doutros; ademais, o persoal a cargo do seu coidado, debe vestir batas e luvas para limitar a proliferación de cepas bacterianas virulentas.[27] Con frecuencia, os pacientes afectados por bacterias particularmente perigosas reciben atención en días e en edificios diferentes aos asignados a quen non teñen esas infeccións. Ademais da infección bacteriana, os pacientes con fibrose quística están predispostos á colonización por fungos pola capacidade que teñen algúns colonizar a vía respiratoria inferior e polos frecuentes ciclos de antibióticos que precisan para o control da enfermidade.[28] Os fungos que se cultivan con máis frecuencia son o Aspergillus fumigatus e a Candida albicans, esta colonización tradúcese nunha taxa elevada de resposta inflamatoria fronte aos fungos.[29] Na actualidade non está ben definido o papel dos fungos na fibrose quística, aínda que se consideran que son non patóxenos, excepto nos casos de asperxilose invasiva e de asperxilose broncopulmonar alérxica.
Xenética[editar | editar a fonte]

Trátase dunha enfermidade autosómica recesiva. Na súa forma máis común, unha mutación dun aminoácido (falta unha fenilalanina na posición 508) conduce a un fallo do transporte celular e localización na membrana celular da proteína CFTR. Describíronse máis de 1.800 mutacións,[30] sendo a maioría delas pequenas delecións, aínda que con diferentes efectos, como cambios no marco de lectura, cambios de aminoácidos, terminación prematura da proteína ou alteracións no splicing.
O xene CFTR está localizado no brazo longo do cromosoma 7, na posición 7q31.2, ocupando 180.000 pares de bases: máis precisamente, desde o par 116.907.252 ao 117.095.950 do cromosoma. É un xene de gran tamaño, que posúe 250 kb e que inclúe 27 exóns. Foi localizado e secuenciado por mapeo xenético.
Este xene codifica a síntese dun canle iónico de 1480 aminoácidos, unha proteína que transporta ións cloruro a través das células epiteliais, e que controla a regulación doutros transportadores. Nas persoas con fibrose quística, esta proteína está ausente ou ben se atopa en proporcións sensiblemente menores ás habituais.
A penetranza da enfermidade é variable segundo o alelo, e á súa vez, a expresión do alelo depende da contorna e do xenoma da persoa afectada.
Bioloxía molecular[editar | editar a fonte]
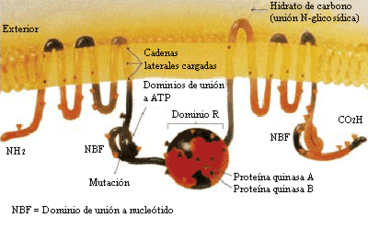
Son diversos os mecanismos polos cales estas mutacións causan problemas na proteína CFTR. En particular, a mutación ΔF508, xera unha proteína que acaba sendo degradada pola célula. Varias mutacións comúns na poboación asquenací dan lugar á síntese de proteínas demasiado curtas, por mor dunha conclusión anticipada da súa produción. Outras mutacións menos frecuentes orixinan proteínas que non utilizan a enerxía como cómpre, non permiten que o cloruro pase a membrana apropiadamente, ou son degradadas a unha taxa máis rápida que a normal. Certas mutacións poden conducir tamén a unha diminución na produción de copias da proteína CFTR.[8]
Estruturalmente, o xene CFTR pertence á denominada superfamilia de transportadores ABC (acrónimo para o inglés ATP Binding casete, "casete de unión a ATP").[8] A estrutura terciaria da proteína codificada por este xene, consta de dous dominios capaces de hidrolizar adenosín trifosfato, o que permite á proteína utilizar enerxía na forma de ATP. Así mesmo, outro par de dominios, cada un constituído por seis hélices alfa, posibilita o paso da proteína a través da membrana celular. A activación concrétase por reacción de fosforilación nun sitio de unión regulador, sobre todo mediante a proteína quinase A (PKA, Modelo:EC número antes denominada cAPK ou proteína quinase dependente do adenosín monofosfato cíclico).[8] O carboxilo terminal (C-) da proteína está unido ao citoesqueleto por interacción con dominios proteicos PDZ.[31]
Diagnóstico[editar | editar a fonte]
Diagnóstico tradicional (métodos non moleculares)[editar | editar a fonte]
Existen unha serie de probas que veñen realizando de forma común para determinar as anomalías dos metabolitos relacionados coa fibrose quística (especialmente o cloro). Entre elas atópanse:
- Proba de electrólitos na suor: adminístrase pilocarpina para estimular a suor e mídese cun eléctrodo a concentración de sales. Esta técnica era a máis usada antigamente, pero actualmetne caeu en desuso porque dá lugar a moitos falsos negativos
- Proba da diferenza de potencial eléctrico nasal.
- Proba do tripsinógeno inmunoreactivo: é unha proba que se realiza sobre o sangue e que mide a concentración dunha encima pancreática.
Diagnóstico molecular[editar | editar a fonte]
O diagnóstico molecular da enfermidade é complexo, xa que en novembro de 2010 atopámonos con 1824 mutacións descritas.[30] Estas mutacións agrúpanse en función do efecto que teñen sobre o xene e sobre o fenotipo da enfermidade. Ademais da variabilidade das mutacións en si mesmas, as distintas poboacións teñen frecuencias diferentes para as mesmas, polo que os estudos e test diagnósticos deben xestionarse considerando este aspecto. No entanto, a máis común na maioría das poboacións é a deleción 508 F.
Actualmente aos nenos nada máis nacer fáiselles un diagnóstico xenético mediante secuenciación do xene CFTR para saber se teñen a enfermidade, xa que é unha enfermidade tratable. Cando antes comeza o tratamento, maior calidade de vida e maior lonxevidade.
- Diagnóstico molecular indirecto: basicamente realizado a través de análise de ligamento. leva a cabo emediante:
- RFLP: método antigo baseado en restrición actualmente en desuso.
- Marcadores microsatélites: é o método seguido actualmente. Os estudos só son válidos dentro do mesma árbore familiar.
- Macadores SNP: serán os usados nun futuro próximo, pois teñen a vantaxe de que os resultados obtidos son aplicables entre persoas non emparentadas.
- Diagnóstico molecular directo: poderiamos secuenciar o xene CFTR, pero o que está á orde do día é a detección das mutacións, que basicamente se realiza a partir de dúas estratexias:
- Rastrexo de mutacións: técnicas de detección de mutacións, pero sen identificación da mutación. Algunhas das máis usadas neste proceso son a electroforese en xel con gradiente de desnaturalización, así como algunhas variantes de PCR
- Identificación de mutacións: técnicas baseadas en hibridación específica co alelo mutado. Por exemplo, os kits ASO:dot blot, ONDA (ensaio de ligazón de oligonucleótidos), ou o ensaio máis tradicional de Southern blot.
- ASO: dot blot: é utilizado para a detección de mutacións definidas coñecidas previamente. Readquire a amplificación do ADN a estudar. Porteriormente fíxase a unha membrana (sen tratamento nin electroforese previos). Entón hibrídase con oligonucleótidos específicos do alelo duns 20 pares de bases que se atopan marcados para a súa posterior detección. Trátase dunha técnica sinxela, barata, rápida e segura se se estuda (como no caso da fibrose quística) un único xene con poucas mutacións. Aínda que resulta caro se hai que rehibridar moitas veces. Para eses casos temos ASO: dot blot inverso, no que a membrana ten fixada os distintos alelos e estes son hibridados co produto amplificado xenómico marcado.
- ONDA: é o método máis usado actualmente no estudo de fibrose quística, pero cando chegue a secuenciación predeciblemente quedará desprazado por esta. Son necesarios dous pasos: un primeiro paso consiste nunha PCR multiplex dos fragmentos xénicos a estudar. Posteriormente dous ciclos de ligamento con ligase termoestable e oligonucleótidos específicos dos alelos. Estes primeiros pasos realízanse todos no mesmo tubo de reacción. Realízase entón un estudo dos fragmentos por electroforese capilar. As vantaxes deste proceso é a súa automatización, aínda que é custoso debido á necesidade dun secuenciador automático.
Diagnóstico prenatal[editar | editar a fonte]
As parellas que están a atravesar un embarazo ou teñen plans respecto da xestación, poden ser avaliadas en busca de mutacións do xene CFTR, co obxecto de determinar as probabilidades de que o seu fillo naza con fibrose quística. A proba adóitase realizar nun dos pais ou en ambos e, en caso de detectarse un risco elevado de fibrose quística, efectúase tamén no feto. Debido a que o diagnóstico prenatal non habilita formas de tratamento superiores ou alternativas, a principal razón pola que leva a cabo é, na práctica, proporcionar a posibilidade do aborto no caso de que o feto presente a enfermidade. A proba para fibrose quística en parellas ofrécese de maneira xeneralizada en países como os Estados Unidos,[32] e o Colexio Americano de Obstetras e Xinecólogos (ACOG, polas súas siglas en inglés) recomenda a proba en parellas que posúen un historial de fibrose quística entre os seus familiares directos ou parentes próximos, así como tamén naquelas con risco elevado debido ao seu filiación étnica.[33]
Debido a que o desenvolvemento da fibrose quística no feto require que cada pai transmita unha copia do xene CFTR mutante, e ao alto custo do exame prenatal, a proba adoita realizarse, inicialmente, só nun dos proxenitores. Se este resulta ser portador dunha mutación do xene CFTR, entón examínase ao outro para determinar o risco de que o seu fillo teña a enfermidade. A fibrose quística pode resultar de máis un milleiro de mutacións diferentes e, ao ano 2006, non é posible efectuar estudos de laboratorio para cada unha delas. A proba remítese a analizar o sangue en busca das máis comúns, como ΔF508 - a maioría das modalidades dispoñibles comercialmente detectan non máis de 32 variantes distintas. Se se coñece o dato de que unha familia ten unha mutación pouco común, esta última pode buscarse especificamente. Como consecuencia de que non todas as mutacións coñecidas son detectadas polas probas correntes, un resultado negativo non garante que o neno vaia a estar libre da enfermidade.[34] Doutra banda, dado que as mutacións sondadas son necesariamente aquelas máis comúns nos grupos de máis alto risco, as probas en etnias de baixo risco son menos exitosas, xa que as mutacións máis estendidas nestes grupos son menos frecuentes na poboación xeral.
As parellas en situación de risco, a miúdo realizan probas adicionais durante o embarazo ou antes de que este se produza. A fecundación in vitro con diagnóstico xenético preimplantacional ofrece a posibilidade de examinar o embrión antes da súa colocación no útero. Esta proba realízase tres días despois da fecundación e procura determinar a presenza de xenes CFTR anormais. Se, nun embrión, resultan identificados dous xenes CTRF mutantes, este será excluído da transferencia, implantándose outro que conte con, polo menos, un xene normal.
Durante o transcurso do embarazo, é posible realizar probas tanto sobre a placenta (biopsia de vilosidades coriónicas) como sobre o líquido amniótico que rodea ao feto (amniocentese), coa axuda do ultrasón. Con todo, a biopsia de vilosidades coriónicas correlaciónase con risco de morte fetal nunha taxa de 1 en 100, e a amniocentese, de 1 en 200,[35] polo que é esencial determinar os beneficios adecuadamente para sopesar os riscos, antes de proceder coa proba. Alternativamente, algunhas parellas elixen someterse a técnicas de reprodución asistida con óvulos doantes (recorrendo á fecundación in vitro) ou con esperma doante (inseminación artificial por doante).
Tratamento[editar | editar a fonte]
Un aspecto fundamental na terapéutica da fibrose quística é o control e tratamento do dano pulmonar causado polo moco espeso e polas infeccións, co obxecto de mellorar a calidade de vida do paciente. Para o tratamento das infeccións crónicas e agudas adminístranse antibióticos por vías intravenosa, inhalatoria e oral. Tamén se utilizan dispositivos mecánicos e fármacos (en forma de inhaladores) para controlar as secrecións, e desta maneira desconxestionar e desobstruir as vías respiratorias. Outros aspectos da terapia relaciónanse co tratamento da diabetes con insulina, da enfermidade pancreática con substitución encimática. Adicionalmente, postúlase a eficacia de distintos procedementos, como o transplante e a terapia xénica, para resolver algúns dos efectos asociados a esta enfermidade.
Unha dieta sa, elevado exercicio e tratamentos agresivos con antibióticos está a aumentar a esperanza de vida dos enfermos.
Antibióticos para tratar a enfermidade pulmonar[editar | editar a fonte]
Os antibióticos prescríbense sempre que exista sospeita de pneumonía ou se constate deterioración na función pulmonar. Habitualmente, escóllense en función do historial de infeccións que afectaron ao paciente previamente. Moitas das bacterias comúns na fibrose quística son resistentes a gran cantidade de antibióticos e requiren semanas de tratamento intravenoso con vancomicina, tobramicina, meropenem, ciprofloxacina e piperacilina.

A terapia prolongada a miúdo require hospitalización e canalización dunha vía intravenosa permanente, por exemplo un catéter central inserido percutáneamente (PICC). Así mesmo, é frecuente a indicación simultánea de antibióticos administrados por inhalación, como a tobramicina, a colistina e a gentamicina, por varios meses, co obxecto de mellorar a función pulmonar impedindo a proliferación bacteriana.[36][37] Algúns antibióticos orais como a ciprofloxacina ou a azitromicina utilízanse ás veces para axudar a previr a infección ou para controlala unha vez que está en curso.[38] Nalgúns casos pasan anos entre sucesivas hospitalizacións, mentres que noutros se require a internación cada ano para poder realizar o tratamento.
En tratamentos prolongados, varios dos antibióticos máis comúns (como a tobramicina e a vancomicina) poden causar perda de audición por ototoxicidad ou problemas nos riles. Co obxecto de previr tales efectos secundarios, é habitual medir cuantitativamente as concentracións destes medicamentos en sangue e, de ser necesario, axustar a dosificación.
Outros métodos para tratar a enfermidade pulmonar[editar | editar a fonte]

Son diversas as técnicas que se implementan co obxecto de fluidificar o esputo e facilitar a súa expectoración. No medio hospitalario utilízase a fisioterapia; un terapeuta practica unha serie de manobras mediante presións e percusións (palmoteo) exercidas sobre o exterior do peito (tórax) varias veces ao día. Os dispositivos mecánicos que actúan baixo o mesmo principio que aquelas técnicas básicas de drenaxe postural, inclúen o ventilador de alta frecuencia oscilatoria e os aparellos de ventilación percusiva intrapulmonar, dos que existen modelos portátiles, adaptables ao uso hogareño.[39] O exercicio aeróbico é altamente beneficioso para as persoas con fibrose quística, xa que non só promove o desconxestionamento do esputo, senón que mellora a saúde cardiovascular e o estado xeral.

Entre as substancias administradas por inhalación que axudan a alixeirar as secrecións e facilitan a súa expulsión, atópanse a dornase alfa e a solución salina hipertónica.[40] A dornase é unha desoxirribonuclease (DNase) humana recombinante, que descompón o ADN no esputo, reducindo así a viscosidade deste último.[41] A N-acetilcisteína (un derivado do aminoácido cisteína) tamén actúa fluidificando o esputo, pero as investigacións e a experiencia dispoñibles demostraron que os beneficios son pouco significativos. Por último, broncodilatadores como o salbutamol e o salmeterol (ambos os axentes, antagonistas β2-adrenérxicos) ou o bromuro de ipratropio (un antagonista do receptor colinérgxico, derivado cuaternario da atropina) utilízanse para aumentar o tamaño das vías respiratorias máis pequenas, ao relaxar o músculo liso bronquial.
Na medida en que se agrava a condición pulmonar, pode requirirse soporte respiratorio mecánico. Polas noites, algúns pacientes deben usar máscaras especiais que actúan empuxando o fluxo aéreo até os pulmóns. A ventilación non invasiva mediante máscara nasal e presión positiva (VPAP, polo acrónimo para o inglés variable positive airway pressure), axuda a previr, durante o soño, caídas significativas nos niveis sanguíneos de osíxeno. Tamén pode usarse no curso da fisioterapia respiratoria para favorecer a expulsión de esputo.[42] Con todo, en casos severos, pode ser necesario poñer en funcionamento formas invasivas de asistencia respiratoria con intubación endotraqueal (isto é, colocación dun tubo ou sonda na traquea).
Tratamento doutros aspectos da fibrose quística[editar | editar a fonte]

Os recentemente nados con íleo meconial tipicamente requiren cirurxía; polo xeral, non sucede o mesmo en adultos con síndrome de obstrución intestinal distal. O tratamento da insuficiencia pancreática baseado en substitución das encimas dixestivas minguadas permite que os intestinos absorban de maneira apropiada nutrientes e vitaminas que, doutro xeito, perderíanse nas feces. Aínda así, a maioría dos individuos con fibrose quística deben recibir doses adicionais de vitaminas A, D, E e K a partir de suplementos, e seguir unha dieta de alto valor calórico. A diabetes que adoita acompañar a fibrose quística trátase con inxeccións de insulina.[43] O desenvolvemento de osteoporose pode previrse coa suplementación de vitamina D e calcio, e a miúdo trátase con bifosfonatos.[44] En canto ao atraso no crecemento, procúrase contrarrestalo mediante a inserción dun tubo de alimentación (gastrostomía) para aumentar así a inxesta de calorías a partir de nutrición adicional; tamén se administran con este fin inxeccións de hormona de crecemento.[45]
As infeccións dos seos paranasais adoitan tratarse cun prolongado réxime de antibióticos. O desenvolvemento de pólipos, así como outros cambios estruturais de tipo patolóxico no interior dos condutos nasais, poden restrinxir o fluxo aéreo e complicar o cadro. Por este motivo, é frecuente a práctica cirúrxica en procura de aliviar a obstrución e limitar o desenvolvemento de novas infeccións. Tamén se administran corticosteroides intranasais, como a fluticasona, para reducir a inflamación.[46] Doutra banda, a infertilidade feminina pode combaterse recorrendo a técnicas de reprodución asistida. Aquela que afecta o home tamén ten tratamento: por exemplo, mediante a inxección intracitoplasmática de esperma.[47]
Transplante e terapia xénica[editar | editar a fonte]
Polo xeral, considérase procedente o transplante de pulmón en persoas con deterioración progresiva da función pulmonar e crecente intolerancia ao exercicio (fatiga ou esgotamento muscular desproporcionados para o exercicio realizado). Aínda que o transplante dun único pulmón é viable noutras enfermidades, nos pacientes con fibrose quística ambos deben ser substituídos xa que, doutro xeito, as bacterias aloxadas no órgano remanente poderían infectar a aquel que foi trasplantado. Así mesmo, pode practicarse simultaneamente un transplante de páncreas ou de fígado co propósito de aliviar a enfermidade hepática ou a diabetes.[48] A opción do transplante de pulmón avalíase cando a función pulmonar vese afectada en grao tal que se vexa ameazada a supervivencia ou se requira a asistencia con dispositivos mecánicos.[49]
A terapia xénica representa unha vía futura na loita contra a enfermidade. Mediante esta técnica, procúrase inserir unha copia normal do xene CFTR nas células afectadas. Debido á incapacidade dos retrovirus para alcanzar células que non se dividen, realizáronse análises clínicas para inserir xenes en adenovirus. Na actualidade, estes virus están a utilizarse en ensaios nos que o xene CFTR normal adminístrase, por un método en aerosol, ás células epiteliais que revisten os pulmóns (terapia xénica in vivo). Espérase que os adenovirus insiran o xene normal, inducindo unha función pertinente das canles de cloro nestas células.
Algúns estudos sinalaron que para previr as manifestacións pulmonares da fibrose quística, só se require a expresión xénica de entre un 5 e un 10% dos valores normais de proteína CFTR.[50] Un inconveniente dos adenovirus é que non se integran no ADN da célula hóspede. Por tanto, finalmente pérdense, orixinando unha expresión do xene transitoria e a necesidade de reintroducción do vector. Propuxéronse diversas abordaxes e iniciáronse numerosos estudos clínicos pero, ao ano 2006, persisten múltiples obstáculos, que será preciso superar para que a terapia xénica resulte exitosa.[51]
Epidemioloxía[editar | editar a fonte]

A fibrose quística é, entre as persoas de ascendencia europea, a máis frecuente das enfermidades autosómicas recesivas potencialmente fatais. Nos Estados Unidos, aproximadamente 30.000 individuos padecen fibrose quística; na súa maioría, son diagnosticados ao seis meses de idade. Canadá ten preto de 3.000 habitantes con esta condición. Estímase que unha de cada 25 persoas de ascendencia europea e unha de cada 29 persoas de ascendencia askenazí son portadores dunha mutación de fibrose quística. Aínda que é menos común nestes grupos, aproximadamente un de cada 46 hispanoamericanos, un de cada 65 africanos e un de cada 90 asiáticos son portadores de polo menos un xene CFTR anormal.[52][53][54] A Arxentina representa unha excepción no contexto de América Latina, cunha incidencia de casos moito maior á media da rexión e moi próxima á rexistrada nos Estados Unidos ou Canadá, e unha prevalencia de portadores sans na poboación xeral de 1 en 30.
A fibrose quística diagnostícase tanto en homes como en mulleres. Por razóns que só en parte coñécense, a esperanza de vida ao nacer resulta ser maior entre os homes afectados que entre as mulleres.[55] Aquel indicador tende a variar principalmente en función do alcance e a calidade da atención fornecida polos sistemas de saúde pública. En 1959, a supervivencia media en nenos con fibrose quística era de 6 meses. Para os nados en 2006 nos Estados Unidos, este valor rubiría aos 36,8 anos, de acordo aos datos compilados pola Fundación da Fibrose quística.[56] A taxa de esperanza de vida evolucionou en forma análoga para boa parte de Occidente, exceptuando os países menos desenvolvidos, onde se reportan cifras sensiblemente menores, e nos cales a maioría da poboación afectada non sobrevive máis aló do dez anos de idade.
A Fundación da Fibrose quística compila, ademais, información sobre o estilo de vida dos adultos estadounidenses con fibrose quística. En 2004, a fundación reportou que o 91% desta poboación completara a ensino medio, e o 54% accedera a algunha forma de educación universitaria. Os datos en materia de emprego revelaron que o 12,6% destes adultos estaba imposibilitado para traballar (quedando fóra da poboación economicamente activa), e o 9,9% estaba desocupado. Doutra banda, a información marital sinalou que un 59% era solteiro e un 36% estaba casado ou vivindo en parella. En 2004, 191 mulleres con fibrose quística atopábanse embarazadas nos Estados Unidos.[57]
Teorías sobre a prevalencia da fibrose quística[editar | editar a fonte]
Estímase que a mutación ΔF508 pode ter até uns 52.000 anos de antigüidade.[58] Formuláronse numerosas hipóteses tentando explicar por que unha mutación letal como esta persistiu e estendeuse entre a poboación humana. Algunhas enfermidades autosómicas recesivas comúns como a anemia falciforme revelaron a propiedade de protexer aos seus portadores doutras afeccións, concepto coñecido como vantaxe heterocigota. Co descubrimento de que a toxina do cólera require que os seus hóspedes sexan proteínas CFTR normais para poder funcionar apropiadamente, postulouse que os portadores de xenes CFTR mutantes obtiveron o beneficio da resistencia ao cólera e a outras causas de diarrea.[59] Con todo, estudos posteriores non confirmaron esta hipótese.[60][61]
A presenza de proteínas CFTR normais é condición necesaria para o ingreso de Salmonella typhi (serotipo de Salmonella enterica, proteobacteria gramnegativa do xénero Salmonella) nas células,[62] o que suxire que os portadores de xenes CFTR mutantes poderían ser resistentes á febre tifoide. Con todo, ningún estudo in vivo confirmou esta hipótese. En calquera dos casos, a baixa incidencia de fibrose quística fóra de Europa, en sitios onde tanto o cólera como a febre tifoide son *endémicos, carece de explicación inmediata.
Historia[editar | editar a fonte]
Aínda que o espectro clínico completo da fibrose quística non foi recoñecido até os anos 1930, certos aspectos foron identificados moito antes. Carl von Rokitansky describiu un caso de morte fetal con peritonite meconial, unha complicación do íleo meconial asociado coa fibrose quística. O íleo meconial foi descrito por primeira vez en 1905 por Karl Landsteiner.[63]

En 1938, Dorothy Andersen publicou un artigo intitulado Cystic fibrosis of the páncreas and its relation to celiac disease: a clinical and pathological study ("A fibrose quística do páncreas e a súa relación coa enfermidade celíaca: un estudo clínico e patolóxico") na revista American Journal of Diseases of Children. Deste xeito, era a primeira investigadora en definir esta entidade nosolóxica (denominada, por aquel entón, "fibrose quística do páncreas"), e en ligala cos trastornos pulmonares e intestinais prominentes.[7] Tamén postulou que era unha enfermidade recesiva e utilizou a substitución de encimas pancreáticas como tratamento para os nenos afectados. En 1952, Paul dei Sant' Agnese descubriu anomalías nos electrólitos da suor. Sobre a base desa evidencia, desenvolveuse e perfeccionou o exame da suor durante o curso da seguinte década.[64]
En 1985, investigadores de Londres, Toronto e Salt Lake City trazaron o mapa do xene CFTR no cromosoma 7q. Catro anos máis tarde, no 1989, Francis Collins, Lap-Chee Tsui e John R. Riordan descubriron a primeira mutación para a fibrose quística, ΔF508, nese cromosoma. Investigacións posteriores a aquel achado, identificaron máis de mil mutacións diferentes que dan orixe á enfermidade. Lap-Chee Tsui liderou o equipo de científicos do Hospital for Sick Children (un hospital escola en convenio coa Universidade de Toronto) que descubriu o xene responsable da fibrose quística. Trátase do primeiro trastorno xenético dilucidado estritamente mediante o proceso de xenética inversa. Debido a que as mutacións do xene CFTR son xeralmente pequenas, as técnicas da xenética clásica ou formal non foron capaces de determinar con precisión o xene mutante.[65] Utilizando marcadores proteicos, os estudos de ligamento xenético lograron trazar un mapa da mutación do cromosoma 7. As técnicas de paseo e salto cromosómicos serviron entón para identificar e secuenciar o xene.[66] Este xene foi un dos primeiros xenes en ser localizado e secuenciado por mapeo xenético, e algúns dos participantes neste proxecto, como Francis Collins estiveron implicados máis tarde no Proxecto Xenoma Humano
A identificación da mutación específica responsable da fibrose quística nun paciente pode ser útil para predicir a evolución da enfermidade. Por exemplo, os pacientes homocigotos para a mutación ΔF508 presentan, en case todos os casos, insuficiencia pancreática e teñen, polo xeral, un grao relativamente severo de afectación respiratoria. Con todo, existen excepcións que indican a posibilidade de que factores adicionais (quizais, xenes noutros loci) interveñan na expresión da enfermidade. Doutra banda, a clonación do xene da fibrose quística abriu a posibilidade da terapia xénica, tal e como se describiu na sección pertinente.
Na actualidade, os rexistros da enfermidade indican que o 40% dos pacientes con fibrose quística viven máis dos 18 anos.
Bibliografía[editar | editar a fonte]
- Dapena Fernández, Francisco Javier. Fibrosis quística. Salobreña: Alhulia, 1998, 1ª ed. ISBN 84-95136-13-9
- Salcedo Pousadas, Antonio; García Novo, María Dolores. Fibrosis quística. Madrid: Díaz de Santos, 1998, 1ª ed. ISBN 84-7978-368-0
- Segal, Edgardo. Fibrosis quística. Buenos Aires: Journal, 2004, 1ª *ed. ISBN 987-97739-7-7
- Segal E, et al. "Consenso de Fibrosis Quística." Arch.argent.pediatr. 1999;97(3):188. Dispoñible en liña (PDF)
Ligazóns externas[editar | editar a fonte]
| Wikimedia Commons ten máis contidos multimedia na categoría: Fibrose quística |
- Protocolo diagnóstico e terapéutico para fibrose quística (PDF) Por Héctor Escobar e Amaya Sojo, Asociación Española de Pediatría.
- Infeccións respiratorias na fibrose quística Por José González Valdés e Gladys Abreu Suárez. Acta Médica 2000;9(1-2):39-43.
- Consenso nacional de fibrose quística Por Ignacio Sánchez D, M Angélica Pérez H, M. Lina Boza C, et al. Rev. chil. pediatr. xul. 2001; 72(4):356-80. ISSN 0370-4106.
- En inglés
- CFTR-Related Disorders (GeneReviews, US National Library of Medicine, NIH)
- Fibrose quística en MEDLINE
- Fibrose quística en OMIM
- Genetics Home Reference Variedade de recursos informativos sobre esta enfermidade; contidos producidos polos National Institutes of Health (publicados baixo dominio público).
- Geneva Foundation for Medical Education and Research Imaxes relacionadas con fibrose quística. Universidade de Xenebra, Suíza.
- Fibrose quística
Notas[editar | editar a fonte]
- ↑ Definición de fibrose no Dicionario de Galego de Ir Indo e a Xunta de Galicia.
- ↑ Diccionario galego de termos Médicos. Real Academia de Medicina e Cirurxía de Galicia. 2002. Páxina 320.
- ↑ Vocabulario de Medicina. Servizo de Normalización Lingüística. Universidade de Santiago de Compostela. 2008. Páxina 217.
- ↑ Rosa María Girón Moreno e Antonio Salcedo Pousadas FIBROSIS QUÍSTICA. Monografías NEUMOMADRID.VOLUME VIII / 2005.[1] Edita: ERGON. C/ Arboleda, 1. 28220 Majadahonda (Madrid).(15 de decembro de 2005).
- ↑ Jorde, Lynn; Carey, John; White, Raymond. Xenética médica. Madrid: Mosby, 1996. ISBN 84-8174-161-2
- ↑ New Statistics Show CF Patients Living Longer Arquivado 14 de marzo de 2016 en Wayback Machine. Cystic Fibrosis Foundation (26 de abril, 2006). Consultado o 26-07-2006.
- ↑ 7,0 7,1 Andersen DH. "Cystic fibrosis of the pancreas and its relation to celiac disease: a clinical and pathological study." Am J Dis Child 1938; 56:344-399
- ↑ 8,0 8,1 8,2 8,3 8,4 8,5 Rowe SM, Miller S, Sorscher Ex. "Cystic fibrosis." N Engl J Med. 2005 may 12;352(19):1992-2001. PMID 15888700
- ↑ Maldonado M, Martínez A, Alobid I, Mullol J. The antrochoanal polyp. Rhinology. 2004 dic;42(4):178-82. Rev. PMID 15626248
- ↑ Ramsey B, Richardson MA. Impact of sinusitis in cystic fibrosis. Allergy Clin Immunol. 1992 sep;90(3 Pt 2):547-52. PMID 1527348
- ↑ Eggermont E, De Boeck K. Small-intestinal abnormalities in cystic fibrosis patients. Eur J Pediatr. 1991 oct;150(12):824-8. Rev. PMID 1743211
- ↑ Kulczycki LL, Shwachman H. "Studies in cystic fibrosis of the pancreas; occurrence of rectal prolapse." N Engl J Med. 1958 ag 28;259(9):409-12. PMID 13578072
- ↑ Cohn JA, Friedman KJ, Noone PG, Knowles MR, Silverman LM, Jowell PS. Relation between mutations of the cystic fibrosis gene and idiopathic pancreatitis. N Engl J Med. 1998 sep 3;339(10):653-8. PMID 9725922
- ↑ Malfroot A, Dab I. New insights on gastro-oesophageal reflux in cystic fibrosis by longitudinal follow up. Arch Dis Child. 1991 nov;66(11):1339-45. PMID 175564
- ↑ Khoshoo V, Udall JN Jr. Meconium ileus equivalent in children and adults. Am J Gastroenterol. 1994 feb;89(2):153-7. PMID 8304294
- ↑ Williams SG, Westaby D, Tanner MS, Mowat AP. Liver and biliary problems in cystic fibrosis. Br Med Bull. 1992 oct;48(4):877-92. PMID 1458306
- ↑ Moran A, Pyzdrowski KL, Weinreb J, Kahn BB, Smith SA, Adams KS, Seaquist ER. "Insulin sensitivity in cystic fibrosis." Diabetes. Agosto 1994;43(8):1020-6. PMID 8039595
- ↑ Haworth CS, Selby PL, Webb AK, Dodd ME, Musson H, McL Niven R, Economou G, Horrocks AW, Freemont AJ, Mawer EB, Adams JE. "Low bone mineral density in adults with cystic fibrosis." Thorax. 1999 nov;54(11):961-7. PMID 10525552
- ↑ Gibson LLE, Cooke RE. "A test for concentration of electrolytes in sweat in cystic fibrosis of the pancreas utilising pilocarpine by iontophoresis." Pediatrics mar;23(3):545-9. PMID 13633369
- ↑ Stern, RC. "The diagnose of cystic fibrosis." N Engl J Med 1997; 336:487. PMID 9017943
- ↑ 21,0 21,1 Saiman L. Microbiology of early CF lung disease. Paediatr Respir Rev. 2004;5 Supl A:S367-9. PMID 14980298
- ↑ Tummler B, Koopmann Ou, Grothues D, Weissbrodt H, Steinkamp G, von der Hardt H. Nosocomial acquisition of Pseudomonas aeruginosa by cystic fibrosis patients. J Clin Microbiol. 1991 jun;29(6):1265-7. PMID 1907611
- ↑ Centers for Disease Control and Prevention (CDC). Pseudomonas cepacia at summer camps for persons with cystic fibrosis. MMWR Morb Mortal Wkly Rep. 1993 jun 18;42(23):456-9. PMID 7684813
- ↑ Pegues DÁ, Carson A, Tablan OC, FitzSimmons SC, Roman SB, Miller JM, Jarvis WR.Acquisition of Pseudomonas cepacia at summer camps for patients with cystic fibrosis. Summer Camp Study Group. J Pediatr. 1994 may;124(5 Pt 1):694-702. PMID 7513755
- ↑ Pankhurst CL, Philpott-Howard J. The environmental risk factors associated with medical and dental equipment in the transmission of Burkholderia (Pseudomonas) cepacia in cystic fibrosis patients. J Hosp Infect. 1996 Apr;32(4):249-55. PMID 8744509
- ↑ Jones AM, Govan JR, Doherty CJ, Dodd ME, Isalska BJ, Stanbridge TN, Webb AK. Identification of airborne dissemination of epidemic multiresistant strains of Pseudomonas aeruginosa at a CF centre during a cros infection outbreak. Thorax. 2003 jun;58(6):525-7. PMID 12775867
- ↑ Hoiby N. Isolation and treatment of cystic fibrosis patients with lung infections caused by Pseudomonas (Burkholderia) cepacia and multiresistant Pseudomonas aeruginosa. Neth J Med. 1995 jun;46(6):280-7. PMID 7643943
- ↑ Blaschke et al. Mycologucal surveillance of chlidren wiyh cystic fibrosis. Mycoses. 1991;34 Suppl 1:43-7
- ↑ Maiz L et al. Serologic IGE inmune responses against Aspergillus fumigatus and Candida albicans in patient with cystic fibrosis. Chest 2002;121:782-8
- ↑ 30,0 30,1 http://www.genet.sickkids.on.ca/cftr/statisticspage.html
- ↑ Short DB, Trotter KW, Reczek D, Kreda SM, Bretscher A, Boucher RC, Stutts MJ, Milgram SL. An apical PDZ protein anchors the cystic fibrosis transmembrane conductance regulator to the cytoskeleton. J Biol Chem. 1998 jul 31;273(31):19797-801. PMID 9677412
- ↑ ACOG Committee Opinion #325: "Update on Carrier Screening for Cystic Fibrosis". Obstet Gynecol 2005; 106:1465.
- ↑ American College of Obstetricians and Gynecologists and American College of Medical Genetics. Preconception and prenatal carrier screening for cystic fibrosis. Clinical and laboratory guidelines. American College of Obstetricians and Gynecologists, Washington, DC, outubro 2001.
- ↑ Elias, S, Annas, GJ, Simpson, JL. Carrier screening for cystic fibrosis: Implications for obstetric and gynecologic practice. Am J Obstet Gynecol 1991; 164:1077. PMID 2014829
- ↑ Tabor A, Philip J, Madsen M, Bang J, Obel EB, Norgaard-Pedersen B. Randomised controlled trial of genetic amniocentesis in 4606 low-risk women. *Lancet. 1986 jun 7;1(8493):1287-93. PMID 2423826
- ↑ Pai VB, Nahata MC. Efficacy and safety of aerosolized tobramycin in cystic fibrosis. Pediatr Pulmonol. 2001 oct;32(4):314-27. Rev. PMID 11568993
- ↑ Westerman EM, Lle Brun PP, Touw DJ, Frijlink HW, Heijerman HG. Effect of nebulized colistin sulphate and colistin sulphomethate on lung function in patients with cystic fibrosis: a pilot study. J Cyst Fibros. 2004 mar;3(1):23-8. PMID 15463883
- ↑ Hansen CR, Pressler T, Koch C, Hoiby N.Long-term azithromycin treatment of cystic fibrosis patients with chronic Pseudomonas aeruginosa infection; an observational cohort study. J Cyst Fibros. 2005 mar;4(1):35-40. PMID 15752679
- ↑ van der Schans C, Prasad A, Main E. Chest physiotherapy compared to non chest physiotherapy for cystic fibrosis. Cochrane Database Syst Rev. 2000;(2):CD001401. Rev. PMID 10796781
- ↑ Kuver R, Le SP. Hypertonic saline for cystic fibrosis. N Engl J Med. 2006 abr 27;354(17):1848-51; resposta do autor 1848-51. PMID 16642591
- ↑ Lieberman J. "Dornase aerosol effect on sputum viscosity in cases of cystic fibrosis." JAMA. 1968 jul 29;205(5):312-3. PMID 5694947
- ↑ Moran F, Bradley J. Non-invasive ventilation for cystic fibrosis. Cochrane Database Syst Rev. 2003;(2):CD002769. Rev. PMID 12804435
- ↑ Onady GM, Stolfi A. Insulin and oral agents for managing cystic fibrosis-related diabetes. Cochrane Database Syst Rev. 2005 jul 20;(3):CD004730. Rev. PMID 16034943
- ↑ Conway SP, Oldroyd B, Morton A, Truscott JG, Peckham DG. Effect of oral bisphosphonates on bone mineral density and body composition in adult patients with cystic fibrosis: a pilot study. Thorax. 2004 ag;59(8):699-703. PMID 15282392
- ↑ Hardin DS, Rice J, Ahn C, Ferkol T, Howenstine M, Spears S, Prestidge C, Seilheimer DK, Shepherd R. Growth hormone treatment enhances nutrition and growth in children with cystic fibrosis receiving enteral nutrition.J Pediatr. 2005 mar;146(3):324-8. PMID 15756212
- ↑ Marks SC, Kissner DG. Management of sinusitis in adult cystic fibrosis. Am J Rhinol. 1997 en-feb;11(1):11-4. PMID 9065342
- ↑ Phillipson GT, Petrucco OM, Matthews CD. Congenital bilateral absence of the vas deferens, cystic fibrosis mutation analysis and intracytoplasmic sperm injection. Hum Reprod. 2000 feb;15(2):431-5. PMID 10655317
- ↑ Simultaneous liver and pancreas transplantation in patients with cystic fibrosis. Transplant Proc. 2005 oct;37(8):3567-9. PMID 16298663
- ↑ Belkin RA, Henig NR, Singer LG, Chaparro C, Rubenstein RC, Xie SX, Yee JY, Kotloff RM, Lipson DÁ, Bunin GR. Risk factors for death of patients with cystic fibrosis awaiting lung transplantation. Am J Respir Crit Care Med. 2006 mar 15;173(6):659-66. Epub 2005 dic 30. PMID 16387803
- ↑ Ramalho AS, Beck S, Meyer M, Penque D, Cutting GR, Amaral MD. Five percent of normal cystic fibrosis transmembrane conductance regulator mRNA ameliorates the severity of pulmonary disease in cystic fibrosis. Am J Respir Cell Mol Biol. 2002 nov;27(5):619-27. PMID 12397022
- ↑ Tate S, Elborn S. Progress towards gene therapy for cystic fibrosis.Expert Opin Drug Deliv. 2005 mar;2(2):269-80. Rev. PMID 16296753
- ↑ Rosenstein BJ and Cutting GR. The diagnose of cystic fibrosis: a consensus statement. Cystic Fibrosis Foundation Consensus Panel. J Pediatr. 1998 abr;132(4):589-95. Rev. PMID 9580754
- ↑ Hamosh A, Fitz-Simmons SC, Macek M Jr, Knowles MR, Rosenstein BJ, Cutting GR. Comparison of the clinical manifestations of cystic fibrosis in black and white patients. J Pediatr. 1998 feb;132(2):255-9. PMID 9506637
- ↑ Kerem B, Chiba-Falek Ou, Kerem E. Cystic fibrosis in Jews: frequency and mutation distribution. Genet Test. 1997;1(1):35-9. Rev. PMID 10464623
- ↑ Rosenfeld, M, Davis, R, FitzSimmons, S, et al. Gender gap in cystic fibrosis mortality. Am J Epidemiol 1997 145,794-803
- ↑ New Statistics Show CF Patients Living Longer Arquivado 14 de marzo de 2016 en Wayback Machine. Cystic Fibrosis Foundation (26 de abril, 2006). Consultado o 27-07-2006.
- ↑ Cystic Fibrosis Foundation data (PDF) Arquivado 24 de xullo de 2006 en Wayback Machine. Consultado o 27/07/2006.
- ↑ Wiuf *C. Do delta F508 heterozygotes have a selective advantage? Genet Res. 2001 ag;78(1):41-7. PMID 11556136
- ↑ Gabriel SE, Brigman KN, Koller BH, Boucher RC, Stutts MJ. Cystic fibrosis heterozygote resistance to cholera toxin in the cystic fibrosis mouse model. Science. 1994 oct 7;266(5182):107-9. PMID 7524148
- ↑ Cuthbert AW, Halstead J, Ratcliff R, Colledge WH, Evans MJ. The genetic advantage hypothesis in cystic fibrosis heterozygotes: a murine study. J Physiol. 1995 xaneiro 15;482 (Pt 2):449-54. PMID 7714835
- ↑ Hogenauer C, Santa Ana CA, Porter JL, Millard M, Gelfand A, Rosenblatt RL, Prestidge CB, Fordtran JS. Active intestinal chloride secretion in human carriers of cystic fibrosis mutations: an evaluation of the hypothesis that heterozygotes have subnormal active intestinal chloride secretion. Am J Hum Genet. 2000 dic;67(6):1422-7. Epub 2000 oct 30. PMID 11055897.
- ↑ Pier GB, Grout M, Zaidi T, Meluleni G, Mueschenborn SS, Banting G, Ratcliff R, Evans MJ, Colledge WH. Salmonella typhi uses CFTR to enter intestinal epithelial cells. Nature. 1998 may 7;393(6680):79-82. PMID 9590693
- ↑ Busch R. "On the history of cystic fibrosis." Acta Univ Carol [Med] (Praga). 1990;36(1-4):13-5. PMID 2130674
- ↑ Dei Sant' Agnese PA, Darling RC, Perera GA, et al. Abnormal electrolyte composition of sweat in cystic fibrosis of the pancreas: clinical implications and relationship to the disease. Pediatrics 1953; 12:549-563.
- ↑ Riordan JR, Rommens JM, Kerem B, Alon N, Rozmahel R, Grzelczak Z, Zielenski J, Lok S, Plavsic N, Chou JL, et al. Identification of the cystic fibrosis gene: cloning and characterization of complementary DNA. Science. 1989 sep 8;245(4922):1066-73. Erratum in: Science 1989 sep 29;245(4925):1437. PMID 2475911
- ↑ Rommens JM, Iannuzzi MC, Kerem B, Drumm ML, Melmer G, Dean M, Rozmahel R, Cole JL, Kennedy D, Hidaka N, et al. Identification of the cystic fibrosis gene: chromosome walking and jumping. Science. 1989 sep 8;245(4922):1059-65. PMID 2772657

