Sacarosa
| Sacarosa | |
|---|---|
 | |
 | |
 | |
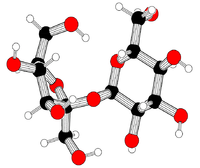
(2R,3R,4S,5S,6R)-2-[(2S,3S,4S,5R)-3,4-dihidroxi-2,5-bis(hidroximetil)oxolan-2-il]oxi-6-(hidroximetil)oxano-3,4,5-triol | |
Outros nomes Azucre de mesa; α-D-glicopiranosil-(1→2)-β-D-frutofuranósido; β-D-frutofuranosil-(2→1)-α-D-glicopiranósido; β-(2S,3S,4S,5R)-frutofuranosil-&alfa;-(1R,2R,3S,4S,5R)-glicopiranósido; &alfa;-(1R,2R,3S,4S,5R)-glicopiranosil-β-(2S,3S,4S,5R)-frutofuranósido | |
| Identificadores | |
| Número CAS | 57-50-1 |
| PubChem | 5988 |
| ChemSpider | 5768 |
| UNII | C151H8M554 |
| Número CE | 200-334-9 |
| DrugBank | DB02772 |
| ChEBI | CHEBI:17992 |
| ChEMBL | CHEMBL253582 |
| Número RTECS | WN6500000 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades[1] | |
| Fórmula molecular | C12H22O11 |
| Masa molecular | 342,30 g/mol |
| Aspecto | sólido branco |
| Densidade | 1,587 g/cm3, sólido |
| Punto de fusión | Ningún; decomponse a 186 °C |
| Solubilidade en auga | 2000 g/L (25 °C) |
| log P | −3,76 |
| Estrutura | |
| Estrutura cristalina | Monoclínico |
| Grupo espacial | P21 |
| Perigosidade | |
| EU Index | non listado |
| NFPA 704 | |
| Compostos relacionados | |
| Compostos relacionados | Lactosa Maltosa |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
A sacarosa ou azucre común é un disacárido formado por unha molécula de glicosa e outra de frutosa. Non ten poder redutor sobre o licor de Fehling.
O seu nome químico é alfa-D-glucopiranosil(1->2)-beta-D-fructofuranósido.
A súa fórmula química é: (C12H22O11)
Na natureza está presente nun 20% en peso na cana de azucre e nun 15% do peso na remolacha azucreira, da que se obtén o azucre de mesa. O mel tamén contén gran cantidade de sacarosa parcialmente hidrolizada. O azucre de mesa é o edulcorante máis utilizado para adozar os alimentos.
Unha curiosidade da sacarosa é que presenta triboluminiscencia, que produce luz mediante unha acción mecánica.
Estrutura e función[editar | editar a fonte]
A sacarosa (azucre de mesa) é un disacárido de glicosa e frutosa. Sintetízase nas plantas, pero non en animais superiores. Non contén ningún átomo de carbono anomérico libre, posto que os carbonos anoméricos das dúas unidades monosacáridas constituíntes están unidos entre si, covalentemente, mediante un enlace O-glucosídico. Por esta razón, a sacarosa non é un azucre redutor e tampouco posúe un extremo redutor.
O seu nome abreviado pode escribirse como Glc(a -1à 2)Fru ou como Fru(b 2à 1)Glc. A sacarosa é un produto intermedio principal da fotosíntese. En moitas plantas constitúe a forma principal de transporte de azucre dende as follas a outras partes da planta. Nas sementes xerminadas de plantas, algunhas graxas e proteínas almacenadas convértense en sacarosa para o seu transporte a partir da planta en desenvolvemento.
A sacarosa como nutriente[editar | editar a fonte]
| Valor nutricional por 100 g | |
|---|---|
| Enerxía | 1 620 kJ (390 kcal) |
100 g | |
0 g | |
0 g | |
| Vitaminas | Cantidade %DV† |
| Tiamina (B1) | 0% 0 mg |
| Riboflavina (B2) | 0% 0 mg |
| Niacina (B3) | 0% 0 mg |
| Vitamina C | 0% 0 mg |
| Minerais | Cantidade %DV† |
| Ferro | 0% 0 mg |
| Fósforo | 0% 0 mg |
| Potasio | 0% 2.0 mg |
| Selenio | 1% 0.6 μg |
| |
| †As porcentaxes son aproximadas empregando a recomendación de US para os adultos. Fonte: Base de datos USDA Nutrient | |
A sacarosa úsase nos alimentos polo seu poder adozante. Ó chegar ó estómago sofre unha hidrólise ácida e unha parte desdóbrase nos seus compoñentes glicosa e frutosa. O resto de sacarosa pasa ao intestino delgado, onde o enzima sacarase convértea en glicosa e frutosa.
Precaucións[editar | editar a fonte]
Se se quenta pasa a estado líquido, no que é moi perigosa, xa que se atopa a moi alta temperatura e pode queimar a pel. Debido a súa baixa calor de fusión , pasa a estado líquido moi rapidamente, e pégase ó recipiente que o conten con moita facilidade.
O seu consumo excesivo pode causar diabetes, carie dental, o incluso a caída dos dentes. Hai persoas que sofren intolerancia á sacarosa, debido á falta do enzima sacarase, e que non poden tomar sacarosa, xa que lles provoca problemas intestinais.
Uso comercial[editar | editar a fonte]
A sacarosa é o edulcorante máis utilizado no mundo industrializado, aínda que ten sido substituída en parte na preparación industrial de alimentos por outros adozantes tales como xaropes de glicosa, ou por combinacións de ingredientes funcionais e adozantes de alta intensidade.
Extraese xeralmente da cana de azucre ou da remolacha requirindo un proceso de purificación e cristalización. Outras fontes comerciais (de menor importancia) son o sorgo doce e o xarope de pradairo.
A utilización da sacarosa debese ó seu poder adozante a ás súas propiedades funcionais, como a consistencia; por tal motivo é importante para a estrutura de moitos alimentos incluíndo galletas, merengues, claras a punto de neve e sorbetes. Ademais emprégase na conservación de alimentos (marmelo) e en moita da chamada "comida lixo".

