Conformación do ciclohexano

A conformación do ciclohexano é a forma tridimensional que esta molécula pode adoptar mantendo a integridade dos seus enlaces, e que pode presentarse en varias formas distintas.
Os ángulos interno dun hexágono regular plano son de 120º, pero o ángulo entre os carbonos nunha cadea hidrocarbonada é normalmente de 109º. Por tanto, o anel do ciclohexano tende a adoptar certas conformacións non planas (deformadas), as cales teñen todos os ángulos máis preto dos 109º e, por tanto, unha enerxía tensional menor ca a forma hexagonal plana. As formas máis importantes, denominadas confórmeros, que pode adoptar o ciclohexano denomínanse: cadeira, media cadeira, bote, e bote torcido.[1] A molécula pode facilmente cambiar entre estas conformacións, e só dúas delas, a cadeira e o bote torcido, poden illarse puras.
A conformación do ciclohexano foi moi estudada en química orgánica porque son o exemplo clásico de isomerismo conformacional, e polas complexas interrelacións entre os diferentes confórmeros do ciclohexano e os seus derivados. Confórmeros diferentes poden ter propiedades diferentes, incluíndo a estabilidade e reactividade química.
Fondo histórico[editar | editar a fonte]
A primeira suxestión de que o ciclohexano podería non ser unha molécula plana data de hai moito tempo. En 1890, Hermann Sachse, un asistente de 28 anos en Berlín, publicou instrucións para dobrar unha folla de papel para representar dúas formas de ciclohexano que chamou simétrica e non simétrica (o que agora chamamos cadeira e bote). Entendeu claramente que estas formas teñen dúas posicións posibles para os hidróxenos (en terminoloxía moderna axial e ecuatorial), que dúas cadeiras probablemente se interconverterían, e mesmo explicou como certos substituístes favorecerían as formas en cadeira. Debido a que expresou todo en linguaxe matemático, poucos químicos da época entenderon os seus argumentos. Fixo algúns intentos de publicar as súas ideas, pero ningún conseguiu atraer a atención dos químicos. A súa morte en 1893, á idade de 31 anos, significou que as súas ideas se esquecesen. En 1918 Ernst Mohr, usando a nova técnica da cristalografía de raios X, puido determinar a estrutura do diamante, recoñecéndose nesa estrutura o modelo de cadeira de Sachse.[2][3][4]
Derek Barton e Odd Hassel compartiron o Premio Nobel polo seu traballo sobre as conformacións do ciclohexano e outras moléculas.
Conformación en cadeira[editar | editar a fonte]
Debido á tendencia dos orbitais híbridos sp3 dos átomos de carbono tetravalentes a formar ángulos de enlace de 109.5 °, o ciclohexano non adopta unha disposición hexagonal plana con ángulos interiores de 120 °. A conformación en cadeira é un termo usado para a conformación química máis estable dun anel de seis átomos de carbono unidos por enlace simple, como o do ciclohexano.
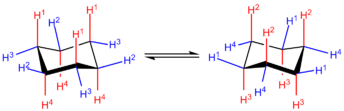
Na conformación en cadeira de mínima enerxía, 6 dos 12 hidróxenos están en posición axial (en cor vermella), é dicir, os seus enlaces C-H son paralelos uns a outros e parecen sobresaír por arriba e abaixo da estrutura do anel, os outros 6 están en posición ecuatorial (en azul), e están dispostos arredor do perímetro do anel. Na imaxe obsérvase ademais que un hidróxeno en cada posición está "arriba" respecto ao outro que está "abaixo" en dita posición.
Ao percorrermos o anel arredor, pode verse que as posicións axiais cara a arriba (H1 na estrutura da esquerda) alternan coas posicións ecuatoriais cara a arriba (H2). Ademais, as posicións axiais alternan lados arredor do anel (H1 axial-arriba fronte a H4 axial-abaixo) e do mesmo modo as posicións ecuatoriais (H2 ecuatorial-arriba fronte a H3 ecuatorial-abaixo). Para dous substituíntes unidos a carbonos adxacentes no anel como no trans-1,2-ciclohexano, os substituíntes deben ser ambos axiais ou ecuatoriais, para permaneceren en lados opostos do anel. De xeito similar, para o cis-1,2-ciclohexano, unha substitución debe ser axial e a outra ecuatorial, ou viceversa. Son posibles outros varios esquemas de substitución, cada un seguindo os mesmos esquemas de posicionamiento xeométrico relativo.
Nun proceso coñecido como inversión do anel ou inversión da cadeira, a conformación do anel cambia, o que fai que os hidróxenos axiais pasen a ser ecuatoriais, e os hidróxenos ecuatoriais a ser axiais. Porén, a dirección relativa dos hidróxenos con respecto ao anel segue sendo a mesma: un hidróxeno axial "arriba", cando se inverte, permanece como un hidróxeno ecuatorial "arriba". As dúas conformacións en cadeira poden diferir en estabilidade, dependendo da identidade dos grupos funcionais. Xeralmente, os substituíntes son máis estables cando están en posicións ecuatoriais, xa que neste caso non hai interacción diaxial 1,3 entre o grupo substituínte axial e calquera outro grupo axial no anel. Por exemplo, se hai un grupo metilo no carbono 1 nunha posición axial, interaccionará cos hidróxenos axiais no carbono 3 e carbono 5. Porén, cando hai heteroátomos electronegativos involucrados, pode observarse o contrario; isto denomínase efecto anomérico. Nunha mostra as moléculas de ciclohexano atópanse na conformación en cadeira nun 99,99% dos casos a 25 °C.
A preferencia dun substituínte pola conformación ecuatorial está medida en termos do seu valor A, que é a diferenza na enerxía libre de Gibbs entre os confórmeros ecuatorial e axial. Un valor positivo de A indica preferencia pola posición ecuatorial. O valor de A varía de case cero para substituíntes moi pequenos como o deuterio, ata aproximadamente 5 kcal/mol para substituíntes moi voluminosos como o grupo ter-butilo.
Conformación en bote[editar | editar a fonte]
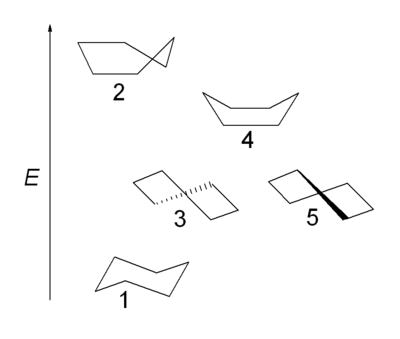
Ademais da conformación en cadeira (1) con simetría D3d, o ciclohexano pode existir nos confórmeros de media cadeira, de sobre (2), torcida ou bote torcido (3,5) con simetría D2 e bote (4). Só a forma torcida é illable posto que, igual que a forma en cadeira, representa un mínimo de enerxía. A conformación bote non sofre tensión angular, pero ten unha enerxía máis alta ca a forma cadeira debido á tensión estérica orixinada polos dous átomos de hidróxeno 1,4 na denominada interacción de pau de bandeira. A tensión torsional na conformación bote ten un valor máximo porque dous dos enlaces de carbono están eclipsados. Comparado coa conformación alternada dos enlaces na forma cadeira, e a ausencia completa de tensión torsional, ou a conformación de bote torcido con 4 dos 6 enlaces parcialmente alternados. Na conformación en media cadeira, 4 átomos de carbono están situados nun plano, no que dous enlaces están completamente eclipsados.
As formas de bote e sobre son estados de transición entre as formas torcida e cadeira, e son imposibles de illar. A conformación en bote torcido é 5,5 kcal/mol (23 kJ/mol) menos estable ca a conformación en cadeira. As enerxías dos dous estados de transición son 6,6 kcal/mol (28 kJ/mol) (bote) e 10,8 kcal/mol (45 kJ/mol) (media cadeira) maiores ca a de cadeira.[5] O proceso de inversión de anel pode ser descrito agora con maior precisión como se tivese lugar a través dunha conformación de bote torcido, e dous estados de transición de media cadeira.
A diferenza de enerxía entre a conformación en cadeira e en bote torcido pode medirse indirectamente tomando a diferenza da enerxía de activación para a conversión da conformación en cadeira á de bote torcido, e da isomerización inversa. A proporción de conformación de bote torcido a temperatura ambiente é moi baixa (menor do 0,1%) pero a 1073 K, esta concentración pode chegar ao 30%. A reacción inversa mídese por espectroscopia infravermella despois de arrefriar rapidamente o ciclohexano desde 1073 K a 40 K, conxelando cando está en gran proporción na conformación en bote torcido.

O [6.6]quiralano[6][7] é unha molécula composta completamente de ciclohexanos idénticos en bote torcido. O twistano é outro composto cunha conformación forzada en bote torcido.
Derivados do ciclohexano[editar | editar a fonte]
Os substituíntes encontrados no ciclohexano adoptan formacións cis e trans e non poden intercambiarse doadamente por unha rotación simple de enlace sigma como pasa coas moléculas liñais. A formación cis significa que ambos os substituíntes están no lado superior dos dous sitios substituíntes en cada carbono, entanto que trans significa que están en lados opostos. Malia que os átomos de carbono no ciclohexano están unidos por un enlace simple, o anel permanece ríxido, debido a que o intercambio de cis a trans requiriría a rotura do anel. A nomenclatura para cis indícase por (Z), e para trans por (E) situadas diante do nome IUPAC.
Para aneis de ciclohexano disubstituídos (por exemplo, dous grupos no anel), a orientación relativa dos dous substituíntes afecta á enerxía das conformacións posibles. Para o ciclohexano 1,2- e 1,4-disubstituído, unha configuración cis orixina un grupo axial e un ecuatorial. Esta configuración pode sufrir inversión en cadeira. Para o ciclohexano con substitucións 1,2 e 1,4, unha configuración trans orixina, ou ben ambos os dous grupos axiais, ou ben ambos os dous ecuatoriais. Neste caso, a conformación diaxial é evitada efectivamente polo seu alto impedimento estérico (catro interaccións gauche máis ca a diecuatorial). Para os ciclohexanos 1,3-disubstituídos, a forma cis é diecuatorial e a conformación invertida sofre interaccións estéricas adicionais entre os dous grupos axiais. Os ciclohexanos 1,3-disubstituídos en trans son como o cis-1,2- e cis-1,4- e pode inverterse entre as dúas formas equivalentes axial/ecuatorial.
Existen derivados do ciclohexano que teñen unha conformación en bote torcido máis estable. Un exemplo é o 1,2,4,5-tetratiano, un composto organoaxofrado con 4 grupos metileno substituídos por un grupo xofre, eliminando así as desfavorables interaccións diaxiais 1,3. No análogo tetrametil 3,3,6,6-tetrametil-1,2,4-5-tetratiano, a conformación en bote torcido é a que domina realmente. Tamén na ciclohexano-1,4-diona coa interacción estérica de hidróxeno 1,4 eliminada, a conformación máis estable é a de bote torcido.
O cis-1,4-di-ter-butilciclohexano ten un grupo axial ter-butil na conformación cadeira, e a conversión á conformación bote torcido sitúa a ambos os grupos nas posicións ecuatoriais que son máis favorables. Como resultado, a conformación en bote torcido é máis estable por 0,47 kcal/mol (1,96 kJ/mol) a 125K, segundo foi medido por espectroscopía de resonancia magnética nuclear (RMN).
Efecto dos substituíntes polares
- O cis-ciclohexano-1,3-diol prefire a conformación diaxial por formación dun enlace de hidróxeno intramolecular.
- O 2,5-di-ter-butil-1,4-ciclohexanodiol preséntase en conformación bote ou bote torcido debido a que tamén forma un enlace de hidróxeno intramolecular.
- A 2-bromociclohexanona prefire un Br axial, porque se minimiza así a repulsión dipolar.
- A 2-bromo-4,4-dimetilciclohexanona prefire un Br ecuatorial (con interacción diaxial 1,3) mellor que unha repulsión dipolar.
- O trans-1,2-dibromociclohexano preséntase en forma axial en solventes non polares, posto que os dipolos se cancelan, entanto que o fai en posición ecuatorial en solventes polares, dado que os dipolos se reforzan.
Notas[editar | editar a fonte]
- ↑ Nelson, Donna J. (2011). "Toward Consistent Terminology for Cyclohexane Conformers in Introductory Organic Chemistry". Journal of Chemical Education (American Chemical Society) 88: 292–294. doi:10.1021/ed100172k.
- ↑ H. Sachse, Chem. Ber, 1890, 23, 1363; Z. Physik. Chem, 1892, 10, 203; Z. Physik. Chem., 1893, 11, 185-219.
- ↑ E. Mohr, J. Prakt. Chem., 1918, 98, 315 and Chem. Ber., 1922, 55, 230.
- ↑ Esta historia resúmese brevemente aquí (en Inglés) Arquivado 07 de xullo de 2010 en Wayback Machine..
- ↑ Conformational Study of cis-1,4-Di-tert-butylcyclohexane by Dynamic NMR Spectroscopy and Computational Methods. Observation of Chair and Twist-Boat Conformations Gill, G.; Pawar, D. M.; Noe, E. A J. Org. Chem. (Article); 2005; 70(26); 10726-10731. DOI: 10.1021/jo051654z Abstract
- ↑ http://www.mazepath.com/uncleal/chiral2.gif Arquivado 07 de setembro de 2009 en Wayback Machine. Chiralane
- ↑ "Copia arquivada". Arquivado dende o orixinal o 07 de setembro de 2009. Consultado o 12 de setembro de 2011.
Véxase tamén[editar | editar a fonte]
| Wikimedia Commons ten máis contidos multimedia na categoría: Conformación do ciclohexano |