Superantíxeno



Os superantíxenos (SAgs) son un tipo de antíxeno que causa a activación non específica de células T, o que ten como resultado a activación policlonal de células T e a liberación masiva de citocinas. Os superantíxenos poden producilos microbios patoxénicos, como virus, micoplasmas, e outras bacterias[1] como un mecanismo de defensa contra o sistema inmunitario do hóspede.[2] Comparada cunha resposta normal das células T inducida por antíxeno na cal só se activan entre o 0,001-0,0001% das células T do corpo, os superantíxenos poden activar unha proporción moito maior das células T do corpo. Ademais, os anticorpos anti-CD3 e anti-CD28 (CD28-SuperMAB) tamén son superantíxenos moi potentes (e poden activar ata o 100% das células T).
O gran número de células T activadas polos superantíxenos xera unha resposta inmunitaria masiva que non é específica para ningún epítopo determinado do superantíxeno, o que mina unha das bases fundamentais do sistema inmunitario adaptativo, como é a súa capacidade de dirixirse contra os antíxenos con alta especificidade. Máis importante aínda é que as células T activadas segregan unha gran cantidade de citocinas, a máis importante das cales é o interferón gamma (IFN-γ). Esta cantidade excesiva de IFN-γ á súa vez activa aos macrófagos. Os macrófagos activados, á súa vez, orixinan unha sobreprodución de citocinas proinflamatorias como a interleucina-1, interleucina-6 e TNF-alfa. O TNF-alfa é especialmente importante como parte da resposta inflamatoria do corpo. En circunstancias normais libérase localmente en baixos niveis e axuda ao sistema inmunitario a derrotar aos patóxenos. Porén, cando se libera sistemicamente no sangue e en altos niveis (debido á activación en masa de células T resultante da unión de superantíxenos), pode causar síntomas moi severos que poden chegar a ser mortais, como choque circulatorio e fallo multiorgánico.
Estrutura[editar | editar a fonte]
Os superantíxenos prodúcense intracelularmente nas bacterias e libéranse durante as infeccións como toxinas maduras extracelulares.[3]
As secuencias destas toxinas están relativamente conservadas entre diferentes subgrupos de suprantíxenos microbianos. Máis importante que a homoloxía na secuencia é a homoloxía na estrutura tridimensional que presentan os diferentes superantíxenos, que dá como resultado efectos funcionais similares entre diferentes grupos.[4][5]
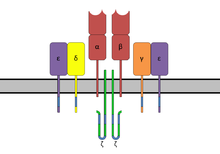
As estruturas cristalinas das enterotoxinas revelan que son proteínas elipsoidais compactas que comparten un patrón de pregamento de dous dominios característico, que consta dun dominio globular en barril β coñecido como o pregamento oligosacárido / oligonucleótido, unha longa hélice α que se estende diagonalmente no centro da molécula, e un dominio globular C-terminal.[4]
Os dominios teñen rexións de unión para o complexo maior de histocompatibilidade de clase II (MHC de clase II) e o receptor de células T (TCR), respectivamente.[6]
Unión dos superantíxenos[editar | editar a fonte]
Os superantíxenos únense primeiro ao MHC de clase II e despois coordínanse coas cadeas variable alfa ou a beta dos receptores TCR.[2][5][7]
Unión ao MHC de clase II[editar | editar a fonte]
Os superantíxenos mostran preferencia pola forma HLA-DQ da molécula.[7] A unión da cadea α coloca o superantíxeno na posición apropiada para coordinarse co TCR.
Menos comunmente, o superantíxeno únese á polimórfica cadea β do MHC de clase II por medio dunha interacción mediada por un complexo de coordinación do ión cinc entre tres residuos de superantíxeno e unha rexión moi conservada da cadea β do HLA-DR.[5] O uso dun ión cinc nesta unión fai que a afinidade da interacción sexa máis alta.[4] Varios superantíxenos de estafilococos poden establecer enlaces cruzados con moléculas do MHC ao unirse a ambas as cadeas α e β.[4][5] Este mecanismo estimula a expresión de citocinas e a súa liberación nas células presentadoras de antíxenos e tamén induce a produción de moléculas coestimuladoras que lle permiten á célula unirse e activar ás células T máis efectivamente.[5]
Unión ao receptor de células T[editar | editar a fonte]
A rexión de unión á célula T dun superantíxeno interacciona coa rexión variable da cadea beta do receptor de células T. Un determinado superantíxeno pode activar unha gran proporción da poboación de células T porque o repertorio de células T humanas comprende só uns 50 tipos de elementos Vβ e algúns superantíxenos son capaces de unirse a múltiples tipos de rexións Vβ. Esta interacción varía lixeiramente entre os diferentes grupos de superantíxenos.[6] A variabilidade observada en diferentes persoas nos tipos de rexións das células T que son máis predominantes explica por que algunhas persoas responden máis fortemente a certos superantíxenos. Os superantíxenos do grupo I contactan coa Vβ no CDR2 e na rexión armazón da molécula.[8][9] Os superantíxenos do grupo II interaccionan coa rexión Vβ utilizando mecanismos que dependen da conformación da proteína. Estas interaccións son na súa maior parte independentes das cadeas laterais de aminoácidos da Vβ específicos. Os superantíxenos do grupo IV líganse aos tres bucles CDR de certas formas de Vβ.[8][9] A interacción ten lugar nun suco da molécula entre os dominios pequeno e grande do superantíxeno e isto permite que o superantíxeno actúe como unha cuña entre o TCR e o MHC. Isto despraza o péptido antixénico do TCR e evita o mecanismo normal para a activación das células T.[5][10]
A forza biolóxica do superantíxeno (a súa capacidade de estimular) está determinada pola súa afinidade polo TCR. Os superantíxenos que teñen a maior afinidade polo TCR son os que desencadean unha resposta máis forte.[11] O SPMEZ-2 é o superantíxeno máis potente descuberto ata agora.[11]
Sinalización das células T[editar | editar a fonte]
O superantíxeno establece enlaces cruzados entre o MHC e o TCR inducindo unha vía de sinalización que dá lugar a unha proliferación das células e á produción de citocinas. Encontráronse baixos niveis de Zap-70 nas células T activadas polos superantíxenos, o que indica que a vía de sinalización normal para a activación das células T está interrompida.[12]
Hipotetízase que se activa o encima Fyn en vez de Lck, que son tirosina quinases, o que leva á indución adaptativa de anerxia.[13]
Tanto a vía da proteína quinase C coma as outras vías das proteínas tirosina quinases están activadas, o que ten como resultado a sobreprodución de citocinas proinflamatorias.[14]
Esta vía alternativa de sinalización desaxusta as vías do calcio/calcineurina e da Ras/MAPquinase lixeiramente,[13] pero permite unha resposta inflamatoria no foco.
Efectos directos[editar | editar a fonte]
A estimulación por superantíxenos das células presentadoras de antíxenos e das células T orixina unha resposta que é principalmente inflamatoria, centrada na acción de células T axudantes Th1. Algúns dos pridutos principais son interleucina-1, interleucina-2, interleucina-6, TNF-α, interferón gamma (IFN-γ), proteína inflamatoria de macrófagos 1α (MIP-1α), MIP-1β, e proteína quimioatractora de monocitos 1 (MCP-1).[14]
Esta liberación de citocinas excesivamente descoordinada, (especialmente de TNF-α), sobrecarga o corpo con eses produtos e orixina erupcións, febre, e pode dar lugar a un fallo multiorgánico, ao coma e á morte.[7][9]
A deleción ou anerxia de células T activadas segue á infección. Esta resulta da produción de interleucina-4 e interleucina-10 pola exposición prolongada á toxina. A IL-4 e a IL-10 regulan á baixa a produción de IFN-gamma, MHC de clase II, e moléculas coestimuladoras da superficie das células presentadoras de antíxenos. Estes efectos producen células de memoria que non responden á estimulación polo antíxeno.[15][16]
Un mecanismo polo cal isto e posible implica a supresión de células T mediada por citocinas. Os enlaces cruzados co MHC tamén activan unha vía de sinalización que suprime a hematopoese e incrementa a apoptose mediada polo receptor Fas.[17]
O IFN-α é outro produto orixinado pola exposición prolongada a superantíxenos. Esta citocina está moi ligada á indución de autoinmunidade,[18] e a enfermidade autoinmune chamada enfermidade de Kawasaki sábese que está causada pola infección de superantíxenos.[11]
A activación de superantíxenos nas células T causa a produción do ligando CD40 que activa o cambio de isotipo nas células B das IgG, IgM e IgE.[19]
Resumindo, as células T son estimuladas e producen un exceso de citocinas causando unha supresión mediada por citocinas de células T e a deleción das células activadas cando o corpo retorna á homeostase. Os efectos tóxicos dos microbios e superantíxenos tamén danan os tecidos e sistemas orgánicos, orixinando a síndrome de choque tóxico.[19]
Se a inflamación inicial se supera, as células hóspede fanse anérxicas ou son delecionadas, orixinando unha grave deficiencia no sistema inmunitario.
Efectos independentes (indirectos) dos superantíxenos[editar | editar a fonte]
Ademais da súa actividade mitoxénica, os superantíxenos poden causar síntomas que son característicos das infeccións.[1]
Un deses efectos é o vómito. Este efecto aparece en casos de intoxicación alimentaria, cando as bacterias que producen superantíxenos liberan a toxina, que é moi resistente á calor. Existe unha determinada rexión da molécula que é activa na indución de toxicidade gastrointestinal.[1] Esta actividade é tamén moi potente, e pequenas cantidades de só 20-35 ug de superantíxeno son suficientes para inducir o vómito.[7]
Os superantíxenos poden estimular o recrutamento de neutrófilos ao lugar da infección dun modo independente da estimulación das células T. Este efecto débese á capacidade dos superantíxenos de activar aos monocitos, estimulando a liberación da citocina TNF-α, causando o incremento da expresión de moléculas de adhesión que recrutan leucocitos nas rexións infectadas. Isto causa inflamación nos pulmóns, tecido intestinal, e en calquera lugar que a bacteria colonizase.[20] Aínda que un certo grao de inflamación é natural e beneficioso, unha inflamación excesiva orixina a destrución dos tecidos.
Un dos efectos indirectos máis perigoso da infección por superantíxenos débese á capacidade dos superantíxenos de aumentar os efectos das endotoxinas no corpo. Isto realízase ao reducir o limiar para a endotoxicidade. Schlievert demostrou que os efectos dos superantíxenos e as endotoxinas, cando se administran conxuntamente, aumentan unhas 50.000 veces.[2] Isto pode deberse á redución da eficiencia do sistema inmunitario inducida pola infección por superantíxenos. Ademais da relación sinérxica entre a endotoxina e o superantíxeno, o efecto de “dobre golpe” da actividade da endotoxina e do superantíxeno produce efectos máis deletéreos ca os observados nunha infección bacteriana típica. Isto tamén implica aos superantíxenos na progresión da sepse en pacientes con infeccións bacterianas.[19]
Enfermidades asociadas coa produción de superantíxenos[editar | editar a fonte]
- Síndrome de choque tóxico
- Enfermidade de Kawasaki
- Eccema
- Psoríase gutata
- Artrite reumatoide
- Diabetes mellitus
- Escarlatina[7]
- Pólipos nasais[21]
Tratamento[editar | editar a fonte]
O principal obxectivo do tratamento médico destes casos é eliminar o microbio que produce os superantíxenos. Isto pode realizarse utilizando vasoconstritores, hidratación e antibióticos.[1]
O corpo produce naturalmente anticorpo para algúns superantíxenos, e este efecto pode aumentarse estimulando a súa produción nas células B.[22]
O conxunto de inmunoglobulinas do corpo pode neutralizar anticorpos específicos e impide a activación das células T. Creáronse anticorpos e péptidos sintéticos que imitan as rexións de unión para os superantíxenos no MHC de clase II, bloqueando a interacción e impedindo a activación da célula T.[1]
Os inmunosupresores tamén se empregan para impedir a activación das células T e a liberación de citocinas. Os corticosteroides utilízanse para reducir os efectos inflamatorios.[19]
Evolución da produción de superantíxenos[editar | editar a fonte]
A produción de superantíxenos distorsiona de forma efectiva a resposta inmune, o que permite que o microbio que segrega o superantíxeno sexa transportado e transmitido sen ser detectado polo sistema inmunitario. Un mecanismo polo que isto ten lugar é inducindo anerxia das células T para os antíxenos e superantíxenos.[12][15] Lussow e MacDonald demostraron isto ao expoñeren sistematicamente animais ao antíxeno estreptocócico. Encontraron que a exposición a outros antíxenos despois da infección de superantíxenos non conseguía activar unha resposta inmunitaria.[15] Noutros experimentos, Watson e Lee descubriron que as células T de memoria creadas pola estimulación por antíxenos normais eran anérxicas para a estimulación por superantíxenos e que as células T de memoria creadas despois da infección por superantíxenos eran anérxicas a toda estimulación por antíxenos. O mecanismo polo cal isto ocorre non foi determinado.[12] Os xenes que regulan a expresión de superantíxenos tamén regulan mecanismos de evasión inmune como a proteína M e a expresión da cápsula bacteriana, o que apoia a hipótese de que a produción de superantixenos evolucionou principalmente como un mecanismo de evasión inmune.[23]
Cando se comparou a estrutura de dominios dun determinado superantíxeno con outras proteínas estreptocócicas de unión ás inmunoglobulinas (como as toxinas producidas por E. coli) o resultado atopado foi que os dominios lembran separadamente a membros destas familias. Esta homoloxía suxire que os superantíxenos evolucionaron por medio da recombinación de dous motivos en cadea B máis pequenos.[24]
Superantíxenos endóxenos[editar | editar a fonte]
As exototoxinas menores estimulantes de linfocitos (Mls) descubríronse nas células do estroma do timo do rato. Estas toxinas estaban codificadas por xenes de superantíxenos que foron incorporados no xenoma do rato a partir do virus do tumor mamario de rato (MMTV). A presenza destes xenes no xenoma do rato permite que o rato exprese o antíxeno no timo como un medio para seleccionar negativamente os linfocitos que teñan unha rexión variable beta que é susceptible de estimulación polo superantíxeno viral. O resultado é que estes ratos son inmunes á infección polo virus posteriormente durante a súa vida.[1]
Unha selección dependente de superantíxenos endóxenos similar aínda non foi identificada no xenoma humano, pero si se descubriron superantíxenos endóxenos e sospéitase que xogan un papel integral nas infeccións virais. A infección polo virus Epstein-Barr, por exemplo, causa a produción dun superantíxeno nas células infectadas, aínda que non se encontrou ningún xene para a toxina no xenoma do virus. O virus manipula a célula infectada para expresar aos seus propios xenes de superantíxenos, e isto axuda a evitar o sistema inmunitario do hóspede. Atopáronse resultados similares co virus da rabia, citomegalovirus, e VIH.[1]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 Llewelyn M, Cohen J (2002). "Superantigens: microbial agents that corrupt immunity". Lancet Infect Dis 2 (3): 156–62. PMID 11944185. doi:10.1016/S1473-3099(02)00222-0.
- ↑ 2,0 2,1 2,2 Schlievert PM (1982). "Enhancement of host susceptibility to lethal endotoxin shock by staphylococcal pyrogenic exotoxin type C". Infect. Immun. 36 (1): 123–8. PMC 351193. PMID 7042568. Arquivado dende o orixinal o 13 de decembro de 2019. Consultado o 06 de febreiro de 2013.
- ↑ Sriskandan S, Faulkner L, Hopkins P (2007). "Streptococcus pyogenes: Insight into the function of the streptococcal superantigens". Int. J. Biochem. Cell Biol. 39 (1): 12–9. PMID 17029999. doi:10.1016/j.biocel.2006.08.009.
- ↑ 4,0 4,1 4,2 4,3 Petersson K, Forsberg G, Walse B (2004). "Interplay between superantigens and immunoreceptors". Scand. J. Immunol. 59 (4): 345–55. PMID 15049778. doi:10.1111/j.0300-9475.2004.01404.x.
- ↑ 5,0 5,1 5,2 5,3 5,4 5,5 Mehindate K, Thibodeau J, Dohlsten M, Kalland T, Sékaly RP, Mourad W (1995). "Cross-linking of major histocompatibility complex class II molecules by staphylococcal enterotoxin A superantigen is a requirement for inflammatory cytokine gene expression". J. Exp. Med. 182 (5): 1573–7. PMC 2192187. PMID 7595227. doi:10.1084/jem.182.5.1573.
- ↑ 6,0 6,1 Papageorgiou AC, Tranter HS, Acharya KR (1998). "Crystal structure of microbial superantigen staphylococcal enterotoxin B at 1.5 A resolution: implications for superantigen recognition by MHC class II molecules and T-cell receptors". J. Mol. Biol. 277 (1): 61–79. PMID 9514739. doi:10.1006/jmbi.1997.1577.
- ↑ 7,0 7,1 7,2 7,3 7,4 Alouf JE, Müller-Alouf H (2003). "Staphylococcal and streptococcal superantigens: molecular, biological and clinical aspects". Int. J. Med. Microbiol. 292 (7–8): 429–40. PMID 12635926. doi:10.1078/1438-4221-00232.
- ↑ 8,0 8,1 Brouillard JN, Günther S, Varma AK; et al. (2007). "Crystal structure of the streptococcal superantigen SpeI and functional role of a novel loop domain in T cell activation by group V superantigens". J. Mol. Biol. 367 (4): 925–34. PMID 17303163. doi:10.1016/j.jmb.2007.01.024.
- ↑ 9,0 9,1 9,2 Buonpane RA, Moza B, Sundberg EJ, Kranz DM (2005). "Characterization of T cell receptors engineered for high affinity against toxic shock syndrome toxin-1". J. Mol. Biol. 353 (2): 308–21. PMID 16171815. doi:10.1016/j.jmb.2005.08.041.
- ↑ Li H, Llera A, Tsuchiya D; et al. (1998). "Three-dimensional structure of the complex between a T cell receptor beta chain and the superantigen staphylococcal enterotoxin B". Immunity 9 (6): 807–16. PMID 9881971. doi:10.1016/S1074-7613(00)80646-9.
- ↑ 11,0 11,1 11,2 Arcus VL, Proft T, Sigrell JA, Baker HM, Fraser JD, Baker EN (2000). "Conservation and variation in superantigen structure and activity highlighted by the three-dimensional structures of two new superantigens from Streptococcus pyogenes". J. Mol. Biol. 299 (1): 157–68. PMID 10860729. doi:10.1006/jmbi.2000.3725.
- ↑ 12,0 12,1 12,2 Watson AR, Lee WT (2006). "Defective T cell Receptor-mediated Signal Transduction in Memory CD4 T Lymphocytes Exposed to Superantigen or anti-T cell Receptor Antibodies". Cell. Immunol. 242 (2): 80–90. PMC 1829409. PMID 17083922. doi:10.1016/j.cellimm.2006.09.008.
- ↑ 13,0 13,1 Choi S, Schwartz RH (2007). "MOLECULAR MECHANISMS FOR ADAPTIVE TOLERANCE AND OTHER T CELL ANERGY MODELS". Semin. Immunol. 19 (3): 140–52. PMC 2045643. PMID 17400472. doi:10.1016/j.smim.2007.02.005.
- ↑ 14,0 14,1 Stiles BG, Krakauer (2005). "Staphylococcal Enterotoxins: a Purging Experience in Review, Part I". Clinical Microbiology Newsletter 27: 23.
- ↑ 15,0 15,1 15,2 Lussow AR, MacDonald HR (1994). "Differential effects of superantigen-induced "anergy" on priming and effector stages of a T cell-dependent antibody response". Eur. J. Immunol. 24 (2): 445–9. PMID 8299694. doi:10.1002/eji.1830240227.
- ↑ Miller C, Ragheb JA, Schwartz RH (1999). "Anergy and Cytokine-Mediated Suppression as Distinct Superantigen-Induced Tolerance Mechanisms in Vivo". J. Exp. Med. 190 (1): 53–64. PMC 2195559. PMID 10429670. doi:10.1084/jem.190.1.53.
- ↑ Yamaguchi M, Nadler S, Lee JW, Deeg HJ (1999). "Induction of negative regulators of haematopoiesis in human bone marrow cells by HLA-DR cross-linking". Transpl. Immunol. 7 (3): 159–68. PMID 10608299. doi:10.1016/S0966-3274(99)80035-5.
- ↑ Stauffer Y, Marguerat S, Meylan F; et al. (2001). "Interferon-alpha-induced endogenous superantigen. a model linking environment and autoimmunity". Immunity 15 (4): 591–601. PMID 11672541. doi:10.1016/S1074-7613(01)00212-6.
- ↑ 19,0 19,1 19,2 19,3 Jabara HH, Geha RS (1996). "The superantigen toxic shock syndrome toxin-1 induces CD40 ligand expression and modulates IgE isotype switching". Int. Immunol. 8 (10): 1503–10. PMID 8921429. doi:10.1093/intimm/8.10.1503.
- ↑ Diener K, Tessier P, Fraser J, Köntgen F, McColl SR (1998). "Induction of acute inflammation in vivo by staphylococcal superantigens I: Leukocyte recruitment occurs independently of T lymphocytes and major histocompatibility complex Class II molecules". Lab. Invest. 78 (6): 647–56. PMID 9645755.
- ↑ Van Cauwenberge P, Gevaert P, Van Hoecke H, Van Zele T, Bachert C. (2005). "New insights into the pathology of nasal polyposis: the role of superantigens and IgE". Verh K Acad Geneeskd Belg. 67 (5-28). PMID 15828304.
- ↑ Erlandsson E, Andersson K, Cavallin A, Nilsson A; et al. (2003). "Identification of the Antigenic Epitopes in Staphylococcal Enterotoxins A and E and Design of a Superantigen for Human Cancer Therapy". J. Mol. Biol. 333 (5): 893–905. PMID 14583188. doi:10.1016/j.jmb.2003.09.009.
- ↑ Cleary PP, McLandsborough L, Ikeda L, Cue D, Krawczak J, Lam H (1998). [hhttps://onlinelibrary.wiley.com/doi/full/10.1046/j.1365-2958.1998.00786.x "High-frequency intracellular infection and erythrogenic toxin A expression undergo phase variation in M1 group A streptococci"]. Mol. Microbiol. 28 (1): 157–67. PMID 9593304. doi:10.1046/j.1365-2958.1998.00786.x.
- ↑ Bachert C, Gevaert P, van Cauwenberge P (2002). "Staphylococcus aureus enterotoxins: a key in airway disease?". Allergy 57 (6): 480–7. PMID 12028112. doi:10.1034/j.1398-9995.2002.02156.x.
Véxase tamén[editar | editar a fonte]
Bibliografía[editar | editar a fonte]
- Superantigen Web Database at Birkbeck, University of London
- List of Superantigen ProteinsArquivado 18 de setembro de 2019 en Wayback Machine. from UniProt
- MeshName - Superantigens [1]
