Sinalización celular
A sinalización celular ou comunicación celular é unha parte do complexo sistema de comunicación que controla as actividades celulares básicas e coordina as accións celulares. As células comunícanse liberando moléculas, que chegan a receptores doutra célula e producen nela un efecto ou resposta. A capacidade das células de percibiren e responderen correctamente ao seu microambiente está na base do desenvolvemento, reparación de tecidos, inmunidade e homeostase dos tecidos. Os erros no procesamento da información celular son responsables de enfermidades como o cancro, autoinmunidade, e diabetes.
O traballo tradicional en bioloxía neste campo estaba enfocado ao estudo de partes concretas das vías de sinalización celular. A investigación en bioloxía de sistemas axúdanos a comprender a estrutura subxacente das redes de sinalización celular e como poden afectar os cambios nestas redes á transmisión e fluxo de información. Tales redes son sistemas complexos na súa organización e poden mostrar diversas propiedades emerxentes como a biestabilidade (con dous estados estables) e ultrasensibilidade. A regulación alostérica de amplo rango é a miúdo un compoñente significativo dos procesos de sinalización celular.[1]
Sinalización celular en organismos unicelulares e multicelulares[editar | editar a fonte]

A sinalización celular foi moi estudada no contexto de doenzas humanas e na sinalización entre células dun só organismo. Porén, a sinalización celular pode tamén ter lugar entre células de diferentes organismos.
En moitos mamíferos, as células do embrión nas súas fases iniciais intercambian sinais coas células do útero.[2] No tracto gastrointestinal humano, as bacterias intercambian sinais unhas con outras e coas células epiteliais e inmunitarias humanas.[3] Nos lévedos Saccharomyces cerevisiae durante o apareamento entre os tipos "a" e "alfa", algunhas células liberan un péptido de sinalización (factor de apareamento similar a unha feromona) no seu ambiente; o péptido do factor de apareamento pode unirse a un receptor da superficie celular doutras células de lévedo e indúceos a que se preparen para o apareamento.[4]
Tipos de sinais[editar | editar a fonte]
As células comunícanse por contacto directo (sinalización xustácrina), ou a curta distancia (sinalización parácrina), ou a gran distancia e/ou escala (sinalización endócrina).
Algunhas comunicacións célula-célula requiren o contacto directo entre elas. Algunhas células poden formar unións comunicantes que conectan o seu citoplasma co citoplasma das células adxacentes. No músculo cardíaco, as unións comunicantes entre células adxacentes permiten a propagación de potenciais de acción a partir da rexión do corazón que funciona como marcapasos cardíaco para que o potencial eléctrico se propague e cause a contracción coordinada do corazón.
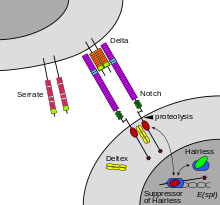
O mecanismo da sinalización de Notch é un exemplo de sinalización xustácrina (tamén chamada sinalización dependente do contacto) na cal dúas células adxacentes deben establecer contacto físico para comunicarse. Este requirimento dun contacto directo permite un control moi preciso da diferenciación celular durante o desenvolvemento embrionario. No verme Caenorhabditis elegans, dúas células da gónada en desenvolvemento teñen cada unha a mesma posibilidade de ou ben diferenciarse completamente ou ben converterse nunha célula precursora uterina que continúa dividíndose. A elección de cal das dúas células continuará dividíndose está controlada pola competición de sinais na superficie celular. Unha célula casualmente producirá máis cantidade dunha proteína da superficie celular que activa os receptores Notch da célula adxacente. Isto activa un sistema ou bucle de retroalimentación que reduce a expresión de Notch na célula que se diferenciará e que incrementa a cantidade de Notch na superficie da célula que continúa sendo unha célula troncal.[5]
Transpórtanse moitos outros sinais por moléculas que se liberan desde unha célula e se desprazan para facer contacto con outra célula. Os sinais endócrinos denomínanse hormonas. As hormonas son producidas polas células endócrinas e viaxan a través do sangue e chegan a todas partes do corpo. A especificidade da sinalización pode controlarse porque só algunhas das células poden responder a unha determinada hormona. Os sinais parácrinos como o ácido retinoico diríxense só ás células que están nas proximidades da célula emisora.[6] Os neurotransmisores son outro exemplo de sinal parácrino. Algunhas moléculas de sinalización poden funcionar tanto como hormonas coma como neurotransmisores. Por exemplo, a adrenalina (epinefrina) e a noradrenalina (norepinefrina) poden funcionar como hormonas cando se liberan da glándula suprarrenal e son transportadas ao corazón por vía sanguínea. A noradrenalina pode tamén producirse nas neuronas para funcionar como neurotransmisor no cerebro.[7] O estróxeno pode liberarse no ovario e funcionar como unha hormona ou actuar localizadamente por vía parácrina (nas células próximas) ou por sinalización autócrina (na mesma célula que a produciu).[8] As especies reactivas do osíxeno, como o óxido nítrico (NO) poden tamén actuar como mensaxeiros celulares. Este proceso denomínase sinalización redox.
Receptores para a a mobilidade celular e a diferenciación[editar | editar a fonte]
As células captan a información que envían as súas células veciñas por medio de proteínas, xeralmente de membrana, chamadas receptores. Por exemplo, Notch é unha proteína da superficie celular que funciona como receptor [9]. Os animais teñen un pequeno conxunto de xenes que codifican proteínas sinalizadoras que interaccionan especificamente cos receptores Notch e estimulan unha resposta nas células que expresan Notch na súa superficie. As moléculas que activan (ou, en certos casos inhiben) os receptores poden clasificarse como hormonas, neurotransmisores, citocinas, e factores de crecemento, e todos eles se denominan ligandos de receptores. Os detalles das interaccións ligando-receptor son fundamentais para a sinalización celular.
Como se mostra na figura 2 de máis arriba, no caso de Notch, esta actúa como un receptor para ligandos que se expresan en células adxacentes. Aínda que moitos receptores son proteínas de superficie, hai tamén receptores no interior das células. Por exemplo, o estróxeno é unha molécula hidrofóbica que pode pasar a través da bicapa lipídica da membrana plasmática. Os receptores de estróxenos intracelulares que se encontran en diversos tipos de células poden ser activados polos estróxenos producidos nos ovarios.
Existen diversos receptores transmembrana [10][11] específicos para pequenas moléculas e hormonas peptídicas [12] xunto con receptores intracelulares para as hormonas esteroides, que lle dan ás células a capacidade de responderen a un gran número de estímulos hormonais e farmacolóxicos. En certas enfermidades, é frecuentre que as proteínas que interaccionan cos receptores sexan activadas de forma anormal, orixinando vías de sinalización constitutivamente activadas.[13]
Para varios tipos de moléculas de sinalización intercelular que non poden atravesar a membrana celular hidrofóbica debido á súa natureza química hidrofílica, os receptores que son as súas dianas están expresados na membrana. Cando a molécula sinalizadora se une e activa ao seu receptor, o sinal xeramnelte é levado ao interior da célula por medio dunha molécula que funciona como segundo mensaxeiro, como o AMP cíclico.[14][15]
Tipos de ligandos[editar | editar a fonte]
Os ligandos que interveñen na sinalización celular poden clasificarse en tres tipos:
- Ligandos solubles, como hormonas, factores de crecemento, citocinas etc.
- Ligandos fixos na superficie doutra célula. As dúas células teñen que establecer contacto.
- Ligandos fixos na matriz extracelular.
Vías de sinalización[editar | editar a fonte]

A sinalización celular funciona normalmente por medio de rutas de activación secuencial de substancias, que se denominan vías de sinalización. Nalgúns casos, a activación do receptor causada pola unión a el do seu ligando está directamente combinada coa resposta celular ao ligando. Por exemplo, o neurotransmisor GABA pode activar un receptor da superficie celular que é parte dunha canle iónica. A unión do GABA a un receptor GABA A dunha neurona fai que se abra unha canle iónica selectiva para o cloruro que é parte do receptor. A activación do receptor GABA A permite que os ións cloruro cargados negativamente se movan cara ao interior da neurona, onde inhiben a capacidade da neurona de producir potenciais de acción. Porén, para moitos receptores da superficie celular, as interaccións ligando-receptor non están dunha forma directa ligadas á resposta celular, xa que esta ten lugar de forma indirecta. O receptor activado debe interaccionar primeiro con outras proteínas dentro da célula antes de que os efectos fisiolóxicos finais causados polo ligando produzan un determinado comportamento na célula. A miúdo, despois da activación do receptor altérase a actividade dunha cadea de varias proteínas celulares que interaccionan con outros compoñentes celulares. O conxunto completo de cambios inducidos pola activación do receptor denomínase vía de transdución de sinais.[16]
No caso da sinalización mediada por Notch, o mecanismo de transdución de sinais pode ser relativamente simple. Como se mostra na figura 2, a activación de Notch pode causar que a proteína Notch sexa alterada por unha protease. Parte da proteína Notch libérase da membrana superficial e toma parte na regulación xénica. A investigación da sinalización celular comprende o estudo das dinámicas espaciais e temporais dos receptores e dos compoñentes das vías de sinalización que son activados polos receptores en diversos tipos celulares.[17]
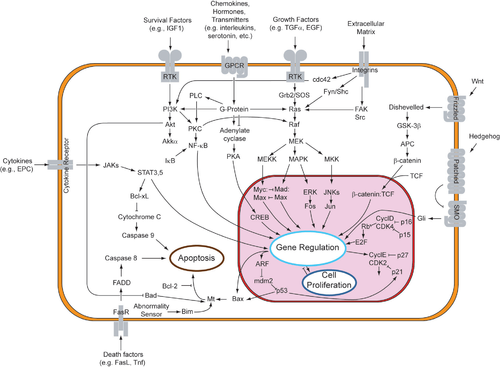
Unha vía máis complexa de transdución de sinais é a que se mostra na figura 3. Esta vía implica cambios nas interaccións proteína-proteína dentro da célula, inducidas por un sinal externo. Moitos factores de crecemento únense aos receptores na superficie celular e estimulan que as células avancen nas sucesivas fases do ciclo celular e se dividan. Varios destes receptores son quinases que empezan a fosforilarse elas mesmas e a outras proteínas cando se unen a un ligando. Esta fosforilación pode xerar un sitio de unión para unha proteína diferente e así induce unha interacción proteína-proteína. Na figura 3, o ligando (chamado factor de crecemento epidérmico ou EGF) únese ao receptor (chamado EGFR). Este actíva o receptor para que se autofosforile. O receptor fosforilado únese a unha proteína adaptadora (GRB2), a cal transmite o sinal aos procesos de sinalización posteriores da vía. Por exemplo, unha das vías de transdución de sinais que se activan é a chamada vía da proteína quinase activada por mitóxeno (vía MAPK). O compoñente da transdución de sinais denominado "MAPK" na vía foi inicialmente chamado "ERK," polo que a vía se chama vía MAPK/ERK. A proteína MAPK é un encima proteína quinase que pode unir fosfatos a proteínas diana como o factor de transcrición MYC e, deste xeito, alterar a transcrición de xenes e, finalmente, a progresión do ciclo celular. Actívanse moitas proteínas celulares nos pasos seguintes das vías dos receptores dos factores de crecemento (como EGFR) que inician esta vía de transdución de sinais.[18]
Algunhas vías de transdución de sinais responden de forma diferente, dependendo da cantidade de sinalización recibida pola célula. Por exemplo, a proteína hedgehog ("ourizo") activa diferentes xenes, dependendo da cantidade de proteína hedgehog presente.[19]
As vías de transdución de sinais de multicompoñentes complexos proporcionan oportunidades para a retroalimentación, amplificación do sinal, e interaccións dentro dunha célula entre diversos sinais e vías de sinalización.
Clasificación da comunicación intercelular[editar | editar a fonte]
En endocrinoloxía (que estuda a sinalización intercelular nos animais) a sinalización intercelular pode ser dos seguintes tipos:
- Intrácrina. Os sinais son producidos e actúan dentro da propia célula diana.
- Autócrina. Os sinais teñen como diana a propia célula que os produciu e funcionan saíndo da célula e uníndose a un receptor de membrana. Algunhas veces os sinais das células autócrinas poden chegar a outras células veciñas próximas sempre que sexan do mesmo tipo ca a que produciu o sinal. Un exemplo son as células inmunitarias. Moitas células en crecemento como as células do embrión ou as células cancerosas producen factores de crecemento e os receptores para eses mesmos factores e así perpetúan a súa proliferación, controlada no caso do embrión e descontrolada no caso do cancro.
- Xustácrina. É a comunicación por contacto entre dúas células ou coa matriz extracelular, por medio de moléculas de adhesión celular. A adhesión entre células homólogas (do mesmo tipo) é fundamental para o control do crecemento celular e a formación dos tecidos; entre células heterólogas (diferentes) é tamén moi importante para o recoñecemento que realiza o sistema inmune. Os sinais son transmitidos polas membranas celulares por medio de proteínas ou lípidos que son compoñentes integrais das membranas e que poden afectar ás células emisoras ou a células en contacto con elas, ou por medio de unións comunicantes.
- Parácrina. As células diana están relativamente próximas á célula emisora, sen que exista unha estrutura especializada como a sinapse (nese caso falariamos de neurotransmisión). Trátase dunha comunicación local. Realízase por medio de mensaxeiros químicos peptídicos como citocinas, factores de crecemento, neurotrofinas ou derivados do ácido araquidónico como prostaglandinas, tromboxanos e leucotrienos. Algunhas hormonas poden funcionar de modo endócrino ou parácrino. Tamén por histamina e outros aminoácidos.
- Endócrina. Os sinais chegan a células diana que están a bastante distancia. As células endócrinas, situadas en glándulas endócrinas especializadas, producen hormonas que viaxan polo sangue e chegan a todas as partes do corpo, e únense só ás células que teñan receptores para elas, que poden estar a gran distancia.
Comunicación nerviosa: sinapse e células neuroendócrinas[editar | editar a fonte]
Un tipo especial de comunicación celular, que no seu funcionamento é xeralmente similar á de tipo parácrino, pero que require estruturas especializadas (terminal sináptico, unión neuromuscular) é a comunicación nerviosa ou neurotransmisión, que é de tipo electroquímico. A despolarización do axón da neurona chega á sinapse, onde un pequeno espazo ou fenda sináptica separa unha neurona da seguinte, e alí vértense neurotransmisores, que chegan a receptores da outra neurona (postsináptica), onde producen despolarizacións e unha resposta. Nas unións neuromusculares existe unha estrutura especial chamada placa motora na que o vertido dun neurotransmisor por parte dunha neurona, activa os receptores da célula muscular, provocando a súa contracción.
Algunhas neuronas, ademais de transmitir o impulso nervioso, realizan unha función neuroendócrina, xa que verten hormonas fóra da sinapse, que chegan por vía sanguínea ás células diana e ás veces de forma parácrina. Estas neurohormonas son distintas dos neurotransmisores, pero ás veces poden ser os propios neurotransmisores, que actúan fóra da sinapse.
Notas[editar | editar a fonte]
- ↑ Bu Z, Callaway DJ (2011). "Proteins MOVE! Protein dynamics and long-range allostery in cell signaling". Advances in Protein Chemistry and Structural Biology. Advances in Protein Chemistry and Structural Biology 83: 163–221. ISBN 978-0-12-381262-9. PMID 21570668. doi:10.1016/B978-0-12-381262-9.00005-7.
- ↑ Mohamed OA, Jonnaert M, Labelle-Dumais C, Kuroda K, Clarke HJ, Dufort D (2005). "Uterine Wnt/β-catenin signaling is required for implantation". Proc Natl Acad Sci U.S.A. 102 (24): 8579–84. PMC 1150820. PMID 15930138. doi:10.1073/pnas.0500612102.
- ↑ Clarke MB, Sperandio V (2005). "Events at the host-microbial interface of the gastrointestinal tract III. Cell-to-cell signaling among microbial flora, host, and pathogens: there is a whole lot of talking going on". Am. J. Physiol. Gastrointest. Liver Physiol. 288 (6): G1105–9. PMID 15890712. doi:10.1152/ajpgi.00572.2004.
- ↑ Lin JC, Duell K, Konopka JB (2004). "A Microdomain Formed by the Extracellular Ends of the Transmembrane Domains Promotes Activation of the G Protein-Coupled α-Factor Receptor". Mol Cell Biol 24 (5): 2041–51. PMC 350546. PMID 14966283. doi:10.1128/MCB.24.5.2041-2051.2004.
- ↑ Greenwald I (1998). "LIN-12/Notch signaling: lessons from worms and flies". Genes Dev 12 (12): 1751–62. PMID 9637676. doi:10.1101/gad.12.12.1751.
- ↑ Duester G (2008). "Retinoic Acid Synthesis and Signaling during Early Organogenesis". Cell 134 (6): 921–31. PMC 2632951. PMID 18805086. doi:10.1016/j.cell.2008.09.002.
- ↑ Cartford MC, Samec A, Fister M, Bickford PC (2004). "Cerebellar norepinephrine modulates learning of delay classical eyeblink conditioning: Evidence for post-synaptic signaling via PKA". Learn Mem 11 (6): 732–7. PMC 534701. PMID 15537737. doi:10.1101/lm.83104.
- ↑ Jesmin S, Mowa CN, Sakuma I; et al. (2004). "Aromatase is abundantly expressed by neonatal rat penis but downregulated in adulthood" (PDF). J Mol Endocrinol 33 (2): 343–59. PMID 15525594. doi:10.1677/jme.1.01548. Arquivado dende o orixinal (PDF) o 11 de setembro de 2018. Consultado o 10 de setembro de 2018.
- ↑ Artavanis-Tsakonas, Spyros et al. (1999-04-30). "Notch Signaling: Cell Fate Control and Signal Integration in Development (Review)". Science 284 (5415): 770–776. Bibcode 1999Sci...284..770A. doi:10.1126/science.284.5415.770. PMID 10221902.
- ↑ Domazet I, Holleran BJ, Martin SS, Lavigne P, Leduc R, Escher E, Guillemette G (2009-05-01). "The Second Transmembrane Domain of the Human Type 1 Angiotensin II Receptor Participates in the Formation of the Ligand Binding Pocket and Undergoes Integral Pivoting Movement during the Process of Receptor Activation". J Biol Chem 284 (18): 11922–9. PMC 2673261. PMID 19276075. doi:10.1074/jbc.M808113200.
- ↑ Hislop JN, Henry AG, Marchese A, von Zastrow M (2009-07-17). "Ubiquitination Regulates Proteolytic Processing of G Protein-coupled Receptors after Their Sorting to Lysosomes". J Biol Chem 284 (29): 19361–70. PMC 2740561. PMID 19433584. doi:10.1074/jbc.M109.001644.
- ↑ Meng H, Zhang X, Hankenson KD, Wang MM (2009-03-20). "Thrombospondin 2 Potentiates Notch3/Jagged1 Signaling". J Biol Chem 284 (12): 7866–74. PMC 2658079. PMID 19147503. doi:10.1074/jbc.M803650200.
- ↑ Copland JA, Sheffield-Moore M, Koldzic-Zivanovic N, Gentry S, Lamprou G, Tzortzatou-Stathopoulou F, Zoumpourlis V, Urban RJ, Vlahopoulos SA (2009 Jun). "Sex steroid receptors in skeletal differentiation and epithelial neoplasia: is tissue-specific intervention possible?". BioEssays 31 (6): 629–41. PMID 19382224. doi:10.1002/bies.200800138.
- ↑ Goh SL, Looi Y, Shen H, Fang J, Bodner C, Houle M, Ng AC, Screaton RA, Featherstone M (2009-07-10). "Transcriptional Activation by MEIS1A in Response to Protein Kinase A Signaling Requires the Transducers of Regulated CREB Family of CREB Co-activators". J Biol Chem 284 (28): 18904–12. PMC 2707216. PMID 19473990. doi:10.1074/jbc.M109.005090.
- ↑ Wojtal KA, Hoekstra D, Van IJzendoorn SC (2008 Feb). "cAMP-dependent protein kinase A and the dynamics of epithelial cell surface domains: moving membranes to keep in shape". BioEssays 30 (2): 146–55. PMID 18200529. doi:10.1002/bies.20705.
- ↑ Dinasarapu AR,Saunders B,Ozerlat I,Azam K, and Subramaniam S (2011). "Signaling gateway molecule pages—a data model perspective". Bioinformatics 27 (12): 1736–1738. PMC 3106186. PMID 21505029. doi:10.1093/bioinformatics/btr190.
- ↑ Oswald F, Täuber B, Dobner T, Bourteele S, Kostezka U, Adler G, Liptay S, Schmid RM (November 2001). "p300 acts as a transcriptional coactivator for mammalian notch-1". Mol. Cell. Biol. 21 (22): 7761–74. doi:10.1128/MCB.21.22.7761-7774.2001. PMC 99946. PMID 11604511. //www.ncbi.nlm.nih.gov/pmc/articles/PMC99946/.
- ↑ Herbst RS (2004). "Review of epidermal growth factor receptor biology". Int. J. Radiat. Oncol. Biol. Phys. 59 (2 Suppl): 21–6. doi:10.1016/j.ijrobp.2003.11.041. PMID 15142631.
- ↑ Ingham, P. W.; McMahon, AP (2001). "Hedgehog signaling in animal development: Paradigms and principles". Genes & Development 15 (23): 3059–87. doi:10.1101/gad.938601. PMID 11731473.
Bibliografía[editar | editar a fonte]
- Handbook of Cell Signaling / editado por Ralph Bradshaw e Edward Dennis. Academic Press, 2009. ISBN 0-12-374145-9
- Cox, Rody P., 1926-). [1974]. Cell communication, edited by Rody P. Cox. Nova York, Wiley. ISBN 0-471-18135-8
- Cell communication in health and disease : readings from Scientific American magazine / edited by Howard Rasmussen. Nova York : Freeman, c1991. xii, 185 p. : ill. (some col.) ; 24 cm. ISBN 0-7167-2224-0
- Cell communication in nervous and immune system / [edited by] Eckart D. Gundelfinger, Constanze I. Seidenbecher, Burkhart Schraven. 1st ed. Nova York : Springer, 2006. ISBN 3-540-36828-0.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Signaling Gateway Free summaries of recent research and the Molecule Pages database.
- Protein signalling domains
- NCI-Nature Pathway Interaction Database: authoritative information about signaling pathways in human cells.
