Complexo maior de histocompatibilidade
O complexo maior de histocompatibilidade (CMH), abreviado xeralmente como MHC (do seu nome en inglés, major histocompatibility complex) e tamén chamado nalgunhas fontes complexo principal de histocompatibilidade[1], é unha molécula proteica da superficie celular codificada por unha gran familia de xenes presente en todos os vertebrados, que é fundamental para o funcionamento do sistema inmunitario. As proteínas MHC median as interaccións entre os distintos leucocitos, que son as células inmunitarias, e entre estes e outras células. O MHC é fundamental para a presentación de antíxenos que activa o sistema inmunitario, e determina a compatibilidade entre doante e receptor no transplante de órganos, e a susceptibilidade de sufrir unha enfermidade autoinmune por inmunización por reacción cruzada.
Por razóns históricas, nos humanos o MHC tamén se chama "antíxeno leucocitario humano" ou HLA (human leukocyte antigen). Nos humanos, os xenes MHC forman o denominado sistema HLA, porque estas proteínas se descubriron como antíxenos nos leucocitos, que podían detectarse con anticorpos.
Na presentación do antíxeno primeiro as proteínas que entran no corpo e as propias da célula son procesadas dentro da célula e divididas, e un fragmento delas (epítopo) será exposto (presentado) na superficie celular unido ás moléculas do MHC, onde pode ser recoñecido polos linfocitos.[2] O antíxeno presentado pode ser recoñecido como "propio" ou "non propio".
A familia de xenes MHC divídese en tres subgrupos ou clases: clase I, clase II, e clase III. A diversidade observada na presentación dos antíxenos, que está mediada polos MHC das clases I e II, conséguese de múltiples maneiras: (1) a codificación xenética dos MHC é polixénica, (2) os xenes MHC son moi polimórficos e teñen moitas variantes ou alelos, (3) varios xenes MHC exprésanse a partir dos dous alelos que se herdaron.
O MHC na inmunidade animal[editar | editar a fonte]
Das tres clases de MHC identificadas, as máis importantes nos humanos son as das clases I e II. O MHC de clase II media a inmunidade a un antíxeno específica de inmunización. O MHC de clase I media a destrución das células hóspede que leven ese antíxeno.
Algúns leucocitos maduros da liñaxe dos linfocitos residentes en tecidos linfoides periféricos, como os ganglios linfáticos, levan receptores que se unen ao MHC. Co MHC interaccionan as células T, que son linfocitos que interveñen na inmunidade específica, e as células asasinas naturais ou NK, que son linfocitos que actúan de forma innata. Cando a expresión dos MHC de clase I é baixa en conxunto, o que suxire un funcionamento anormal, as células NK estimulan a morte celular programada da célula. (As células B, que son os outros linfocitos que median na inmunidade específica, segregan anticorpos, pero non se ligan ao MHC.)
Aínda que o MHC de clase II pode expresarse condicionalmente en todos os tipos celulares, o normal é que só apareza nas células presentadoras de antíxenos "profesionais", como son: macrófagos, células B, e especialmente células dendríticas. Unha célula presentadora de antíxenos capta un antíxeno, realiza o procesamento do antíxeno no que este é dividido en cachos, e devolve un fragmento da molécula do antíxeno (o epitotpo) á superficie da célula presentadora unido a unha molécula do MHC de clase II. O MHC de clase II realiza así a presentación do antíxeno que está unido a el. Na presentación ten lugar un dobre contacto: os receptores CD4 que levan na súa superficie as células T axudantes virxes únense ao MHC de clase II, mentres que o epítopo unido á molécula do MHC de clase II se une ao receptor de células T (TCR) da célula T axudante virxe. A célula T axudante pode ser de tipo 1 (Th1), tipo 2 (Th2), tipo 17 (Th17), ou de fenotipo regulatorio (Treg). Deste modo o MHC de clase II media a inmunización para un determinado antíxeno ou, se intervén un linfocito Treg, media a inmunotolerancia.
Os MHC de clase I aparecen en todas as células nucleadas do corpo (basicamente todas menos os glóbulos vermellos, que perden o núcleo durante a súa maduración, e non os presentan ou só moi escasamente[3]). O MHC de clase I fai a presentación de epítopos ás células T citotóxicas, tamén chamadas células T asasinas, que expresan a molécula CD8. Cando o seu CD8 se une ao MHC de clase I, se o seu TCR recoñece o epítopo que encaixa con el, a célula T asasina induce a apoptose da célula. Así, o MHC de clase I media na inmunidade celular. (As células B expresan o MHC de clase II para presentar o antíxeno a linfocitos Th0, pero cando o seu receptor de células B se une ao epítopo que encaixa con el (interacción na que non media o MHC), a célula B activada segrega inmunoglobulinas solubles, é dicir, anticorpos, dos que depende a inmunidade humoral.)
Xenes MHC[editar | editar a fonte]
A rexión do brazo curto do cromosoma 6 humano que contén os xenes do MHC posúe a información que codifica o seguinte:
- certas glicoproteínas da membrana plasmática implicadas nos mecanismos de presentación e procesamento de antíxenos aos linfocitos T chamadas α e β. Agrúpanse nos xenes de clase II (que codifican as proteínas MHC-II) e os xenes de clase I (que codifican as proteínas MHC-I)
- citocinas e proteínas do sistema do complemento, importantes na resposta inmunolóxica, mais que non teñen nada que ver cos xenes do MHC; estes xenes agrúpanse na clase III.
Ambos os tipos de moléculas participan na resposta inmunitaria, que permite a identificación das moléculas propias e das estrañas (invasoras), para eliminar estas últimas mediante diferentes mecanismos.
Encóntranse familias de xenes MHC en todos os vertebrados, aínda que a súa cantidade varía amplamente, e as galiñas teñen o menor número coñecido de rexións MHC (19 xenes). Nos humanos a rexión MHC está situada no cromosoma 6, entre os marcadores xenéticos MOG e COL11A2 (desde 6p22.1 a 6p21.3 ~29Mb a 33Mb no conxunto hg19), e contén 140 xenes que ocupan 3,6 megapares de bases (3,6 Mb ou 3 600 000 bases).[4] Arredor da metade teñen funcións inmunitarias coñecidas.
Os mesmos marcadores no opóssum Monodelphis domestica, un marsupial, esténdense 3,95 Mb e teñen 114 xenes, 87 deles compartidos cos humanos.[5] A variación xenotípica do MHC marsupial é intermedia entre a dos mamíferos euterios e a das aves, pero é máis próxima en organización á dos non mamíferos, e os xenes do MHC de clase I dos marsupiais sufriron unha amplificación na rexión da clase II, orixinando unha rexión clase I/II única.[5]
A clase III funciona de xeito moi diferente das outras dúas clases, pero o seu locus xenético está entre os das outras dúas clases (nos humanos no cromosoma 6) e xeralmente se trata deles en conxunto.
| Clase | Codificación | Expresión |
| I | (1) proteínas de unión ao péptido, que seleccionan secuencias curtas de aminoácidos para a presentación do antíxeno, e (2) moléculas que axudan no procesamento do antíxeno (como o TAP e a tapasina). | Unha cadea, chamada α, cuxos ligandos son o receptor CD8 (que levan as células T citotóxicas) e receptores inhibitorios que levan as células NK. |
| II | (1) proteínas de unión ao péptido e (2) proteínas que axudan a cargar o antíxeno nas proteínas de unión ao péptido do MHC de clase II (como MHC II DM, MHC II DQ, MHC II DR, e MHC II DP). | Dúas cadeas, chamadas α e β, cuxos ligandos son os receptores CD4 que levan as células T axudantes. |
| III | Outras proteínas inmunitarias que non interveñen no procesamento e presentación do antíxeno, como os compoñentes do sistema do complemento (por exemplo, C2, C4, factor B), as citocinas de sinalización inmunitaria (como o TNF-α), e proteínas de choque térmico que protexen as células dos estreses. | Varias. |
Proteínas MHC[editar | editar a fonte]
As proteínas MHC teñen unha estrutura similar á das inmunoglobulinas. Poden ser:
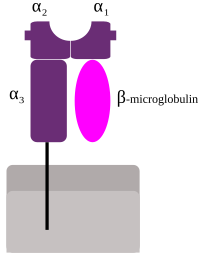

Clase I[editar | editar a fonte]
- Artigo principal: MHC de clase I.
O MHC I é unha glicoproteína chamada cadea α que está unida á pequena proteína β2 microglobulina. A cadea α está composta por tres dominios: α1, α2, α3. O α1 está situado sobre a β2 microglobulina (que non é unha proteína de tipo MHC e está codificada no cromosoma 15 humano). A subunidade α3 é transmembrana, e mantén ancorado o MHC de clase I á membrana plasmática. O péptido que vai ser presentado é sostido polo fondo da fenda ou suco de unión ao péptido, na rexión central do heterodímero α1/α2. A secuencia xeneticamente codificada e expresada de aminoácidos, do fondo do suco de unión ao péptido é a que determina os péptidos específicos que se poden unir alí.[6]
As moléculas MHC clásicas presentan os epítopos aos TCRs dos linfocitos T CD8+. As moléculas non clásicas (MHC de clase IB) mostran limitados polimorfismo, patróns de expresión, e de antíxenos presentados; este grupo subdivídese nun grupo codificado nos loci MHC (como HLA-E, -F, -G) e noutros que non (como ligandos de estrés como ULBPs, Rae1, H60); o antíxeno/ligando para moitas destas moléculas non se coñece, pero poden interaccionar tanto con células T CD8+ coma con células NKT e células NK.
Clase II[editar | editar a fonte]
- Artigo principal: MHC de clase II.
O MHC de clase II está formado por dúas cadeas, α e β, cada unha das cales ten dous dominios, chamados α1 e α2 e β1 e β2, respectivamente, e cada cadea ten un dominio transmembrana, o α2 e o β2, que mantén ancorada a molécula do MHC de clase II á membrana plasmática.[7] Ambas as dúas son glicoproteínas. O suco de unión ao péptido está formado por un heterodímero de α1 e β1.
As moléculas do MHC de clase II humanas teñen de 5 a 6 isotipos. As moléculas clásicas fan a presentación de péptidos a linfocitos CD4+. As moléculas non clásicas, accesorias e con funcións intracelulares, non están expostas nas membranas plasmáticas, senón en membranas internas nos lisosomas, normalmente cargan os péptidos antixénicos nas moléculas MHC de clase II clásicas.
Clase III[editar | editar a fonte]
As moléculas de clase III teñen funcións fisiolóxicas, a diferenza das clases I e II, pero están codificadas entre elas no brazo curto do cromosoma 6 humano. As moléculas de clase III inclúen varias proteínas segregadas con funcións inmunes: compoñentes do sistema do complemento (como C2, C4, e factor B), citocinas (como TNF-α, LTA, LTB), e proteínas de choque térmico (hsp).
Presentación e procesamento do antíxeno[editar | editar a fonte]

Os péptidos son procesados e presentados utilizando dúas rutas clásicas:
- Nos fagocitos con MHC de clase II como os macrófagos e células dendríticas inmaturas cáptanse elementos externos por fagocitose e son introducidos en fagosomas (pero as células B utilizan a forma máis xeral de endocitose en endosomas), que se fusionan con lisosomas cuxos encimas que funcionan a pH ácido clivan as proteínas captadas dividíndoas en moitos péptidos. Por medio de dinámica fisicoquímica na interacción molecular con determinadas variantes do MHC de clase II que ten o hóspede (codificados no xenoma do hóspede) un determinado péptido mostrará inmunodominancia e será cargado na molécula do MHC de clase II. Estes péptidos son levados e expostos no exterior na superficie celular.[8]
- No caso do MHC de clase I calquera célula nucleada presentará normalmente péptidos citosólicos, principalmente péptidos propios derivados do recambio das proteínas da célula e de produtos ribosómicos defectuosos. Durante as infeccións virais, as infeccións por microorganismos intracelulares, ou nas transformacións canceríxenas, estas proteínas son degradadas no proteasoma e son tamén cargadas nas moléculas do MHC de clase I e expostas na superficie celular. Para que os linfocitos T poidan detectar un péptido exposto na superficie celular abonda con que só estea unido a do 0,1% ao 1% das moléculas MHC.
| Características | Ruta MHC-I | Ruta MHC-II |
|---|---|---|
| Composición do complexo péptido-MHC estable | Cadea α polimórfica e β2 microglobulina, péptido unido á cadea α | Cadeas α e β polimórficas, o péptido únese a ambas as dúas |
| Tipos de células presentadoras do antíxeno (APC) | Todas as células nucleadas | células dendríticas, fagocitos mononucleares, linfocitos B, algunhas células endoteliais, epitelio do timo |
| Linfocitos T capaces de responder | linfocitos T citotóxicos (CD8+) | linfocitos T axudantes (CD4+) |
| Orixe das proteínas antixénicas | Proteínas citosólicas (principalmente sintetizadas pola célula) ; poden tamén entrar desde o medio extracelular por medio de fagosomas | Proteínas presentes en endosomas ou lisosomas (principalmente internalizadas desde o medio extracelular) |
| Encimas responsables da xeración de péptidos | Proteasoma citosólico | Proteases dos endosomas e lisosomas (por exemplo, catepsina) |
| Localización da carga do péptido na molécula MHC | Retículo endoplasmático | Compartimentos vesiculares especializados |
| Moléculas implicadas no transporte de péptidos e na súa carga nas moléculas MHC | Transportador asociado co procesamento do antíxeno (TAP) | DM, cadea invariante |
Restrición no recoñecemento dos linfocitos T[editar | editar a fonte]
No seu desenvolvemento no timo, os linfocitos T son seleccionados para recoñeceren moléculas do MHC do hóspede pero non para recoñecer outros antíxenos propios. Despois da selección, cada linfocito T mostra unha especificidade dual: o receptor de células T (TCR) recoñece os MHC propios pero só os antíxenos non propios.
A restrición do MHC ocorre durante o desenvolvemento do linfocito no timo por medio dun proceso chamado selección posititva. As células T poden agora recibir un sinal positivo de supervivencia mediado principalmente por células epiteliais do timo que lles presentan péptidos propios unidos a moléculas do MHC. Os linfocitos T que non reciben este sinal no seu receptor de células T (TCR) sofren apoptose. A selección positiva asegura que as células T maduras poden recoñecer funcionalmente moléculas do MHC na periferia (é dicir noutras partes do corpo, fóra do timo).
Os TCRs dos linfocitos T recoñecen só epítopos secuenciais, tamén chamados epítopos lineares, soamente de péptidos e soamente se están acoplados ás moléculas do MHC. (Por outra parte, os anticorpos segregados polas células B activadas únense a diversos epítopos, como peptidos, lípidos, carbohidratos, e ácidos nucleicos, e recoñecen epítopos conformacionais, os cales teñen unha estrutura tricimensional.)
O MHC na selección da parella sexual[editar | editar a fonte]
As moléculas do MHC fan posible que o sistema inmunitario exerza unha vixilancia sobre o conxunto de moléculas proteicas da célula hóspede, e unha maior diversidade do MHC permitirá unha maior diversidade na presentación do antíxeno. En 1976 Yamazaki et al demostraron que existía unha preferencia dos ratos macho a elixir para o apareamento a femias con distintos MHC. Obtivéronse resultados similares con especies de peixes [9] e aves.[10] Algúns datos sinalan que hai menores taxas de abortos espontáneos en parellas humanas con xenes MHC diferentes.[11]
Propúxose que o MHC está relacionado coa elección de parella nalgunhas poboacións humanas, unha teoría que está apoiada en estudos feitos por Ober e colegas en 1997,[12] e por Chaix e colegas en 2008.[13] O fenómeno podería estar mediado polo olfacto, xa que o fenotipo MHC parece estar moi implicado na forza e sensación pracenteira dos compostos olorosos percibidos presentes na suor. Os ésteres de ácidos graxos, como o metil undecanoato, metil decanoato, metil nonanoato, metil octanoato e metil hexanoato, que forman parte dos olores corporais, mostran unha forte conexión co MHC.[14]
En 1995 Claus Wedekind encontrou que nun grupo de mulleres estudantes universitarias ás que se lle fixo cheirar camisetas suadas usadas por estudantes masculinos durante dúas noites (sen desodorizante, colonias ou xabóns aromáticos), estas, con grande diferenza, elixían camisetas que foran usadas por homes con MHCs diferentes, unha preferencia que se invertía se as mulleres estaban tomando contraceptivos orais.[15] Os resultados dun experimento de 2002 suxiren igualmente que os cheiros asociados cos alelos HLA (outra denominación do MHC) inflúen na preferencia polo olor e poden mediar sinais sociais.[16] En 2005 nun grupo de 58 suxeitos, as mulleres estaban máis indecisas cando se lles presentaba a homes con MHCs iguais aos seus,[17] aínda que se tomaban contraceptivos orais as mulleres mostraron preferencia polos MHC similares aos seus, e se non os tomaban non mostraban ningunha preferencia especial.[18]
O MHC e a diversidade evolutiva[editar | editar a fonte]
A maioría dos mamíferos teñen variantes do MHC similares ás dos humanos, os cales posúen unha gran diversidade alélica para eses xenes, especialmente entre os nove xenes clásicos (seguramente debido en grande medida a duplicación xénica), aínda que as rexións MHC humanas teñen moitos pseudoxenes. Os loci máis diversos, principalmente HLA-A, HLA-B, e HLA-DRB1, teñen aproximadamente 1000, 1600, e 870 alelos coñecidos, respectivamente. Moitos alelos HLA son antigos, ás veces con maior homoloxía cos do chimpancé que con algúns outros alelos humanos do mesmo xene.
A explicación da gran diversidade alélica do MHC foi un reto para os biólogos evolutivos. A maioría postulan unha selección balanceada (ver polimorfismo (bioloxía)), que é un proceso de selección natural na que ningún alelo único é considerado de forma absoluta como o máis vantaxoso, tal como a selección dependente da frecuencia e a vantaxe do heterocigoto. Modelos recentes suxiren que non é posible manter un alto número de alelos só por vantaxe dos heterocigotos.
Unha contrahipótese é a coevolución patoxénica, que postula que os alelos comúns son os que están baixo a maior presión patoxénica, orixinándose por este motivo unha selección positiva de alelos raros, que son brancos máis difíciles para os patóxenos. A medida que decrece a presión patoxénica sobre os alelos que previamente eran comúns, a súa frecuencia na poboación estabilízase, e permanecen circulando nunha ampla poboación. A pesar do gran polimorfismo do MHC a nivel de poboación, un individuo leva como moito 18 alelos MHC I ou MHC II.
Observouse unha diversidade relativamente baixa do MHC no guepardo (Acinonyx jubatus),[19] no castor (Castor fiber),[20] e no panda xigante (Ailuropoda melanoleuca).[21] En 2007 atribuíuselle á baixa diversidade do MHC un papel na susceptibilidade á enfermidade do demo de Tasmania (Sarcophilus harrisii), nativo da illa de Tasmania, que ten como consecuencia que un antíxeno dun tumor transmisible, implicado na enfermidade tumoral facial do demo, parece que é recoñecido como un antíxeno propio.[22] Para compensar a endogamia, suxeriuse facer esforzos para manter a diversidade xenética nas poboacións de especies en perigo e de animais en catividade.
O MHC no rexeitamento de transplantes[editar | editar a fonte]
Nos transplantes de órganos, tecidos e células nai é importante controlar os tipos de moléculas MHC de doante e receptor, xa que debido á variabilidade que teñen xeralmente non coinciden. As moléculas do MHC actúan como antíxenos e poden provocar respostas inmunitarias no receptor, o que orixina o rexeitamento do transplante. As moléculas MHC foron identificadas e nomeadas polo seu papel no rexeitamento dos transplantes de órganos entre ratos de distintas cepas, aínda que se tardou uns 20 anos en comprender o papel do MHC na presentación dos antíxenos peptídicos aos linfocitos T citotóxicos.[23]
Todas as células humanas expresan seis alelos MHC de clase I (un alelo HLA-A, -B, e -C de cada proxenitor) e de seis a oito alelos MHC de clase II (un alelo HLA-DP e -DQ, e un ou dous HLA-DR de cada proxenitor, e combinacións deles). A variación no MHC nas poboacións humanas é alta, e hai polo menos 350 alelos para os xenes HLA-A, 620 alelos para os HLA-B, 400 alelos para DR, e 90 para DQ. Dúas persoas calquera que non sexan xemelgos idénticos expresan diferentes moléculas MHC. Todas as moléculas MHC poden mediar no rexeitamento de transplantes, pero o HLA-C e o HLA-DP son menos importantes porque mostran un baixo polimorfismo.
Cando maduran no timo, os linfocitos T son seleccionados segundo a capacidade dos seus receptores de superficie característicos (receptor de células T ou TCR) de recoñecer antíxenos propios. Porén, os linfocitos T poden reaccionar contra o suco de unión ao péptido dos MHC do doante, a rexión variable do MHC onde leva o epítopo do antíxeno presentado para o recoñecemento do TCR, que é o parátopo que encaixa con el. Os linfocitos T do receptor consideran o suco de unión ao péptido incompatible como un antíxeno non propio. O recoñecemento polos linfocitos T dos MHC alleos como propios denomínase alorrecoñecemento.
O rexeitamento de transplantes pode ser de dous tipos, que están mediados polo MHC (HLA):
- Rexeitamento hiperagudo. Ocorre cando, antes do transplante, o receptor fabricou antiocorpos anti-HLA, probablemente porque recibiu previamente transfusións de sangue (un tecido doante que contén linfocitos que expresan moléculas HLA), ou ben por xeración de anticorpos anti-HLA durante o embarazo (dirixidos aos HLA do pai expresados polo feto), ou por transplantes anteriores.
- Rexeitamento humoral agudo e disfunción crónica. Ocorre cando se forman anticorpos anti-HLA do receptor dirixidos contra as moléculas HLA presentes nas células endoteliais do tecido transplantado.
Nesas situacións, a resposta inmunitaria diríxese contra o órgano transplantado, orixinando lesións. A proba de reacción cruzada entre células doantes potenciais e o soro do receptor serve para detectar a presenza de anticorpos anti-HLA no receptor potencial que recoñecen as moléculas HLA do doante, o que prevén un rexeitamento hiperagudo. En circunstancias normais, avalíase a compatibilidade entre as moléculas HLA-A, -B, e -DR. Canto maior é o número de incompatibilidades, menor é a taxa de supervivencia a cinco anos. As bases de datos globais con información dos doantes facilitan a procura de doantes compatibles.
A terminoloxía HLA[editar | editar a fonte]

Os MHC das clases I e II humanos denomínanse tamén antíxeno leucocitario humano (HLA). Para clarificar o uso, parte da literatura biomédica utiliza o HLA para referirse especificamente ás molécula proteicas HLA e reserva o acrónimo MHC para a rexión do xenoma que codifica esta molécula, pero isto non é unha convención consistente.
Os xenes HLA máis intensamente estudados son os nove chamados xenes MHC clásicos: HLA-A, HLA-B, HLA-C, HLA-DPA1, HLA-DPB1, HLA-DQA1, HLA-DQB1, HLA-DRA, e HLA-DRB1. Nos humanos, o MHC está dividido en tres rexións: clases I, II, e III. Os xenes A, B, C, E, F, e G pertencen ao MHC de clase I, mentres que os seis xenes D pertencen á clase II.
Os xenes MHC exprésanse de modo codominante.[7] Isto significa que os alelos (variantes) herdados de ambos os proxenitores se expresan dun modo equivalente:
- Como hai 3 xenes da clase I, denominados nos humanos HLA-A, HLA-B e HLA-C, e como cada persoa herda un conxunto de xenes de cada proxenitor, todas as células dun individuo poden expresar seis tipos distintos de moléculas MHC de clase I (ver figura).
- No locus da clase II, cada persoa herda un par de xenes HLA-DP (DPA1 e DPA2, que codifican as cadeas α e β), un par de xenes HLA-DQ (DQA1 e DQA2, para as cadeas α e β), un xene HLA-DRα (DRA1) e un ou dous xenes HLA-DRβ (DRB1 e DRB3). Iso significa que unha persoa heterocigota pode herdar 6 ou 8 alelos da clase II, tres ou catro de cada proxenitor.
O conxunto de alelos que está presente en cada cromosoma denomínase haplotipo MHC. Nos humanos, cada alelo HLA desígnase cun número. Por exemplo, para un individuo dado, o seu haplotipo podería ser HLA-A2, HLA-B5, HLA-DR3 etc... Cada individuo heterocigoto ten dous haplotipos MHC, un en cada cromosoma (un de orixe paterna e outro de materna).
Os xenes MHC son moi polimórficos, o que significa que hai moitos alelos distintos en cada individuo da poboación. O polimorfismo é tan alto que nunha poboación mixta (é dicir, non endogámica) non hai dous individuos que teñan exactamente o mesmo conxunto de xenes MHC e moléculas, coa excepción dos xemelgos idénticos.
As rexións polimórficas de cada alelo están localizadas na rexión para o contacto co péptido, que será exhibida polo linfocito. Por esta razón, a rexión de contacto de cada alelo ou molécula MHC é moi variable, xa que os residuos polimórficos do MHC crean sucos ou fendas específicas nos cales só poden entrar certos tipos de péptidos. Isto impón que a unión entre a molécula do MHC e o peṕtido sexa moi específica, e isto implica que cada variante do MHC pode unirse especificamente só a aqueles péptidos que poden entrar correctamente no suco da molécula do MHC, o cal varía para cada alelo. Deste modo, as moléculas teñen unha especificidade ampla, no sentido de que poden unirse a moitos, aínda que non a todos, os tipos de péptidos posibles. Isto é unha característica esencial das moléculas MHC: Nun individuo dado, abonda con ter unhas poucas destas moléculas diferentes para poder "presentar" unha gran variedade de péptidos.
Por outra parte, dentro dunha poboación, a presenza de moitos alelos distintos asegura que haberá sempre un individuo cunha molécula do MHC específica coa capacidade de cargar o péptido correcto para recoñecer un microbio específico. A evolución do polimorfismo do MHC asegura que unha poboación non sucumbirá ante a aparición dun patóxeno novo ou mutado, porque polo menos algúns individuos poderán desenvolver unha resposta inmunitaria axeitada para derrotar ao patóxeno. As variacións nas moléculas do MHC (responsables do polimorfismo) son o resultado da herdanza de diferentes xenes para as moléculas do MHC, e non están inducidas por recombinación, como é o caso dos receptores para os antíxenos.
Notas[editar | editar a fonte]
- ↑ Bruce Alberts et al. Biología Molecular de la Célula. Omega. 1986. Páxina 1072. ISBN 84-282-0752-6.
- ↑ Kimball's Biology Arquivado 07 de marzo de 2018 en Wayback Machine., Histocompatibility Molecules
- ↑ de Villartay, JP; Rouger, P, Muller, JY, Salmon, C (1985 Jul). "HLA antigens on peripheral red blood cells: analysis by flow cytofluorometry using monoclonal antibodies.". Tissue antigens 26 (1): 12-9. PMID 3898468.
- ↑ MHC Sequencing Consortium (1999). "Complete sequence and gene map of a human major histocompatibility complex". Nature 401 (6756): 921–923. PMID 10553908. doi:10.1038/44853.
- ↑ 5,0 5,1 Belov K, Deakin JE, Papenfuss AT, Baker ML, Melman SD, Siddle HV, Gouin N, Goode DL, Sargeant TJ, Robinson MD, Wakefield MJ, Mahony S, Cross JG, Benos PV, Samollow PB, Speed TP, Graves JA, Miller RD (2006). "Reconstructing an ancestral mammalian immune supercomplex from a marsupial major histocompatibility complex". PLoS Biol. 4 (3): e46. PMC 1351924. PMID 16435885. doi:10.1371/journal.pbio.0040046.
- ↑ Toh H, Savoie CJ, Kamikawaji N, Muta S, Sasazuki T, Kuhara S (2000). "Changes at the floor of the peptide-binding groove induce a strong preference for proline at position 3 of the bound peptide: molecular dynamics simulations of HLA-A*0217". Biopolymers 54 (5): 318–27. PMID 10935972. doi:10.1002/1097-0282(20001015)54:5<318::AID-BIP30>3.0.CO;2-T.
- ↑ 7,0 7,1 Abbas; Lichtman A.H. (2009). "Ch.3 Antigen capture and presentation to lymphocytes". Basic Immunology. Functions and disorders of the immune system (3rd ed.). p. A.B. ISBN 978-1-4160-4688-2.
- ↑ Aderem A, Underhill DM (1999). "Mechanisms of phagocytosis in macrophages". Annu. Rev. Immunol. 17: 593–623. PMID 10358769. doi:10.1146/annurev.immunol.17.1.593.
- ↑ Boehm T; Zufall F (2006). "MHC peptides and the sensory evaluation of genotype". Trends Neurosci 29 (2): 100–107. PMID 16337283. doi:10.1016/j.tins.2005.11.006.
- ↑ Smith, S.B.; Webster, M.S.; Holmes, R.T. (2005). "The heterozygosity theory of extra-pair mate choice in birds: a test and a cautionary note". Journal of Avian Biology 36: 146–154.
- ↑ Haig D (1997). "Maternal-fetal interactions and MHC polymorphism". J. Reprod. Immunol. 35 (2): 101–9. PMID 9421795.
- ↑ Ober C, Weitkamp LR, Cox N, Dytch H, Kostyu D, Elias S (1997). "HLA and mate choice in humans.". Am. J. Hum. Genet. 61 (3): 497–504. PMID 9326314. doi:10.1086/515511.
- ↑ Chaix R, Chen C, Donnelly P (2008). "Is Mate Choice in Humans MHC-Dependent?". PLoS Genetics 4 (9): e1000184. PMC 2519788. PMID 18787687. doi:10.1371/journal.pgen.1000184.
- ↑ Janeš D, Klun I, Vidan-Jeras B, Jeras M, Kreft S (2010). "Influence of MHC on odour perception of 43 chemicals and body odor". Central European Journal of Biology 5 (3): 324–330. doi:10.2478/s11535-010-0020-6.
- ↑ Wedekind C, Seebeck T, Bettens F, Paepke AJ (1995). "MHC-dependent mate preferences in humans". Proc. Biol. Sci. 260 (1359): 245–9. PMID 7630893. doi:10.1098/rspb.1995.0087.
- ↑ Jacob S, McClintock MK, Zelano B, Ober C (2002). "Paternally inherited HLA alleles are associated with women's choice of male odor". Nat. Genet. 30 (2): 175–9. PMID 11799397. doi:10.1038/ng830.
- ↑ Santos, P S; Schinemann JA, Gabardo J, Bicalho MG (2005). "New evidence that the MHC influences odor perception in humans: A study with 58 southern Brazilian students". Horm Behav. 47 (4): 384–388. PMID 15777804. doi:10.1016/j.yhbeh.2004.11.005.
- ↑ "The pill makes women pick bad mates"
- ↑ Castro-Prieto A, Wachter B, Sommer S (2011). "Cheetah paradigm revisited: MHC diversity in the world's largest free-ranging population". Mol. Biol. Evol. 28 (4): 1455–68. PMID 21183613. doi:10.1093/molbev/msq330.
- ↑ Babik W, Durka W, Radwan J (2005). "Sequence diversity of the MHC DRB gene in the Eurasian beaver (Castor fiber)". Mol. Ecol. 14 (14): 4249–57. PMID 16313590. doi:10.1111/j.1365-294X.2005.02751.x.
- ↑ Zhu L, Ruan XD, Ge YF, Wan QH, Fang SG (2007). "Low major histocompatibility complex class II DQA diversity in the Giant Panda (Ailuropoda melanoleuca)". BMC Genet. 8: 29. PMC 1904234. PMID 17555583. doi:10.1186/1471-2156-8-29.
- ↑ Siddle HV, Kreiss A, Eldridge MD, Noonan E, Clarke CJ, Pyecroft S, Woods GM, Belov K (2007). "Transmission of a fatal clonal tumor by biting occurs due to depleted MHC diversity in a threatened carnivorous marsupial". Proc. Natl. Acad. Sci. U.S.A. 104 (41): 16221–6. PMC 1999395. PMID 17911263. doi:10.1073/pnas.0704580104.
- ↑ Abbas; Lichtman A.H. (2009). "Ch.10 Immune responses against tumors and transplant". Basic Immunology. Functions and disorders of the immune system (3rd ed.). p. A.B. ISBN 978-1-4160-4688-2.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Molecular individuality Arquivado 29 de xaneiro de 2013 en Wayback Machine., libro en liña.(en alemán)
- Sexual attraction is linked to MHC compatibility
- NetMHC 3.0 server — predicts binding of peptides to a number of different MHC (HLA) alleles
- T-cell Group - Cardiff University
- The story of 2YF6: A Chicken MHC[Ligazón morta]
- RCSB Protein Data Bank: Molecule of the Month - Major Histocompatibility ComplexArquivado 28 de maio de 2010 en Wayback Machine.
- dbMHC Home, NCBI's database of the Major Histocompatibility Complex
