Glicólise

A glicólise (do grego glycos, azucre e lysis, rotura), é a vía metabólica encargada de converter a glicosa en piruvato para obter enerxía para a célula. Consta de 10 reaccións encimáticas consecutivas que converten a glicosa en dúas moléculas de piruvato, o cal pode seguir outras vías metabólicas nas que cederá enerxía á célula.[1]
O tipo de glicólise máis común e máis coñecida é a vía de Embden-Meyerhof, explicada inicialmente por Gustav Embden e Otto Fritz Meyerhof . O termo pode incluír outras vías alternativas, como a vía de Entner-Doudoroff. Porén, glicólise úsase con grande frecuencia como sinónimo de vía de Embden-Meyerhof. É a vía inicial do catabolismo (degradación) de carbohidratos.
Durante a glicólise obtense un rendemento neto de dúas moléculas de ATP e dúas de NADH; o ATP pode usarse como fonte de enerxía para realizar traballo metabólico, mentres que o NADH pode ter diferentes destinos. Pode usarse como fonte de poder redutor en reaccións anabólicas; se hai osíxeno, pode oxidarse na cadea respiratoria, obténdose tres ATP por cada NADH; se non hai osíxeno, úsase para reducir o piruvato a lactato (fermentación láctica), ou a CO2 e etanol (fermentación alcohólica), sen obtención adicional de enerxía.
As funcións da glicólise son:
- Xeración de moléculas de alta enerxía (ATP e NADH) como fonte de enerxía celular en procesos de respiración aeróbica (presenza de osíxeno) e fermentación (ausencia de osíxeno).
- Xeración de piruvato que pasará ao ciclo de Krebs, como parte da respiración aeróbica.
- Produción de intermediarios de 6 e 3 carbonos que poden ser utilizados noutros procesos celulares.
En eucariotas e procariotas, a glicólise ocorre no citosol da célula. En células vexetais, algunhas das reaccións glicolíticas danse tamén no ciclo de Calvin, que ocorre dentro dos cloroplastos. A ampla conservación evolutiva desta vía inclúe os organismos filoxeneticamente máis antigos, e por isto considérase unha das vías metabólicas máis antigas.[2]
Descubrimento[editar | editar a fonte]
Os primeiros estudos informais dos procesos glicolíticos foron iniciados en 1860, cando Louis Pasteur descubriu que os microorganismos son os responsables da fermentación,[3] e en 1897 cando Eduard Buchner encontrou que certos extractos celulares podían realizar fermentacións. A seguinte grande contribución foi de Arthur Harden e William Young en 1905, que determinaron que para que a fermentación teña lugar son necesarias unha fracción celular de masa molecular elevada e termosensible (encimas) e unha fracción citoplasmática de baixa masa molecular e termorresistente (ATP, ADP, NAD+ e outros cofactores). Os detalles da vía determináronse en 1940, cos traballos de Otto Meyerhoff e algúns anos despois por Luis Leloir. As maiores dificultades en determinar o intricado da vía foron a curta vida e as baixas concentracións dos intermediarios nas rápidas reaccións glicolíticas.
Visión xeral[editar | editar a fonte]
A glicólise é a forma máis rápida de conseguir enerxía para unha célula e, no metabolismo de carbohidratos, é xeralmente a primeira vía á cal recorre a célula para ese mester. Está estruturada en 10 reaccións encimáticas que permiten a transformación dunha molécula de glicosa en dúas moléculas de piruvato por medio dun proceso catabólico.
A glicólise adoita a dividirse para o súa explicación en dúas fases: fase de gasto de enerxía e fase de obtención de enerxía.
A primeira fase consiste en transformar unha molécula de glicosa en dúas moléculas de gliceraldehido (unha molécula de baixa enerxía) gastando 2 ATP. Isto permite duplicar os resultados da segunda fase, a de obtención enerxética. Na segunda fase, o gliceraldehido transfórmase nun composto de alta enerxía, que ao hidrolizarse xera unha molécula de ATP, e como se xeraron dúas moléculas de gliceraldehido, obtéñense en realidade dúas moléculas de ATP. Esta obtención de enerxía conséguese grazas á combinación dunha reacción fortemente exergónica despois doutra levemente endergónica, que se realiza en dúas ocasións, xerando dúas moléculas de piruvato. Desta maneira, na segunda fase obteñense 4 moléculas de ATP.
Reacción[editar | editar a fonte]
A reacción global da glicólise é:[1]

|
 + + 
|
Onde o reactivo inicial é a glicosa e os produtos finais son:
- O ATP é a fonte de enerxía universal da célula.
- NADH e H+, outorgan a capacidade de reducir outros compostos pertencentes a outras vías metabólicas, ou ben para sintetizar ATP.
- O piruvato é a molécula que seguirá oxidándose no ciclo de Krebs, como parte da respiración aeróbica, onde dará orixe a máis moléculas de NADH, que poderán producir máis ATP na mitocondria.
- Auga.
Destino do piruvato e do NADH[editar | editar a fonte]
- Artigos principais: Fermentación e Ciclo de Krebs.
A glicólise pode funcionar tanto en condicións aerobias coma anaerobias, pero o destino do pìruvato varía dependendo desas condicións. En situación anaerobia, o piruvato citosólico é fermentado. O tipo de fermentación depende do organismo. No home dáse nas células que quedan sen ATP nun momento dado, como sucede no músculo en situación de exercicio físico moi intenso na que o osíxeno que chega á célula non é dabondo para manter a respiración aerobia ; nese caso o músculo realiza a fermentación homoláctica, convertendo o piruvato en lactato, e sen obter máis ATP ca as dúas moléculas formadas nas últimas reaccións da glicólise. Tamén sucede nos eritrocitos, que carecen de mitocondrias. Polo contrario, en condicións aerobias o piruvato entra nas mitocondrias (en eucariotas) para ser descarboxilado, entrar no ciclo de Krebs e completar a súa respiración aerobia, xerando uns 15 ATP por cada piruvato (ata 38 por glicosa).
O NADH pode usarse no anabolismo ou pode ceder os electróns que recolleu dos substratos da glicólise á cadea de transporte electrónico, pero dita cadea está na mitocondria (en eucariotas) e o NADH non pode atravesar a membrana mitocondrial. Pero pode entrar nas mitocondrias utilizando un conxunto de reaccións chamadas lanzadeiras (lanzadeira do malato e lanzadeira do glicerol-fosfato) nas que se converte primeiro noutra molécula que pode entrar na mitocondria, que, unha vez dentro da mitocondria, rexenera o equivalente de redución do NADH. Deste modo, o poder redutor do citosol pode pasar ao interior da mitocondria.
Fases da glicólise[editar | editar a fonte]
A glicólise divídese en dúas fases e dez reaccións encimáticas, que se describen a continuación.
Fase de gasto de enerxía (ATP)[editar | editar a fonte]
Esta primeira fase da glicólise consiste en transformar unha molécula de glicosa (hexosa) en dúas moléculas de gliceraldehido (triosa). Durante esta fase non se produce enerxía, senón que se gasta. Esta enerxía gastada pode considerarse un "investimento" que fai a célula para obter "beneficios" enerxéticos despois. Gástanse agora 2 ATP e despois produciranse 4, cun beneficio neto de 2.
1º paso: Hexoquinase[editar | editar a fonte]
- Artigo principal: Hexoquinase.
|
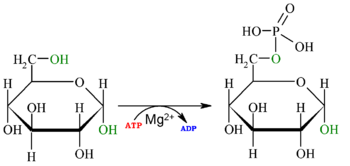
| Glicosa + ATP → Glicosa-6-fosfato + ADP [4] |
A primeira reacción da glicólise é a fosforilación da glicosa, para activala (aumentar a súa enerxía) e así poder utilizala noutros procesos cando sexa necesario. Esta activación ocorre pola transferencia dun grupo fosfato do ATP, unha reacción catalizada polo encima hexoquinase,[5] o cal pode fosforilar (engadir un grupo fosfato) a moléculas similares á glicosa, como a frutosa e a manosa.
As vantaxes de fosforilar a glicosa son dúas: A primeira é facer da glicosa un metabolito máis reactivo, e a segunda é que a glicosa-6-fosfato (G6P), que é unha substancia cargada no seu fosfato, non pode atravesar a membrana celular (a diferenza da glicosa), porque na célula non existe un transportador para a G6P. Desta forma evítase a perda dun substrato enerxético para a célula.
A hexoquinase só fosforila as D-hexosas, e utiliza de substrato para obter fosfatos o MgATP2+, xa que o catión permite que o último fosfato do ATP (fosfato gamma, γ-P ou Pγ) sexa un branco máis fácil para o ataque nucleofílico que realiza o grupo hidroxilo (OH) do sexto carbono da glicosa, o que é posible debido ao Mg2+ que tapa as cargas dos outros dous fosfatos.[1][6]
Esta reacción posúe unha enerxía libre de Gibbs negativa, e, por tanto, trátase dunha reacción na que se libera enerxía. En numerosas bacterias esta reacción está combinada coa última reacción da glicólise (de fosfoenolpiruvato a piruvato) para poder aproveitar a enerxía sobrante da reacción: o fosfato do fosfoenolpiruvato transfírese dunha a outra proteína dun sistema de transporte fosfotransferase, e en última instancia, o fosfato pasará a unha molécula de glicosa que é tomada do exterior da célula e liberada en forma de G6P no interior celular. Trátase, por tanto, de combinar a primeira e a última reacción desta vía e usar o excedente de enerxía para realizar un tipo de transporte a través de membrana denominado translocación de grupo.
Unha hexoquinase especial que se encontra só no fígado, páncreas, intestino delgado e partes do encéfalo é a glicoquinase. Nos hepatocitos o 95% da actividade de hexoquinase está a cargo da glicoquinase, o cal é fundamental para a glicólise e síntese de glicóxeno no fígado.
2º paso: Glicosa-6-P isomerase[editar | editar a fonte]
- Véxase tamén: Glicosa-6-fosfato isomerase.

|
| Glicosa-6-fosfato ⇌ Frutosa-6-fosfato [4] |
Este é un paso importante, posto que aquí se define a xeometría molecular que afectará aos dous pasos críticos na glicólise: O próximo paso, que agregará un grupo fosfato ao produto desta reacción, e o paso 4, cando se creen dúas moléculas de gliceraldehido que finalmente serán as precursoras do piruvato.[1]
Nesta reacción, a glicosa-6-fosfato isomerízase a frutosa-6-fosfato (F6P), por medio do encima glicosa-6-fosfato isomerase, tamén chamado fosfohexosa isomerase. A isomerización ocorre nunha reacción de 4 pasos, que implica a abertura do anel do azucre e un traspaso de protóns a través dun intermediario cis-enediol[7]
Posto que a enerxía libre desta reacción é igual a +1,7 kJ/mol, a reacción non é espontánea e debe estar combinada con outra.
3º paso: Fosfofrutoquinase[editar | editar a fonte]
- Véxase tamén: Fosfofrutoquinase 1.

|
| Frutosa-6-fosfato + ATP → Frutosa-1,6-difosfato + ADP [4] |
Consiste na fosforilación da frutosa-6-fosfato no carbono 1, con gasto dun ATP, a través do encima fosfofrutoquinase 1 (PFK1). Tamén este fosfato terá unha baixa enerxía de hidrólise. Polo mesmo motivo que na primeira reacción, o proceso é irreversible. O novo produto denominarse frutosa-1,6-difosfato (F1,6BP).
A irreversibilidade desta reacción é importante, xa que a fai ser o punto de control da glicólise. Como hai outros substratos á parte da glicosa que entran na glicólise, o punto de control non está colocado na primeira reacción, senón nesta. A fosfofrutoquinase ten centros alostéricos, sensibles ás concentracións de intermediarios como citrato e ácidos graxos, ADP e AMP. En moitas plantas e microorganismos existe un encima con función similar chamado fosfofrutoquinase dependente de pirofosfato, que usa pirofosfato como doante de fosfatos en vez do ATP.
4º paso: Aldolase[editar | editar a fonte]
- Véxase tamén: Frutosa-bisfosfato aldolase.

|
| Frutosa-1,6-difosfato ⇌ Dihidroxiacetona-fosfato + Gliceraldehido-3-fosfato [4] |
O encima aldolase (nome completo frutosa-bisfosfato aldolase), por medio dunha reacción que é reversible, rompe a frutosa-1,6-difosfato en dúas moléculas de tres carbonos (triosas): dihidroxiacetona-fosfato (DHAP) e gliceraldehido-3-fosfato (GA3P ou GAP). Existen dous tipos de frutosa-bisfosfato aldolase glicolítica, que difiren tanto no tipo de organismos onde se expresan, coma nos intermediarios de reacción.
Esta reacción ten unha enerxía libre (ΔG) de entre 20 a 25 kJ/mol, polo tanto en condicións estándar non acontece de maneira espontánea. Porén, en condicións intracelulares a enerxía libre é pequena debido á baixa concentración dos substratos, o que permite que esta reacción sexa reversible.[1]
5º paso: Triosa fosfato isomerase[editar | editar a fonte]
- Véxase tamén: Triosa fosfato isomerase.

|
| Dihidroxiacetona-fosfato ⇌ Gliceraldehido-3-fosfato [4] |
Posto que só o gliceraldehido-3-fosfato pode seguir os pasos restantes da glicólise, a outra molécula xerada pola reacción anterior (dihidroxiacetona-fosfato) é convertida (isomerizada xa que as dúas son isómeros) en gliceraldehido-3-fosfato. Esta reacción posúe unha enerxía libre en condicións estándar positiva, o cal implicaría un proceso non favorecido, non obstante, igual que para a reacción 4, considerando as concentracións intracelulares reais do reactivo e o produto, resulta que a enerxía libre total é negativa, polo que a dirección favorecida é cara á formación de gliceraldehido-3-fosfato.
Este é o último paso da "fase de gasto de enerxía". Só se consumiu ATP no primeiro paso (hexoquinase) e no terceiro paso (fosfofrutoquinase 1). Como ao final desta fase se orixinaron dúas moléculas de gliceraldehído-3-fosfato (4º e 5º pasos), de aquí en adiante as reaccións están duplicadas, xa que haberá unha en cada molécula de gliceraldehido-3-fosfato e as derivadas delas.
Fase de obtención de enerxía[editar | editar a fonte]
Nesta fase vanse producir 4 ATP (que restados aos 2 ATP gastados na fase anterior dan un rendemento neto de 2 ATP), 2 piruvatos e 2 NADH.
6º paso: Gliceraldehido-3-fosfato deshidroxenase[editar | editar a fonte]
- Véxase tamén: Gliceraldehido-3-fosfato deshidroxenase.
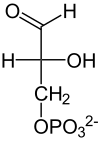 |
NAD+ NADH + Pi + H+  Gliceraldehído-3-fosfato deshidroxenase |
|
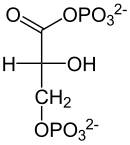
| Gliceraldehido-3-fosfato + Pi + NAD+ |
 |
1,3-difosfoglicerato + NADH + H+ |
| [4] |
Esta reacción consiste en oxidar o gliceraldehido-3-fosfato utilizando NAD+ para engadir un ión fosfato á molécula, o cal é realizado polo encima gliceraldehido-3-fosfato deshidroxenase (GAPDH) en 5 pasos, e deste xeito aumentar a enerxía do composto.
O grupo aldehido oxídase a un grupo acil-fosfato, que é un derivado dun carboxilo fosfatado. Este composto posúe unha enerxía de hidrólise moi alta (próxima aos 50 kJ/mol) polo que se inician as reaccións que permitirán recuperar o ATP máis adiante.
Mentres que o grupo aldehido se oxida, o NAD+ redúcese, o que fai desta reacción unha reacción redox. O NAD+ redúcese pola incorporación dalgún H+ dando como resultado unha molécula de NADH de carga neutra.
7º paso: Fosfoglicerato quinase[editar | editar a fonte]
- Véxase tamén: Fosfoglicerato quinase.
 |
ADP ATP Fosfoglicerato quinase |
|
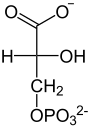
| 1,3-difosfoglicerato + ADP |
 |
3-fosfoglicerato + ATP |
| [4] |
Neste paso, o encima fosfoglicerato quinase transfire o grupo fosfato do 1,3-difosfoglicerato a unha molécula de ADP, xerando así a primeira molécula de ATP producida na vía. Como a glicosa se transformou en dúas moléculas de gliceraldehido, en total recupéranse 2 ATP nesta etapa. Nótese que o encima foi nomeado pola reacción inversa á mostrada, e que esta opera en ambas as direccións (reversible).
Os pasos 6 e 7 da glicólise mostran un caso de combinación de reaccións, onde unha reacción enerxeticamente desfavorable (paso 6º) vai seguida dunha reacción moi favorable enerxeticamente (paso 7º) que impulsa a primeira reacción. Noutras palabras, como a célula se mantén en equilibrio, o descenso nas reservas de 1,3 difosfoglicerato empurra o encima GAP deshidroxenase a aumentar ditas reservas. A cuantificación da enerxía libre para combinar ambas as reaccións é de arredor de -12 kJ/mol.
Esta maneira de obter ATP sen a necesidade de O2 na que o fosfato pasa duns substrato fosfatado rico enerxeticamente ao ADP, denomínase fosforilación a nivel de substrato.
8º paso: Fosfoglicerato mutase[editar | editar a fonte]
- Véxase tamén: Fosfoglicerato mutase.

|
| 3-fosfoglicerato ⇌ 2-fosfoglicerato [4] |
Isomerízase o 3-fosfoglicerato procedente da reacción anterior dando 2-fosfoglicerato. O encima que cataliza esta reacción é a fosfoglicerato mutase. O único que ocorre aquí é o cambio de posición do fosfato do C3 ao C2. Son enerxías similares e, por tanto, reversibles, cunha variación de enerxía libre de case cero.
9º paso: Enolase[editar | editar a fonte]
- Véxase tamén: Enolase.

|
| 2-fosfoglicerato ⇌ Fosfoenolpiruvato + H2O [4] |
O encima enolase cataliza a formación dun dobre enlace no 2-fosfoglicerato, eliminando unha molécula de auga formada polo hidróxeno do C2 e o OH do C3. O resultado é o fosfoenolpiruvato (PEP).
O fosfoenolpiruvato é un composto fosfatado de alta enerxía. En realidade o 2-fosfoglicerato e o fosfoenolpiruvato teñen a mesma cantidade total de enerxía, pero hai unha redistribución de enerxía dentro da molécula, que fai que o fosfato do fosfoenolpiruvato produza ao hidrolizarse (o que acontecerá na seguinte reacción da vía) unha liberación de enerxía moito maior, que se aproveitará para producir ATP.
10º paso: Piruvato quinase[editar | editar a fonte]
- Véxase tamén: Piruvato quinase.

|
| Fosfoenolpiruvato ⇌ Piruvato [4] |
Ten lugar a desfosforilación do fosfoenolpiruvato, obténdose piruvato e ATP. Reacción irreversible mediada pola piruvato quinase. Vólvese a formar ATP, que como as reaccións da fase de obtención de enerxía están duplicadas debido á isomerización das triosas-fosfato, son outros 2 ATP máis. O fosfoenolpiruvato pasa á forma enolpiruvato e este inmediatamente pasa á forma cetopiruvato (denominado normalmente piruvato).
O encima piruvato quinase é dependente de magnesio e potasio. A enerxía libre é de -31,4 kJ/mol, polo tanto a reacción é favorable e irreversible.
O piruvato formado pode ser fermentado (en condicións anaerobias) ou vai ás mitocondrias (nos eucariotas, en condicións aerobias) para ser descarboxilado, entrar no ciclo de Krebs e incorporarse á respiración aerobia.
Regulación[editar | editar a fonte]
Regulación encimática[editar | editar a fonte]

A glicólise regúlase encimaticamente nos tres puntos irreversibles desta ruta, que son: a primeira reacción (G →G6P), por medio da hexoquinase; a terceira reacción (F6P → F1,6BP) por medio da fosfofrutoquinase 1, e no último paso (PEP → piruvato) pola piruvato quinase.
- A hexoquinase é un punto de regulación pouco importante, xa que a G6P se utiliza para outras vías, e inhíbese cando hai moita glicosa-6-fosfato no músculo.
- A fosfofrutoquinase 1 é o encima principal da regulación da glicólise, se está activa cataliza a obtención de moita frutosa-1,6-difosfato, o que permitirá aos encimas seguintes orixinar moito piruvato. Se está inhibida, obtéñense baixas concentracións de produto e, por tanto, orixínase ao final pouco piruvato.
- Este encima está controlado por regulación alostérica da seguinte maneira: Por un lado actívase cando hai niveis enerxéticos elevados de ADP e AMP, e inhíbese en abundancia de ATP e citrato, e por outro actívase en presenza dun regulador xerado pola fosfofrutoquinase 2 que é a frutosa-2,6-difosfato, que non é un metabolito nin da glicólise nin da gliconeoxénese, senón un regulador de ambas as vías, que reflicte o nivel da hormona glicagón en sangue.
- A lóxica da inhibición e activación é a seguinte:
- Efecto do ATP: inhibe este encima, porque se hai unha alta concentración de ATP, a célula xa non precisa producir máis.
- Efecto do citrato: Se a concentración de citrato é alta, o ciclo de Krebs vai máis a modo ca o ritmo ao que se degrada o acetil-CoA, e a concentración de glicosa será máis alta. No ciclo de Krebs prodúcese moito NADH e FADH2, e para que se reciclen deben reoxidarse na cadea de transporte electrónico creando un gradiente de protóns, e se isto non sucede, o ciclo de Krebs para. O citrato funciona como inhibidor alostérico da fosfofrutoquinase 1, especialmente no músculo.
- Efecto do AMP e ADP: a alta concentración destas moléculas implica que hai unha escaseza de ATP, polo que é necesario activar a glicólise, para xerar piruvato e enerxía.
- En resumo, a fosfofrutoquinase 1 inhíbese polo ATP e citrato, e actívase polo ADP, AMP e frutosa-2,6-difosfato.
- A piruvato quinase regúlase de diferente xeito segundo o tecido no que traballe, pero no fígado inhíbese en presenza de ATP e Acetil-CoA, e actívase pola frutosa-2,6-difosfato e a concentración alta de fosfoenolpiruvato. Os niveis altos de ácidos graxos son inhibidores.
Regulación por insulina[editar | editar a fonte]
Ao aumentar a glicosa no sangue, despois dunha comida, as células beta do páncreas estimulan a produción de insulina, e esta á súa vez aumenta a actividade da glicoquinase nos hepatocitos.
As concentracións altas de glicagón e as baixas de insulina diminúen a concentración intracelular de frutosa-2,6-difosfato. Isto trae como consecuencia a diminución da glicólise e o aumento da gliconeoxenése.
Metabolitos da glicólise desviados a outras vías[editar | editar a fonte]
Os metabolitos intermedios da vía glicolítica poden ser utilizados tamén por outras vías de tipo anabólico, polo que o fluxo de moléculas na glicólise é fundamental para fornecer de esqueletos carbonados as biosínteses celulares.
As principais vías metabólicas que utilizan metabolíticos da glicólise son:
- Gliconeoxénese
- Metabolismo lipídico
- Vía da pentosa fosfato
- Ciclo do ácido cítrico, que á súa vez conduce a:
O NADH da glicólise tamén pode ter un papel no anabolismo, xa que as reaccións anabólicas requiren o poder redutor que pode subministrar o NADH, quer directamente quer indirectamente reducindo a outros coencimas como o NADP+ (formaríase NADPH).
Incorporación doutros metabolitos á glicólise[editar | editar a fonte]
Na glicólise non só se pode catabolizar glicosa. Outros metabolitos distintos da glicosa poden incorporarse á vía glicolítica a distintos niveis. Os polisacáridos e disacáridos deben hidrolizarse para render monosacáridos soltos, e estes poden entrar na glicólise. A galactosa pode orixinar UDP-galactosa e despois glicosa-1-fosfato, que se incorpora á glicólise. A manosa pode fosforilarse formando frutosa-6-fosfato, que se incorpora á glicólise. A frutosa no músculo e riles, principalmente, pode fosforilarse a frutosa-6-fosfato, que se incorpora á glicólise, e no fígado acaba orixinando gliceraldehido-3-fosfato, que se incorpora á glicólise. O glicóxeno ao sufrir fosforólise orixina glicosa-1-fosfato, que se incorpora á glicólise. A glicerina procedente dos lípidos pode acabar por orixinar gliceraldehido-3-fosfato, que é un metabolito da glicólise.
Doenzas relacionadas coa glicólise[editar | editar a fonte]
Doenzas xenéticas[editar | editar a fonte]
As mutacións que afectan á glicólise son en xeral raras debido á importancia central desta vía metabólica, o que significa que a maioría das mutacións deste tipo que aparecen causan a incapacidade da célula para respirar, e, por tanto, provocan a morte da célula rapidamente. Porén, coñécense algunhas destas mutacións, como por exemplo a que causa a deficiencia de piruvato quinase, que orixina anemia hemolítica crónica.
Cancro[editar | editar a fonte]
As células tumorais malignas de rápido crecemento mostran tipicamente unha actividade glicolítica ata 200 veces maior ca a das células normais. Este fenómeno foi xa descrito en 1930 por Otto Warburg e coñécese como efecto Warburg. A hipótese de Warburg considera que o cáncer está causado principalmente por disfuncións no metabolismo mitocondrial, máis que polo crecemento incontrolable das células. Hai diversas teorías que tratan de explicar o efecto Warburg.
Esta alta taxa de glicólise das células tumorais ten importantes aplicacións médicas, como o diagnóstico e monitorización dos tumores malignos e das respostas aos tratamentos por medio da visualización por tomografía de emisión de positróns do consumo pola célula de 218-F-2-desoxiglicosa radioactiva (un substrato modificado da hexoquinase), que se subministra ao paciente.[8][9]
Estase investigando tamén como se pode afectar o metabolismo mitocondrial para tratar o cáncer reducindo as taxas de glicólise e así matar as células, usando diversas estratexias, como a dieta cetoxénica.
Enfermidade de Alzheimer[editar | editar a fonte]
Disfuncións na glicólise ou no metabolismo de glicosa nos córtex fronto-temporo-parietal e cingulado foron asociadas coa enfermidade de Alzheimer,[10] probablemente debido á diminución no líquido cefalorraquídeo do péptido beta amiloide (1-42) (Aβ42) e incremento da proteína tau fosforilada.[11]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 1,2 1,3 1,4 David Nelson & Michael Cox (2004). "Glycolysis, Gluconeogenesis and the Pentose Phosphate Pathway". Lehningher's Principles of Biochemistry. W.H.Freeman. 0716743396.
- ↑ Romano AH & Conway T. Evolution of carbohydrate metabolic pathways. Res Microbiol. 147(6-7):448-55 (1996) PMID 9084754
- ↑ Papers de Pasteur
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 Valores tomados de Lehningher's Principles of Biochemistry (ISBN 0-7167-4339-6) e do Volume 3 de Biochemistry por J. Stenesh (ISBN 0-306-45733-4)
- ↑ Meyerhof, O. Ueber die enzymatische Milch-säurebildung im Muskelextrakt; die Milch-säurebildung aus den gärfähigen Hexosen. Biochem Z. 183:176 (1927)
- ↑ Colowick, S. y Kalckar H.. The role of myokinase in trans-phosphorylations; the enzymatic phosphorylation of hexoses by adenyl pyrophosphate. J. Biol. Chem. 148: 117 (1943).
- ↑ Irwin A. Rose (2006). "Mechanism of the Aldose-Ketose Isomerase Reactions". Advances in Enzymology - and Related Areas of Molecular Biology, Volume 43. Wiley Interscience. ISBN 0471591788. - doi 10.1002/9780470122884.ch6
- ↑ "PET Scan: PET Scan Info Reveals ...". Consultado o December 5, 2005.
- ↑ "4320139 549..559" (PDF). Consultado o December 5, 2005.
- ↑ Hunt, A .; Schonknecht, P; Henze, M; Seidl, U; Haberkorn, U; Schroder, J; et al. (2007). "Reduced cerebral glucose metabolism in patients at risk for Alzheimer's disease". Psychiatry Research: Neuroimaging 155 (2): 147–154. PMID 17524628. doi:10.1016/j.pscychresns.2006.12.003.
- ↑ Hunt, A .; Van Der Flier, WM; Blankenstein, MA; Bouwman, FH; Van Kamp, GJ; Barkhof, F; Scheltens, P; et al. (2008). "CSF and MRI markers independently contribute to the diagnosis of Alzheimer's disease". Neurobiology of Aging 29 (5): 669–675. PMID 17208336. doi:10.1016/j.neurobiolaging.2006.11.018.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- soko.com.ar: Explicación máis extensa (en castelán).
- www2.ufp.pt: A lógica química da Glicólise (en portugués).
- www.pdb.org: The Glycolytic Enzymes, información en Protein Data BankArquivado 28 de xaneiro de 2011 en Wayback Machine. (en inglés).
| Wikimedia Commons ten máis contidos multimedia na categoría: Glicólise |











