Transporte de membrana
En bioloxía celular denomínase transporte de membrana o conxunto de mecanismos que regulan o paso de solutos, como ións e pequenas moléculas, a través das membranas celulares, é dicir, de bicapas lipídicas que inclúen proteínas. Dita propiedade débese á selectividade de membrana, unha característica das membranas celulares que lles permite actuar como axentes de separación específica de substancias quimicamente distintas, posibilitando a permeabilidade de certas substancias, pero non a doutras.[1]
Os movementos de case todos os solutos a través da membrana están mediados por proteínas transportadoras de membrana, máis ou menos especializadas no transporte de moléculas concretas. Como a diversidade e fisioloxía das distintas células dun organismo está relacionada en grande medida coa súa capacidade de captar determinados elementos externos, postúlase que debe existir un conxunto de proteínas transportadoras específico para cada tipo celular e para cada momento fisiolóxico;[1] dita expresión diferencial está regulada por medio da transcrición diferencial dos xenes que codifican esas proteínas e da súa tradución, é dicir, por mecanismos xenético-moleculares, mais tamén pola bioloxía celular: ditas proteínas poden requirir unha activación mediada por rutas de sinalización celular, activación a nivel bioquímico ou, mesmo, de localización en vesículas do citoplasma.[2]
Introdución[editar | editar a fonte]
Termodinamicamente, o fluxo de substancias dun compartimento a outro pode realizarse a favor ou en contra dun gradiente de concentración ou electroquímico. Se o intercambio de substancias se realiza a favor do gradiente, é dicir, no sentido dos potenciais decrecentes, o requirimento de enerxía externo ao sistema é nulo; pero se o transporte se fai en contra do gradiente, requírese un gasto de enerxía, enerxía metabólica neste caso.[3] Por exemplo, un mecanismo químico de separación clásico que non require un achegamento de enerxía externo é a diálise: nela, unha membrana semipermeable separa dúas solucións que difiren na concentración dun mesmo soluto. Se a membrana permite o paso de auga pero non o do soluto, ocorre que a auga flúe cara ao compartimento máis concentrado en soluto, coa fin de establecer un equilibrio no cal a enerxía do sistema sexa mínima. Para que ocorra este fluxo, dado que a auga se despraza a favor de gradiente desde un lugar moi concentrado a outro moi diluído (o soluto está na situación oposta), non se require un achegamento de enerxía externo.

A natureza das membranas biolóxicas, especialmente a dos seus lípidos, é anfipática, o que se traduce en que forman unha bicapa que ten unha parte interna hidrofóbica e unha externa hidrofílica, o que permite que surxa unha posibilidade de transporte chamada difusión simple ou difusión pasiva, que consiste na difusión de substancias ao seu través sen gasto de enerxía metabólica e sen axuda de proteínas transportadoras. No caso de que a substancia a transportar posúa unha carga neta, difundirá non só en resposta a un gradiente de concentración, senón tamén ao potencial de membrana, é dicir, ao gradiente electroquímico.
- Permeabilidade relativa dunha bicapa de fosfolípidos a distintas substancias[1]
| Tipo de substancia | Exemplos | Comportamento |
|---|---|---|
| Gases | CO2, N2, O2 | Permean |
| Moléculas polares pequenas sen carga | Urea, auga, etanol | Permean, total ou parcialmente |
| Grandes moléculas polares sen carga | glicosa, frutosa | Non permean |
| Ións | K+, Na+, Cl-, HCO3- | Non permean |
| Moléculas polares cargadas | ATP, aminoácidos, glicosa 6-fosfato | Non permean |
Como son poucas as moléculas que poden difundir a través dunha membrana lipídica, a maioría dos procesos de transporte implican a proteínas de transporte. Trátase de proteínas transmembrana que posúen moitas estruturas en hélice alfa inmersas na matriz lipídica ou ben, polo menos en bacterias, en folla beta.[4] Dita estrutura probablemente implica unha vía de entrada a través de contornos hidrofílicos proteicos que causarían unha distorsión no medio moi hidrofóbico constituído polos lípidos.[1] As proteínas interveñen de diversas formas no transporte: actúan tanto como bombas impulsadas pola enerxía metabólica do ATP, ou como canles de difusión facilitada.
Termodinámica[editar | editar a fonte]
Un proceso fisiolóxico só pode levarse a cabo se non contravén os principios termodinámicos elementais. O transporte de membrana obedece algunhas leis físicas que definen as súas capacidades e utilidade biolóxica.
Un principio xeral da termodinámica que goberna a transferencia de substancias a través de membranas ou outras superficies é que o cambio da enerxía libre, ΔG, para o transporte dun mol dunha substancia cunha concentración C1 nun compartimento, cara a un lugar no que a súa concentración é C2, é de:[5]
Polo que se C2 é menor ca C1, ΔG é tamén negativo, e o proceso é termodinamicamente favorable. Consonte se vai transferindo a enerxía dun compartimento a outro, e se non interveñen outros factores, chégase a un equilibrio onde C2=C1, e, por tanto, ΔG=0. Porén, existen tres circunstancias nas que pode evitarse esta igualdade, circunstancias vitais para o funcionamento in vivo das membranas biolóxicas:[5]
- As macromoléculas dun lado da membrana poden unirse especificamente a un determinado composto ou modificalo quimicamente. Deste modo, aínda que a concentración do composto sexa realmente diferente a ambos os lados da membrana, a súa dispoñibilidade reducida nun dos compartimentos pode facer que, a efectos prácticos, non exista un gradiente que favoreza o transporte.
- Pode existir un potencial eléctrico de membrana a través dela que inflúa na distribución de ións. Por exemplo, para un proceso no que haxa transporte de ións desde o exterior ao interior, ocorre que:
- Onde F é a constante de Faraday e ΔP o potencial de membrana, en voltios. Se ΔP é negativo e Z é positivo, o termo ZFΔP contribúe de forma negativa a ΔG, é dicir, favorece o transporte de catións cara ao interior da célula. Se a diferenza de potencial se mantén, o estado de equilibrio ΔG=0 non corresponderá a unha cantidade equimolecular de ións a ambos os lados da membrana.
- Se se combina ao proceso outro proceso cunha ΔG negativa, o ΔG global deberá ser modificado. Esta situación, común no transporte activo, descríbese segundo:
- Onde ΔGb corresponde a unha reacción favorecida termodinamicamente, como a hidrólise de ATP, ou o cotransporte dun composto que se desprace a favor do seu gradiente.
Tipos[editar | editar a fonte]
Difusión simple[editar | editar a fonte]
- Artigos principais: Difusión e Difusión a través de membrana celular.
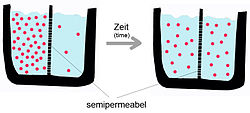
Como se mencionou anteriormente, a difusión pasiva é un fenómeno espontáneo, xa que ten lugar incrementando a entropía do sistema, e diminuíndo a enerxía libre.[5] Non require a intervención de proteínas de membrana, pero si das características da substancia a transportar e da natureza da bicapa. Para o caso dunha membrana fosfolipídica pura, a velocidade de difusión dunha substancia depende do seu:
- gradiente de concentración,
- hidrofobicidade,
- tamaño,
- carga, se a molécula posúe carga neta.
Estes factores afectan de diversa maneira á velocidade de difusión pasiva:
- canto maior gradiente de concentración, maior velocidade de difusión,
- canta maior hidrofobicidade, é dicir, maior coeficiente de partición, maior solubilidade en lípidos e, por tanto, maior velocidade de difusión,
- canto maior tamaño, menor velocidade de difusión,
- dado un potencial de membrana, é dicir, a diferenza de potencial entre a cara exoplasmática e a endoplasmática da membrana, e un gradiente de concentración defínese un gradiente electroquímico que determina as direccións de transporte enerxeticamente favorables dunha molécula cargada, dependendo da natureza desta e do signo do potencial, aínda que a maior parte das células animais posúen carga negativa no seu exterior.[6]
A difusión simple a través da membrana lipídica mostra unha cinética de non saturación, o que significa que a taxa neta de entrada está determinada só pola diferenza no número de moléculas a cada lado da membrana, polo que a entrada aumenta en proporción á concentración de soluto no fluído extracelular. Esta característica distingue a difusión simple dos mecanismos de penetración por canles de transporte mediado.[6]
Difusión facilitada[editar | editar a fonte]

Baixo o mesmo principio termodinámico aplicado no caso da difusión simple, é dicir, que o soluto a transportar se move a favor de gradiente, a difusión facilitada opera de modo similar, pero está facilitada pola existencia de proteínas canle, que son as que facilitan o transporte de, neste caso, auga ou algúns ións e moléculas hidrófilas. Estas proteínas integrais de membrana conforman estruturas en forma de poro inmersas na bicapa, que deixan unha canle interna hidrofílica que permite o paso de moléculas moi lipófobas como as mencionadas anteriormente. A apertura desta canle interna pode ser constitutiva (continua) e desregulada, nos canles non regulados, ou pode requirir un sinal que medie a súa apertura ou peche: é o caso dos canles reguladas.[1]
Transporte activo e cotransporte[editar | editar a fonte]
Nesta modalidade efectúase un transporte en contra do gradiente de concentración ou electroquímico e, para conseguilo, as proteínas transportadoras implicadas consomen enerxía metabólica (comunmente adenosín trifosfato). A hidrólise do composto que actúa como moeda enerxética pode ser moi evidente, como no caso dos transportadores que son ATPases, ou pode ter unha orixe indirecta: por exemplo, os cotransportadores empregan gradientes de determinados solutos para impulsar o transporte dun determinado composto en contra do seu gradiente, a costa da disipación do primeiro gradiente mencionado. Podería parecer que neste caso non intervén un gasto enerxético, mais non é así porque o establecemento do gradiente da substancia transportada colateralmente ao composto obxectivo requiriu a hidrólise de ATP para a súa xeración por medio duns determinados tipos de proteínas denominados bombas.[2]
Defínese transporte activo primario como aquel que hidroliza ATP de forma directa para transportar o composto en cuestión, e transporte activo secundario como aquel que utiliza a enerxía almacenada nun gradiente electroquímico.
O descubrimento da existencia deste tipo de transportadores produciuse ao estudar cineticamente a transferencia de moléculas a través das membranas: para algúns solutos, observouse que a velocidade de entrada chega a unha meseta na súa gráfica ao acadar certa concentración externa a partir da cal non se produce un incremento significativo de velocidade de captación, o que se denomina resposta tipo curva loxística. Interpretouse que o transporte aquí se produce pola formación dun complexo substrato-transportador, conceptualmente idéntico ao complexo encima-substrato da cinética encimática. Cada proteína transportadora posúe unha constante de afinidade polo soluto que é igual á concentración do soluto cando a velocidade de transporte é a metade do seu valor máximo (equivalería, para o caso dun encima, á constante de Michaelis-Menten).[6]
Algunhas características importantes do transporte activo, ademais da súa capacidade de intervir mesmo en contra de gradiente, a súa cinética e o emprego de ATP, son: o seu elevado grao de selectividade e a súa facilidade de inhibición farmacolóxica selectiva.[6]
Transportadores[editar | editar a fonte]
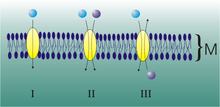
Un transportador pode mobilizar diversos ións e moléculas. Segundo a direccionalidade, distínguense:
- antiportadores: aqueles que transportan un tipo de molécula en contra do seu gradiente ao mesmo tempo que desprazan un ou máis ións diferentes a favor do seu, sendo ambos os gradientes contrapostos.
- simportadores: os que desprazan o composto a transportar en contra do seu gradiente combinando este transporte co desprazamento simultáneo dun ou máis ións diferentes a favor do seu, que, neste caso, é equivalente ao da molécula a transportar.
Ambos os dous reciben o nome de cotransportadores, xa que se transportan dúas cousas á vez.
Bombas[editar | editar a fonte]

Unha bomba é unha proteína que hidroliza ATP para transportar a través dunha membrana un determinado soluto coa fin de xerar un gradiente electroquímico que lle confira á membrana unhas características de potencial. Dito gradiente posúe un interese como un indicador do estado da célula medindo parámetros como o potencial de Nernst, pero ademais intervén activamente no transporte de substancias a través da membrana porque aumenta a entropía do sistema no cotransporte de substancias en contra do seu gradiente.
Unha das bombas de maior importancia en células animais é a bomba de sodio-potasio, que opera por medio do seguinte mecanismo:[7]
- Unión de tres Na+ aos seus sitios activos.
- Fosforilación da cara citoplasmática da bomba que induce a un cambio de conformación na proteína. Esta fosforilación prodúcese pola transferencia do grupo fosfato terminal do ATP a un residuo de ácido aspártico da proteína.
- O cambio de conformación fai que o Na+ se libere ao exterior.
- Unha vez liberado o Na+, únense dúas moléculas de K+ aos seus respectivos sitios de unión da cara extracelular da proteína.
- A proteína desfosforílase producíndose nela un cambio conformacional, o que produce unha transferencia dos ións de K+ ao citosol.
Selectividade de membrana[editar | editar a fonte]
Como a característica primordial do transporte a través dunha membrana biolóxica é a selectividade desta e a súa actuación como barreira específica para determinadas substancias, a fisioloxía subxacente deste fenómeno foi estudada profusamente. Clasicamente, dividiuse o estudo desta propiedade entre electrólitos e non electrólitos.
Selectividade para electrólitos[editar | editar a fonte]
As canles iónicas definen un diámetro interno que permite o paso de pequenos ións de forma máis ou menos específica. Dado que o tamaño do ión está relacionado coa especie química, poderíase asumir a priori que unha canle cun diámetro de poro dabondo grande para que pase por el o ión permitiría tamén o paso doutros de menor tamaño, cousa que na realidade non ocorre na maioría dos casos. Existen dúas características alleas ao tamaño que son importantes na determinación da selectividade dos poros da membrana: a facilidade de deshidratación e a interacción coas cargas do interior do poro.[6]
Para que un ión penetre no poro, debe disociarse das moléculas de auga que o cobren en sucesivas capas de solvatación. A tendencia a deshidratarse, ou a facilidade para facelo, está relacionada co tamaño do ión: os ións grandes fano con máis facilidade cós pequenos, polo que un poro con centros polares febles admitirá preferentemente ións grandes, antes ca pequenos.[6]
Cando o interior da canle está revestido de grupos polares, procedentes das cadeas laterais dos aminoácidos que o compoñen,[7] a interacción do ión deshidratado con estes centros pode ser máis importante cá facilidade de deshidratación para conferir a especificidade da canle. Por exemplo, unha canle revestida de histidinas e arxininas, con grupos cargados positivamente, repelerá de forma selectiva aos ións cargados co mesmo signo, pero facilitará o paso dos cargados negativamente. Ademais, neste caso, os ións máis pequenos poden interaccionar de forma máis próxima por cuestións estéricas, o cal incrementa moito as interaccións carga-carga e, xa que logo, esaxera o efecto.[6]
Selectividade para non electrólitos[editar | editar a fonte]
Os non electrólitos, substancias que xeralmente son hidrófobas e lipófilas, adoitan atravesar a membrana por disolución na bicapa lipídica por difusión simple. A facilidade para difundir neste caso é dependente do coeficiente de partición K, polo xeral, aínda que existen algúns non electrólitos que atravesan a membrana por transporte mediado por un transportador.
No caso de que o non electrólito estea parcialmente cargado, é dicir, sexa máis ou menos polar, como é o caso do etanol, metanol ou urea, permítese o paso a través da membrana por medio de canles acuosas inmersas na membrana. É interesante salientar que non existe un mecanismo de regulación efectivo que estableza barreiras a este transporte, o que implica unha vulnerabilidade intrínseca das células á penetración destas moléculas.[6]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 1,2 1,3 1,4 Lodish; et al. (2005). Buenos Aires: Médica Panamericana, ed. Biología celular y molecular. ISBN 950-06-1974-3.
- ↑ 2,0 2,1 Alberts; et al. (2004). Barcelona: Omega, ed. Biología molecular de la célula. ISBN 54-282-1351-8.
- ↑ Cromer, A.H. (1996). Física para ciencias de la vida. Reverté ediciones. ISBN para España 84-291-1808-X.
- ↑ Prescott, L.M. (1999). McGraw-Hill Interamericana de España, S.A.U., ed. Microbiología. ISBN 84-486-0261-7.
- ↑ 5,0 5,1 5,2 Mathews, C. K. , Van Holde, K.E ; Ahern, K.G (2003). Bioquímica (3ª ed.). ISBN 84-7892-053-2.
- ↑ 6,0 6,1 6,2 6,3 6,4 6,5 6,6 6,7 Randall, D. ; Burggren, W. ; French, K. (1998). Eckert Fisiología animal (4ª ed.). ISBN 84-486-0200-5.
- ↑ 7,0 7,1 Lehninger, Albert (1993). Worth Publishers, ed. Principles of Biochemistry, 2nd Ed. ISBN 0-87901-711-2.
Véxase tamén[editar | editar a fonte]
- Difusión
- Difusión a través de membrana celular
- Transporte activo
- Sinalización celular
- Transdución de sinais



