Glicoquinase
| Glicoquinase | |||||||||
|---|---|---|---|---|---|---|---|---|---|

| |||||||||
| Glicoquinase (hexoquinase 4), baseada en PDB 1GLK | |||||||||
| Identificadores | |||||||||
| Número EC | 2.7.1.2 | ||||||||
| Número CAS | 9001-36-9 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| Gene Ontology | AmiGO / EGO | ||||||||
| |||||||||
A glicoquinase (GK, con Número EC:2.7.1.2) é un encima que cataliza a fosforilación da glicosa a glicosa 6-fosfato. A glicoquinase está presente nas células do fígado, páncreas, intestino, e cerebro de humanos e da maioría dos outros vertebrados. Neses órganos exerce un importante papel na regulación do metabolismo dos carbohidratos ao actuar como un sensor de glicosa, que impulsa cambios no metabolismo ou as funcións celulares en resposta ao incremento ou diminución dos niveis de glicosa, como os que ocorren despois dunha comida ou no xaxún. As mutacións no xene deste encima poden causar formas infrecuentes de diabetes ou hipoglicemia.
A glicoquinase é un isoencima hexoquinase, relacionado con polo menos outras tres hexoquinases homólogas.[1] Todas as hexoquinases poden mediar a fosforilación da glicosa a glicosa 6-fosfato (G6P), que é o primeiro paso na síntese do glicóxeno e na glicólise. Porén, a glicoquinase está codificada nun xene diferente e as súas propiedades cinéticas distintivas permítenlle que interveña nun variado conxunto de funcións. A glicoquinase ten unha menor afinidade pola glicosa que as outras hexoquinases, e a súa actividade está localizada nuns poucos tipos celulares, mentres que as outras tres hexoquinases son as máis importantes na preparación da glicosa para a glicólise e a síntese de glicóxeno na maioría dos tecidos e órganos. Debido á súa reducida afinidade, a actividade da glicoquinase nas condicións fisiolóxicas normais varía substancialmente segundo a concentración de glicosa.[2]
Nomenclatura[editar | editar a fonte]
Outros nomes alternativos deste encima son: hexoquinase IV humana, hexoquinase D, e ATP:D-hexosa 6-fosfotransferase, EC 2.7.1.1 (previamente 2.7.1.2). O nome común glicoquinase deriva da súa relativa especificidade pola glicosa en condicións fisiolóxicas e de que é un encima que fosforila (quinase).
Algúns bioquímicos teñen argumentado que o nome glicoquinase debería ser abandonado por ser enganoso, xa que este encima pode fosforilar outras hexosas nas condicións axeitadas e non só a glicosa, e porque hai encimas distantemente relacionados con ela en bacterias que teñen unha especificidade máis absoluta pola glicosa e que, por esa razón, merecerían máis o nome de glicoquinase e o EC 2.7.1.2Arquivado 19 de outubro de 2003 en Wayback Machine..[2][3] Non obstante, o nome glicoquinase segue a ser o preferido nos campos da medicina e fisioloxía de mamíferos.
Descubriuse en 2004 outra glicosa quinase de mamíferos chamada glicoquinase específica de ADP.[4] O xene deste encima é distinto e similar ao de organismos primitivos. Depende do ADP en vez do ATP (o que suxire a posibilidade de que teña unha función máis efectiva durante a hipoxia), e o seu papel metabólico e importancia aínda debe ser dilucidado.
Catálise[editar | editar a fonte]
Substratos e produtos[editar | editar a fonte]
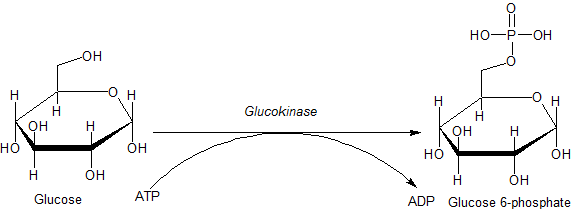
O principal substrato de importancia fisiolóxica deste encima é a glicosa, e o produto máis importante é a glicosa 6-fosfato (G6P). Outro substrato necesario, do cal deriva o fosfato, é a adenosina trifosfato (ATP), que se converte en adenosina difosfato (ADP) cando perde o fosfato. A reacción catalizada pola glicoquinase é:
O ATP participa na reacción en forma dun complexo co ión magnesio como un cofactor. Ademais, en certas condicións, a glicoquinase, igual que outras hexoquinases, pode inducir a fosforilación doutras hexosas (azucres de seis carbonos) e moléculas similares. Xa que logo, a reacción xeral da glicoquinase descríbese máis exactamente como:[3]
- Hexosa + MgATP2- → hexosa-PO32- + MgADP- + H+
Entre as hexosas que funcionan como substratos están a manosa, frutosa, e glicosamina, pero a afinidade da glicoquinase por elas require concentracións que non se encontran nas células, polo que non hai unha actividade significativa.[5]
Cinética[editar | editar a fonte]
A glicoquinase ten dúas importantes propiedades cinéticas que a distinguen doutras hexoquinases, e que lle permiten realizar o seu papel especial de sensor da glicosa.
- A glicoquinase ten unha afinidade pola glicosa menor que outras hexoquinases. A glicoquinase cambia a súa conformación e función en paralelo aos aumentos das concentracións de glicosa no rango fisioloxicamente importante entre 4 e 10 mmol/L (72–180 mg/dL). Está semisaturada a unha concentración de glicosa duns 8 mmol/L (144 mg/dL).[6][7]
- A glicoquinase non é inhibida polo seu produto, a glicosa 6-fosfato.[6] Isto permite unha continua saída do sinal (por exemplo, para promover a liberación de insulina) aínda que haxa cantidades significativas do seu produto.[7]
Estas dúas características fan que poida regular unha vía metabólica "impulsada pola subministración", é dicir, a velocidade de reacción está impulsada pola subministración de glicosa e non pola demanda dos produtos finais.
Outra propiedade distintiva da glicoquinase é a súa moderada cooperatividade con glicosa, cun coeficiente de Hill (nH) de aproximadamente 1,7.[7] A glicoquinase ten un único sitio de unión para a glicosa e é o único encima regulatorio monomérico coñecido que mostra cooperatividade de substrato. Postulouse que a natureza da cooperatividade implica unha "transición lenta" entre dous estados do encima diferentes con distintas taxas de actividade. Se consideramos que o estado dominante depende das concentracións de glicosa, a cooperatividade aparente que produciría sería similar á observada.[8]
Debido a esta cooperatividade, a interacción cinética da glicoquinase coa glicosa non segue a clásica cinética de Michaelis-Menten. En vez de utilizar a Km para a glicosa, é mellor neste encima describir o seu nivel de semisaturación S0,5, que é a concentración á cal o encima está saturado ao 50% e activo.
O S0,5 e o nH extrapólanse a un "punto de inflexión" da curva describindo a actividade encimática como unha función da concentración de glicosa e 4 mmol/L.[9] Noutras palabras, a unha concentración de glicosa de aproximadamente 72 mg/dL, que está preto do extremo baixo do rango normal, a actividade da glicoquinase é máis sensible a pequenos cambios na concentración de glicosa.
A relación cinética co outro substrato, o complexo MgATP, pode describirse pola cinética clásica de Michaelis-Menten, cunha afinidade de aproximadamente 0,3-0,4 mmol/L, bastante por debaixo da típica concentración intracelular de 2,5 mmol/L. O feito de que hai case sempre un exceso de ATP dispoñible implica que as concentracións de ATP raramente inflúen na actividade da glicoquinase.
A actividade específica máxima (kcat, tamén coñecida como taxa de recambio ou turnover rate) da glicoquinase cando está saturada con ambos os substratos é de 62/s.[6]
Ideouse un "modelo matemático mínimo" baseado na información cinética mencionada para predicir a taxa de fosforilación da glicosa nas células beta (BGPR) da glicoquinase normal ("tipo salvaxe") e das súas formas mutantes coñecidas. A BGPR para a glicoquinase salvaxe é dun 28% a unha concentración de glicosa do 5 mmol/L, o que indica que o encima está funcionando a un 28% da capacidade ao limiar usual de glicosa necesario para causar a liberación de insulina.
Mecanismo[editar | editar a fonte]
Os grupos sulfhidrilo de varias cisteínas (Cys) rodean o sitio de unión da glicosa no encima. Todas excepto a Cys 230 son esenciais para o proceso catalítico, xa que forman varias pontes disulfuro durante a interacción cos substratos e reguladores. Polo menos nas células beta do páncreas, a proporción de moléculas de glicoquinase activas e inactivas está en parte determinada polo balance de oxidación dos grupos sulfhidrilo ou a redución de pontes disulfuro.
Estes grupos sulfhidrilo son bastante sensibles ao estado de oxidación das células, o que fai que a glicoquinase sexa un dos compoñentes celulares máis vulnerables ao esterés oxidativo, especialmente nas células beta.
Estrutura[editar | editar a fonte]
| ||||||||||||||||||||||||||||
A glicoquinase é unha proteína monomérica de 465 aminoácidos e unha masa molecular duns 50 kD. Hai polo menos dúas fisuras no encima para a unión de substancias, unha é o sitio activo, onde se une a glicosa e o MgATP, e a outra é para un suposto activador alostérico, que non foi aínda identificado.[11][12]
O encima ten a metade do tamaño doutras hexoquinases, que manteñen un grao de estrutura dimérica. Comparte con outras hexoquinases e glicoquinases de mamífero e outras proteínas varias secuencias e a estrutura tridimensional dos sitios activos esenciais, como o sitio de unión para o ATP, por exemplo, e a estrutura común denomínase pregamento de actina.
Xenética[editar | editar a fonte]
A glicoquinase humana está codificada polo xene GCK do cromosoma 7. Este xene autosómico simple ten 10 exóns.[13][14] Os xenes da glicoquinase doutros animais son homólogos do xene GCK humano.[6][15]
Unha característica distintiva do xene é que comeza con dúas rexións promotoras posibles.[16] O primeiro exón empezando polo extremo 5' contén dúas rexións promotoras específicas de tecido. A transcrición pode empezar por calquera dos promotores (dependendo do tecido) para que así o mesmo xene poida producir unha molécula lixeiramente diferente no fígado e noutros tecidos. As dúas isoformas da glicoquinase difiren só en 13-15 aminoácidos no extremo N-terminal da molécula, o cal produce só unha mínima diferenza na estrutura. As dúas isoformas teñen as mesmas características cinéticas e funcionais.[2]
O primeiro promotor desde o extremo 5', denominado promotor de "augas arriba" (upstream) ou promotor neuroendócrino, é activo nas células dos illotes pancreáticos, tecido nervioso, e enterocitos do intestino delgado e produce neles a "isoforma neuroendócrina" da glicoquinase.[16] O segundo promotor, o de "augas abaixo" (downstream) ou promotor hepático, é activo nos hepatocitos e dirixe a produción da "isoforma hepática".[17] Os dous promotores teñen pouca ou ningunha homoloxía de secuencia e están separados por unha secuencia de 30 kbp, que non se atopou que teña diferenzas funcionais entre as isoformas.[2] Os dous promotores son funcionalmente exclusivos e gobernados por un conxunto distinto de factores regulatorios, para que así a expresión da glicoquinase poida ser regulada por separado en diferentes tecidos.[2] Os dous promotores correspóndense con dous grandes tipos de funcións da glicoquinase: no fígado, a glicoquinase actúa como portal para o "procesamento en masa" da glicosa dispoñible, mentres que nas células neuroendócrinas actúa como sensor, iniciando respostas celulares que afectan ao metabolismo de carbohidratos de todo o corpo.
Distribución nos órganos[editar | editar a fonte]
A glicoquinase atopouse en células específicas de catro tipos de tecidos de mamíferos, que son: fígado, páncreas, intestino delgado, e partes do encéfalo. En todos xoga un papel fundamental na resposta ao aumento ou diminución dos niveis de glicosa no sangue.
- As células predominantes do fígado son os hepatocitos, e a glicoquinase encóntrase no fígado exclusivamente nelas. Durante a dixestión dunha comida de carbohidratos, cando a glicosa sanguínea está elevada e os niveis de insulina son altos, os hepatocitos retiran a glicosa do sangue e almacénana no seu interior en forma de glicóxeno. Despois de completarse a dixestión e absorción, o fígado fabrica glicosa tanto a partir de substratos non compostos de glicosa (por gliconeoxénese) coma do glicóxeno (glicoxenólise), e expórtaa ao sangue, para manter un adecuado nivel de glicosa sanguíneo durante o xaxún. Como a actividade da glicoquinase se eleva rapidamente a medida que a concentración de glicosa aumenta, o encima serve como un interruptor metabólico central que cambia o metabolismo hepático dos carbohidratos entre os estados de saciedade e xaxún. A fosforilación da glicosa a glicosa 6-fosfato feita pola glicoquinase facilita o almacenamento da glicosa en forma de glicóxeno e o seu uso para a glicólise. O promotor hepático adicional do seu xene permite que a glicoquinase sexa regulada de forma diferente nos hepatocitos e nas células neuroendócrinas.
- As células neuroendócrinas do páncreas, intestino, e cerebro comparten algúns aspectos comúns da produción de glicoquinase, regulación, e función.[18] As células destes tecidos denomínanse en conxunto células "neuroendócrinas" neste contexto.
- As células beta e alfa dos illotes de Langerhans pancreáticos.
- As células beta liberan insulina en resposta ao aumento dos niveis de glicosa. A insulina promoverá en moitos tipos de células a importación e uso da glicosa, e sinaliza ao fígado para que sintetice glicóxeno. As células alfa producen menos glicagón en resposta á elevación dos niveis de glicosa, e máis glicagón se a glicosa sanguínea está baixa. O glicagón serve como sinal ao fígado para que este degrade o glicóxeno e libere glicosa ao sangue. A glicoquinase nas células beta serve como un sensor de glicosa, amplificando a secreción de insulina a medida que aumenta a glicosa no sangue.
- Neuronas sensibles á glicosa do hipotálamo.
- En resposta ao aumento ou diminución dos niveis de glicosa, as células do hipotálamo polarízanse e despolarízanse. Entre as reaccións neuroendócrinas do sistema nervioso central á hipoglicemia está a activación das respostas adrenérxicas do sistema nervioso autónomo. A glicoquinase probablemente serve como un sinal de glicosa tamén aquí. A glicoquinase tamén se encontrou nas células da pituitaria anterior.
- Os enterocitos do intestino delgado.
- Este é o sistema sensor da glicoquinase peor comprendido. Parece probable que as respostas á entrada de glicosa durante a dixestión xoguen un papel na amplificación da incretina da secreción de insulina durante a comida, ou na xeración de sinais de saciedade desde o intestino ao cerebro.
- As células beta e alfa dos illotes de Langerhans pancreáticos.
Distribución entre as especies[editar | editar a fonte]
A glicoquinase hepática está amplamente distribuída entre as especies de vertebrados, pero non universalmente. A estrutura do xene e a secuencia de aminoácidos están moi conservadas entre a maioría dos animais (por exemplo, a glicoquinase da rata e a humana son homólogas en máis dun 80%). Porén, hai algunhas excepcións infrecuentes: Por exemplo, non se descubriu en gatos nin en morcegos, aínda que a posúen algúns réptiles, aves, anfibios, e peixes. Non está claramente determinado se a glicoquinase aparece por igual en páncreas e outros órganos. Postulouse que a presenza de glicoquinase no fígado é un reflexo da facilidade coa que estes animais poden incluír os carbohidratos na súa dieta.
Función e regulación[editar | editar a fonte]
A maioría da glicoquinase nos mamíferos encóntrase no fígado, e da glicoquinase depende aproximadamente o 95% da actividade de hexoquinase nos hepatocitos. A fosforilación da glicosa a glicosa 6-fosfato (G6P) pola glicoquinase é o primeiro paso da síntese de glicóxeno e da glicólise no fígado.
Cando está dispoñible unha gran cantidade de glicosa, a síntese de glicóxeno ten lugar na periferia dos hepatocitos ata que as células están ateigadas de glicóxeno. O exceso de glicosa convértese despois cada vez en maior medida en triglicéridos para a exportación e almacenamento no tecido adiposo. A actividade da glicoquinase no citoplasma aumenta e diminúe segundo a dispoñibilidade de glicosa.
A G6P, que é o produto da glicoquinase, é o principal substrato da síntese de glicóxeno, e a glicoquinase ten unha estreita asociación funcional e regulatoria coa síntese de glicóxeno. Cando a glicoquinase está activa ao máximo, a glicóxeno sintase parece estar localizada nas mesmas áreas periféricas do citoplasma dos hepatocitos nas cales ten lugar a síntese de glicóxeno. A subministración de G6P afecta á velocidade de síntese do glicóxeno non só como substrato primario, senón por estimulación directa da glicóxeno sintase e a inhibición da glicóxeno fosforilase.
A actividade glicoquinase pode ser rapidamente amplificada ou reducida en resposta a cambios na subministración de glicosa, que se orixinan normalmente pola inxestión de comida e o xaxún. A regulación ocorre a varios niveis e velocidades, e está influenciada por moitos factores que afectan principalmente a dous mecanismos xerais:
- A actividade da glicoquinase pode ser amplificada ou reducida en minutos pola acción da proteína reguladora da glicoquinase (GKRP). As accións desta proteína están influenciadas por pequenas moléculas como a glicosa e a frutosa.
- A cantidade de glicoquinase pode ser incrementada pola súa síntese en maior cantidade. A insulina é o sinal principal para que se incremente a súa transcrición, e opera principalmente por medio dun factor de transcrición chamado proteína de unión ao elemento regulatorio esterol-1c (SREBP1c) excepto no fígado. Isto ocorre unha hora despois do incremento dos niveis de insulina, como despois dunha comida abundante en carbohidratos.
Transcricional[editar | editar a fonte]
A insulina actúa por medio da proteína de unión ao elemento regulatorio esterol-1c (SREBP1c), e crese que é o activador directro máis importante da transcrición do xene da glicoquinase nos hepatocitos. A SREBP1c é un factor de transcrición de cremalleira de leucina de hélice básica-bucle-hélice (bHLHZ) transactivador. Este tipo de transactivadores únense á secuencia "caixa E" dos xenes de varios encimas regulatorios. O promotor hepático do primeiro exón do xene da glicoquinase contén unha caixa E, que parece ser o elemento de resposta á insulina principal deste xene nos hepatocitos. Pensábase inicialmente que a SREBP1c tiña que estar presente para que tivese lugar a transcrición da glicoquinase nos hepatocitos, pero comprobouse recentemente que a transcrición da glicoquinase podía realizarse normalmente en ratos knockout para a SREBP1c (que non a expresan). Os niveis de SREBP1c increméntanse en resposta a unha dieta alta en carbohidratos, presumiblemente como un efecto directo das frecuentes elevacións de insulina. O incremento da transcrición pode detectarse menos dunha hora despois de que os hepatocitos sexan expostos a un incremento dos niveis de insulina.
A frutosa 2,6-bisfosfato (F2,6P2) tamén estimula a transcrición da glicoquinase, e parece que o fai a través de Akt2 en vez de por medio de SREBP1c. Non se sabe se este efecto é un dos efectos xerados corrente abaixo da activación dos receptores da insulina ou independentemente da acción da insulina. Os niveis de F2,6P2 xogan outros papeis amplificadores na glicólise dos hepatocitos.
Outros factores que actúan en trans que se sospeita que xogan un papel na regulación da transcrición nas células hepáticas son:
- O factor nuclear hepático-4-alfa (HNF4α) é un receptor nuclear orfo importante na transcrición de moitos xenes de encimas do metabolismo de carbohidratos e lípidos. Activa a transcrición do xdene GCK.
- O factor estimulatorio corrente arriba 1 (USF1) é outro factor de transcrición de cremalleira de leucina de hélice-bucle-hélice básica (bHLHZ) transactivador.
- O factor nuclear hepático 6 (HNF6) é un regulador da transcrición homeodominio da clase de "un corte". O HNF6 está tamén implicado na regulación da transcrición de encimas gliconeoxénicos como a glicosa-6-fosfatase e a fosfoenolpiruvato carboxiquinase.
Hormonal e dietaria[editar | editar a fonte]
A insulina é con diferenza o hormona máis importante que ten efectos directos ou indirectos na expresión da glicoquinase e a súa actividade no fígado. A insulina parece afectar tanto á transcrición da glicoquinase coma a actividade por medio de moitas vías directas e indirectas. Aínda que o incremento dos niveis de glicosa na vea porta fai aumentar a actividade da glicoquinase, o aumento concomitante de insulina amplifica este efecto por indución da síntese da glicoquinase. A transcrición da glicoquinase empeza a aumentar unha hora despois do aumento dos niveis de insulina. A transcrición da glicoquinase faise case indetectable en períodos de fame prolongados, deprivación grave de carbohidratos, ou diabetes deficiente en insulina non tratada.
Os mecanismos polos cales a insulina induce a síntese de glicoquinase pode implicar as dúas principais vías intracelulares da acción da insulina, a cascada da quinase regulada por sinal extracelular (ERK 1/2), e a cascada da fosfoinosítido 3-quinase (PI3-K). Esta última pode operar por medio do transactivador FOXO1.
Non obstante, como se podería agardar dado o seu efecto antagonista sobre a síntese do glicóxeno, o glicagón e o seu segundo mensaxeiro intracelular o AMPc suprimen a transcrición e actividxade da glicoquinase, mesmo en presenza de insulina.
Outras hormonas como a triiodotironina (T3) e os glicocorticoides orixinan efectos permisivos ou estimulatorios sobre a glicoquinase en certas circunstancias. A biotina e o ácido retinoico incrementan a transcrición do ARNm do xene GCK e a actividade da glicoquinase. Os ácidos graxos en cantidades significativas amplifican a actividade da glicoquinase no fígado, mentres que o acilo de cadea longa-CoA o inhibe.
Hepática[editar | editar a fonte]
A glucoquinase pode ser activada e inactivada rapidamente nos hepatocitos por unha proteína reguladora chamada proteína reguladora da glicoquinase (GKRP), que opera para manter inactiva a reserva de glicoquinase, a cal pode rapidamente quedar dispoñible en resposta ao aumento do nivel de glicosa na vea porta.[19]
A GKRP móvese do núcleo ao citoplasma e viceversa dos hepatocitos e pode quedar enganchada aos microfilamentos do citoesqueleto. Forma complexos 1:1 reversibles coa glicoquinase, e pode movela do citoplasma ao núcleo. Actúa como inhibidor competitivo coa glicosa, para que a actividade do encima se reduza a case cero mentres está unida. Os complexos glicoquinase:GKRP quedan confinados no núcleo mentres que os niveis de glicosa e frutosa sexan baixos. O confinamento nuclear pode servir para protexer á glicoquinase da degradación pola acción das proteases citoplásmicas. A glicoquinase pode ser liberada rapidamente da súa unión coa GKRP en resposta ao incremento dos niveis de glicosa. A diferenza da glicoquinase das células beta, a glicoquinase dos hepatocitos non está asociada coas mitocondrias.
A frutosa en moi pequenas cantidades, micromolares, (despois da fosforilación pola cetohexoquinase a frutosa 1-fosfato) acelera a liberación da glicoquinase da GKRP. Esta sensibilidade ante a presenza de pequenas cantidades de frutosa permite que a GKRP, a glicoquinase, e a cetohexoquinase actúen como un "sistema sensor da frutosa", que sinala que se está a dixerir unha comida con diversos carbohidratos, e acelera a utilización da glicosa. Porén, a frutosa 6-fosfato potencia a unión da glicoquinase coa GKRP. A frutosa 6-fosfato fai decrecer a fosforilación da glicosa pola glicoquinase cando a glicoxenólise ou gliconeoxénese están funcionanado. Tanto a frutosa 1-fosfato coma a frutosa 6-fosfato únense ao mesmo sitio de unión na GKRP. Postúlase que se producen dúas conformacións da GKRP, unha que pode unirse á glicoquinase e a outra non.
Pancreática[editar | editar a fonte]
Aínda que a maioría da glicoquinase do corpo está no fígado, hai pequenas cantidades nas células beta e alfa do páncreas, en certas neuronas hipotalámicas, e en células específicas (enterocitos) do intestino, que xogan un papel que cada vez se considera máis importante na regulación do metabolismo de carbohidratos. No contexto da función da glicoquinase, estes tipos de células denomínanse en conxunto como tecidos neuroendócrinos, e comparten algúns aspectos da regulación e función da glicoquinase, especialmente o promotor neuroendócrino común. Das células neuroendócrinas, as células beta dos illotes de Langerhans son as mellor estudadas e coñecidas. É probable que moitas das relacións regulatorias descubertas nas células beta existan noutros tecidos neuroendócrinos que teñen glicoquinase.
Un sinal para a insulina[editar | editar a fonte]
Nas células beta dos illotes, a actividade da glicoquinasae serve como un control principal da secreción de insulina en resposta ao aumento dos niveis de glicosa en sangue. A medida que se consome a glicosa 6-fosfato, as cantidades crecentes de ATP inician unha serie de procesos que orixinan unha liberación de insulina. Unha das consecuencias inmediatas do incremento da respiración celular é un aumento nas concentracións de NADH e NADPH (abreviados en conxunto como NAD(P)H). Este cambio no estado redox das células beta orixina un incremento dos niveis de calcio intracelular, pechando as canles de KATP, a despolarización da membrana plasmática, a fusión dos gránulos secretorios de insulina coa membrana, e a liberación da insulina no sangue.
O feito de que a glicoquinase exerza o maior efecto nos niveis de azucre sanguíneo e na dirección global do metabolismo de carbohidratos é un sinal para a liberación da insulina . A glicosa, á súa vez, influencia tanto a actividade inmediata coma a cantidade de glicoquinase producida nas células beta.
Regulación das células beta[editar | editar a fonte]
A glicosa amplifica inmediatamente a actividde da glicoquinase por un efecto cooperativo.
Un segundo e importante regulador rápido da actividade da glicoquinase nas células beta é a interacción directa proteína-proteína entre a glicoquinase e o "encima bifuncional" (fosfofrutoquinase-2/frutosa-2,6-bisfosfatase), que tamén xoga un papel na regulación da glicólise. Esta asociación física estabiliza a glicoquinase nunha conformación cataliticamente favorable (o oposto do efecto que fai a unión da GKRP) que potencia a súa actividade.
En só 15 minutos, a glicosa pode estimular a transcrición do xene GCK e a síntese de glicoquinase por medio da insulina. A insulina prodúcena as células beta, pero parte dela actúa sobre os receptores de insulina de tipo B das células beta, exercendo unha amplificación por retroalimentación positiva autócrina da actividade da glicoquinase. Hai ademais unha amplificación pola acción da insulina nos receptores de tipo A que estimulan a súa propia transcrición.
A transcrición do xene GCK iníciase por medio do promotor de "augas arriba" ou neuroendócrino. Este promotor, a diferenza do promotor hepático, ten elementos homólogos con outros promotores de xenes inducidos pola insulina. Entre os probables factores que actúan en trans están Pdx-1 e PPARγ. Pdx-1 é un factor de transcrición homeodominio implicado na diferenciación do páncreas. PPARγ é un receptor nuclear que responde aos fármacos glitazone ao aumentar a sensibilidade á insulina.
Asociación cos gránulos secretores de insulina[editar | editar a fonte]
Moita da glicoquinase que se encontra no citoplasma das células beta (pero non toda) está asociada cos gránulos secretores de insulina e coas mitocondrias. A proporción de encima unido a eles cae rapidamente en resposta a un aumento da glicosa e da secreción de insulina. Suxeriuse que a unión do encima nestes lugares ten un propósito similar á da proteína reguladora da glicoquinase hepática, que protexe á glicoquinase da degradación para que estea rapidamente dispoñible cando aumentan os niveis de glicosa. O efecto é amplificar a resposta da glicoquinase á glicosa máis rapidamente do que podería facerse mediante a transcrición de máis encima.[20]
Supresión do glicagón nas células alfa[editar | editar a fonte]
Propúxose tamén que a glicoquinase ten un papel de sensor da glicosa nas células alfa pancreáticas, pero as evidencias son menos consistentes, e algúns investigadores non atoparon probas de actividade de glicoquinase nesas células. As células alfa encóntranse nos illotes de Langerhans pancreáticos, mesturadas coas células beta e outras células. Aínda que as células beta responden aos aumentos no nivel de glicosa segregando insulina, as células alfa responden reducindo a secreción de glicagón. Cando a concentración de glicosa en sangue diminúe ata niveis hipoglicémicos, as células alfa liberan glicagón. O glicagón é unha hormona proteica que bloquea o efecto da insulina nos hepatocitos, inducindo a glicoxenólise e gliconeoxénese, e reducindo a actividade da glicoquinase nos hepatocitos. Non está aínda claro o grao no cal a supresión do glicagón pola glicosa é un efecto directo da glicosa a través da vía da glicoquinase nas células alfa, ou, polo contrario, un efecto indirecto mediado pola insulina ou outros sinais das células beta.
Hipotalámica[editar | editar a fonte]
Aínda que todas as neuronas utilizan a glicosa como fonte de enerxía, certas neuronas sensibles á glicosa alteran a súa velocidade de envío de impulsos en resposta ao incremento ou diminución dos niveis de glicosa. Estas neuronas sensibles á glicosa están concentradas principalmente no núcleo ventromedial e no núcleo arqueado do hipotálamo, os cales regulan moitos aspectos da homeostase da glicosa (especialmente a resposta á hipoglicemia), utilización de fontes de enerxía, saciedade e apetito, e mantemento do peso corporal. Estas neuronas son máis sensibles aos cambios de glicosa no intervalo de concentracións de 0,5-3,5 mmol/L de glicosa.
A glicoquinase atopouse no encéfalo fundamentalmente nas mesma áreas que conteñen neuronas sensibles á glicosa, como os dous núcleos hipotalámicos mencionados. A inhibición da glicoquinase elimina a resposta do núcleo ventromedial á comida. Porén, os niveis da glicosa no cerebro son menores que os niveis plasmáticos, normalmente de 0,5-3,5 mmol/L. Aínda que este rango de concentracións corresponde co da sensibilidade das neuronas sensibles á glicosa, está por debaixo da sensibilidade de inflexión óptima para a glicoquinase. A presunción, baseada en probas indirectas e especulacións, é que a glicoquinase neuronal está dalgún modo exposta aos niveis de glicosa do plasma sanguíneo mesmo nas neuronas.
Os enterocitos e a incretina[editar | editar a fonte]
Aínda que a glicoquinase aparece en certas células do intestino delgado (enterocitos) e estómago, a súa función e regulación non é ben comprendida. Suxeriuse que tamén aquí a glicoquinase funciona como sensor de glicosa, o que permite que estas células realicen a primeira resposta metabólica á entrada de carbohidratos no corpo. Sospéitase que estas células están implicadas nas funcións de incretina.
Importancia clínica[editar | editar a fonte]
Como a insulina é un dos reguladores da síntese da glicoquinase máis importantes, se non o que máis, todos os tipos de diabetes diminúen a síntse de glicoquinase e a súa actividade mediante varios mecanismos. A actividade da glicoquinase é sensible ao estrés oxidativo das células, especialmente nas células beta.
Descubríronse unhas 200 mutacións do xene da glicoquinase humana GCK, que poden cambiar a eficiencia da unión da glicosa ao encima e da fosforilación, incrementar ou diminuír a sensibilidade da secreción de insulina nas células beta en resposta á glicosa, e producir unha hiperglicemia ou hipoglicemia clinicamente significativas.
Diabetes[editar | editar a fonte]
Unhas 190 destas mutacións reducen a eficiencia funcional da glicoquinase. Os heterocigotos para os alelos con actividade reducida para o encima orixinan que haxa un limiar máis alto para a liberación de insulina e unha hiperglicemia leve persistente. esta condición denomínase MODY2 (maturity onset diabetes of the young type 2).
Os homocigotos para os alelos GCK coa función reducida poden causar deficiencia de insulina conxénita grave, que dá lugar a unha diabetes neonatal persistente.
Hipoglicemia hiperinsulinémica[editar | editar a fonte]
Ata 2004 descubríranse 5 mutacións que aumentaban a secreción de insulina. A heterocigosidade para as mutacións que producen unha ganancia de función reducen o limiar de glicosa que activa a liberación de insulina. Isto crea hipoglicemia con patróns variados, como o hiperinsulinismo conxénito persistente ou transitorio, ou a hipoglicemia reactiva ou do xaxún que aparece na idade adulta.
Non se atoparon casos de homocigosidade para as mutacións de ganancia de función.
Diana de fármacos[editar | editar a fonte]
Varios laboratorios financiados por compañías farmacéuticas están investigando moléculas que activan a glicoquinase coa esperanza de que isto sexa útil no tratamento da diabetes mellitus de tipo 2.[21][22] O potencial activador da glicoquinase MK-0941 orixina melloras na glicemia non sostidas, e un incremento da presión arterial e do risco de hipoglicemia.[23]
Notas[editar | editar a fonte]
- ↑ Kawai S, Mukai T, Mori S, Mikami B, Murata K (2005). "Hypothesis: structures, evolution, and ancestor of glucose kinases in the hexokinase family". J. Biosci. Bioeng. 99 (4): 320–30. PMID 16233797. doi:10.1263/jbb.99.320.
- ↑ 2,0 2,1 2,2 2,3 2,4 Iynedjian PB (2009). "Molecular physiology of mammalian glucokinase". Cell. Mol. Life Sci. 66 (1): 27–42. PMC 2780631. PMID 18726182. doi:10.1007/s00018-008-8322-9.
- ↑ 3,0 3,1 Cardenas, M.L. (2004). "Comparative biochemistry of glucokinase". En Matschinsky, F.M.; Magnuson, M.A. Glucokinase And Glycemic Disease: From Basics to Novel Therapeutics (Frontiers in Diabetes). Basel: S. Karger AG (Switzerland). pp. 31–41. ISBN 3-8055-7744-3.
- ↑ Ronimus RS, Morgan HW (2004). "Cloning and biochemical characterization of a novel mouse ADP-dependent glucokinase". Biochem. Biophys. Res. Commun. 315 (3): 652–8. PMID 14975750. doi:10.1016/j.bbrc.2004.01.103.
- ↑ Magnuson, M.A.; Matschinsky, F.M. (2004). "Glucokinase as a glucose sensor: past, present, and future". En Matschinsky, F.M.; Magnuson, M.A. Glucokinase And Glycemic Disease: From Basics to Novel Therapeutics (Frontiers in Diabetes). Basel: S. Karger AG (Switzerland). pp. 18–30. ISBN 3-8055-7744-3.
- ↑ 6,0 6,1 6,2 6,3 Bell, G.I.; Cuesta-Munoz, A.; Matschinsky, F.M. (2002). "Glucokinase". Encyclopedia of Molecular Medicine. Hoboken: John Wiley & Sons. ISBN 978-0-471-37494-7.
- ↑ 7,0 7,1 7,2 Matschinsky FM (1996). "Banting Lecture 1995. A lesson in metabolic regulation inspired by the glucokinase glucose sensor paradigm". Diabetes 45 (2): 223–41. PMID 8549869. doi:10.2337/diabetes.45.2.223.
- ↑ Heredia VV, Thomson J, Nettleton D, Sun S (2006). "Glucose-induced conformational changes in glucokinase mediate allosteric regulation: transient kinetic analysis". Biochemistry 45 (24): 7553–62. PMID 16768451. doi:10.1021/bi060253q.
- ↑ Matschinsky FM, Glaser B, Magnuson MA (1998). "Pancreatic beta-cell glucokinase: closing the gap between theoretical concepts and experimental realities". Diabetes 47 (3): 307–15. PMID 9519733. doi:10.2337/diabetes.47.3.307. Arquivado dende o orixinal o 30 de maio de 2020. Consultado o 03 de decembro de 2013.
- ↑ Lunin VV, Li Y, Schrag JD, Iannuzzi P, Cygler M, Matte A (2004). "Crystal structures of Escherichia coli ATP-dependent glucokinase and its complex with glucose". J. Bacteriol. 186 (20): 6915–27. PMC 522197. PMID 15466045. doi:10.1128/JB.186.20.6915-6927.2004.
- ↑ Mahalingam B, Cuesta-Munoz A, Davis EA, Matschinsky FM, Harrison RW, Weber IT (1999). "Structural model of human glucokinase in complex with glucose and ATP: implications for the mutants that cause hypo- and hyperglycemia". Diabetes 48 (9): 1698–705. PMID 10480597. doi:10.2337/diabetes.48.9.1698.
- ↑ Kamata K, Mitsuya M, Nishimura T, Eiki J, Nagata Y (2004). "Structural basis for allosteric regulation of the monomeric allosteric enzyme human glucokinase". Structure 12 (3): 429–38. PMID 15016359. doi:10.1016/j.str.2004.02.005.
Fermosas imaxes estruturais que ilustran os cambios conformacionais e os mecanismos regulatorios potenciais.
- ↑ Matsutani A, Janssen R, Donis-Keller H, Permutt MA (1992). "A polymorphic (CA)n repeat element maps the human glucokinase gene (GCK) to chromosome 7p". Genomics 12 (2): 319–25. PMID 1740341. doi:10.1016/0888-7543(92)90380-B.
- ↑ Stoffel M, Froguel P, Takeda J, Zouali H, Vionnet N, Nishi S, Weber IT, Harrison RW, Pilkis SJ, Lesage S (1992). "Human glucokinase gene: isolation, characterization, and identification of two missense mutations linked to early-onset non-insulin-dependent (type 2) diabetes mellitus". Proc. Natl. Acad. Sci. U.S.A. 89 (16): 7698–702. PMC 49778. PMID 1502186. doi:10.1073/pnas.89.16.7698.
- ↑ Wilson, J.E. (2004). "The hexokinase gene family". En Matschinsky, F.M.; Magnuson, M.A. Glucokinase And Glycemic Disease: From Basics to Novel Therapeutics (Frontiers in Diabetes). Basel: S. Karger AG (Switzerland). pp. 18–30. ISBN 3-8055-7744-3.
- ↑ 16,0 16,1 Iynedjian PB, Pilot PR, Nouspikel T; et al. (1989). "Differential expression and regulation of the glucokinase gene in liver and islets of Langerhans". Proc. Natl. Acad. Sci. U.S.A. 86 (20): 7838–42. PMC 298166. PMID 2682629. doi:10.1073/pnas.86.20.7838.
- ↑ Iynedjian PB, Jotterand D, Nouspikel T, Asfari M, Pilot PR (1989). "Transcriptional induction of glucokinase gene by insulin in cultured liver cells and its repression by the glucagon-cAMP system". J. Biol. Chem. 264 (36): 21824–9. PMID 2557341. Arquivado dende o orixinal o 30 de maio de 2020. Consultado o 03 de decembro de 2013.
- ↑ Jetton TL, Liang Y, Pettepher CC; et al. (1994). "Analysis of upstream glucokinase promoter activity in transgenic mice and identification of glucokinase in rare neuroendocrine cells in the brain and gut". J. Biol. Chem. 269 (5): 3641–54. PMID 8106409. Arquivado dende o orixinal o 30 de maio de 2020. Consultado o 03 de decembro de 2013.
- ↑ Cárdenas, María Luz (1995). "Glucokinase": Its Regulation and Role in Liver Metabolism (Molecular Biology Intelligence Unit). R G Landes Co. ISBN 1-57059-207-1.
This is the most detailed treatment of liver glucokinase
- ↑ Arden C, Harbottle A, Baltrusch S, Tiedge M, Agius L (2004). "Glucokinase is an integral component of the insulin granules in glucose-responsive insulin secretory cells and does not translocate during glucose stimulation". Diabetes 53 (9): 2346–52. PMID 15331544. doi:10.2337/diabetes.53.9.2346.
- ↑ Jain, A. Glucokinase Activators in Diabetes Management
- ↑ Matschinsky, Franz (17 April 2009). "Assessing the potential of glucokinase activators in diabetes therapy" 8 (5): 399–419. doi:10.1038/nrd2850. Consultado o 4/1/2011.
- ↑ Meininger GE, Scott R, Alba M, Shentu Y, Luo E, Amin H, Davies MJ, Kaufman KD, Goldstein BJ (2011). "Effects of MK-0941, a novel glucokinase activator, on glycemic control in insulin-treated patients with type 2 diabetes.". Diabetes Care 34 (12): 2560–6. PMID 21994424.