Metaloproteína

Unha metaloproteína é unha proteína que contén un ión metálico como cofactor.[1] As funcións das metaloproteínas son moi variadas nas células, actuando como encimas, proteínas de transporte e almacenamento, e na transdución de sinais. De feito, aproximadamente dun cuarto a un terzo de todas as proteínas requiren metais para levar a cabo as súas funcións,[2] e algunhas estimacións indican que poderían chegar a case a metade.[3] O metal adoita estar coordinado por átomos de nitróxeno, oxíxeno ou xofre pertencentes aos aminoácidos da cadea polipeptídica e/ou a un ligando macrocíclico incorporado á proteína. A presenza dos ións metálicos nos metaloencimas permítelles levar a cabo funcións tales como reaccións redox que non poden realizarse facilmente polo conxunto limitado de grupos funcionais que se encontran nos aminoácidos.[4]
Química de coordinación nas metaloproteínas[editar | editar a fonte]
Nas metaloproteínas os ións metálicos están normalmente coordinados por centros de nitróxeno, oxíxeno ou xofre que pertencen a residuos de aminoácidos da proteína. Estes grupos doantes proporciónanos a miúdo as cadeas laterais dos aminoácidos. Son especialmente importantes os substituíntes imidazol da histidina, ou os tiolato da cisteína, e os grupos carboxilato do aspartato. Dada a gran diversidade do metaloproteoma, viuse que virtualmente todos os residuos de aminoácidos poden unirse a centros metálicos. O esqueleto do péptido tamén proporciona grupos doantes, que inclúen amidas desprotonadas e os centros amida oxíxeno do carbonilo.
Ademais dos grupos doantes proporcionados polos aminoácidos, funcionan tamén como ligandos un gran número de cofactores orgánicos. Quizais os máis famosos son os ligandos tetradentados N4 macrocíclicos incorporados nas hemoproteínas. Ligandos inorgánicos como o sulfuro e óxido son tamén comúns.
Metaloproteínas de almacenamento e transporte[editar | editar a fonte]
Transportadores de oxíxeno[editar | editar a fonte]
A hemoglobina (Hb) é o principal transportador de oxíxeno en humanos. Ten catro subunidades nas que o ión de ferro(II) está coordinado polo ligando plano macrocíclico protoporfirina IX (PIX) e o átomo de nitrógeno do imidazol dun residuo de histidina, formando un grupo hemo. O sesto sitio de coordinación contén unha molécula de auga ou unha molécula de dioxíxeno (O2). O sitio activo encóntrase nun peto hidrofóbico, o que é importante, xa que doutro modo o ferro(II) se oxidaría de forma irreversible a ferro(III). A constante de equilibrio para a formación de HbO2 ten un valor que permite que o oxíxeno sexa captado ou liberado en función da presión parcial de oxíxeno nos pulmóns ou nos músculos. Na hemoglobina as catro subunidades mostran un efecto cooperativo, que permite unha doada transferencia de oxíxeno da hemoglobina sanguínea á mioglobina muscular.
A hemeritrina é outro transportador de oxíxeno que contén ferro. O sitio de unión do oxíxeno é un centro de ferro binuclear. Os átomos de ferro están coordinados á proteína a través de carboxilatos das cadeas laterais de glutamato, aspartato e cinco residuos de histidina. A incorporación de O2 pola hemeritrina está acompañada da oxidación de dous electróns do centro reducido binuclear, coa produción de peróxido (OOH-). Os mecanismos de captura e liberación de oxíxeno coñécense en detalle.[5][6]
As hemocianinas transportan oxíxeno no sangue da maioría dos moluscos e algúns artrópodos como o cangrexo ferradura (Limulus polyphemus). É o segundo encima transportador de oxíxeno máis abundante, despois da hemoglobina. Na oxixenación os dous átomos de cobre(I) do sitio activo oxídanse a cobre(II) e as moléculas de dioxíxeno (O2) redúcense a peróxido (O22-).[7][8]
Citocromos[editar | editar a fonte]
Os citocromos posúen un átomo de ferro que na maioría dos casos se encontra coordinado a un grupo hemo. Os citocromos funcionan como vectores de transferencia de electróns oxidando ferro(II) a ferro(III). As diferenzas entre os citocromos están nas distintas cadeas laterais; por exemplo o citocromo a ten un grupo prostético hemo A e un citocromo b ten un grupo prostético hemo B. Estas diferenzas tradúcense en diferentes potenciais redox Fe2+/Fe3+ de tal maneira que son varios os citocromos que participan na cadea de transporte de electróns mitocondrial.[9]
Os encimas do citocromo P450 desempeñan a función de inserción dun átomo de oxíxeno nun enlace C-H, unha reacción de oxidación.[10][11]
Rubredoxina[editar | editar a fonte]
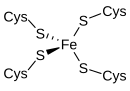
A rubredoxina é un portador de electróns encontrado en bacterias e arqueas que metabolizan xofre. O sitio contén un ión de ferro que é coordinado polos átomos de xofre de catro residuos de cisteína, que forman un tetraedro case regular. As rubredoxinas realizan procesos de transferencia dun electrón. O estado de oxidación do átomo de ferro muda entre os estados +2 e +3. En ambos os estados de oxidación do metal hai un spin alto o que axuda a minimizar os cambios estruturais.
Plastocianina[editar | editar a fonte]

A familia da plastocianina está formada por proteínas do cobre azuis implicadas en reaccións de transferencia de electróns. O sitio de unión ao cobre descríbese como "piramidal trigonal distorsionado".[12] O plano trigonal da base piramidal está composto por dous átomos de nitróxeno (N1 e N2) de dúas histidinas distintas e un xofre (S1) dunha cisteína. O xofre (S2) dunha metionina axial forma o ápice. A "distorsión" ocorre nas lonxitudes dos enlaces entre os ligandos cobre e o xofre. O contacto Cu-S1 é máis curto (207 picómetros) ca o Cu-S2 (282 pm). O enlace alongado Cu-S2 desestabiliza a forma do CuII e incrementa o potencial redox da proteína. A cor azul (pico de absorción de 597 nm) débese ao enlace Cu-S1, no que ocorre unha transferencia de carga do Spπ ao Cudx2-y2.[13]
Na forma reducida da plastocianina, a His-87 está protonada cunha pKa de 4,4. A protonación evita que actúe como un ligando e a xeometría do sitio do cobre faise trigonal planar.
Almacenamento e transferencia de ferro[editar | editar a fonte]
O ferro é almacenado como ferro(III) na ferritina. A natureza exacta do sitio de unión non se determinou aínda. O ferro parece estar presente como un produto de hidrólise, como FeO(OH) e é transportado pola transferrina cuxo sitio de unión consiste en dúas tirosinas, un ácido aspártico e unha histidina.[14]
O corpo humano non ten ningún mecanismo de excreción de ferro, e isto pode orixinar problemas de sobrecarga de ferro en pacientes tratados con transfusións de sangue, como, por exemplo, os pacientes de β-talasemia.
Ceruloplasmina[editar | editar a fonte]
A ceruloplasmina é a principal proteína portadora de cobre do sangue. Mostra actividade oxidase, o cal está asociado coa posible oxidación do Fe2+ (ión ferroso) en Fe3+ (ión férrico), polo tanto, axuda no seu transporte no plasma, en asociación coa transferrina, a cal só pode transportar ferro en estado férrico.
Metaloencimas[editar | editar a fonte]
Os metaloencimas teñen unha característica en común: o ión metálico únese á proteína cun sitio de coordinación lábil. Como ocorre con todos os encimas, a forma do sitio activo é crucial; o metal encóntrase normalmente nun peto da molécula, a cuxa forma se adapta o substrato. Os ións metálicos catalizan reaccións que son difíciles de conseguir en química orgánica.
Anhidrase carbónica[editar | editar a fonte]

- CO2 + H2O ←→ H2CO3
Esta reacción é moi lenta en ausencia dun catalizador, mais é rápida en presenza do ión hidróxido
- CO2 + OH- ←→ HCO3-
Unha reacción semellante a esta é case instantánea coa anhidrase carbónica. A estrutura do sitio activo coñécese ben; componse dun ión cinc coordinado por tres átomos de nitróxeno do imidazol de tres unidades de histidina. O cuarto sitio de coordinación está ocupado por unha molécula de auga. Esta coordinación de ións cinc é aproximadamente tetraédrica, a carga positiva dos ións cinc polariza a molécula de auga coordinada e prodúcese un ataque nucleofílico pola porción hidróxido cargado negativamente sobre o dióxido de carbono. O ciclo catalítico produce ións de bicarbonato e de hidróxeno, xa que o equilibrio favorece a disociación do ácido carbónico a valores de pH fisiolóxico.[15]
- H2CO3 ←→ HCO3- + H+
Encimas dependentes da vitamina B12[editar | editar a fonte]
A vitamina B12 cataliza a transferencia de metilo (-CH3) entre dous grupos de moléculas, o que implica a rotura de enlaces C-C, un proceso que é enerxeticamente custoso en reaccións orgánicas. Os ións de metal diminúen a enerxía de activación para o proceso de transición por medio da formación dun enlace transitorio Co-CH3.[16] A estrutura deste coencima determinouna Dorothy Hodgkin, polo cal recibiu o premio Nobel.[17] Consta dun ión cobalto (II) coordinado por catro átomos de nitróxeno dun anel de corrina e un quinto átomo de nitróxeno do grupo imidazol. No estado de repouso hai un enlace σ Co-C co carbono 5 ' da adenosina.[18] Este é un composto organometálico que se encontra na natureza, o que explica a súa función na transmetilación, como a levada a cabo pola metionina sintase.
Nitroxenase[editar | editar a fonte]
O encima bacteriano nitroxenase é un dos poucos encimas que poden catalizar o proceso de fixación do nitróxeno atmosférico. Posúe un átomo de molibdeno no sitio activo e grupos de ferro-xofre que participan no transporte dos electróns que cómpren para reducir o nitróxeno. A reacción pode escribirse así:
A estrutura exacta do sitio activo foi difícil de determinar. Parece conter un centro de MoFe7S8 que pode unirse á molécula de dinitróxeno e, probablemente, permitir que comece o proceso de redución.[19] Os electróns son transportados polo centro asociado "P", que contén dous centros cúbicos Fe4S4 unidos por pontes de xofre.[20]
Superóxido dismutase[editar | editar a fonte]

O ión superóxido, O2- xérase nos sistemas biolóxicos por redución do oxíxeno molecular. Ten un electrón desapareado, polo que se comporta como un radical libre e é un poderoso axente oxidante. Estas propiedades fan que o ión superóxido sexa moi tóxico e o utilicen os fagocitos para mataren microorganismos invasores. En caso contrario, o superóxido debe ser destruído antes de que cause danos non desexados ás células. O encima superóxido dismutase realiza esta función de maneira moi eficiente.[21]
O estado de oxidación dos átomos de oxíxeno é ½. En solucións a pH neutro, o ión superóxido dismuta a oxíxeno molecular e peróxido de hidróxeno:
- 2 O2− + 2 H+ → O2 + H2O2
As superóxido dismutases, abreviadas como SOD, aumentan a taxa de reacción ata case o límite de difusión.[22] A chave para explicar a acción destes encimas é o seu ión metálico con estados de oxidación variables, que pode actuar como axente oxidante ou como redutor.
- Oxidación: M(n+1)+ + O2− → Mn+ + O2
- Redución: Mn+ + O2− + 2H+ → M(n+1)+ + H2O2.
En humanos o metal activo é cobre, en forma de Cu2+ ou de Cu+, coordinado tetraedricamente por residuos de histidina. Este encima ten tamén ións cinc. Outras isoencimas poden conter ferro, manganeso ou níquel. A Ni-SOD é especialmente interesante, xa que presenta níquel(III), o que é un estado de oxidación infrecuente para dito elemento. A xeometría do sitio activo de Ni cíclase desde o Ni(II) cadrado plano, con tiolato (Cys2 e Cys6) e nitróxeno (His1 e Cys2), a un Ni(III) cadrado piramidal cunha cadea lateral His1 axial como ligando.[23]
Proteínas que conteñen clorofila[editar | editar a fonte]
A clorofila desempeña un papel crucial na fotosíntese. Contén un ión magnesio encerrado nun anel de clorina. Porén, o ión magnesio non está directamente implicado na función fotosintética e poden substituírse por outro ión divalente con só unha lixeira perda de actividade. Polo contrario, o fotón é absorbido polo anel de clorina, que ten unha estrutura electrónica adaptada para esta finalidade.
Inicialmente, a absorción dun fotón provoca que un electrón sexa excitado a un estado singulete da banda Q. O estado excitado sométese a un cruzamento intersistema dun estado singulete a un estado triplete no que hai dous electróns con spin paralelo. Esta especie é un radical libre, polo cal é moi reactivo e permite que un electrón sexa transferido a aceptores adxacentes á clorofila no cloroplasto. Neste proceso a clorofila oxídase. Logo, no ciclo fotosintético volve a reducirse aceptando un electrón, e o produto final da oxidación é oxíxeno molecular, cuxos átomos proveñen de moléculas de auga.
Metaloproteínas de transdución de sinais[editar | editar a fonte]
Calmodulina[editar | editar a fonte]
A calmodulina é un exemplo de proteína de transdución de sinais. Trátase dunha pequena proteína que contén catro motivos man EF, cada un dos cales pode unirse a un ión de Ca2+.
Nun bucle de man EF os ións de calcio están coordinados nunha configuración pentagonal bipiramidal. Na unión participan seis residuos de ácido glutámico e ácido aspártico situados nas posicións 1, 3, 5, 7, e 9 da cadea do polipéptido. Na posición 12 hai un ligando de glutamato ou aspartato, que se comporta como un ligando bidentado, proporcionando dous átomos de oxíxeno. O noveno residuo no bucle debe ser necesariamente unha glicina debido a esixencias conformacionais da cadea polipeptídica. A esfera de coordinación do calcio contén só átomos de oxíxeno do carboxilato e ningún átomo de nitróxeno.
A proteína ten dous dominios aproximadamente simétricos, separados por unha rexión "bisagra" flexible. A unión de calcio provoca un cambio conformacional na proteína. A calmodulina participa nos sistemas de sinalización intracelular ao actuar como un segundo mensaxeiro difusible do estímulo inicial.[24][25]
Factores de transcrición[editar | editar a fonte]

Moitos factores de transcrición conteñen unha estrutura coñecida como dedo de zinc, que se trata dun módulo estrutural onde unha rexión da proteína se prega en torno a un ión cinc. O cinc non toma contacto co ADN ao que se unen estas proteínas, senón que o cofactor é esencial para a estabilidade da cadea da proteína pregada moi axustadamente.[26] Nestas proteínas o ión cinc xeralmente está coordinado por pares de cadeas laterais de cisteína e histidina.
Outros metaloencimas[editar | editar a fonte]
| Ión | Exemplos de encimas que conteñen este ión |
|---|---|
| Magnesio | Glicosa 6-fosfatase Hexoquinase ADN polimerase |
| Vanadio | Vanabina |
| Manganeso | Arxinase |
| Ferro | Catalase Hidroxenase IRE-BP Aconitase |
| Níquel[27] | Urease Hidroxenase |
| Cobre | Citocromo oxidase Plastocianina Lacase |
| Cinc | Alcohol deshidroxenase Carboxipeptidase Aminopeptidase |
| Molibdeno | Nitrato redutase |
| Selenio | Glutatión peroxidase |
| Varios | Metalotioneína Fosfatase |
Notas[editar | editar a fonte]
- ↑ Shriver, D.F.; Atkins, P.W. (1999). "Chapter 19, Bioinorganic chemistry". Inorganic chemistry (3rd. ed.). Oxford University Press. ISBN 9780716734383.
- ↑ Waldron KJ, Robinson NJ (2009). "How do bacterial cells ensure that metalloproteins get the correct metal?". Nat. Rev. Microbiol. 7 (1): 25–35. PMID 19079350. doi:10.1038/nrmicro2057.
- ↑ "Bio-inorganic chemistry" Thomson A.J.; Gray H.B. Current Opinion in Chemical Biology, 1998, Volume 2, pp. 155-158. doi 10.1016/S1367-5931(98)80056-2 [1]
- ↑ Messerschmidt, A. ; Huber, R.;Wieghardt,K.;Poulos, T. (2001). Handbook of Metalloproteins. Wiley. ISBN 0-471-62743-7.
- ↑ Stenkamp, R.E. (1994). "Dioxygen and hemerythrin". Chem. Rev. 94: 715–726. doi:10.1021/cr00027a008.
- ↑ Wirstam M., Lippard, S.J., Friesner R.A. (2003). "Reversioble Dioxygen Binding to Hemerythrin". J. Am. Chem. Soc. 125: 3980–3987. doi:10.1021/ja017692r.
- ↑ K. D. Karlin, R. W. Cruse, Y. Gultneh, A. Farooq, J. C. Hayes and J. Zubieta (1987). "Dioxygen-copper reactivity. Reversible binding of O2 and CO to a phenoxo-bridged dicopper(I) complex". J. Am. Chem. Soc. 109 (9): 2668–2679. doi:10.1021/ja00243a019.
- ↑ N. Kitajima, K. Fujisawa, C. Fujimoto, Y. Morooka, S. Hashimoto, T. Kitagawa, K. Toriumi, K. Tatsumi and A. Nakamura (1992). "A new model for dioxygen binding in hemocyanin. Synthesis, characterization, and molecular structure of the μ-η2:η2 peroxo dinuclear copper(II) complexes, [Cu(HB(3,5-R2pz)3)]2(O2) (R = isopropyl and Ph)". J. Am. Chem. Soc. 114 (4): 1277–1291. doi:10.1021/ja00030a025.
- ↑ Moore, G.R.; Pettigrew, G.W. (1990). Cytochrome c:structural and physicochemical aspects. Springer - Berlin.
- ↑ Astrid Sigel, Helmut Sigel and Roland K.O. Sigel, ed. (2007). The Ubiquitous Roles of Cytochrome450 Proteins. Metal Ions in Life Sciences 3. Wiley. ISBN 978-0-470-01672-5.
- ↑ Ortiz de Montellano, P.R. (2005). Cytochrome P450 Structure, Mechanism, and Biochemistry (3rd. ed.). Springer. ISBN 978-0-306-48324-0.
- ↑ Colman, P. M.; Freeman, H. C.; Guss, J. M.; Murata, M.; Norris, V. A.; Ramshaw, J. A. M.; Venkatappa, M. P. (1978). "X-Ray Crystal-Structure Analysis of Plastocyanin at 2.7 A Resolution". Nature 272 (5651): 319–324. doi:10.1038/272319a0.
- ↑ Solomon, E.I.; Gewirth, A.A.; Cohen,S.L. (1986). "Spectroscopic Studies of Active Sites. Blue Copper and Electronic Structural Analogs". ACS Symposium Series 307: 236–266. doi:10.1021/bk-1986-0307.ch016.
- ↑ Anderson BF, Baker HM, Dodson EJ; et al. (1987). "Structure of human lactoferrin at 3.2-A resolution". Proc. Natl. Acad. Sci. U.S.A. 84 (7): 1769–73. PMC 304522. PMID 3470756.
- ↑ Lindskog S (1997). "Structure and mechanism of carbonic anhydrase". Pharmacol. Ther. 74 (1): 1–20. PMID 9336012. doi:10.1016/S0163-7258(96)00198-2.
- ↑ Astrid Sigel, Helmut Sigel and Roland K.O. Sigel, ed. (2008). Metal Ions in Life Sciences - Metal-carbon bonds in enzymes and cofactors 6. Wiley. ISBN 978-1-84755-915-9.
- ↑ "The Nobel Prize in Chemistry 1964". Nobelprize.org.
- ↑ Hodgkin, D.C. (1965). "The Structure of the Corrin Nucleus from X-ray Analysis". Proc. Roy. Soc. A 288: 294–305. doi:10.1098/rspa.1965.0219.
- ↑ Orme-Johnson, W.H. (1993). Steifel, E.I; Coucouvannis, D.; Newton, D.C., ed. Advances in chemystry, Symposium series no. 535 - Molybdenum enzymes, cofactors and model systems. Washington, DC: American Chemical Society. p. 257.
- ↑ Chan, M.K.; Kim, J.; Rees, D.C. (1993). "The nitrogenase FeMo-cofactor and P-cluster pair: 2.2 A resolution structures". Science 260: 792. PMID 8484118. doi:10.1126/science.8484118.
- ↑ Packer, L. (editor) (2002). Superoxide Dismutase: 349 (Methods in Enzymology). Academic Press. ISBN 0121822524.
- ↑ Heinrich, Peter; Georg Löffler; Petro E. Petrides (2006). Biochemie und Pathobiochemie (Springer-Lehrbuch) (German Edition). Berlin: Springer. pp. 123. ISBN 3-540-32680-4.
- ↑ Barondeau, D.P.; Kassmann C.J.; Bruns C.K.; Tainer J.A.; Getzoff E.D. (2004). "Nickel superoxide dismutase structure and mechanism". Biochemistry 43 (25): 8038–8047. PMID 15209499.
- ↑ Stevens FC (1983). "Calmodulin: an introduction". Can. J. Biochem. Cell Biol. 61 (8): 906–10. PMID 6313166.
- ↑ Chin D, Means AR (2000). "Calmodulin: a prototypical calcium sensor". Trends Cell Biol. 10 (8): 322–8. doi:10.1016/S0962-8924(00)01800-6.
- ↑ Berg JM (1990). "Zinc finger domains: hypotheses and current knowledge". Annu Rev Biophys Biophys Chem 19: 405–21. PMID 2114117. doi:10.1146/annurev.bb.19.060190.002201.
- ↑ Astrid Sigel, Helmut Sigel y Roland K.O. Sigel (2008). Metal Ions in Life Sciences - Nickel and Its Surprising Impact in Nature 2. Wiley. ISBN 978-0-470-01671-8.
Véxase tamén[editar | editar a fonte]
| Wikimedia Commons ten máis contidos multimedia na categoría: Metaloproteína |
