Transferrina
| Transferrina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Identificadores | |||||||||
| Símbolo | Transferrina | ||||||||
| Pfam | PF00405 | ||||||||
| InterPro | IPR001156 | ||||||||
| PROSITE | PDOC00182 | ||||||||
| SCOPe | 1lcf / SUPFAM | ||||||||
| OPM superfamily | 161 | ||||||||
| OPM protein | 1lfc | ||||||||
| |||||||||
As transferrinas son glicoproteínas do plasma sanguíneo que se unen ao ferro e controlan o nivel de ferro libre nos fluídos biolóxicos.[1]
As transferrinas únense moi fortemente ao ferro, pero de forma reversible. Aínda que o ferro unido á transferrina é menos do 0,1% (4 mg) do total de ferro corporal, é a fonte máis importante de ferro, cunha alta taxa de recambio (25 mg/24 h). A transferrina ten un peso molecular de arredor de 80 KDa e contén dous sitios de unión para o Fe(III) de alta afinidade. A afinidade da transferrina polo Fe(III) é extremadamente alta (1023 M−1 a pH 7,4)[2] pero decrece progresivamente ao diminuír o pH por debaixo da neutralidade. Na superficie das células existen receptores da transferrina.
A ferritina pode estar unida a un ión férrico, a dous ou a ningún. Cando non está unida ao ferro, coñécese como apotransferrina.
O xene que codifica a transferrina nos humanos é o TF,[3] que está localizado no cromosoma 3 banda 3q21.[3]
Mecanismo de transporte[editar | editar a fonte]
Cando a proteína transferrina cargada con ferro encontra un receptor de transferrina na superficie dunha célula (por exemplo, en precursores dos eritrocitos da medula ósea), únese a el e, como consecuencia, é transportada á célula nunha vesícula por endocitose mediada por receptor. O pH da vesícula redúcese pola acción de bombas de hidróxeno (H+ ATPases) ata aproximadamente 5,5, causando que a transferrina libere os seus ións férricos. O receptor (co seu ligando a transferrina unida) é despois transportado a través do ciclo endocítico de novo á superficie celular, e queda listo para outra rolda de captación de ferro. Cada molécula de transferrina ten a capacidade de transportar dous ións de ferro en forma férrica (Fe3+).
O ferro que se absorbe nos alimentos, é transportado polo sangue pola transferrina e almacenado na proteína celular ferritina, para ser utilizado na síntese de citocromos, de encimas e outras proteínas que conteñen ferro como a mioglobina e a hemoglobina e utilizado pola medula ósea para a eritropoese (formación de glóbulos vermellos).
Os profesionais da medicina poden comprobar o nivel de transferrina sérica en casos de deficiencias de ferro, hemocromatosee, e outros trastornos de sobrecarga de ferro.
Estrutura[editar | editar a fonte]
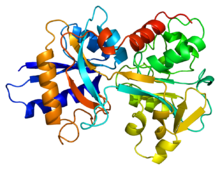
Nos humanos, a transferrina consiste nunha cadea polipeptídica de 679 aminoácidos. A proteína está composta por hélices alfa e láminas beta que forman dous dominios proteicos.[4] As secuencias dos extremos N-terminal e C-terminal están representadas por lóbulos globulares e entre estes dous lóbulos está o sitio de unión ao ferro.
Os aminoácidos da transferrina que se unen ao ión ferro son idénticos en ambos os lóbulos: dúas tirosinas, unha histidina, e un ácido aspártico. As tres cargas negativas que se encontran nos hidroxilos de dous residuos de tirosina e no carboxilo do ácido aspártico compénsanse coas 3 cargas positivas do ión férrico, que tamén se une ao N da histidina[5]. Para que se una o ión férrico cómpre ademais un anión, preferiblemente carbonato (CO32−), que se une tamén ao ferro polos seus dous osíxenos, e que é colocado no seu sitio por residuos de arxinina e treonina da proteína.[4] En total o ión férrico está ligado por seis enlaces (4 dos aminoácidos e dous do carbonato).[6]
A transferrina tamén ten un receptor, que é un homodímero unido por ponte disulfuro.[7] Nos humanos cada monómero consta de 760 aminoácidos. Permite a unión de dúas moléculas de transferrina. Cada monómero consta de tres dominios: o dominio protease, o helicoidal, e o apical. A forma do receptor da transferrina lembra á dun complexo con forma de bolboreta, debido aos tres dominios de forma claramente definida.[4]
Distribución nos tecidos[editar | editar a fonte]
O fígado é o principal sitio de síntese de transferrina, pero outros tecidos e órganos, como o cerebro, tamén a producen. O principal papel da transferrina é entregar a todos os tecidos o ferro tomado nos centros de absorción no duodeno e nos macrófagos (que destrúen eritrocitos vellos e os seus grupos hemo). A transferrina xoga un papel chave nos lugares onde teñen lugar a hematopoese ou unha activa división celular.[7] O receptor axuda a manter a homeostase do ferro nas células ao controlar as concentracións de ferro.[7]
Sistema inmunitario[editar | editar a fonte]
A transferrina está tamén asociada co sistema inmunitario innato. Encóntrase nas mucosas e capta ferro, creando así un ambiente baixo en ferro que impide a supervivencia bacteriana nun proceso chamado retención do ferro. O nivel de transferrina diminúe nas inflamacións.[10]
Papel en enfermidades[editar | editar a fonte]
- Véxase tamén: Metabolismo do ferro humano.
O desequilibrio da transferrina pode ter graves efectos sobre a saúde tanto nas persoas que teñen niveis baixos coma altos no seu soro sanguíneo. Un paciente cun nivel de transferrina elevado no soro xeralmente sofre de anemia por deficiencia de ferro.[7] Os pacientes con niveis baixos de transferrina poden sufrir de enfermidades por sobrecarga de ferro e malnutrición proteica. A ausencia de transferrina dáse nun raro trastorno xenético coñecido como atransferrinemia; unha condición caracterizada por anemia e hemosiderose no corazón e fígado que orixina moitas complicacións, incluíndo a insuficiencia cardíaca. Máis recentemente, viuse que a transferrina e o seu receptor diminúen as células tumorais usando o receptor para atraer anticorpos.[7]
Outros efectos[editar | editar a fonte]
As propiedades de unión a metais da transferrina teñen unha grande influencia na bioquímica do plutonio en humanos (contaminación radioactiva).
A proba de laboratorio chamada transferrina deficiente en carbohidratos (CDT) úsase para detectar os consumos elevados de alcohol. Os valores desta proba increméntanse con consumos elevados de etanol.[11]
Patoloxía[editar | editar a fonte]
A deficiencia de transferrina está asociada coa atransferrinemia.
Rangos de referencia[editar | editar a fonte]
Os rangos de referencia normais para a transferrina son 204–360 mg/dL.[12]

Un alto nivel de transferrina pode indicar unha anemia por deficiencia de ferro. Os niveis de ferro sérico e a capacidade de unión ao ferro total (TIBC) utilízanse xunto coa transferrina para especificar calquera anormalidade.
Interaccións[editar | editar a fonte]
A transferrina interacciona co IGF-2[13] e o IGFBP3.[14] A regulación transcricional da trasnferrina é regulada á alza polo ácido retinoico.[15]
Proteínas relacionadas[editar | editar a fonte]
As proteínas membros da familia proteica da transferrina son, ademais da propia transferrina (tamén chamada siderofilina[16] ou, máis raramente, serotransferrina sanguínea); a lactotransferrina (lactoferrina) ou transferrina do leite; a ovotransferrina da clara de ovo (conalbumina); e a melanotransferrina asociada a membranas.[17]
Notas[editar | editar a fonte]
- ↑ Crichton RR, Charloteaux-Wauters M (1987). "Iron transport and storage". Eur. J. Biochem. 164 (3): 485–506. PMID 3032619. doi:10.1111/j.1432-1033.1987.tb11155.x.
- ↑ Aisen P, Leibman A, Zweier J (1978). "Stoichiometric and site characteristics of the binding of iron to human transferrin" (PDF). J. Biol. Chem. 253 (6): 1930–7. PMID 204636.
- ↑ 3,0 3,1 Yang F, Lum JB, McGill JR, Moore CM, Naylor SL, van Bragt PH, Baldwin WD, Bowman BH (1984). "Human transferrin: cDNA characterization and chromosomal localization". Proceedings of the National Academy of Sciences of the United States of America 81 (9): 2752–6. PMC 345148. PMID 6585826. doi:10.1073/pnas.81.9.2752.
- ↑ 4,0 4,1 4,2 "Transferrin Structure". St. Edward's University. 2005-07-18. Arquivado dende o orixinal o 11 de decembro de 2012. Consultado o 2009-04-24.
- ↑ "John Tweedie. transferrin structure". Arquivado dende o orixinal o 01 de xuño de 2011. Consultado o 07 de xullo de 2013.
- ↑ "A tour or transferrin. University of Toronto". Arquivado dende o orixinal o 20 de maio de 2015. Consultado o 07 de xullo de 2013.
- ↑ 7,0 7,1 7,2 7,3 7,4 Macedo MF, de Sousa M (2008). "Transferrin and the transferrin receptor: of magic bullets and other concerns". Inflammation & Allergy Drug Targets 7 (1): 41–52. PMID 18473900. doi:10.2174/187152808784165162. Arquivado dende o orixinal o 18 de xaneiro de 2017. Consultado o 15 de setembro de 2018.
- ↑ PDB 1suv; Cheng Y, Zak O, Aisen P, Harrison SC, Walz T (2004). "Structure of the human transferrin receptor-transferrin complex". Cell 116 (4): 565–76. PMID 14980223. doi:10.1016/S0092-8674(04)00130-8.
- ↑ PDB 2nsu; Hafenstein S, Palermo LM, Kostyuchenko VA, Xiao C, Morais MC, Nelson CD, Bowman VD, Battisti AJ, Chipman PR, Parrish CR, Rossmann MG (2007). "Asymmetric binding of transferrin receptor to parvovirus capsids". Proceedings of the National Academy of Sciences of the United States of America 104 (16): 6585–9. PMC 1871829. PMID 17420467. doi:10.1073/pnas.0701574104.
- ↑ Ritchie RF, Palomaki GE, Neveux LM, Navolotskaia O, Ledue TB, Craig WY (1999). "Reference distributions for the negative acute-phase serum proteins, albumin, transferrin and transthyretin: a practical, simple and clinically relevant approach in a large cohort". J. Clin. Lab. Anal. 13 (6): 273–9. PMID 10633294. doi:10.1002/(SICI)1098-2825(1999)13:6<273::AID-JCLA4>3.0.CO;2-X.
- ↑ Sharpe PC (2001). "Biochemical detection and monitoring of alcohol abuse and abstinence". Ann. Clin. Biochem. 38 (Pt 6): 652–64. PMID 11732647. doi:10.1258/0004563011901064.
- ↑ "Normal Reference Range Table". Interactive Case Study Companion to Pathlogical Basis of Disease. The University of Texas Southwestern Medical Center at Dallas. Arquivado dende o orixinal o 25 de decembro de 2011. Consultado o 2008-10-25.
Kumar V, Hagler HK (1999). Interactive Case Study Companion to Robbins Pathologic Basis of Disease (6th Edition (CD-ROM for Windows & Macintosh, Individual) ed.). W B Saunders Co. ISBN 0-7216-8462-9. - ↑ Storch S, Kübler B, Höning S, Ackmann M, Zapf J, Blum W, Braulke T (2001). "Transferrin binds insulin-like growth factors and affects binding properties of insulin-like growth factor binding protein-3". FEBS Lett. 509 (3): 395–8. PMID 11749962. doi:10.1016/S0014-5793(01)03204-5.
- ↑ Weinzimer SA, Gibson TB, Collett-Solberg PF, Khare A, Liu B, Cohen P (2001). "Transferrin is an insulin-like growth factor-binding protein-3 binding protein". J. Clin. Endocrinol. Metab. 86 (4): 1806–13. PMID 11297622. doi:10.1210/jc.86.4.1806.
- ↑ Hsu SL, Lin YF, Chou CK (1992). "Transcriptional regulation of transferrin and albumin genes by retinoic acid in human hepatoma cell line Hep3B". Biochem. J. 283 (2): 611–5. PMC 1131079. PMID 1315521.
- ↑ The Free Dictionary
- ↑ M Ching-Ming Chung (1984). "Structure and function of transferrin". Biochemical Education 12 (4): 146–154. doi:10.1016/0307-4412(84)90118-3.
Véxase tamén[editar | editar a fonte]
Bibliografía[editar | editar a fonte]
- Hershberger CL, Larson JL, Arnold B; et al. (1992). "A cloned gene for human transferrin". Ann. N. Y. Acad. Sci. 646: 140–54. PMID 1809186. doi:10.1111/j.1749-6632.1991.tb18573.x.
- Bowman BH, Yang FM, Adrian GS (1989). "Transferrin: evolution and genetic regulation of expression". Adv. Genet. Advances in Genetics 25: 1–38. ISBN 9780120176250. PMID 3057819. doi:10.1016/S0065-2660(08)60457-5.
- Parkkinen J, von Bonsdorff L, Ebeling F, Sahlstedt L (2003). "Function and therapeutic development of apotransferrin". Vox Sang. 83 (Suppl 1): 321–6. PMID 12617162. doi:10.1111/j.1423-0410.2002.tb05327.x.
Outros artigos[editar | editar a fonte]
- Beta-2 transferrina
- Receptor da transferrina
- Ferritina
- Endosoma
- Sistema endomembranoso
- Elemento de resposta ao ferro (IRE)
- Ferroportina
Ligazóns externas[editar | editar a fonte]
- MeshName - Transferrin [1]

![Transferrina unida ao seu receptor.[8]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/b2/PDB_1suv_EBI.jpg/120px-PDB_1suv_EBI.jpg)
![Complexo receptor de transferrina.[9]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/b1/PDB_2nsu_EBI.jpg/120px-PDB_2nsu_EBI.jpg)