MicroARN

O microARN ou miARN[1] (en inglés miRNA) é un ARN monocatenario, dunha lonxitude de entre 21 e 25 nucleótidos, que ten a capacidade de regular a expresión de xenes por medio de diversos procesos, utilizando a ruta da interferencia de ARN (RNAi).[2]
Foron descritos inicialmente en 1993 por Lee e colaboradores no laboratorio de Victor Ambros,[3] pero o termo "microRNA" (sic) non se acuñou ata 2001, ano en que apareceu nun conxunto de tres artigos publicados en Science (26 de outubro de 2001).[4] A principios de 2008, certas análises computacionais realizadas por IBM suxerían a presenza de arredor de 50.000 miARN diferentes no xenoma humano, cada un talvez con miles de dianas de ARNm potenciais (despois non se atoparon tantos).[5]
Definición[editar | editar a fonte]
Unha vez descubertos os ARN interferentes pequenos (siRNA) e a existencia nas células de proteínas que catalizan a degradación do ARNm, os investigadores preguntáronse se os siRNA tamén estaban codificados no xenoma, e empezaron a purificar pequenos ARN (de 19-25 nucleótidos) en diferentes especies animais. Porén, non encontraron siRNA, senón os denominados microARN, que se identificaran anteriormente de forma independente.[3]

Os miARN son moléculas de ARN transcritas a partir de xenes de ADN, pero non son traducidas a proteínas. Exprésanse nunha ampla variedade de organismos, desde plantas ata vermes e humanos. As secuencias de moitos miARN están ben conservadas entre especies,[7] e moitos compoñentes da maquinaria dos miARN se encontraron mesmo nas Archaea e eubacterias, o que revela que a súa orixe é moi antiga. Algúns recontos de miARN en humanos identificaban ata 800, o que implicaría que os miARN poderían representar como mínimo o 3% de todos os xenes humanos.[8]
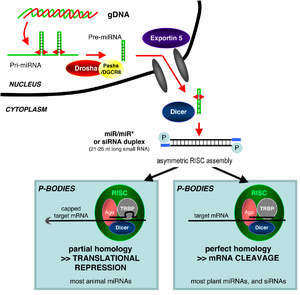
A secuencia de ADN que codifica un xene de miARN ten unha lonxitude que supera o tamaño final do propio miARN e inclúe a rexión miARN e unha rexión que é complementaria á anterior, o que permite o seu emparellamento por pontes de hidróxeno. Isto comporta que, durante a transcrición desta secuencia de ADN, se forman rexións que teñen a capacidade de formar unha forquita e xerar un ARN bicatenario primario longo coñecido como pri-miARN. Posteriormente, un encima nuclear chamado drosha corta as bases da forquita, formando o que se denomina pre-miARN. Este pre-miARN é transportado desde o núcleo ao citoplasma pola proteína exportina 5. Unha vez que o pre-miRNA está no citoplasma é fragmentado polo encima Dicer, que o corta ata a lonxitude final de 20-25 nucleótidos.[6]
Funcións[editar | editar a fonte]
A función dos miARN está relacionada coa regulación da expresión xénica. Un miARN é complementario dunha parte dun ou máis ARN mensaxeiros (ARNm). Os miARN de animais adoitan mostrar complementariedade imperfecta coa rexión 3' UTR, e xeralmente inhiben a tradución do ARNm, entanto que os das plantas adoitan mostrar complementariedade perfecta con rexións codificantes e inducen o corte e a posterior degradación do ARNm diana (como acontece cos siRNA en animais).[6]
Antes de clasificalos como parte da vía da RNAi, os miARN foron identificados inicialmente en vermes, nos que regulan as fases do desenvolvemento,[9] pero actualmente sabemos que están implicados nunha ampla variedade de procesos do desenvolvemento e poderían ter unha función no establecemento de redes e no axuste fino da expresión xénica na célula.[7][10] Dado que o número de dianas potenciais dos miARN é de miles (arredor do 30% dos xenes humanos), os miARN poderían constituír outro nivel máis do circuíto regulatorio que existe nas células.[11] Isto implica que calquera desregulación dos miARN podería supoñer grandes problemas regulatorios na célula, inducindo quizais fenotipos cancerosos. De feito, demostrouse que os perfís de expresión dos miARN están modificados nun gran número de tipos de cáncer[12] e que a sobreexpresión forzada dos miARN podería conducir ao desenvolvemento de tumores.[13]
Características dos miARN[editar | editar a fonte]
Os miRNA transcríbense en diferentes localizacións do xenoma como longos transcritos primarios (pri-miRNA) pola ARN polimerase II.[14]
Os miARN poden atoparse en moitos tipos de loci no xenoma:[15]
- A transcrición dos miARN pode estar regulada independentemente por promotores específicos, como ocorre con miR-1–1 e miR-133a-2, que están regulados polos factores de transcrición SRF (Serum Response Factor) e MyoD[16] (ver o apartado "Funcións durante o desenvolvemento"). Tales miARN poden de todas as maneiras estar localizados en intróns pero a miúdo cunha orientación antisentido.
- A maioría dos precursores de miARN presentes en intróns teñen a mesma orientación ca o xene no que se sitúan e son inicialmente transcritos como parte do seu ARN precursor.[7] Por exemplo, miR-208, que se expresa especificamente no corazón humano e de rato, reside no intrón 28 da cadea pesada da α-miosina cardíaca. Os pri-miARN intrónicos poden producirse por corte do intrón pola endonuclease Drosha, despois de que se producise o proceso de splicing.
- Con poucas excepcións, os miARN que están integrados ou se superpoñen con exóns de transcritos coñecidos, teñen sempre a mesma orientación, e a maioría encóntranse nas rexións non codificantes UTR 5′ ou 3′ (por exemplo, miR-198 en follistatin-like 1).
Aproximadamente o 50% dos miARN están en clusters de miARN que están inicialmente codificados como un transcrito policistrónico (que inclúe varios xenes),[17] que posteriormente se fragmenta en múltiples miARN. Na maioría dos casos, os miARN policistrónicos comparten o mesmo patrón de expresión. Porén, os niveis relativos dos miRNA dentro do clúster parecen estar regulados dunha maneira dependiente do desenvolvemento e a homeostase, o que suxire unha complexidade aínda non definida na regulación da expresión xénica.
Bioxénese e procesamento[editar | editar a fonte]

Os xenes que codifican miARN son moito máis longos cós miARN procesados maduros; os miARN transcríbense inicialmente como transcritos primarios ou pri-miARN cunha gorra ou carapucha no extremo 5' e unha cola de poli-adeninas (poli-A) no 3' e procésanse no núcleo celular en estruturas curtas de 70 nucleótidos en forma de talo-lazo (stem-loop) coñecidas como pre-miARN. En animais este procesamento realízase por un complexo proteico chamado Microprocesador, que consta da nuclease Drosha[18] e a proteína de unión a ARN de dobre hélice Pasha.[19][20] Estes pre-miARN son logo procesados a miARN maduros no citoplasma por medio da interacción coa endonuclease Dicer, que tamén inicia a formación do complexo RISC (RNA-induced silencing complex, complexo silenciador inducido por ARN).[21] Este complexo é o responsable do silenciamento de xenes que se observa debido á expresión dos miARN e á interferencia de ARN mediada por siRNAs. A vía varía lixeiramente en plantas, debido a que carecen de homólogos de Drosha; no seu lugar son só homólogos de Dicer os que realizan algúns dos pasos do procesamento.[22] A vía tamén é diferente para os miARN derivados de talos-lazos (stem-loops) procedentes de secuencias intrónicas; neste caso procésanse por Dicer pero non por Drosha.[23] Tanto a fibra con sentido coma a antisentido do ADN poden funcionar como molde para producir miARN.[24]
Drosha[25] (RNASEN en humanos)[26] é unha proteína nuclear dun tamaño entre 130 e 160 kDa (quiloDalton). Contén os dominios seguintes:
- Dous dominios ARNase III (os dominios catalíticos).
- Un dominio dsRBD (double-strand RNA-binding domain, dominio de unión ao ARN de dobre cadea).
- Dominios conservados (na parte N-terminal), dos que non se coñece a función.
Drosha funciona nun complexo (o Microprocesador), conxuntamente cunha proteína de unión ao ARN (denominada Pasha en Drosophila ou DGCR8 en mamíferos). DGCR8[27][28] é unha proteína de unión ao ADN que recoñece a zona de unión entre o ARN de dobre cadea e o monocatenario e sitúa a ribonuclease Drosha a unha distancia de 11 nucleótidos (que corresponde a unha volta de hélice) desde a zona de unión. Por tanto, a función de DGCR8 no complexo Microprocesador é análoga ao dominio PAZ de Dicer; DGCR8 proporciona especificidade de substrato e sitúa axeitadamente o centro da ribonuclease Drosha. Porén, no caso de Drosha-DGCR8, o dominio de especificidade está localizado nunha cadea polipeptídica separada dos dominios ARNase III. Propúxose que o dominio WW de unión a prolinas de DGCR8 interacciona co extremo N-terminal de Drosha, rico en prolinas. É posible que Drosha teña outras posibles proteínas asociadas que presenten dominios WW que lle dean especificidades de substrato alternativas e funcións biolóxicas adicionais de Drosha.
O procesamento eficiente dos pre-miARN por Drosha require da presenza de longas colas de ARN de fibra simple tanto no extremo 3' coma no 5' da molécula en forquita.[29] Estes motivos que presenta o ARN de fibra simple poden variar en composición, pero a súa lonxitude é de grande importancia para que o procesamento teña lugar. Unha análise bioinformática de pri-miARN en humanos e moscas identificou rexións estruturais similares, denominadas "segmentos basais" (basal segments), "talos inferiores" (lower stems), "talos superiores" (upper stems) e "lazos terminais" (terminal loops); baseándose nestas estruturas conservadas, determináronse perfís termodinámicos dos pri-miARN.[30] O complexo de Drosha (o Microprocesador) corta a molécula de ARN aproximadamente dúas voltas de hélice a partir do lazo terminal e aproximadamente unha volta de hélice a partir dos segmentos basais. Na maioría das moléculas analizadas esta rexión contén nucleótidos non emparellados con outros e a enerxía libre do dúplex é relativamente alta en comparación coas rexións "talo superior" e "talo inferior". A maior parte dos pre-miARN non presentan unha estrutura de ARN de dobre fibra perfecta cun lazo terminal final. Existen algunhas explicacións posibles para esta selectividade. Unha podería ser que os ARN de dobre fibra que teñen unha lonxitude maior de 21 pares de bases activan a resposta de interferón e a maquinaria antiviral da célula. Outra explicación aceptable podería ser que o perfil termodinámico do pre-miARN determina cal será a fibra incorporada no complexo Dicer. De feito, detectáronse claras similitudes entre pri-miARN codificados tanto en fibras 5' coma 3'.[30]
Unha vez xerado o pre-miARN, Dicer corta o talo-lazo (stem-loop) e fórmanse dúas moléculas complementarias curtas, pero só unha se integra no complexo RISC (a antisentido), como ocorre cos siRNAs. Esta fibra coñécese como a fibra guía, que é seleccionada pola proteína Argonauta, a ARNase cataliticamente activa no complexo RISC, en función da estabilidade do extremo 5'.[31] A outra fibra (a con sentido), coñecida como anti-guía ou fibra pasaxeira, é degradada polo complexo RISC.[32] Despois da súa integración no complexo RISC, agora activado, os miARN emparéllanse de acordo coa súa secuencia de bases coa molécula de ARNm complementaria, e en animais, a diferenza co que pasa cos siRNA, na maioría dos casos inducen a inhibición da tradución de dito ARNm.
Porén, malia que Dicer é un encima fundamental no procesamento dos microARN, identificouse unha vía de bioxénese de miARN independente de Dicer que utiliza a actividade catalítica de corte de Argonauta2 (Ago2). Así, a diferenz doutros miARN, os niveis dalgúns miARN (miR-451-5', miR-2190-5', miR-2190-3', e miR-735-5') non se alteran en mutantes con perda de función de Dicer, pero diminúen en mutantes MZago2 (maternal-zygotic). No caso de miR-451 (un miARN implicado na diferenciación da liña eritroide[33]), o procesamento de pre-miR-451 require a actividade catalítica de Ago2 in vivo. Os mutantes MZago2 mostran un atraso na eritropoese que pode recuperarse utilizando Ago2 de tipo salvaxe ou con dúplex de miR-451, pero non con Ago2 cataliticamente inactiva. Por iso, suxeriuse que Ago2 pode xerar miARN funcionais independentemente de Dicer.[34] Resultados similares observáronse en organismos diferentes.[35]
Como se indica no caso dos siRNA, aínda non está claro como o complexo RISC activado localiza os ARNm complementarios no interior celular. As proteínas Argonauta, os compoñentes catalíticos de RISC, están localizadas en rexións específicas do citoplasma denominadas corpos P (tamén corpos citoplásmicos ou corpos GW, porque conteñen a proteína GW182), os cales son rexións con altas taxas de degradación de ARNm;[36] tamén se detectou actividade miARN nos corpos P.[37] A alteración dos corpos P diminúe a eficiencia do proceso de RNAi (interferencia), o que suxire que os corpos P poderían ser un lugar crítico para o proceso de RNAi.[38] Non obstante, estudos posteriores demostraron que os corpos P non son imprescindibles para o proceso de RNAi, xa que células sen corpos P poden producir silenciamento tanto con siRNA coma con miARN.[39]
Modo de funcionamento[editar | editar a fonte]
Malia o importante progreso realizado na comprensión da bioxénese e a función dos miARN, os mecanismos utilizados polos miARN para regularen a expresión xénica seguen debaténdose intensamente.[40] Existen traballos publicados que indican que os miARN en células animais reprimen a expresión xénica de catro formas diferentes:
- degradación da proteína durante a tradución
- inhibición da elongación da tradución
- terminación prematura da tradución (disgregación dos ribosomas)
- inhibición da iniciación da tradución
Ademais, os miARN en animais poden inducir unha degradación significativa dos ARNm diana (como fan os miARN de plantas), a pesar do emparellamento de bases imperfecto ARNm-miARN. Porén, o mecanismo de degradación adoita ser diferente: os miARN inducen a degradación dos ARNm diana por medio da eliminación da carapucha (no extremo 5') e da cola de poliadeninas (poli-A, no extremo 3').[41] Finalmente, os microARN poderían tamén silenciar os seus ARNm dianas secuestrándoos en puntos citoplásmicos discretos, os cales serían os corpos de procesamento de ARNm ou corpos P, que carecen de maquinaria de tradución. Porén, a pesar das discrepancias existentes entre os diferentes mecanismos propostos, os apoios experimentais para cada mecanismo son variados, e son obxecto actualmente de intensos estudos, para tratar de aclaralas. Suxeriuse que as diferenzas observadas se deben a deficiencias nos experimentos realizados, nalgúns casos orixinadas pola utilización de modelos errados nos estudos de regulación da tradución.[42]
Por último, en estudos recentes detectouse que en determinadas condicións, os miARN poden tamén activar a síntese proteica.[43]
Características xerais do funcionamento dos miARN:[40]
- asócianse á rexión 3’ UTR dos ARNm diana.
- fan falta moitos sitios de unión para activar a resposta dos miARN (a unión dun só non produce efectos significativos).
- un ARNm pode estar regulado por diferentes miARN.
- un único miARN pode controlar a actividade de centos de ARNm diferentes.[44] Os primeiros estudos a grande escala publicados en Nature en 2008, que utilizan unha variante da técnica de espectrometría de masas denominada SILAC (marcado estable con isótopos de aminoácidos en cultivo celular, Stable Isotope Labelling with Amino acids in Cell culture) para detectar as proteínas afectadas ao reducir ou aumentar os niveis dun miARN concreto, mostran que en efecto, un único miARN pode reducir os niveis de centos de proteínas por medio do bloqueo da súa tradución, e non só degradando os seus ARNm.[45][46] O descubrimento máis rechamante destes estudos é que os efectos dos miARN sobre as proteínas son habitualmente bastante modestos, modificando os seus niveis de expresión tan só nun factor 2. Porén, a pesar de que os efectos dos miARN poden ser sutís, tamén poden ser potentes:
- os miARN parecen intervir na regulación da expresión xénica realizando un axuste fino, de forma complexa e interconectada.
- a especificidade e a función dos miARN están determinadas polos nucleótidos 2 a 7 da parte 5' dos miARN maduros (a chamada rexión "semente" do miARN): ditos nucleótidos deben ser obrigatoriamente complementarios ao ARNm diana.[47]
- un miARN pode ser funcional aínda que non fose sintetizado no núcleo: un miARN introducido na célula por transfección pode inhibir eficazmente a síntese de proteínas. Neste caso, como ocorre cos siRNA, o efecto do miARN pódese modular extracelularmente utilizando moléculas químicas pequenas. Nun estudo publicado en agosto de 2008, realizouse un ensaio baseado en células para monitorizar a actividade da vía do RNAi, e os autores detectaron que a molécula enoxacina (Penetrex) mellora a degradación do ARNm mediada por siRNA, e promove a bioxénese dos miARN endóxenos.[48] Este artigo proba que pequenas moléculas químicas poden mellorar a eficacia da vía do RNAi, o que podería ser útil no desenvolvemento de ferramentas para a investigación e terapéuticas.
- o miARN é o responsable da especificiade de substrato (o ARNm diana) do miRNP (complexo micro-ribonucleoproteico, o miARN unido ao complexo RISC).
Funcións biolóxicas[editar | editar a fonte]
Funcións na infección viral e resposta inmunitaria[editar | editar a fonte]
- Función anti-viral: o miARN miR-32 ten como diana unha secuencia presente na UTR do extremo 3’ de todos os ARNm de retrovirus[49]
- Función pro-viral: o miARN miR-122, que se expresa especificamente no fígado, é necesario para que o virus da hepatite C se exprese de maneira eficiente.[50]
- Moitos miARN que están regulados diferencialmente en liñas celulares hematopoéticas teñen funcións importantes na regulación do desenvolvemento e a función das células do sistema inmune, e nas interaccións hóspede-patóxeno.[51]
Funcións no cáncer[editar | editar a fonte]
Os miARN poden funcionar como supresores de tumores ou como oncoxenes; queda por demostrar a súa influencia concreta en cada tipo de cáncer.[52] De feito, un estudo mostrou que preto do 50% dos miARN en humanos están localizados en áreas do xenoma coñecidas como sitios fráxiles,[53] que están asociadas co desenvolvemento de cáncer.
A expresión de certos miARN está correlacionada con varios tipos de cáncer, polo que funcionarían como oncoxenes. Por exemplo, un informe de Sonoki e colaboradores[54] relacionou o xene mir-125b-1 con leucemia, e describiu un paciente con leucemia linfoblástica aguda de precursores de células B que portaba unha inserción do pre-miARN no locus da cadea pesada da inmunoglobulina. Aínda que os investigadores non puideron determinar como se modulaba a expresión de mir-125b-1 nas células tumorais, este estudo apoia o papel deste xene como un oncomir.
A primeira indicación de que os miARN poderían funcionar como supresores de tumores procede dun informe de Calin e colaboradores[55] que mostraba que pacientes diagnosticados cunha forma frecuente de leucemia en adultos (leucemia linfoide crónica das células B ou LLC), presentan a miúdo delecións ou sub-regulación (downregulation) de dous xenes de miARN presentes nun clúster, mir-15a e mir-16-1. Aparecen delecións dentro do locus 13q14 en máis do 65% dos casos de LLC, e en máis do 50% dos linfomas das células do manto, o 16–40% dos mielomas múltiples e o 60% dos cánceres de próstata. Por tanto, propúxose que un xene supresor de tumores debía residir nesta rexión de 30-kb. É interesante notar que mir-15a e mir-16-1 mapean dentro do intrón dun xene de ARN non codificante de proteína, de función descoñecida, denominado LEU2. Por outro lado, alguúns estudos establecen unha conexión entre a redución da expresión de let-7 (que regula a proliferación e diferenciación celular en Caenorhabditis elegans) e o incremento da xénese de tumores e o prognóstico grave dos doentes afectados.[56] Ademais, durante o desenvolvemento normal, LIN28 (un promotor de pluripotencia) pode previr a acumulación de let-7. De acordo con estes resultados, propúxose que let-7 regularía a capacidade pluripotente (stemness) das células, reprimindo a auto-renovación e promovendo a diferenciación, tanto durante o desenvolvemento normal coma no cáncer.
Por outro lado, observouse ademais que os microARN contribúen á progresión maligna do cáncer, especificamente mediando a invasión tumoral e a formación de metástases.[57]
Funcións durante o desenvolvemento[editar | editar a fonte]
Por exemplo, en Caenorhabditis elegans, os miARN permiten un paso rápido a través das diferentes fases do desenvolvemento:[58] os miARN lin-4[59] e let-7[60] controlan o momento no que se define o destino das células neuronais e hipodérmicas durante o desenvolvemento larvario.[61] lin-4, let-7 e outros xenes de miARN están consevados en mamíferos, e a súa función potencial no desenvolvemento embrionario de mamíferos estase a estudar activamente. En C. elegans, os niveis de expresión de LIN-14[62] e LIN-28[63] diminúen debido á expresión do ARN de lin-4 ao final do primeiro estadio larvario, para permitir a progresión a estadios laravarios posteriores. Nos estadios larvarios finais, a expresión de LIN-41[64] e outros xenes podería verse reducida pola expresión do ARN de let-7, liberando a represión da expresión da proteína LIN-29[65] e permitindo a progresión ao estadio adulto. Dado que o ARNm de lin-29 non posúe sitios complementarios ao ARN de let-7, probablemente lin-29 non é unha diana directa de let-7.
Por outro lado, en miocitos de mamíferos, a activación do factor de transcrición SRF[66] induce la expresión de miR-1–1[67] e miR-1–2,[68] que á súa vez reprime a expresión do factor de transcrición Hand2[69] e o ligando de Notch,[70] Delta, afectando, por tanto, a expansión das células proxenitoras ou a súa diferenciación.[71] SRF tamén induce a expresión de miR-133a-1[72] e miR-133a-2,[73] o que inhibe á súa vez SRF nun bucle de retroalimentación. No músculo opera unha vía similar, agás que a inhibición por retroalimentación de Mef2[74] e MyoD[75] acontece cando a expresión de HDAC4[76] está reducida debido ao silenciamento exercido por miR-1–1 e miR-1–2.
Un dos primeiros miARN detectados cunha función no desenvolvemento do sistema inmunitario[51] foi miR-181a;[77] este miARN exprésase en altos niveis nas células do timo e en niveis menores nas células do corazón, os nódulos linfáticos e a medula ósea. Na medula ósea, miR-181a exprésase en niveis maiores por células B B220+ B ca por células T CD3+. Especificamente, a expresión de miR-181a en células B derivadas da medula ósea diminúe durante a maduración das células B desde o estadio do desenvolvemento de pro-célula-B ao estadio pre-célula-B. Ademais, a expresión ectópica de miR-181a en células enriquecidas en células troncais ou nais e proxenitoras hematopoéticas orixina un incremento na porcentaxe de células B CD19+ e un descenso na porcentaxe de células T CD8+ en ensaios de reconstitución da medula ósea a curto prazo en ratos, demostrando que a especificidade de liñas celulares dos miARN podería ter unha función na regulación do desenvolvemento dos linfocitos.
Por outro lado, tamén se detectou unha distribución espacial dos miARN: en embrións do peixe cebra (Danio rerio), os patróns de localización de miARN individuais indican que a súa actividade podería estar limitada aos tecidos e órganos nos que se expresan. Por exemplo, miR-206[78] exprésase sobre todo no músculo, miR-126[79] nos vasos sanguíneos e o corazón, miR-200a[80] no sistema da liña lateral (un sistema mecanosensorial que detecta o movemento da auga) e órganos sensoriais, e miR-30c[81] no precursor dos riles.[82]
Novas funcións embriolóxicas ("efecto materno")[editar | editar a fonte]
Dous estudos independentes en 2007 en ratos[83][84] indican que os cigotos herdan unha cantidade significativa de miARN maternos, e que ditos miARN maternos poderían ter un papel importante nas fases temperás do desenvolvemento embrionario (efecto materno).
Notas[editar | editar a fonte]
- ↑ Nesta palabra micro é un prefixo, non un adxectivo
- ↑ Pillai RS. MicroRNA function: multiple mechanisms for a tiny RNA? RNA 2005 Dec;11(12):1753-6 [1]
- ↑ 3,0 3,1 Lee RC, Feinbaum RL, Ambros V (1993). "The C. elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14.". Cell 75: 843–854. PMID 8252621. doi:10.1016/0092-8674(93)90529-Y.
- ↑ Ruvkun, G. (2001). "Molecular biology. Glimpses of a tiny RNA world.". Science 294 (5543): 797–9. PMID 11679654. doi:10.1126/science.1066315.
- ↑ Glasser V. Tapping miRNA-Regulated Pathways. Arquivado 27 de novembro de 2018 en Wayback Machine. Genetic Eng Biotech News Mar 1 2008 (Vol. 28, No. 5)
- ↑ 6,0 6,1 6,2 Saumet A, Lecellier CH (2006). "Anti-viral RNA silencing: do we look like plants?". Retrovirology 3 (3): 3. PMID 16409629. doi:10.1186/1742-4690-3-3.
- ↑ 7,0 7,1 7,2 Bartel DP. MicroRNAs: genomics, biogenesis, mechanism, and function. Cell 2004 Jan 23;116(2):281-97 [2]
- ↑ Bentwich I, Avniel A, Karov Y, Aharonov R, Gilad S, Barad O, Barzilai A, Einat P, Einav U, Meiri E, Sharon E, Spector Y, Bentwich Z. Identification of hundreds of conserved and nonconserved human microRNAs. Nat Genet. 2005 Jul;37(7):766-70 [3]
- ↑ Wightman B, Ha I, Ruvkun G. Posttranscriptional regulation of the heterochronic gene lin-14 by lin-4 mediates temporal pattern formation in C. elegans. Cell 1993 Dec 3;75(5):855-62 [4]
- ↑ Ambros V. MicroRNA pathways in flies and worms: growth, death, fat, stress, and timing. Cell 2003 Jun 13;113(6):673-6 [5]
- ↑ Bartel DP, Chen CZ. Micromanagers of gene expression: the potentially widespread influence of metazoan microRNA. Nat Rev Genet. 2004 May;5(5):396-400 [6]
- ↑ Lu C, Tej SS, Luo S, Haudenschild CD, Meyers BC, Green PJ. Elucidation of the small RNA component of the transcriptome. Science 2005 Sep 2;309(5740):1567-9 [7]
- ↑ He L, Thomson JM, Hemann MT, Hernando-Monge E, Mu D, Goodson S, Powers S, Cordon-Cardo C, Lowe SW, Hannon GJ, Hammond SM. A microRNA polycistron as a potential human oncogene. Nature 2005 Jun 9;435(7043):828-33 [8]
- ↑ Kim VN. MicroRNA biogenesis: coordinated cropping and dicing. Nat Rev Mol Cell Biol. 2005 May;6(5):376-85 [9]
- ↑ Zhao Y, Srivastava D.A developmental view of microRNA function. Trends Biochem Sci. 2007 Apr;32(4):189-97 [10] Arquivado 25 de marzo de 2009 en Wayback Machine.
- ↑ Zhao Y, Samal E, Srivastava D. Serum response factor regulates a muscle-specific microRNA that targets Hand2 during cardiogenesis. Nature 2005 Jul 14;436(7048):214-20 [11]
- ↑ O'Donnell KA, Wentzel EA, Zeller KI, Dang CV, Mendell JT. c-Myc-regulated microRNAs modulate E2F1 expression. Nature 2005 Jun 9;435(7043):839-43 [12]
- ↑ Drosha
- ↑ Pasha
- ↑ Denli AM, Tops BB, Plasterk RH, Ketting RF, Hannon GJ. (2004). Nature 432(7014):231-5.
- ↑ Bernstein E, Caudy AA, Hammond SM, Hannon GJ. (2001). Role for a bidentate ribonuclease in the initiation step of RNA interference. Nature 409(6818):363-6.
- ↑ Kurihara Y, Watanabe Y. (2004). Arabidopsis micro-RNA biogenesis through Dicer-like 1 protein functions. Proc Natl Acad Sci USA 101(34):12753-8.
- ↑ Gao F-B (2007). "Posttranscriptional control of neuronal development by microRNA networks". Trends in Neurosciences 31: 20. doi:10.1016/j.tins.2007.10.004.
- ↑ Stark A, Bushati N, Jan CH; et al. (2008). "A single Hox locus in Drosophila produces functional microRNA from opposite DNA strands". Genes Dev. 22 (1): 8–13. PMID 18172160. doi:10.1101/gad.1613108.
- ↑ Filipowicz W, Jaskiewicz L, Kolb FA, Pillai RS. Post-transcriptional gene silencing by siRNAs and miRNAs. Curr Opin Struct Biol. 2005 Jun;15(3):331-41 [13] Arquivado 25 de marzo de 2009 en Wayback Machine.
- ↑ RNASEN
- ↑ MacRae IJ, Doudna JA. Ribonuclease revisited: structural insights into ribonuclease III family enzymes. Curr Opin Struct Biol. 2007 Feb;17(1):138-45 [14] Arquivado 25 de marzo de 2009 en Wayback Machine.
- ↑ DGCR8
- ↑ Zeng Y, Cullen BR (2005). "Efficient processing of primary microRNA hairpins by Drosha requires flanking nonstructured RNA sequences". J. Biol. Chem. 280 (30): 27595–603. PMID 15932881. doi:10.1074/jbc.M504714200. Arquivado dende o orixinal o 24 de marzo de 2009. Consultado o 16 de xullo de 2011.
- ↑ 30,0 30,1 Han J, Lee Y, Yeom K-H, Nam J-W, Heo I, Rhee J-K, Sohn SY, Cho Y, Zhang B-T, Kim VN (2006). "Molecular basis for the recognition of primary microRNAs by the Drosha-DGCR8 complex". Cell (en inglés) 125 (5): 887–901. doi:10.1016/j.cell.2006.03.043.
- ↑ Preall JB, He Z, Gorra JM, Sontheimer EJ. (2006). Short interfering RNA strand selection is independent of dsRNA processing polarity during RNAi in Drosophila. Curr Biol 16(5):530-5.
- ↑ Gregory RI, Chendrimada TP, Cooch N, Shiekhattar R. (2005). Human RISC couples microRNA biogenesis and posttranscriptional gene silencing. Cell 123(4):631-40.
- ↑ Zhan, M. and Miller, C.P. and Papayannopoulou, T. and Stamatoyannopoulos, G. and Song, C.Z. (2007). "MicroRNA expression dynamics during murine and human erythroid differentiation". Experimental hematology 35 (7): 1015–1025. PMID 17588470. doi:10.1016/j.exphem.2007.03.014.
- ↑ Cifuentes, D. and Xue, H. and Taylor, D.W. and Patnode, H. and Mishima, Y. and Cheloufi, S. and Ma, E. and Mane, S. and Hannon, G.J. and Lawson, N.; et al. (2010). "A novel miRNA processing pathway independent of dicer requires Argonaute2 catalytic activity". Science 328 (5986): 1694 – 1698. doi:10.1126/science.1190809.
- ↑ Heng-Chi Lee, Liande Li, Weifeng Gu, Zhihong Xue, Susan K. Crosthwaite, Alexander Pertsemlidis, Zachary A. Lewis, Michael Freitag, Eric U. Selker, Craig C. Mello, Yi Liu (2010). "Diverse Pathways Generate MicroRNA-like RNAs and Dicer-Independent Small Interfering RNAs in Fungi". Molecular Cell 38 (6): 803–814. doi:10.1016/j.molcel.2010.04.005.
- ↑ Sen G, Blau H (2005). "Argonaute 2/RISC resides in sites of mammalian mRNA decay known as cytoplasmic bodies". Nat Cell Biol 7 (6): 633–6. PMID 15908945. doi:10.1038/ncb1265.
- ↑ Lian S, Jakymiw A, Eystathioy T, Hamel J, Fritzler M, Chan E (2006). "GW bodies, microRNAs and the cell cycle". Cell Cycle 5 (3): 242–5. PMID 16418578.
- ↑ Jakymiw A, Lian S, Eystathioy T, Li S, Satoh M, Hamel J, Fritzler M, Chan E (2005). "Disruption of P bodies impairs mammalian RNA interference". Nat Cell Biol 7 (12): 1267–74. PMID 16284622. doi:10.1038/ncb1334.
- ↑ Eulalio A, Behm-Ansmant I, Schweizer D, Izaurralde E. P-body formation is a consequence, not the cause, of RNA-mediated gene silencing. Mol Cell Biol. 2007 Jun;27(11):3970-81 [15] Arquivado 18/07/2011, en Wayback Machine.
- ↑ 40,0 40,1 Eulalio A, Huntzinger E, Izaurralde E. Getting to the root of miRNA-mediated gene silencing. Cell 2008 Jan 11;132(1):9-14 [16]
- ↑ Eulalio A, Rehwinkel J, Stricker M, Huntzinger E, Yang SF, Doerks T, Dorner S, Bork P, Boutros M, Izaurralde E. Target-specific requirements for enhancers of decapping in miRNA-mediated gene silencing. Genes Dev. 2007 Oct 15;21(20):2558-70 [17]
- ↑ Kozak M. (2008). "Faulty old ideas about translational regulation paved the way for current confusion about how microRNAs function.". Gene. Jul 22 (Epub ahead of print). [18]
- ↑ Vasudevan S, Tong Y, Steitz JA. Switching from repression to activation: microRNAs can up-regulate translation. Science 2007 Dec 21;318(5858):1931-4 [19]
- ↑ Hayden EC (2008). "Thousands of proteins affected by miRNA". Nature 545. 562. [20]
- ↑ Selbach M, Schwanhäusser B, Thierfelder N, Fang Z, Khanin R, Rajewsky N. (2008). "Widespread changes in protein synthesis induced by microRNAs". Nature. Published online 30 July 2008. [21]
- ↑ Baek D, Villén J, Shin C, Camargo FD, Gygi SP, Bartel DP. (2008). "The impact of microRNAs on protein output". Nature. Published online 30 July 2008. [22]
- ↑ Lewis BP, Burge CB, Bartel DP. Conserved seed pairing, often flanked by adenosines, indicates that thousands of human genes are microRNA targets. Cell 2005 Jan 14;120(1):15-20 [23]
- ↑ Shan G, Li Y, Zhang J, Li W, Szulwach KE, Duan R, Faghihi MA, Khalil AM, Lu L, Paroo Z, Chan AW, Shi Z, Liu Q, Wahlestedt C, He C, Jin P. (2008). "A small molecule enhances RNA interference and promotes microRNA processing.". Nat Biotechnol. 26 (8). 933-40. [24]
- ↑ Lecellier CH, Dunoyer P, Arar K, Lehmann-Che J, Eyquem S, Himber C, Saïb A, Voinnet O. A cellular microRNA mediates antiviral defense in human cells. Science 2005 Apr 22;308(5721):557-60 [25]
- ↑ ="Jopling2005" Jopling CL, Yi M, Lancaster AM, Lemon SM, Sarnow P. Modulation of hepatitis C virus RNA abundance by a liver-specific MicroRNA. Science 2005 Sep 2;309(5740):1577-81 [26]
- ↑ 51,0 51,1 Lodish HF, Zhou B, Liu G, Chen CZ. Micromanagement of the immune system by microRNAs. Nat Rev Immunol. 2008 Feb;8(2):120-30 [27]
- ↑ Esquela-Kerscher A, Slack FJ. Oncomirs - microRNAs with a role in cancer. Nat Rev Cancer. 2006 Apr;6(4):259-69 [28]
- ↑ Calin GA, Sevignani C, Dumitru CD, Hyslop T, Noch E, Yendamuri S, Shimizu M, Rattan S, Bullrich F, Negrini M, Croce CM. Human microRNA genes are frequently located at fragile sites and genomic regions involved in cancers. Proc Natl Acad Sci U S A 2004 Mar 2;101(9):2999-3004 [29]
- ↑ Sonoki T, Iwanaga E, Mitsuya H, Asou N.Insertion of microRNA-125b-1, a human homologue of lin-4, into a rearranged immunoglobulin heavy chain gene locus in a patient with precursor B-cell acute lymphoblastic leukemia. Leukemia 2005 Nov;19(11):2009-10 [30]
- ↑ Calin GA, Dumitru CD, Shimizu M, Bichi R, Zupo S, Noch E, Aldler H, Rattan S, Keating M, Rai K, Rassenti L, Kipps T, Negrini M, Bullrich F, Croce CM. Frequent deletions and down-regulation of micro- RNA genes miR15 and miR16 at 13q14 in chronic lymphocytic leukemia. Proc Natl Acad Sci U S A. 2002 Nov 26;99(24):15524-9 [31]
- ↑ Büssing I, Slack FJ, Großhans H. (2008). "let-7 microRNA in development, stem cells and cancer". Trends Mol Med. Jul 30. (Epub ahead of print). [32]
- ↑ Ma L, Weinberg RA. (2008). "Micromanagers of malignancy: role of microRNAs in regulating metastasis". Trends Genet. Jul 30 (Epub ahead of print). [33]
- ↑ Lau NC, Lim LP, Weinstein EG, Bartel DP. An abundant class of tiny RNAs with probable regulatory roles in Caenorhabditis elegans. Science 2001 Oct 26;294(5543):858-62 [34]
- ↑ lin-4
- ↑ let-7
- ↑ Reinhart BJ, Slack FJ, Basson M, Pasquinelli AE, Bettinger JC, Rougvie AE, Horvitz HR, Ruvkun G. The 21-nucleotide let-7 RNA regulates developmental timing in Caenorhabditis elegans. Nature 2000 Feb 24;403(6772):901-6 [35]
- ↑ LIN-14
- ↑ LIN28
- ↑ LIN-41
- ↑ LIN-29
- ↑ SRF
- ↑ "miR-1-1". Arquivado dende o orixinal o 26 de marzo de 2009. Consultado o 16 de xullo de 2011.
- ↑ "miR-1-2". Arquivado dende o orixinal o 26 de marzo de 2009. Consultado o 16 de xullo de 2011.
- ↑ Hand2
- ↑ Notch
- ↑ Zhao Y, Srivastava D. A developmental view of microRNA function. Trends Biochem Sci. 2007 Apr;32(4):189-97 [36] Arquivado 25 de marzo de 2009 en Wayback Machine.
- ↑ "miR-133a-1". Arquivado dende o orixinal o 26 de marzo de 2009. Consultado o 16 de xullo de 2011.
- ↑ "miR-133a-2". Arquivado dende o orixinal o 26 de marzo de 2009. Consultado o 16 de xullo de 2011.
- ↑ Mef2
- ↑ MyoD
- ↑ HDAC4
- ↑ "miR-181-a". Arquivado dende o orixinal o 26 de marzo de 2009. Consultado o 16 de xullo de 2011.
- ↑ "miR-206". Arquivado dende o orixinal o 13 de maio de 2008. Consultado o 16 de xullo de 2011.
- ↑ "miR-126". Arquivado dende o orixinal o 26 de marzo de 2009. Consultado o 16 de xullo de 2011.
- ↑ "miR-200a". Arquivado dende o orixinal o 26 de marzo de 2009. Consultado o 16 de xullo de 2011.
- ↑ "miR-30c". Arquivado dende o orixinal o 26 de marzo de 2009. Consultado o 16 de xullo de 2011.
- ↑ Wienholds E, Kloosterman WP, Miska E, Alvarez-Saavedra E, Berezikov E, de Bruijn E, Horvitz HR, Kauppinen S, Plasterk RH. MicroRNA expression in zebrafish embryonic development. Science 2005 Jul 8;309(5732):310-1 [37]
- ↑ Murchison EP, Stein P, Xuan Z, Pan H, Zhang MQ, Schultz RM, Hannon GJ. Critical roles for Dicer in the female germline. Genes Dev. 2007 Mar 15;21(6):682-93 [38]
- ↑ Tang F, Kaneda M, O'Carroll D, Hajkova P, Barton SC, Sun YA, Lee C, Tarakhovsky A, Lao K, Surani MA. Maternal microRNAs are essential for mouse zygotic development. Genes Dev. 2007 Mar 15;21(6):644-8 [39]
