Retrovirus
| Retrovirus | |||||
|---|---|---|---|---|---|
 ciclo do retrovirus VIH | |||||
| Clasificación científica | |||||
| |||||
| Xéneros | |||||
|
Subfamilia: Orthoretrovirinae Subfamilia: Spumaretrovirinae | |||||
Un retrovirus é un virus de ARN que se replica nunha célula hóspede facendo unha copia en ADN do seu xenoma. Os máis típicos pertencen á familia Retroviridae. Entre eles está o VIH causante da SIDA. O virus usa primeiramente o seu encima característico, a reversotranscriptase para producir ADN a partir do seu xenoma de ARN, o que é o inverso do procedemento normal (transcrición: ADN→ARN). Este novo ADN de orixe viral é despois incorporado ao xenoma da célula hóspede pola acción dun encima integrase. A célula despois trata ao ADN proviral incorporado como parte do seu propio xenoma, e segue as súas instrucións fielmente, fabricando as proteínas víricas codificadas nos xenes virais necesarias para a ensamblaxe e formación de novas copias do virus. Os retrovirus son virus con envoltura membranosa, que toman da célula infectada.
Unha variedade especial dos retrovirus son os retrovirus endóxenos (ERV) que están integrados no xenoma do hóspede e se herdan dunha xeración a outra.
Hai algúns virus con reversotranscrición que son virus de ADN e non pertencen á familia Retroviridae ou relacionadas (ver grupo VII en "Clasificación" máis abaixo).
O retrovirus almacena o seu material xenético en forma de ARNm (que ten os extremos modificados 5' cap e 3'poliA) dentro do virión, e este serve como medio para liberar o xenoma vírico dentro da célula, e iniciar a infección. Unha vez que está na célula hóspede, o ARN sofre a reversotranscrición no citoplasma e despois integra o seu ADN no xenoma celular. Cando está integrado recibe o nome de provirus.
O ADN proviral do retrovirus pode permanecer integrado moito tempo e non é detectado polo sistema inmunitario. Porén, o provirus nun determinado momento transcribe o seu ADN a ARN para expresar os xenes do virus e producir novas copias do virus. Por tanto, a información contida nun xene retroviral flúe na secuencia: ARN → ADN → ARN → proteína.
Os retrovirus son valiosas ferramentas de investigación en bioloxía molecular e foron utilizados con éxito en sistemas de transferencia de xenes.[1]
Estrutura[editar | editar a fonte]
Os virións dos retrovirus son partículas envoltas duns 100 nm de diámetro. Os virións conteñen dúas moléculas idénticas de ARN monocatenario de 7-10 quilobases (kb) de lonxitude. Aínda que os virións de diferentes retrovirus non teñen a mesma morfoloxía ou bioloxía, todos os compoñentes do virión son moi semellantes.[2]
Os principais compoñentes do virión de retrovirus son:
- Envoltura: composta de lípidos obtidos da membrana plasmática do hóspede por medio dun proceso de evaxinación, e que contén tamén glicoproteínas codificadas polo xene env do virus.
- ARN: consiste nun dímero de ARN. Ten extremos modificados 5'cap e 3'poliA. O xenoma de ARN presenta rexións non codificantes terminais, que son importantes para a replicación, e rexións internas que codifican as proteínas do virión.
- O extremo 5' inclúe catro rexións, que son: R, U5, PBS, e L. A rexión R é unha secuencia curta repetida situada en cada extremo do xenoma usada durante a reversotranscrición para asegurar o salto correcto dun extremo a outro da cadea en crecemento. A rexión U5 é unha secuencia curta única situada entre as rexións R e PBS. A rexión PBS (primer binding site, sitio de unión do cebador) consta de 18 bases complementarias co extremo 3' do primer de ARNt (un ARNt celular que actúa como primer e se hibrida coa rexión PBS). A rexión L é unha rexión líder non traducida que é o sinal para o empaquetamento do xenoma do ARN. A secuencia de nucleótidos no extremo 5' do xenoma do virus do sarcoma das aves foi secuenciado por J. Shine e A. P. Czernilofsky en 1977 [3].
- O extremo 3' comprende tres rexións, que son: rexión PPT (polypurine tract), U3, e R. A rexión PPT é o primer para a síntese da cadea + de ADN durante a reversotranscrición. A rexión U3 é unha secuencia situada entre as rexións PPT e R, que leva o sinal que o provirus pode usar para a transcrición xenética. A rexión R é a secuencia repetida terminal do extremo 3'. A secuencia de nucleótidos do dominio non traducido pero conservado do extremo 3' do xenoma do virus do sarcoma das aves foi publicado por A.P. Czernilofsky en 1980 [4].
- Proteínas: constan das proteínas gag, protease (PR), e as proteínas pol e env. As proteínas gag son os principais compoñentes da cápside viral, a cal está formada por 2000-4000 copias desta proteína por virión. A protease exprésase de xeito diferente nos distintos retrovirus. Funciona facendo clivaxes proteolíticas durante a maduración do virión para producir as proteínas maduras gag e pol. As proteínas pol son responsables da síntese do ADN viral e integración no ADN da célula hóspede despois do inicio da infección. Finalmente, as proteínas env xogan un papel na unión e entrada do virión na célula hóspede, xa que están situadas na envoltura.[5]
Multiplicación[editar | editar a fonte]
Cando os retrovirus integran os seus propios xenomas en células da liña xerminal, os seus xenomas pasan de xeración en xeración. Deste modo orixínanse retrovirus endóxenos (ERVs), que hoxe forman o 5-8% do xenoma humano, e que en xeral levan moito tempo no xenoma. Contrastan cos retrovirus exóxenos, que son dos que trata principalmente este artigo.[6] A maioría das insercións de retrovirus endóxenos non teñen función coñecida e formarían parte do que se denominou "ADN lixo". Porén, moitos retrovirus endóxenos xogan importantes papeis na bioloxía do hóspede, como o control da transcrición de xenes, fusión celular durante o desenvolvemento da placenta no curso da xerminación dun embrión, e resistencia a infeccións por retrovirus exóxenos. Os retrovirus endóxenos recibiron tamén a atención dos investigadores da área da inmunoloxía.[7]
A transcrición ten lugar do ADN ao ARN, pero a reversotranscrición transcribe ARN a ADN. O prefixo "retro" en retrovirus refírese a esta inversión do fluxo xenético do dogma central da bioloxía molecular. A actividade de reversotrinscritase, ademais de nos retrovirus, foi atopada tamén nas células eucariotas, nas que permite a xeración e inserción de novas copias de retrotransposóns no xenoma do hóspede.
Cando o retrovirus inserta o seu xenoma no da célula hóspede, este transcríbese e orixina ARNms que saen ao citosol, onde son traducidos ás proteínas necesarias para formar os novos virus. É importante notar que un retrovirus debe traer con el a súa propia reversotranscriptase dentro da súa cápside, xa que non pode utilizar os encimas das células infectadas.
As drogas terapéuticas denominadas inhibidores da protease e da reversotranscriptase teñen como dianas sitios e secuencias específicos nos seus respectivos encimas. Porén, estas drogas poden perder rapidamente a súa efectividade debido a que as secuencias xénicas que codifican para a protease e a reversoptranscriptase mutan rapidamente. Estes cambios de bases orixinan codóns e sitios específicos nos encimas, que cambian, e, por tanto, evitan ser as dianas das drogas ao perderen os sitios que as drogas utilizan para unirse a eles.
Como a reversotranscrición carece da habitual actividade de corrección de probas da replicación do ADN. Os retrovirus mutan con gran frecuencia. Isto permite que o virus aumente a súa resistencia aos fármacos antivirais rapidamente, e impide o desenvolvemento de vacinas efectivas e inhibidores para os retrovirus.[8]
Un inconveniente de moitos retrovirus, como o retrovirus da leucemia murina Moloney, implica o requirimento de que as células estean dividíndose activamente para que se produza a transdución, o que dificulta o seu uso na terapia xénica. Como resultado, as células como as neuronas son moi resistentes á infección e á transdución por retrovirus, xa que non se dividen. Sempre existe a preocupación de que a mutaxénese insercional debida á integración no xenoma do hóspede poida orixinar un cancro ou leucemia. Isto é diferente ao que fan os Lentiviridae, un subgrupo dentro dos Retroviridae que pode integrar o seu ARN no xenoma de células hóspede que non se están a dividir.
Transmisión[editar | editar a fonte]
Hai tres modos de transmisión entre os retrovirus:
- De célula a célula[9]
- Por medio de fluídos
- Polo aire, como no caso do retrovirus do Jaagsiekte da ovella (o Jaagsiekte é unha enfermidade pulmonar).
Xenes[editar | editar a fonte]
Os xenomas de retrovirus xeralmente conteñen tres marcos de lectura abertos que codifican as proteínas que poden encontrarse no virus maduro. Son:
- antíxeno específico de grupo (gag). Codifica as proteínas estruturais e internas do virus;
- polimerase (pol). Codifica a reversotranscriptase, protease e integrase; e,
- envoltura (env). Codifica as proteínas da envoltura retroviral.
A posesión dunha copia funcional do xene env é o que fai que os retrovirus sexan distintos dos retroelementos.[10] O xene env realiza tres funcións distintas: permite que o retrovirus entre e saia das células hóspede por medio do tráfico de membranas endosómicas na célula, protección do ambiente extracelular por medio da bicapa lipídica, e a capacidade de entrar nas células. A capacidade do retrovirus de unirse á súa célula hóspede utilizando receptores específicos da superficie celular dálla o compoñente de superficie (SU) do env, e a capacidade do retrovirus de entrar na célula por medio da fusión de membranas débese ao compoñente transmembrana ancorado na membrana (TM). Deste xeito, a proteína env é a que permite que o retrovirus sexa infeccioso.
Provirus[editar | editar a fonte]
É o ADN vírico incorporado ao xenoma da célula hóspede en forma de provirus, que pode pasar á proxenie da célula. Cando a célula se divide ten que replicar previamente o seu xenoma e ao facelo replica tamén o provirus integrado, polo que as células fillas levan tamén o provirus. O ADN dalgúns retrovirus insírese aleatoriamente no xenoma da célula hóspede, polo que pode ser inserido nun oncoxene. Deste modo algúns retrovirus poden converter as células normais en células cancerosas. Algúns provirus permanecen latentes na célula durante longos períodos antes de que son activados por algún cambio no seu ambiente.
Primeiras fases da evolución[editar | editar a fonte]
O estudo dos retrovirus levou á primeira demostración da síntese de ADN a partir de moldes de ARN, un modo fundamental de transferir o material xenético entre especies. Especulouse que nas fases máis iniciais da evolución das células os procesos de reversotranscrición do ARN ao ADN utilizados polos retrovirus son os que puideron orixinar a aparición do ADN como material xenético. Neste modelo que se enmarca na hipótese do mundo de ARN, os organismos celulares adoptaron o ADN (molécula quimicamente máis estable) cando os retrovirus evolucionaron para crear ADN a partir de moldes de ARN.
Terapia xénica[editar | editar a fonte]
Os vectores gammarretrovirais e lentivirais utilizados na terapia xénica median a modificación xenética estable de células tratadas por medio da súa integración no xenoma celular. Esta trecnoloxía é útil non só na investigación, senón tamén para a terapia xénica clínica que trata de corrixir os defectos xenéticos das células de forma permanente; por exemplo, en células nai proxenitoras. Desenvolvéronse partículas vector retrovirais que infectan determinados tipos de células. Os vectores gammarretrovirais e lentivirais foron xa usados ata o momento en máis de 300 ensaios clínicos, para tratar diversas doenzas.[1][11]
Cancro[editar | editar a fonte]
Os retrovirus que causan o crecemento de tumores inclúen o virus do sarcoma de Rous e o virus do tumor mamario de rato. O cancro pode ser desencadeado por protooncoxenes que foron incorporados por erro no ADN proviral ou pola disrupción de protooncoxenes celulares. O virus do sarcoma de Rous contén o xene src que desencadea a formación de tumores. Máis tarde atopouse que un xene similar das células estaba implicado na sinalización celular, o cal era moi probablemente extraído co ADN proviral. Os virus non transformantes poden inserir o seu ADN aleatoriamente en protooncoxenes, interrompendo a expresión de proteínas que regulan o ciclo celular. O promotor do ADN do provirus pode tamén causar a sobreexpresión de xenes regulatorios.
Clasificación[editar | editar a fonte]
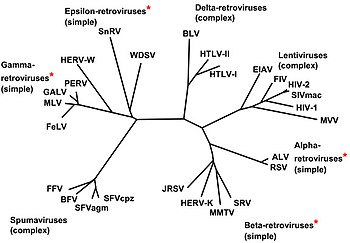
Os virus que presentan reversotranscrición poden clasificarse da seguinte maneira:
Exóxenos[editar | editar a fonte]
Non se transmiten á proxenie directamente polo xenoma, xa que non están definitivamente integrados nel (só o fan durante as infeccións), polo que chegan ao corpo desde o exterior causando a infección. O grupo inclúe os seguintes xéneros:
- Alpharetrovirus; especie tipo: virus da leucose aviaria; outro é o virus do sarcoma de Rous
- Betaretrovirus; especie tipo: virus do tumor mamario de rato
- Gammaretrovirus; especie tipo: virus da leucemia murina; outro é o virus da leucemia felina
- Deltaretrovirus; especie tipo: virus da leucemia bovina; outro é o virus T linfotrópico humano causante de cancro
- Epsilonretrovirus; especie tipo: virus do sarcoma dermal Walleye
- Lentivirus; especie tipo: virus da inmunodeficiencia humana 1; outros son o virus da inmunodeficiencia simia e o virus da inmunodeficiencia felina
- Spumavirus; especie tipo: virus escumoso simio.
Estes xéneros estaban antes clasificados en tres subfamilias (Oncovirinae, Lentivirinae, e Spumavirinae), pero co coñecemento que se ten actualmente dos retrovirus esta división xa non parece apropiada. (Porén, o termo oncovirus aínda se usa correntemente).
Os retrovirus clasificáronse en dous grupos na clasificación de Baltimore, que son os grupos VI e VII de virus. Os detalles da reversotranscrición non son iguais en todos eles.
Virus do grupo VI[editar | editar a fonte]
Son virus de ARN. Todos os membros do grupo VI usan unha reversotranscriptase codificada polo virus, que é unha ADN polimerase ARN dependente, para producir ADN a partir do xenoma inicial viral de ARN. O ADN é a miúdo integrado no xenoma do hóspede, como no caso dos retrovirus e pseudovirus, nos que o xenoma é replicado e transcrito polo hóspede.
O grupo VI inclúe as seguintes familias:
- Metaviridae
- Pseudoviridae
- Retroviridae - Retrovirus, por exemplo, VIH.
Virus do grupo VII[editar | editar a fonte]
Ambas as familias do grupo VII teñen xenomas de ADN nas partículas que infectan as células. O xenoma de ADN é transcrito tanto a un ARNm (usado na síntese proteica) coma a un ARN prexenómico (usado como molde durante a replicación do xenoma vírico por reversotranscrición). Unha reversotranscriptase codificada polo virus utiliza o ARN prexenómico como molde para a creación do ADN viral xenómico para as novas copias do virus.
O grupo VII inclúe as seguintes familias:
- Hepadnaviridae - por exemplo, virus da hepatite B
- Caulimoviridae - por exemplo, virus do mosaico da coliflor.
Endóxenos[editar | editar a fonte]
- Artigo principal: retrovirus endóxenos.
Os retrovirus endóxenos (ERV)s non están formalmente incluídos neste sistema de clasificación, xa que están integrados no xenoma e pasan directamente de xeración en xeración formando parte do xenoma e nunca están no exterior. Deberon orixinarse por infeccións retrovirais nos antepasados das especies hai moito tempo. Clasifícanse en tres clases baseándose na proximidade aos xéneros de retrovirus exóxenos:
- Clase I. Son similares aos gammarretrovirus.
- Clase II. Son máis similares aos betarretrovirus e alfarretrovirus.
- Clase III. Son similares aos espumavirus.
Tratamento[editar | editar a fonte]
As drogas antirretrovirais son medicacións usadas para o tratamento de infeccións por retrovirus, principalmente o VIH. Hai distintas clases de drogas antirretrovirais que actúan en diferentes estadios do ciclo de replicación do VIH. A combinación de varias drogas antirretrovirais (xeralmente tres ou catro) é unha activa terapia antirretroviral.[12]
Tratamento de retrovirus veterinarios[editar | editar a fonte]
As infeccións polo virus da leucemia felina e o virus da inmunodeficiencia felina poden tratarse con produtos como o inmunomodulador chamado inmunomodulador célula T-linfocito (LTCI).[13]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 Kurth, R; Bannert, N (editors) (2010). Retroviruses: Molecular Biology, Genomics and Pathogenesis. Caister Academic Press. ISBN 978-1-904455-55-4.
- ↑ John M. Coffin (1992). "Structure and Classification of Retroviruses". En Jay A. Levy. The Retroviridae (1st ed.). New York: Plenum Press. p. 20. ISBN 0-306-44074-1.
- ↑ J. Shine e Czernilofsky et al. Proc. Natl. Acad. Sci. USA, Vol 75, pp 1473–1477, 1977
- ↑ A.P. Czernilofsky et al. Nucleic Acuds Research, Vol. 8, pp 2967–2984, 1980
- ↑ John M. Coffin (1992). "Structure and Classification of Retroviruses". En Jay A. Levy. The Retroviridae (1st ed.). New York: Plenum Press. pp. 26–34. ISBN 0-306-44074-1.
- ↑ Robert Belshaw; Pereira V; Katzourakis A; Talbot G; Paces J; Burt A; Tristem M. (2004). "Long-term reinfection of the human genome by endogenous retroviruses". Proc Natl Acad Sci USA 101 (14): 4894–9. PMC 387345. PMID 15044706. doi:10.1073/pnas.0307800101.
- ↑ Medstrand P, van de Lagemaat L, Dunn C, Landry J, Svenback D, Mager D (2005). "Impact of transposable elements on the evolution of mammalian gene regulation". Cytogenet Genome Res 110 (1-4): 342–52. PMID 16093686. doi:10.1159/000084966.
- ↑ Svarovskaia ES; Cheslock SR; Zhang WH; Hu WS; Pathak VK. (2003). "Retroviral mutation rates and reverse transcriptase fidelity.". Front Biosci. 8 (1-3): d117–34. PMID 12456349. doi:10.2741/957.
- ↑ Clare Jolly (2011). "Cell-to-cell transmission of retroviruses: Innate immunity and interferon-induced restriction factors.". PubMed Central 411 (251–259): 251–9. PMC 3053447. PMID 21247613. doi:10.1016/j.virol.2010.12.031.
- ↑ Felix J. Kim; Jean-Luc Battini, Nicolas Manel, Marc Sitbon (2004). "Emergence of vertebrate retroviruses and envelope capture". Virology (318): 183–191.
- ↑ Desport, M (editors) (2010). Lentiviruses and Macrophages: Molecular and Cellular Interactions. Caister Academic Press. ISBN 978-1-904455-60-8.
- ↑ Haddad M, Inch C, Glazier RH; et al. (2000). "Patient support and education for promoting adherence to highly active antiretroviral therapy for HIV/AIDS". Cochrane Database of Systematic Reviews (Online) (3): CD001442. PMID 10908497. doi:10.1002/14651858.CD001442.
- ↑ Gingerich DA (2008). "Lymphocyte T-cell immunomodulator (LTCI): Review of the immunopharmacology of a new biologic" (PDF). Intern J Appl Res Vet Med 6 (2): 61–8.
Véxase tamén[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
| Commons ten máis contidos multimedia sobre: Retrovirus |
- ViralZone Un portal pertencente ao Instituto Suízo de Bioinformática con recursos para todas as familias virais, que dá información molecular xeral e epidemiolóxica (ligazóns para "Retro-transcribing viruses")
- Animación Flash sobre retrovirus
- Retrovirology revista científica
- Retrovirus life cycle chapter capítulo do texto en liña de "Bioloxía" de Kimball
- "Retroviruses" ISBN 0-87969-571-4
- Annals of Science: Darwin's Surprise. Michael Specter. The New Yorker. Decembro 3, 2007.
