Glutamina
| L-Glutamina | |
|---|---|
 | |
 | |
Glutamina | |
Outros nomes L-Glutamina | |
| Identificadores | |
| Abreviaturas | Gln, Q |
| Número CAS | 56-85-9 |
| PubChem | 738 |
| ChemSpider | 718 |
| UNII | 0RH81L854J |
| Número CE | 200-292-1 |
| KEGG | C00303 |
| ChEBI | CHEBI:28300 |
| ChEMBL | CHEMBL930 |
| Ligando IUPHAR | 723 |
| Código ATC | A16 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades[1] | |
| Fórmula molecular | C5H10N2O3 |
| Masa molar | 146,14 g mol−1 |
| Punto de fusión | descomponse arredor de 185 °C |
| Solubilidade en auga | soluble |
| Rotación quiral [α]D | +6,5º (H2O, c = 2) |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |


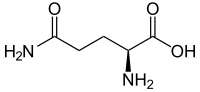
A glutamina (abreviadamente Gln ou Q) é un α-aminoácido que forma parte das proteínas (aminoácido proteinoxénico). A súa cadea lateral -CH2-CH2-CO-NH2 é unha amida formada ao substituír o grupo hidroxilo da cadea lateral do ácido glutámico por un grupo amino. Por tanto, pode considerarse como a amida do ácido glutámico cun grupo carboxiamida. O grupo amino é polar, polo que se considera un aminoácido polar neutro a pH celular. Nas proteínas aparece o isómero L.
Non se considera un aminoácido esencial, pero pode chegar a ser condicionalmente esencial en certas situacións, como adestramento atlético intenso ou trastornos gastrointestinais. Está codificado polos codóns do código xenético CAA e CAG. No sangue humano a glutamina é o aminoácido máis abundante, cunha concentración de arredor 500-900 µmol/L.[2]
Na súa degradación oxidativa a glutamina orixina alfa-cetoglutarato, que pode entrar na gliconeoxénese, polo que é un aminoácido glicoxénico.
Funcións[editar | editar a fonte]
A glutamina desempeña importantes funcións bioquímicas, como as seguintes:
- Síntese proteica, xa que é un compoñente das proteinas.
- Regulación do balance ácido-básico nos riles ao producir amonio.[3]
- Fonte de enerxía celular en certos casos.[4]
- Doazón de nitróxeno para moitos procesos do anabolismo.[2]
- Doazón de carbono, como fonte que "rechea" o ciclo do ácido cítrico.[5]
- Transportador non tóxico de amonio pola corrente sanguínea.
Órganos consumidores e produtores[editar | editar a fonte]
A glutamina sintetízase polo encima glutamina sintetase a partir de glutamato e amoníaco. O tecido máis importante na produción de glutamina é o muscular, que orixina arredor do 90% de toda a glutamina sintetizada. Tamén liberan pequenas cantidades de glutamina os pulmóns e o cerebro.[6] O fígado ten a capacidade de facer unha síntese significativa de glutamina, pero o seu papel no metabolismo da glutamina é máis ben regulatorio, xa que o fígado recibe grandes cantidades de glutamina procedente do intestino.[2]
Os consumidores máis ávidos de glutamina no organismo son as células intestinais,[2] os riles para establecer o equilibrio ácido-básico, as células inmunes activadas[7] e moitas células cancerixenas.[5] Aproveitando isto último, téñense probado diversos fármacos análogos da glutamina como tratamentos anticancerosos, como a 6-Diazo-5-oxo-L-norleucina (DON), azaserina ou acivicina.
Exemplos do uso da glutamina[editar | editar a fonte]
En estados catabólicos de traumatismos ou enfermidades, a glutamina pode chegar a ser un aminoácido esencial e requírese a súa inxesta como suplemento nutricional. A glutamina foi moi estudada durante os últimos 10–15 anos e mostrou ser útil no tratamento de doenzas graves, mancaduras, traumas, queimaduras, e como paliativo dos efectos secundarios do tratamento do cáncer, e como axuda para a curación de feridas cirúrxicas en pacientes postoperatorios [8] e para unha máis rápida recuperación.[9] A glutamina comercialízase como suplemento alimentario para o crecemento muscular. As probas indican que a glutamina cando se administra oralmente pode incrementar os niveis plasmáticos da hormona do crecemento ao estimular a glándula pituitaria anterior.[10] Na investigación biolóxica a L-glutamina engádese habitualmente [11] aos medios de cultivos celulares.
Nutrición[editar | editar a fonte]
Presenza no organismo[editar | editar a fonte]
A glutamina é o aminoácido non esencial máis abundante no corpo humano e un dos poucos aminoácidos que poden cruzar a barreira hemato-encefálica.[12] No corpo atopámola circulando polo sangue ou almacenada nas proteínas do músculo esquelético. Só é necesaria a suplementación en casos de enfermidade ou traumas.
Fontes alimenticias[editar | editar a fonte]
As principais fontes dietarias de L-glutamine son: carne de vaca, polo, peixe, ovos, leite e produtos lácteos, trigo, repolo, remolacha, feixóns, espinacas, e perexil. Tamén se atopan pequenas cantidades de L-glutamina libre en zumes de verduras e alimentos como o tofu.[13]
Notas[editar | editar a fonte]
- ↑ Weast, Robert C., ed. (1981). CRC Handbook of Chemistry and Physics (62nd ed.). Boca Raton, FL: CRC Press. p. C-311. ISBN 0-8493-0462-8.
- ↑ 2,0 2,1 2,2 2,3 Brosnan John T. (2003). "Interorgan amino acid transport and its regulation". J. Nutr. 133 (6): 2068S–72S. PMID 12771367..
- ↑ Arthur C. Guyton, John E. Hall (2005). Saunders, ed. Textbook of Medical Physiology (11th ed.). p. 393. ISBN 0721602401..
- ↑ Aledo J. Carlos (2004). "Glutamine breakdown in rapidly dividing cells: waste or investment?". BioEssays 26 (7): 778–85. PMID 15221859. doi:10.1002/bies.20063..
- ↑ 5,0 5,1 Mariia Yuneva, Nicola Zamboni, Peter Oefner, Ravi Sachidanandam, Yuri Lazebnik (2007). "Defiency in glutamine but not glucose induces MYC-dependent apoptosis in human cells". J. Cell Biol. 178 (1): 93–105. PMC 2064426. PMID 17606868. doi:10.1083/jcb.200703099..
- ↑ P. Newsholme, M. M. R. Lima , J. Procopio, T. C. Pithon-Curi, S. Q. Doi, R. B. Bazotte, R. Curi (2003). "Glutamine and glutamate as vital metabolites". Braz. J. Med. Biol. Res. 36 (2): 153–63. PMID 12563517. doi:10.1590/S0100-879X2003000200002..
- ↑ Newsholme Philip (2001). "Why Is L-Glutamine Metabolism Important to Cells of the Immune System in Health, Postinjury, Surgery or Infection?". J. Nutr. 131 (9): 2515S–22S. PMID 11533304..
- ↑ Morlion Bart J., Stehle Peter, Wachtler Paul, Siedhoff Hans-P., Köller Manfred, König Wolfgang, Fürst Peter, Puchstein Christoph (1998). "Total parenteral nutrition with glutamine dipeptide after major abdominal surgery: a randomized, double-blind, controlled study". Ann. Surg. 227 (2): 302–8. PMC 1191250. PMID 9488531. doi:10.1097/00000658-199802000-00022..
- ↑ University of Maryland Medical Center (ed.). "Glutamine". Consultado o 2009-09-06..
- ↑ TC Welbourne (1995). American Journal of Clinical Nutrition, ed. "Increased plasma bicarbonate and growth hormone after an oral glutamine load". The American journal of clinical nutrition 61 (5): 1058–61. PMID 7733028.
- ↑ "L-glutamine". exactantigen.com. Arquivado dende o orixinal o 20 de decembro de 2009. Consultado o 2009-11-27.
- ↑ Wha-Joon Lee, Richard A. Hawkins, Juan R. Viña, Darryl R. Peterson (1998). "Glutamine transport by the blood-brain barrier: a possible mechanism for nitrogen removal". Am. J. Physiol. Cell Physiol. 274 (4): C1101–7. PMID 9580550..
- ↑ "Glutamine - Vitamins Supplements Guide". Arquivado dende o orixinal o 19 de febreiro de 2012. Consultado o 2007-11-01..
