Saponina
As saponinas son unha clase de compostos químicos, especialmente abondosos en diversas especies de plantas, que son glicósidos anfipáticos agrupados pola súa propiedade de producir unha escuma parecida á do xabón cando se baten en solucións acuosas, de onde lles vén o seu nome (sapo-onis é xabón en latín). Estruturalmente teñen un ou máis residuos de glicósido hidrófilos combinados cun derivado triterpeno lipófilo.[1][2]
As saponinas forman micelas e cambian a tensión superficial dos líquidos. O seu tamaño molecular está entre 600 Da e os 2 700 Da, pero cando forman micelas poden chegar a ter un peso molecular entre 70 e 150 KDa. Aféctalles o pH da solución, xa que a altos pH sofren hidrólise, formándose saponinas de menor peso molecular.
As saponinas teñen unha acción irritante sobre as células. No parénquima pulmonar tradúcese nunha acción expectorante; sobre as células renais produce unha acción diurética e sobre os glóbulos vermellos unha acción hemolítica. Como norma xeral, os fármacos con saponinas producen unha acción expectorante, diurética, depurativa, tónico-venosa e de diminución do colesterol. As saponinas esteroideas serven como materia prima na hemisíntese de hormonas sexuais e corticais. Aínda que se absorben mal no tracto dixestivo, favorecen a absorción doutros compostos: os cardiotónicos.
Variedade estrutural e biosíntese[editar | editar a fonte]
As porcións aglicona (sen glicósido) das saponinas denomínanse sapoxeninas. O número de cadeas de sacárido unidas ao núcleo sapoxenina/aglicona poden variar (dando lugar a outra dimensión de nomenclatura: monodesmosídicas, bidesmosídicas etc.[1]), como tamén a lonxitude de cada cadea. Unha compilación algo antiga sinala que o rango de lonxitudes das cadea sacárida está entre 1 e 11, sendo o máis frecuente de 2 a 5, e poden ter cadeas liñais ou ramificadas.[1] Os monosacáridos da dieta como a D-glicosa e D-galactosa están entre os compoñentes máis comúns das cadeas unidas.[1]
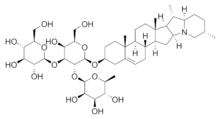
A aglicona lipófila pode ter moi diversas estruturas orgánicas policíclicas orixinadas pola adición en serie de unidades de terpenos de 10 carbonos (C10) para compoñer un esqueleto de triterpeno de 30 carbonos,[3][4] a miúdo cunha posterior alteración para producir un esqueleto esteroide de 27 carbonos.[1] O subconxunto de saponinas que son esteroides denomináronse saraponinas;[2] Os derivados aglicona poden tamén incorporar nitróxeno, polo que algunhas saponinas tamén presentan características químicas e farmacolóxicas de produtos alcaloides naturais. A figura de arriba á dereita representa a estrutura da fitotoxina alcaloide solanina, unha saponina monodesmosídica esteroidea de sacárido ramificado. (A estrutura esteroide lipófila é unha serie de aneis de seis a cinco membros conectados á dereita da estrutura, mentres que os tres aneis de azucre ricos en oxíxenos están á esquerda e abaixo. Nótese o átomo de nitróxeno inserido no esqueleto esteroide á dereita.)
Coñécense máis de 200 saponinas esteroideas, localizadas principalmente nas monocotiledóneas como liliáceas, amarilidáceas e dioscoreáceas, con excepción das escrofulariáceas. Outras saponinas triterpenoides illáronse principalmente de dicotiledóneas.
Fontes[editar | editar a fonte]
As saponinas foron consideradas historicamente como compostos derivados de vexetais, pero foron tamén illados de organismos mariños animais como o cogombro de mar.[1][5] As saponinas encóntranse en moitas plantas,[1][6] e derivan o seu nome das plantas do xénero Saponaria, familia Caryophyllaceae, cuxa raíz foi utilizada historicamente como xabón.[2] As saponinas encóntranse na familia botánica Sapindaceae, co seu xénero Sapindus, e as familias estreitamente emparentadas Aceraceae (pradairos) e Hippocastanaceae. Tamén abundan en Gynostemma pentaphyllum (Gynostemma, Cucurbitaceae) en forma de gypenósidos, e no ginseng (Panax, Araliaceae) en forma de ginsenósidos. Dentro destas familias esta clas e de compostos químicos encóntranse en varias partes da planta: follas, talos, raíces, bulbos, casulos e froitos.[7] Formulacións comerciais de saponinas derivadas de plantas, por exemplo, a do xabón da codia da árbore Quillaja saponaria, e as doutras fontes prodúcense por procesos de fabricación controlados, que permiten usalos como reactivos químicos ou biomédicos.[8]
Probas[editar | editar a fonte]
- Proba da escuma
Esta proba usa como control a codia da planta Entada phaseoloides. O resultado positivo mostra unha escuma con aspecto de panal de abellas maior de 2 cm que persiste durante 10 minutos ou máis.
Debido a que as solucións de saponinas presentan actividade óptica, é común medir o contido de sólidos solubles en solución utilizando un refractómetro (tamén chamado brixómetro) tal e como se fai na industria vitivinícola. A comparación das solucións faise sempre a 1ºBx (grao brix). De ter unha concentración maior, a mostra dilúese. O método é: tomar 1 mL de cada unha das fraccións (polar e apolar) en tubos de ensaio separados, engadir 9 mL de auga a cada un. Utilizar 1 mL desta solución nun tubo de ensaio pequeno, axitar vigorosamente durante 30 segundos e deixar en repouso durante 15 minutos na mostra. A proporción de saponinas mídese de acordo coa altura da escuma sobrenadante así:
- Altura de menos de 5 mm = non se detectaron saponinas.
- Altura de 5 – 9 mm = contido baixo.
- Altura de 10 – 14 mm = contido moderado.
- Altura maior de 15 mm = contido alto.
O método máis exacto para a determinación da concentración de saponinas en solución utiliza a cromatografía líquida de alto rendemento (HPLC). Este método indica a concentración de saponinas e o perfil do extracto ou solución e permite mostrar o efecto da hidrólise polo notable cambio de perfil.
- Medio de Agar Sangue (BAM)
É un método semicuantitativo de copa de ágar que mostra os resultados positivos de halos hemolíticos en cultivos bacterianos.[9]
Papel na ecoloxía das plantas e impacto sobre os herbívoros[editar | editar a fonte]
Nas plantas as saponinas poden servir para protexerse contra os herbívoros,[2][4] e tamén contra microbios e fungos.[10][11][12] Algunhas saponinas de plantas (por exemplo as da cebada e espinaca) poden potenciar a absorción de nutrientes e axudar á dixestión animal. Porén, as saponinas adoitan ser de sabor amargo e poden reducir a comestibilidade da planta (por exemplo, na alimentación do gando), ou incluso facer que a planta teña unha toxicidade letal.[4] Algunhas saponinas son tóxicas para seres vivos de sangue frío e insectos en concentracións determinadas.[4] Cómpre unha maior investigación para definir as funcións destes produtos naturais nos organismos hóspedes, que se describiron como "mal coñecidos" polo de agora.[4]
Etnobotánica[editar | editar a fonte]
A maioría das saponinas disólvense rapidamente en auga e son velenosas para os peixes.[13] Por tanto, en etnobotánica son coñecidas principalmente polo seu uso por pobos indíxenas para conseguir alimentos acuáticos, principalmente peixes. Desde tempos prehistóricos, culturas de todo o mundo utilizaron para pescar plantas que mataban peixes, principalmente as que contiñan saponinas.[14][15]
Aínda que están prohibidas pola lei, as plantas que matan peixes son moi utilizadas polas tribos de Güiana.[16] No subcontinente Indio, as tribos Gond utilizan extractos de plantas para matar peixes.[17] Moitas tribos nativas americanas de California usaban tradicionalmente as plants do xénero Chlorogalum e as raíces de varias especies de iuca, que conteñen saponinas, como veleno para peixes. Pulverizaban as raíces, mesturándoas con auga para crear escuma e despois botaban as escumas nun regato. Isto mataba ou incapacitaba os peixes, que podían ser apañados doadamente da superficie da auga. Entre as tribos que practicaban esta técnica estaban os Lassik, os Luiseños e os Mattole.[18]
Bioactividades e terapéutica[editar | editar a fonte]
Bioactividades[editar | editar a fonte]
Un uso en investigación das saponinas implica a formación de complexos co colesterol para formar poros nas bicapas das membranas celulares, por exemplo, nas membranas dos eritrocitos, onde estes complexos causan a lise do eritrocito (hemólise) por medio dunha inxección intravenosa.[19] Ademais, a natureza anfipática das saponinas dálles actividade de surfactantes que se pode utilizar para potenciar a penetración de macromoléculas como as proteínas a través das membranas celulares.[8]
As saponinas da planta Gypsophila paniculata aumentan significativamente a citotoxicidade de inmunotoxinas e outras toxinas dirixidas contra células cancerosas humanas. Os grupos de investigación dirixidos polo profesor Hendrik Fuchs (Universidade da Charité, Berlín, Alemaña) e o Dr. David Flavell (Hospital Xeral de Southampton, Reino Unido) están a traballar conxuntamente para poder usar as saponinas de Gypsophila en combinación con inmunotoxinas ou outras toxinas dirixidas a diana en pacientes de leucemia, linfoma e outros cancros.
Adxuvante de vacinas[editar | editar a fonte]
As saponinas foron tamén utilizadas como adxuvantes en vacinas,[8] por exemplo Quil A[20] compoñente QS-21, illado da codia de Quillaja saponaria, para estimular a resposta inmune das células Th1 e a produción de linfocitos T citotóxicos contra antíxenos exóxenos. Isto fai que sexan ideais para o seu uso en vacinas de subunidades e vacinas dirixidas contra patóxenos intracelulares, así como nas vacinas contra o cancro terapéuticas, pero cos xa mencionados efectos secundarios de hemólise.[21]
No seu uso como adxuvantes na produción de vacinas, a toxicidade asociada coa complexación cun esterol segue sendo un aspecto ao que se lle presta grande atención.[22]
Usos nutricionais[editar | editar a fonte]
As saponinas están sendo promocionadas comercialmente como suplementos dietéticos e ingredientes de alimentos.[23] Hai probas da presenza de saponinas nas preparacións da medicina tradicional con regalicia,[24][25] onde se espera que a administración oral produza a hidrólise do glicósido do terpenoide (e evite calquera toxicidade asociada coa molécula intacta). Pero, como con frecuencia ocorre coas pretensións terapéuticas xerais comerciais de produtos naturais, nesta aplicación das saponinas:
- As pretensións de beneficios das saponinas para os humanos están a miúdo baseadas en estudos de bioloxía celular ou bioquímicos moi preliminares.[26] and
- Omítese xeralmente a mención da posibilidade de sensibilidade química individual, ou da toxicidade xeral de axentes específicos,[27] e da alta toxicidade de casos seleccionados.
Aínda que estas afirmacións de que son beneficiosas requiren unha constante revisión (e malia as moitas afirmacións ao respecto que se encontran na web dicindo o contrario), son poucos os usos terapéuticos humanos das saponinas aprobados polas axencias gobernamentais da UE, EUA e outros países. Os beneficios terapéuticos son o resultado da administración coidadosa das doses apropiadas.
Uso na alimentación animal[editar | editar a fonte]
As saponinas son moi utilizadas polos seus efectos sobre as emisións de amoníaco na alimentación animal.[28] O modo de acción parece ser unha inhibición do encima urease, que descompón a urea excretada nas feces en amoníaco e dióxido de carbono. Os ensaios animais mostraron que un nivel reducido de amoníaco nas trefas relizadas nas granxas causa menos danos ao tracto respiratorio dos animais, e pode axudar a facelos menos vulnerables ás enfermidades.
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 1,6 Hostettmann, K.; A. Marston (1995). Saponins. Cambridge: Cambridge University Press. p. 3ff. ISBN 0-521-32970-1. OCLC 29670810.
- ↑ 2,0 2,1 2,2 2,3 "Saponins". Universidade Cornell. 14 August 2008. Consultado o 23 February 2009.
- ↑ "Project Summary: Functional Genomics of Triterpene Saponin Biosynthesis in Medicago Truncatula". Consultado o 23 February 2009.
- ↑ 4,0 4,1 4,2 4,3 4,4 Foerster, Hartmut (22 May 2006). "MetaCyc Pathway: saponin biosynthesis I". Consultado o 23 de febreiro de 2009.
- ↑ Riguera, Ricardo (August 1997). "Isolating bioactive compounds from marine organisms". Journal of Marine Biotechnology 5 (4): 187–193.
- ↑ Liener, Irvin E (1980). Toxic constituents of plant foodstuffs. New York City: Academic Press. p. 161. ISBN 0-12-449960-0. OCLC 5447168.
- ↑ http://sun.ars-grin.gov:8080/npgspub/xsql/duke/plantdisp.xsql?taxon=691
- ↑ 8,0 8,1 8,2 "Saponin from quillaja bark". Sigma-Aldrich. Consultado o 23 de febreiro de 2009.
- ↑ Antibacterial activity of leave extracts of Nymphaea lotus (Nymphaeaceae) on Methicillin-resistant Staphylococcus aureus (MRSA) and Vancomycin resistant Staphylococcus aureus (VRSA) isolated from clinical samples. Akinjogunla OJ, Yah CS, Eghafona NO and Ogbemudia FO, Annals of Biological Research, 2010, 1 (2), pages 174-184
- ↑ Patra AK, Saxena J. The effect and mode of action of saponins on the microbial populations and fermentation in the rumen and ruminant production. Nutr Res Rev. 2009 Dec;22(2):204-19. doi: 10.1017/S0954422409990163. PMID 20003589
- ↑ Saponins versus plant fungal pathogens. Journal of Cell and Molecular Biology 5: 13-17, 2006. [1] Arquivado 19 de febreiro de 2009 en Wayback Machine.
- ↑ Rocío González-Lamothe, Gabriel Mitchell, Mariza Gattuso, Moussa S. Diarra, François Malouin, and Kamal Bouarab. Plant Antimicrobial Agents and Their Effects on Plant and Human Pathogens. Int J Mol Sci. 2009 Aug; 10(8): 3400–3419. Published online 2009 Jul 31. doi: 10.3390/ijms10083400 [2]
- ↑ "Fish-poison plants". Bulletin of Miscellaneous Information (Royal Gardens, Kew) 1930 (4): 129–153. 1930. doi:10.2307/4107559.
- ↑ Jonathan G. Cannon, Robert A. Burton, Steven G. Wood, and Noel L. Owen (2004). "Naturally Occurring Fish Poisons from Plants". J. Chem. Educ. 81 (10): 1457. Bibcode:2004JChEd..81.1457C. doi:10.1021/ed081p1457.
- ↑ C. E. Bradley. "Arrow and fish poison of the American southwest". Division of Biology, California Institute of Technology. Arquivado dende o orixinal o 15 de setembro de 2019. Consultado o 06 de outubro de 2017.
- ↑ Tinde Van Andel. "The diverse uses of fish-poison plants in Northwest Guyana". Arquivado dende o orixinal o 15 de setembro de 2019. Consultado o 06 de outubro de 2017.
- ↑ Murthy E N, Pattanaik, Chiranjibi, Reddy, C Sudhakar, Raju, V S (2010). "Piscicidal plants used by Gond tribe of Kawal wildlife sanctuary, Andhra Pradesh, India": 97–101.
- ↑ Campbell, Paul (1999). Survival skills of native California. Gibbs Smith. p. 433. ISBN 978-0-87905-921-7.
- ↑ Francis, George; Zohar Kerem; Harinder P. S. Makkar; Klaus Becker (December 2002). "The biological action of saponins in animal systems: a review". British Journal of Nutrition 88 (6): 587–605. PMID 12493081. doi:10.1079/BJN2002725.
- ↑ Effect of incorporation of the adjuvant Quil A on structure and immune stimulatory capacity of liposomes
- ↑ Sun, Hong-Xiang; Xie, Yong; Ye, Yi-Ping (2009). "Advances in saponin-based adjuvants". Vaccine 27 (12): 1787–1796. doi:10.1016/j.vaccine.2009.01.091.
- ↑ Skene, Caroline D.; Philip Sutton (September 2006). "Saponin-adjuvanted particulate vaccines for clinical use". Methods 40 (1): 53–9. PMID 16997713. doi:10.1016/j.ymeth.2006.05.019.
- ↑ "Tribulus". WebMD. Consultado o 31 de xullo de 2015.
- ↑ Asl, Marjan Nassiri; Hossein Hosseinzadeh (June 2008). "Review of pharmacological effects of Glycyrrhiza sp. and its bioactive compounds". Phytotherapy Research 22 (6): 709–24. PMID 18446848. doi:10.1002/ptr.2362.
- ↑ Xu R; Zhao W; Xu J; Shao B; Qin G (1996). "Studies on bioactive saponins from Chinese medicinal plants". Advances in Experimental Medicine and Biology. Advances in Experimental Medicine and Biology 404: 371–82. ISBN 978-1-4899-1369-2. PMID 8957308. doi:10.1007/978-1-4899-1367-8_30.
- ↑ "MetaCyc Pathway: saponin biosynthesis IV". Consultado o 23 de febreiro de 2009.
- ↑ "Saponin". J.T. Baker. Consultado o 23 February 2009.
- ↑ Zentner, Eduard (July 2011). "Effects of phytogenic feed additives containing quillaja saponaria on ammonia in fattening pigs" (PDF). Consultado o 27 November 2012.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Bibliografía[editar | editar a fonte]
- "Secondary Metabolites and Plant Defense". En: Taiz, Lincoln e Eduardo Zeiger. Plant Physiology, Fourth Edition. Sinauer Associates, Inc. 2006. Capítulo 13.
- Métodos de investigación Fitoquímica. Xorge A. Domínguez. Editorial Limusa. México 1973.
- San Martín, R. & Briones, R. 1999. Industrial Uses and Sustainable Supply Quillaja saponaria (Rosaceae) saponins.Econ. Bot., 53:302-311
- San Martín, R. & Briones, R. 2000. Quality control of commercial quillaja (Quillaja saponaria Molina) extracts by reverse phase HPLC. J. Sci. Food Agric., 80: 2063-2068.
- J.Cavanilles "Las Saponinas y la Botánica"
- "Usos de Extractos Acuosos de Quillay"
Ligazóns externas[editar | editar a fonte]
| Commons ten máis contidos multimedia sobre: Saponina |
- Medical Dictionary on Saponin
- Saponins in Wine, de ScienceDaily, acceso o 9 de setembro de 2003
- Molecular Expressions Phytochemical Gallery - Saponin
- Saponins: Suprising [sic] benefits of desert plants
- Other uses of Quillaja Saponins and derived products, some works of different authors.
- How to survive the world's worst diet
- Quillia Extracts JECFA Food Additives Series 48
