Reacción de Maillard



Co nome de reacción de Maillard (tecnicamente: glicosilación ou glicación non encimática de proteínas) desígnase un conxunto moi complexo de reaccións químicas nas que se producen melanoidinas coloreadas que van desde o amarelo claro deica o café moi escuro e mesmo o negro, ademais de diferentes compostos aromáticos. Para que as transformacións teñan lugar, son necesarios un azucre redutor (cetosa ou aldosa) e un grupo amino lbre, procedente dun aminoácido ou dunha proteína.[1] A reacción de Maillard pode acontecer durante o quentamento dos alimentos ou durante o seu almacenamento prolongado.[2] A esta reacción débese a cor castaña da codia da carne cociñada ou do pan cocido ao forno. Os produtos maioritarios destas reaccións son moléculas cíclicas e policíclicas, que achegan sabor e aroma aos alimentos, aínda que tamén poden orixinarse algúns que poden ser carcinóxenos.
No proceso da reacción xéranse centos de compostos saborosos diferentes. Estes compostos, á súa vez, degrádanse para formar máis compostos saborosos novos, e así sucesivamente. Cada tipo de alimento ten un conxunto distintivo de compostos saborosos que se forman durante a reacción de Maillard. Nestas reaccións o grupo carbonilo reactivo do azucre reacciona co grupo amino nucleofílico do aminoácido, e forma unha complexa mestura de moléculas pouco caracterizadas responsables do conxunto de olores e sabores. Este proceso é acelerado nun ambiente alcalino (por iso, por exemplo, engádese sosa cáustica para escurecer os pretzels), xa que os grupos amino (RNH3+) son desprotonados e, por tanto, incrementan o seu carácter nucleofílico. O tipo de aminoácido determina o sabor resultante. Esta reacción é a base da industria dos saborizantes. A altas temperaturas, pode formarse un potencial carcinóxeno chamado acrilamida.[3]
Historia[editar | editar a fonte]
O primeiro en describir esta reacción foi o químico francés Louis-Camille Maillard a comezos do século XX. En 1912 Maillard (1878-1936) demostrou que os pigmentos marróns e os polímeros que se orixinan durante a pirólise (degradación química producida unicamente por calor) libéranse ao producirse a reacción dun grupo amino cun grupo carbonilo, polo xeral dun azucre redutor. O mecanismo non se describiu en máis detalle ata 1953 cando o químico John E. Hodge estudou as complexas reaccións que se producen.[4] Aínda non se esclareceron todos os aspectos das reaccións de Maillard.
Condicións da reacción[editar | editar a fonte]
A reacción de Maillard é notablemente complexa. Unha sinxela ilustración disto é que a reacción da glicosa con amoníaco rende a formación de máis de quince compostos, mentres que a de glicosa con glicina dá lugar a máis de 24.[5]
Aínda que as transformacións da reacción de Maillard poden ter lugar en variadas condicións, os seguintes factores inflúen nela:[1]
- A reacción acelérase en condicións de alcalinidade e alcanza un máximo de velocidade a pH 10.
- As temperaturas elevadas tamén a aceleran, mais a súa enerxía de activación é baixa, polo que tamén se observa a baixas temperaturas, mesmo en condicións de refrixeración.
- Os alimentos de humidade intermedia son os máis propensos, porque unha actividade acuosa menor de 0,6 non permite a mobilidade dos reactantes, mentres que nunha por riba de 0,9, a auga, ao ser produto da propia reacción, exerce unha acción inhibidora.
- O tipo de aminoácido implicado é decisivo, porque os aminoácidos serán máis reactivos conforme aumente o tamaño da cadea lateral e teñan máis dun grupo amino.
- Os azucres redutores que máis favorecen a reacción de Maillard son, primeiro, as pentosas e, logo, as hexosas; e as aldosas actúan máis facilmente que as cetosas, e os monosacáridos son máis eficientes que os disacáridos.
- Finalmente, algúns metais como o cobre e o ferro teñen un efecto catalizador.
Fases da reacción[editar | editar a fonte]
Na reacción de Maillard hai catro fases sucesivas, que son as que se enumeran a continuación:
- Inicialmente non hai produción de cor. Nesta fase prodúcese a unión entre os azucres e os aminoácidos. Posteriormente ocorre unha fase intermedia entre azucres e proteínas, chamada rearranxo ou transposición de Amadori,[6] punto de partida das posteriores reaccións de dourado ou torrado.
- Hai formación inicial de cores amarelos moi lixeiros, así como a produción de cheiros algo desagradables. Nesta fase prodúcese a deshidratación de azucres formándose as redutonas ou deshidrorredutonas e tras isto sobrevén a fragmentación. No paso posterior, coñecido como degradación de Strecker, xéranse compostos redutores que facilitan a formación dos pigmentos.
- Aquí ten lugar a formación dos pigmentos escuros que se denominan melanoidinas; o mecanismo non se coñece completamente, mais é seguro que implica a polimerización de moitos dos compostos formados na segunda fase.
- Esta última fase é a degradación de Strecker. Nela fórmanse os denominados aldehidos de Strecker, que son compostos con baixo peso molecular doadamente detectables polo olfacto.
Mecanismo químico[editar | editar a fonte]
Máis en detalle, o mecanismo químico da reacción é o seguinte:
- O grupo carbonilo do azucre reacciona co grupo amino do aminoácido, producindo unha glicosilamina N-substituída e auga.
- A glicosilamina inestable sofre un rearranxo de Amadori, formándose cetosaminas.
- Hai varias maneiras nas que as cetosaminas poden reaccionar ulteriormente:
- Producen dúas moléculas de auga e redutonas.
- Poden formarse diacetil, aspirina, piruvaldehido e outros produtos de fisión hidrolíticos de cadea curta.
- Producen polímeros nitroxenados marróns e melanoidinas.
A cadea aberta do produto de Amadori sofre unha posterior deshidratación e desaminación para producir dicarbonilos.[7] Este é un intermediario crucial.
Os dicarbonilos reaccionan con aminas para producir aldehido de Strecker por medio dunha degradación de Strecker.[8]
Pode xerarse como subproduto o composto posiblemente canceríxeno acrilamida[9] por reacción de Maillard entre azucres e aminoácidos, especialmente asparaxina.[10][11]
A reacción de Maillard nos alimentos[editar | editar a fonte]
A reacción de Maillard, un dos mecanismos do "dourado non encimático" dos alimentos, xera moitas das cores, sabores e aromas existentes nos alimentos. Por exemplo, os seguintes:
- O sabor e cor da carne asada[12] (tamén coa contribución doutras reaccións, como a rotura dos aneis tetrapirrol da proteína muscular mioglobina).
- Galletas: a cor torrada do exterior das galletas xera un sabor característico.
- O caramelo elaborado con nata, manteiga e azucre, tamén chamado toffee.
- É a causante da cor marrón do pan ao ser torrado.

- A cor de alimentos como a cervexa, o café, e o xarope de pradairo.
- Produtos para as cremas bronceadoras.
- O sabor e cor das cebolas cociñadas na tixola cando se empezan a escurecer.
- A cor do doce de leite, obtido ao quentar o leite con azucre.
- Café torrado.
- A cor dourada ou torrada das patacas fritidas.
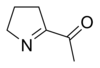
O composto 6-acetil-1,2,3,4-tetrahidropiridina (na imaxe) é o que causa o olor das galletas ou do pan, pombiñas de millo, e produtos de tortas. O composto químico 2-acetil-1-pirrolina (na imaxe) é o responsable dos sabores aromáticos nas variedades de arroz cociñado. Ambos os compostos teñen un nivel olfactivo por debaixo de 0,06 ng/L.[13]
Debe distinguirse a reacción de Maillard da caramelización. A caramelización é un proceso completamente diferente, aínda que o seu resultado sexa similar á vista e ao padal. A caramelización pode ás veces causar que algúns alimentos collan cor marrón, igual que na reacción de Maillard, pero por un proceso distinto. Ambos os procesos son promovidos polo quentamento, pero na reacción de Maillard están implicados os aminoácidos, mentres que a caramelización é simplemente a pirólise de certos azucres. Os caramelos feitos con leite e azucre si son resultado da reacción de Maillard, xa que o letie ten moitas proteínas.
Nos ensilados de herba, un exceso de calor pode producir unha reacción de Maillard, que reduce a cantidade de enerxía e proteínas que quedan dispoñibles para que os animais se alimenten do ensilado.
Efectos negativos en alimentos[editar | editar a fonte]
- Diminución do valor nutritivo e alteración das características organolépticas, ao verse implicados aminoácidos esenciais e vitaminas tales como a K e a C.
- Diminución da solubilidade e dixestibilidade das proteínas.
- Algúns produtos resultantes da reacción son potencialmente tóxicos, como as melanoidinas e pirazinas que presentan capacidade mutaxénica en certas condicións de temperatura, ao contribuíren á produción doutras substancias tóxicas canceríxenas.
- A inxestión dun produto previamente glicosilado (o cal ocorre cando os alimentos son sometidos a elevadas temperaturas ou a radiacións ionizantes nos procesos de esterilización, o que acelera a glicosilación non encimática das proteínas mediante a reacción de Maillard) fai que este se comporte como unha glicotoxina, favorecendo o desenvolvemento de diabetes mellitus tipo II.
Uso na cociña[editar | editar a fonte]
Cando se cociñan lentamente vexetais (que conteñen azucres) e se lles engade un alimento cun contido proteínico, prodúcese a reacción de Maillard. O resultado final é a xeración dunha concentración de sabores e un torrado superficial do alimento, consiguíndose efectos moi saborosos. É moi importante que a intensidade da calor emitida polo foco calorífico sexa directamente proporcional ao grosor da peza de alimento quentada, e que esta se aplique durante o tempo xusto, para non chegar a queimalo nin resecalo por exceso de cocción (isto produce efectos nocivos). Os alimentos que se fan á prancha poden ser pezas pequenas, ou cortados en cachos non moi pequenos. Ao contraio, no forno poden facerse pezas meirandes ou alimentos sen cortar en cachos.
Para acelerar a reacción pódense empregar solucións de azucres nas proteínas. Por exemplo, o pato laqueado ao estilo Pekín cóbrese durante varios días cunha capa de mel. Á inversa, os alimentos con azudres ou amidón poden rociarse cunha solución de proteínas hidrolizadas como o prebe de soia, que acelera a aparición dunha cor dourada. Como os azucres sinxelos reaccionan máis rápido, moitos prebes para grelladas conteñen algún ácido, como zume de limón ou vinagre, que rompen a sacarosa do azucre común en frutosa e glicosa.
Fisioloxía[editar | editar a fonte]
A reacción de Maillard tamén ocorre no corpo humano de forma natural. É un paso na formación de endoprodutos de glicación avanzada (EGAs; en inglés, AGEs).[14] Poden reastrearse medindo a pentosidina.
Aínda que a reacción de Maillard foi estudada máis amplamente nos alimentos, tamén presenta unha correlación con moitas doenzas humanas, especialmente as oculares dexenerativas. En xeral, estas doenzas débense á acumulación de EGAs nos ácidos nucleicos, proteínas e lípidos. Aínda que os EGAs teñen numerosas orixes, poden formarse tamén a partir da oxidación e deshidratación de adutos de Amadori, os cales son o produto de reaccións de Maillard non encimáticas. Ademais das doenzas oculares, cuxa correlación coa química de Maillard foi estudada máis recentemente, tamén se probou que a formación de EGAs pode contribuír a unha ampla variedade de doenzas humanas entre as que están as complicacións diabéticas, fibrose pulmonar, e neurodexeneración. O axente fluorodesoxiglicosa, usado para obter imaxes de tomografía de emisión de positróns, sofre unha reacción de Maillard para formar fluorodesoxiglicosilamina.
Suxeriuse que certos sistemas receptores do corpo evolucionaron para eliminar as moléculas modificadas por glicación, como os EGAs, para anular os seus efectos. Os efectos adversos da acumulación de EGAs parecen estar mediados por numerosos receptores de EGAs diferentes. Exemplos son: AGE-R1, galectina-3, CD36, e, principalmente, o RAGE (o receptor de EGAs).
A glicación avanzada en numerosas localizacións dentro dos ollos é prexudicial. Na córnea, cuxas células endoteliais expresan o RAGE e a galectina-3, a acumulación de AGEs está asociada cun estroma corneal engrosado, edema corneal, e cambios morfolóxicos nos pecientes con diabete. Dentro do cristalino, a química de Maillard foi estudada estensamente no contexto da formación de cataratas. A glicación avanzada altera a integridade da membrana fibrosa do cristalino, e os compostos dicarbonilo causan un incremento da formación de agregados no cristalino. Este efecto está exacerbado tanto na diabete coma no envellecemento. Ademais, crese que os compostos que inhiben os EGAs son efectivos na prevención da formación de cataratas nos diabéticos.
A glicación nas reaccións de Maillard pode levar á desestabilización da estrutura do xel do humor vítreo do ollo por medio dunha innecesaria formación de pontes cruzadas entre as fibrilas de coláxeno. De novo, este proceso obsérvase máis frecuentemente en pacientes diabéticos.
Na retina, a acumulación de EGAs nas drusas e na membrana de Bruch foi asociada coa idade, e foi observada con moit frecuencia en pacientes de dexeneración macular asociada coa idade. Isto maniféstase polo engrosamento da membrana de Bruch. Ademais, observouse que os niveis de EGAs increméntanse coa idade na lamina cribrosa escleral, e os produtos da reacción de Maillard observáronse tamén alí.
Moitas doenzas oculares, especialmente a retinopatía diabética, poden previrse inhibindo a reacción de Maillard. Isto pode conseguirse de diferentes modos: impedindo a formación de AGEs, reducino a efectividade da vía de sinalización de EGAs e as interaccións receptor-ligando, ou rompendo os enlaces cruzados dos EGAs. Este último método xa se conseguiu aplicar en certa medida co fármaco alagebrium, aínda que a súa efectividade contra a retinopatía é descoñecida. Outro método é o uso de amadorinas, que poden impedir formación de intermediarios da reacción de Amadori, que forman EGAs, ao buscaren os carbonilos reactivos.[15]
Referencias[editar | editar a fonte]
- ↑ 1,0 1,1 Badui Dergal, Salvador (1999). Química de los alimentos. Addison Wesley Longman: México.
- ↑ Barreiro Méndez, J.A., y Sandoval Briseño, A.J. (2006). Operaciones de conservación de alimentos por bajas temperaturas. Equinoccio: Caracas.
- ↑ Tareke, E.; Rydberg, P.; Karlsson, Patrik; Eriksson, Sune; Törnqvist, Margareta (2002). "Analysis of acrylamide, a carcinogen formed in heated foodstuffs". J. Agric. Food. Chem. 50 (17): 4998–5006. PMID 12166997. doi:10.1021/jf020302f.
- ↑ Coultate, Tom (2009). Food: The chemistry of its components (quinta ed.). Londres: RSC Publising. pp. 30-33. ISBN 978-0-85404-111-4.
- ↑ Nursten, Harry E. (2005) The Maillard Reaction: Chemistry, Biology And Implications. Royal Society of Chemistry: Londres.
- ↑ Hodge, J.E. (1955) The Amadori rearrangement. Adv. Carbohydrate Chem., 10, 169-205.
- ↑ The Maillard Reaction: Chemistry, Biochemistry, and Implications. By H. E. Nursten.
- ↑ Stadler, R. H.; Robert, F.; Riediker, S.; Varga, N.; Davidek, T.; Devaud, S.; Goldmann, T.; Hau, J.; Blank, I. In-depth mechanistic study on the formation of acrylamide and other vinylogous compounds by the Maillard reaction. Journal of Agricultural and Food Chemistry 2004, 52, 5550–5558.
- ↑ "Copia arquivada". Arquivado dende o orixinal o 20 de novembro de 2016. Consultado o 03 de decembro de 2015.
- ↑ Virk-Baker, M. K., Nagy, T. R., Barnes, S. & Groopman, J. Dietary Acrylamide and Human Cancer: A Systematic Review of Literature. Nutrition and cancer 1–17 (2014). doi:10.1080/01635581.2014.916323.
- ↑ Mottram, D. S., Wedzicha, B. L. & Dodson, A. T. Acrylamide is formed in the Maillard reaction. Nature 419, 448–9 (2002).
- ↑ McGee, Harold (2004). On Food and Cooking: The Science and Lore of the Kitchen. New York: Scribner. pp. 778–9. ISBN 978-0-684-80001-1.
- ↑ 'Harrison, Tyler J.; Dake, Gregory R. (2005). "An Expeditious, High-Yielding Construction of the Food Aroma Compounds 6-Acetyl-1,2,3,4-tetrahydropyridine and 2-Acetyl-1-pyrroline" (Abstract). J. Org. Chem. (en inglés) 70 (26): 10872 – 10874. doi:10.1021/jo051940a.
- ↑ Grandhee, S. K.; Monnier, V. M. (1991-06-25). "Mechanism of formation of the Maillard protein cross-link pentosidine. Glucose, fructose, and ascorbate as pentosidine precursors". The Journal of Biological Chemistry 266 (18): 11649–11653. ISSN 0021-9258. PMID 1904866. Consultado o 19 de maio de 2021.
- ↑ Stitt, Alan W. (2005). "The Maillard Reaction in Eye Diseases". Annals of the New York Academy of Science 1043: 582–97. PMID 16037281. doi:10.1196/annals.1338.066.



