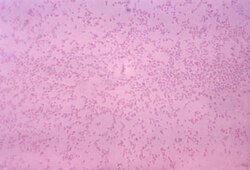
Pasteurella multocida
| Pasteurella | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||
| Clasificación científica | |||||||||||||
| |||||||||||||
| Especie | |||||||||||||
|
Pasteurella multocida | |||||||||||||
Pasteurella multocida é unha especie de bacterias gramnegativas, non móbiles, con forma de cocobacilo e sensibles á penicilina, que pertencen á familia das Pasteurellaceae.[1] As cepas desta especie son xeralmente clasificadas en 5 serogrupos nomeados A, B, D, E, F baseados na súa composición capsular e 16 serovares somáticos (do 1 ao 16). Pasteurella multocida é a causante de diversas enfermidades en mamíferos e aves entre as que está o cólera aviar, rinite atrófica dos porcos, hemorraxias en bovinos e septicemias en vacas e bisontes. Pode tamén causar infeccións zoonóticas en humanos, que son tipicamente o resultado de trabadas ou rabuñazos de animais domésticos. Moitos mamíferos e aves albergan a esta especie como parte da súa flora bacteriana normal respiratoria, incluíndo os gatos domésticos.
Historia[editar | editar a fonte]
Pasteurella multocida foi descuberta en 1878 en aves infectadas de cólera aviar. Porén, non foi illada ata 1880 por Louis Pasteur (en honor do cal o xénero se chama Pasteurella), que traballou na preparación de vacinas contra a enfermidade.[2]
Enfermidades[editar | editar a fonte]
P. multocida causa diversas doenzas en animais salvaxes e domésticos e tamén en humanos. A bacteria pode encontrarse en aves, gatos, cans, coellos, gando vacún e porcos. Nas aves, P. multocida causa o cólera aviar, que é unha importante doenza nas aves domésticas e comerciais de todo o mundo, particularmente nas aves poñedoras de ovos e nas reprodutoras. As cepas de P. multocida que poden causar cólera aviar pertencer aos serovares 1, 3 e 4. Nas aves silvestres o cólera aviar segue a ruta migratoria das aves, especialmente no caso dos gansos. A P. multocida serotipo-1 está máis asociada co cólera aviar en Norteamérica, pero a bacteria non permanece moito tempo nas zonas húmidas.[3]
P. multocida causa rinite atrófica en porcos;[4] e causa pneumonía ou enfermidade respiratoria bovina no gando vacún.[5]
Nos humanos, P. multocida é a causa máis común de infeccións orixinadas a partir de feridas causadas por trabadas de cans e gatos. A infección xeralmente aparece como unha inflamación do tecido brando 24 horas despois da trabada. Xeralmente obsérvanse recontos altos de leucocitos e neutrófilos, que dan lugar a unha reacción inflamatoria no lugar da infección (xealmente unha difusa, e localizada celulite).[6] Pode tamén infectar outras partes, como o tracto respiratorio, e sábese que causa linfoadenopatía rexional (inchamento dos ganglios linfáticos). En casos máis graves, pode aparecer unha bacteremia, causando unha osteomielite ou endocardite. A bacteria pode tamén cruzar a barreira hematoencefálica e causar meninxite.[7]
Virulencia, cultivo e metabolismo[editar | editar a fonte]
P. multocida expresa varios factores de virulencia, como unha cápsula de polisacárido e a molécula de superficie de carbohidrato variable ou lipopolisacárido (LPS). A cápsula das cepas dos serogrupos A e B axúdalles a resistir a fagocitose polas células inmunitarias do hóspede, e as cápsulas do tipo A axudan a resisitir a lise mediada polo complemento.[8][9] O lipopolisacárido producido por P. multocida consta dunha molécula de lípido A hidrofóbica (que ancora o lipopolisacárido á membrana externa), un núcleo ou core interno e un núcleo externo, que consisten ambos nunha serie de azucres ligados de modo específico. Non hai antíxeno O no lipopolisacárido e a molécula é similar ao lipopolisacárido producido por Haemophilus influenzae e ao lipooligosacárido de Neisseria meningitidis. Un estudo sobre a cepa do serovar 1 mostrou que unha molécula de lipopolisacárido de lonxitude completa era esencial para que a bacteria fose plenamente virulenta nos polos.[10]
As cepas que causan a rinite atrófica en porcos son peculiares porque teñen tamén a Toxina de Pasteurella Multocida (PMT), que reside nun bacteriófago que levan. A PMT é unha toxina que é responsable de orixinar os fociños retortos que se observan nos porcos infectados con esta bacteria. Esta toxina activa as GTPases Rho, que se unen e hidrolizan o GTP, e son importantes na formación de fibras de estrés de actina. A formación de fibras de estrés pode axudar á endocitose de P. multocida. O ciclo da célula hóspede está tamén modulado pola toxina, a cal pode actuar como un mitóxeno intracelular.[11]
P. multocida foi observada invadindo e replicándose dentro de amebas, causándolles lise.
P. multocida crece a 37 °C en ágar sangue ou ágar chocolate, pero non se pode cultivar en ágar MacConkey. O crecemento das colonias está acompañado dun característico cheiro a mofo[12][13] debido aos produtos metabólicos producidos.
É un organismo anaerobio facultativo, a proba da oxidase é positiva e tamén a da catalase, e pode tamén fermentar unha gran variedade de carbohidratos cando está en condicións anaerobias.[7] A supervivencia de P. multocida increméntase coa adición de sal no seu ambiente. A variación dos niveis de sacarosa e o pH tamén teñen efectos menores sobre a supervivencia bacteriana.[14]
Diagnose e tratamento[editar | editar a fonte]
A diagnose desta bacteria en humanos baseábase tradicionalmente en signos clínicos e cultivos e probas serolóxicas, pero os falsos negativos eran un problema debido a que P. multocida morría facilmente, e a seroloxía non podía diferenciar entre unha infeccións actual e as exposicións previas. O método máis rápido e exacto para confirmar unha infección activa por P. multocida é a detección molecular utilizando a técnica da PCR.[15]
Esta bacteria pode ser tratada efectivamente con antibióticos beta-lactámicos, que inhiben a síntese da parede celular. Tamén pode tratarse con fluoroquinolonas ou tetraciclinas; as fluoroquinolonas inhiben a síntese de ADN bacteriana e as tetraciclinas interfiren coa síntese de proteínas ao unirse á subunidade de 30S do ribosoma. Os macrólidos, que se unen ao ribosoma, malia os escasos resultados de susceptibilidade in vitro, tamén se poden aplicar no caso de complicación pulmonares. Debido á etioloxía polimicrobiana das infeccións por P. multocida, o tratamento require usar antimicrobianos que eliminen tanto a bacterias gramnegativas aeróbicas coma anaeróbicas. En consecuencia, a amoxicilina-clavulanato (unha combinación de inhibidor de beta-lactamase e unha penicilina) é o tratamento de elección.[16]
Investigacións actuais[editar | editar a fonte]
Os mutantes de P. multocida están a ser investigados pola súa capacidade de causar doenzas. A vacinación contra a rinite atrófica progresiva desenvolveuse usando un derivado recombinante da toxina de P. multocida. A vacinación foi comprobada en porcas novas preñadas que non tiveran crías. Os bacoriños destas porcas que foran inoculadas creceron sans, mentres que os de nais non vacinadas desenvolveron rinite atrófica.[17] Estanse a facer outras investigacións sobre os efectos de proteínas, pH, temperatura, NaCl e sacarosa sobre o desenvolvemento e supervivencia na auga de P. multocida. Parece que a bacteria sobrevive mellor en auga a 18 °C que a 2 °C. A adición de 0,5% de sal (NaCl) tamén aumenta a supervivencia bacteriana, mentres que os niveis de sacarosa e pH teñen efectos menores.[18] Están en marcha investigacións sobre a resposta de P. multocida ao ambiente do hóspede. Estas probas utilizan micromatrices de ADN e técnicas proteómicas. Examinouse a capacidade de mutantes de P. multocida para producir enfermidades, e os resultados indicaron que a bacteria ocupa nichos que a forzan a cambiar a súa expresión xénica para o seu metabolismo enerxético, captación de ferro, aminoácidos e outros nutrientes. Os experimentos in vitro mostraron as respostas da bacteria aos niveis baixos de ferro e diferentes fontes de ferro, como a transferrina e hemoglobina. Os xenes de P. multocida que son regulados á alza nos momentos da infección están xeralmente implicados na captación de nutrientes e no metabolismo. Isto indica que os verdadeiros xenes da virulencia só se poden expresar durante as fases iniciais da infección.[19]
Notas[editar | editar a fonte]
- ↑ Kuhnert P; Christensen H (editors). (2008). Pasteurellaceae: Biology, Genomics and Molecular Aspects. Caister Academic Press. ISBN 978-1-904455-34-9 .
- ↑ Pasteur, Louis. "The Attenuation of the Causal Agent of Fowl Cholera". Arquivado dende o orixinal o 16 de agosto de 2011. Consultado o 06 de xullo de 2013.
- ↑ Blanchlong, JA. “Persistence of pasteurella multocida in wetlands following avian cholera outbreaks.” Journal of Wildlife diseases, vol.42, no.1 (33-39)
- ↑ Eliás B, Hámori D. Data on the aetiology of swine atrophic rhinitis. V. The role of genetic factors. Acta Vet Acad Sci Hung. 1976;26(1):13–19. [PubMed]
- ↑ Irsik, M B Bovine respiratory disease associated with Mannheimia Haemolytica or pastuerella multocida. VM 163, University of Florida
- ↑ Ryan KJ; Ray CG (editors) (2004). Sherris Medical Microbiology (4th ed. ed.). McGraw Hill. ISBN 0-8385-8529-9.
- ↑ 7,0 7,1 Casolari C, Fabio U. Isolation of Pasteurella multocida from Human Clinical Specimens: First Report in Italy. European Journal of Epidemiology. Sept 1988; 4(3):389-90
- ↑ Chung JY, Wilkie I, Boyce JD, Townsend KM, Frost AJ, Ghoddusi M, Adler B: Role of capsule in the pathogenesis of fowl cholera caused by Pasteurella multocida serogroup A. Infect Immun 2001, 69(4):2487-2492.
- ↑ Boyce JD, Adler B: The capsule is a virulence determinant in the pathogenesis of Pasteurella multocida M1404 (B:2). Infect Immun 2000, 68(6):3463-3468.
- ↑ Harper M,Cox, AD, St Michael F, Wilkie IW, Boyce JD, Adler B. A heptosyltransferase mutant of Pasteurella multocida produces a truncated lipopolysaccharide structure and is attenuated in virulence. Infect. Immun. 2004; 72(6):3436-43.
- ↑ [Lacerda HM, Lax AJ, Rozenqurt E. Pasteurella multocida toxin, a potent intracellularly acting mitogen, induces p125FAK and paxillin tyrosine phosphorylation, actin stress fiber formation, and focal contact assembly in Swiss 3T3 cells. J Biol Chem. 5 Jan 1996; 271(1):439-45.
- ↑ P. multocida - "musty" odor
- ↑ Carol Jo T. FajfarR-Whetsone, Lisa Coleman, Diana R. Biggs, and Barry C. Fox. Pasteurella multocida Septicemia and Subsequent Pasteurella dagmatis Septicemia in a Diabetic Patient. Journal of Clinical Microbiology, Jan. 1995, p. 202–204 Vol. 33, No. 1. Cita: "After 24 h of incubation in 5% CO2, small, gray, translucent, nonhemolytic colonies which had a musty odor were observed on the plates" [1] Arquivado 21 de setembro de 2015 en Wayback Machine.
- ↑ Bredy, JP. “The effects of six environmental variables on Pasteurella multocida populations in water.” Journal of Wildlife Diseases, vol. 25, no. 2 (232-239) [2]
- ↑ Miflin, J.K. and Balckall, P.J. (2001) Development of a 23 SrRNA-based PCR assay for the identification of Pasteurella multocida. Lett. Appl. Microbiol. 33: 216-221
- ↑ Red Book: 2006 Report of the Committee on Infectious Diseases - 27th Ed.
- ↑ Nielsen JP Vaccination against progressive atrophic rhinitis with a recombinant “Pasteurella multocida” toxin derivative. Canadian Journal of Veterinary Research, vol.55, no.2 (128-138)
- ↑ Bredy, JP. The effects of six environmental variables on P. multocida populations in water. “Journal of Wildlife Diseases”, vol. 25, no.2 (232-239)
- ↑ Boyce, JD. How does P. multocida respond to the host environment? “Current Opinion in Microbiology” vol.9 no.1 (117-122)
