Piruvato carboxilase
| Piruvato carboxilase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
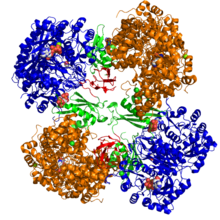
| Estrutura cristalográfica da piruvato carboxilase de Rhizobium etli: dominio biotina carboxilase (azul); dominio de unión alostérica (verde); dominio de unión á biotina (vermello); e dominio carboxil transferase (laranxa)[1] | |||||||||
| Identificadores | |||||||||
| Número EC | 6.4.1.1 | ||||||||
| Número CAS | 9014-19-1 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| Gene Ontology | AmiGO / EGO | ||||||||
| |||||||||
| Piruvato carboxilase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | PYR_CT | ||||||||
| Pfam | PF00682 | ||||||||
| InterPro | IPR000891 | ||||||||
| PROSITE | PDOC50991 | ||||||||
| |||||||||
Piruvato carboxilase
| |
| Identificadores | |
| Símbolo | PC |
| Entrez | 5091 |
| HUGO | 8636 |
| OMIM | |
| RefSeq | NM_000920 |
| UniProt | P11498 |
| Outros datos | |
| Número EC | 6.4.1.1 |
| Locus | Cr. 11 q11-q13.1 |
A piruvato carboxilase (PC) é un encima da clase das ligases que cataliza a carboxilación (irreversible dependendo da especie) do piruvato para formar oxalacetato (OAA) consumindo a enerxía do ATP.
 |
HCO3− ATP ADP + Pi Piruvato carboxilase |

|
| Piruvato | Oxalacetato |
É un importante encima de reaccións anapleróticas que orixinan oxalacetato a partir de piruvato. O encima é unha proteína mitocondrial que contén un grupo prostético biotina,[1] require magnesio ou manganeso e o regulador acetil-CoA.
Este encima descubrírono en 1959 na Western Reserve University M. F. Utter e D. B. Keech.[2][3] Desde entón foi atopado nunha ampla variedade de procariotas e eucariotas incluíndo fungos, bacterias, plantas e animais.[4] Nos mamíferos, a piruvato carboxilase xoga un papel fundamental na gliconeoxénese e lipoxénese, na biosíntese de neurotransmisores, e na secreción de insulina inducida pola glicosa polos illotes pancreáticos. O oxalacetato producido pola PC é un importante intermediato, que se usa nesas vías biosintéticas.[5] Nos mamíferos a PC exprésase dun modo específico de tecido, e a súa actividade é máxima no fígado e riles (tecidos gliconeoxénicos), no tecido adiposo, glándulas mamarias lactantes, e nos illotes de Langerhans do páncreas. A súa actividade é moderada no cerebro, corazón e glándulas adrenais, e mínima nos glóbulos vermellos e fibroblastos do tecido cutáneo.[6]
Estrutura
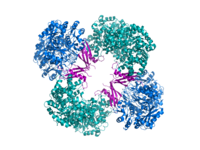
[editar | editar a fonte]Os estudos estruturais da PC realizáronse por microscopía electrónica, por proteólise limitada, e por clonación e secuenciación de xenes e ADNc que codificaba o encima. A maioría das formas ben caracterizadas da PC activa constan de catro subunidades idénticas dispostas formando unha estrutura tetraédrica. Cada subunidade contén un só resto de biotina, que actúa como un brazo móbil que transporta dióxido de carbono ao sitio catalítico que se encontra na interface entre os monómeros adxacentes. Cada subunidade do tetrámero funcional contén catro dominios: o dominio de carboxilación da biotina (BC), o dominio de transcarboxilación (CT), o dominio transportador de biotina carboxilo (BCCP) e o recentemente denominado dominio de tetramerización da PC (PT).[7][8] A partir das dúas estruturas cristalinas máis completas dispooñibles, detectáronse dúas formas da proteína, chamadas asimétrica e simétrica.[9] O tetrámero de Staphylococcus aureus en complexo co seu activador o coencima A é moi simétrico, cunha simetría 222, e foi confirmada por estudos crioelectromicroscópicos.[8] Polo contrario, o encima de Rhizobium etli, tetrámero en complexo co etil-CoA, un análogo non hidrolizable do acetil-CoA, posúe só unha liña de simetría.[9]
A piruvato carboxilase utiliza un cofactor biotina unido covalentemente, que se usa para catalizar a carboxilación dependente de ATP do piruvato a oxalacetato en dous pasos. A biotina carboxílase inicialmente no sitio activo do dominio BC polo ATP e o bicarbonato. O grupo carboxilo é despois transferido pola carboxibiotina a un segundo centro activo no dominio CT, onde o piruvato é carboxilado para xerar oxalacetato. O dominio BCCP transfire o cofactor ligado entre os dous remotos sitios activos. O sitio de unión alostérico na PC é unha diana para modificadores da súa actividade que poden ser útiles no tratamento da obesidade ou diabetes de tipo 2, e as ideas sobre o mecanismo de acción obtidas da descrición estrutural completa do RePC (de R. etli) permiten investigacións detalladas en cada un dos sitios catalíticos e reguladores do encima.[9]
Mecanismo de reacción
[editar | editar a fonte]
(A) carboxilación da biotina dependente de ATP (dominio BC);
(B) Transcarboxilación do piruvato (dominio CT).
O mecanismo de reacción pode subdividirse en dúas reaccións parciais (ver figura da dereita). Na primeira reacción, carboxílase o ATP producindo un anhídrido fosfórico carbónico [–O(–O)P(=O)O–C(=O)O–], que á súa vez carboxila o cofactor biotina que está unido covalentemente a un residuo de lisina do dominio BCCP.[4] O anihídrido fosfórico carbónico decomponse en dióxido de carbono e fosfato antes do ataque pola molécula de biotina unida ao encima. Na maioría das especies, esta reacción require acetil-CoA como activador alostérico que se une ao dominio PT.[8] Na segunda reacción, que ocorre no dominio CT dun monómero adxacente, o dióxido de carbono transfírese á molécula aceptora, piruvato, para formar oxalacetato. A reacción procede por medio da retirada dun protón do piruvato, por un residuo do sitio activo aínda non identificado, para xerar un intermediario enolato. O enolato ataca despois o CO2 que foi liberado transitoriamente pola molécula de biotina unida ao encima. Libérase entón o oxalacetato resultante. A molécula de biotina é protonada polo residuo do sitio activo antes mencionado e liberada do sitio activo do dominio CT para ser recarboxilada.[8][9] O principal regulador da actividade encimática, o acetil-CoA, estimula a clivaxe do ATP na primeira reacción parcial e tamén induce un cambio conformacional na estrutura tetramérica do encima.[5]
Papel na gliconeoxénese
[editar | editar a fonte]Durante a gliconeoxénese, a piruvato carboxilase está implicada na ruta de síntese de fosfoenolpiruvato (PEP) a partir de piruvato. O piruvato convértese primeiro en oxalacetato pola acción da piruvato carboxilase nas mitocondrias, o que require a hidrólise dunha molécula de ATP. o oxalacetato é despois descarboxilado e simultaneamente fosforilado, o cal é catalizado por unha das dúas isoformas da fosfoenolpiruvato carboxiquinase (PEPCK) tanto no citosol coma na mitocondria para producir fosfoenolpiruvato. En condicións normais gliconeoxénicas, o oxalacetato é convertido en fosfoenolpiruvato pola PEPCK mitocondrial; o fosfoenolpiruvato resultante é despois transportado fóra da matriz mitocondrial por un sistema transportador de anións,[10] e convertido en glicosa por encimas gliconeoxénicos citosólicos. Porén, durante unha situación de fame cando a concentración de NADH citosólico é baixa e a de NADH mitocondrial alta, o oxalacetato pode usarse como unha lanzadeira de equivalentes de redución. O oxalacetato é convertido en malato pola malato deshidroxenase mitocondrial (MDH). Despois de ser exportado ao citosol, o malato convértese de novo en oxalacetato, coa redución simultánea de NAD+; o oxalacetato é despois convertido a fosfoenolpiruvato, o cal queda dispoñible para a gliconeoxénese no citosol xunto cos equivalentes de redución NADH transportados.[1]
Niveis moi altos de actividade da piruvato carboxilase, xunto cunha actividade alta doutros encimas gliconeoxénicos, como a PEPCK, frutosa-1,6-bisfosfatase e glicosa-6-fosfatase no fígado e córtex renal, suxiren que un dos papeis principais da piruvato carboxilase é participar na gliconeoxénese neses órganos. Durante o xexún ou unha situación de fame cando se require glicosa endóxena para certos tecidos (cerebro, leucocitos e medula renal), a expresión da pirivato carboxilase e doutros encimas gliconeoxénicos é elevada.[11] Nas ratas e ratos, a alteración do status de nutrición afecta a actividade da piruvato carboxilase hepática.[12] O xexún promove a produción de glicosa hepática mantida por un incremento do fluxo de piruvato, e un incremento da actividade da piruvato carboxilase e a concentración de proteínas; a diabetes fai aumentar de xeito similar a gliconeoxénese por medio do aumento da captación de substrato e un fluxo incrementado pola pirivato carboxilase hepática en ratos e ratas.[13][14] Igual que outros encimas gliconeoxénicos, a piruvato carboxilase está regulada positivamente polo glicagón e os glicocorticoides, e regulada negativamente pola insulina.[4] Outro dato que apoia o papel chave da piruvato carboxilase na gliconeoxénese, en vacas leiteiras, que teñen capacidade de absorción de hexosas a niveis nutricionais adecuados, é que os niveis de piruvato carboxilase e do encima gliconeoxénico asociado PEPCK están marcadamente elevados durante a transición á lactación no proposto apoio da síntese de lactosa para a produción de leite.[15]
Ademais do papel da piruvato carboxilase na gliconeoxénese, este encima ten tamén un papel nas reaccións anapleróticas, unhas reaccións catalizadas encimaticamente que repoñen as reservas de intermediatos do ciclo do ácido cítrico cando estes intermediatos son gastados en diferentes vías biosintéticas. O ciclo do ácido cítrico é esencial para proporcionar oxalacetato.
Importancia clínica
[editar | editar a fonte]Como este encima é un cruzamento de camiños entre o metabolismo de carbohidratos e o de lípidos, a expresión de piruvato carboxilase en tecidos gliconeoxénicos, tecido adiposo e illotes pancreáticos debe estar coordinada. En condicións de sobrenutrición, os niveis de piruvato carboxilase increméntanse nas células β pancreáticas para aumentar o ciclo do piruvato en resposta a niveis elevados crónicos de glicosa.[16] Polo contrario, os niveis do encima piruvato carboxilase no fígado decrecen polo efecto da insulina;[17] durante os períodos de sobrenutrición aumenta a cantidade de tecido adiposo cunha expresión extrema de piruvato carboxilase e outros encimas lipoxénicos.[6][18] O control hepático dos niveis de glicosa aínda segue regulado nunha situación de sobrenutrición, pero na diabetes tipo 2 inducida pola obesidade a regulación dos niveis periféricos de glicosa xa non está baixo a regulación da insulina. En ratas con diabetes mellitus tipo 2, a exposición crónica das células β á glicosa debido á resistencia periférica á insulina dá lugar a unha diminución da actividade do encima piruvato carboxilase e a un decrecemento do ciclo do piruvato.[19][20] A sobreprodución continuada de glicosa polos hepoatocitos causa unha drástica alteración da expresión xénica nas células β cun grande incremento da mesma en xenes normalmente suprimidos, e un decrecemento equivalente na expresión do ARNm da insulina, das bombas iónicas necesarias para a secreción de insulina, e dos encimas metabólicos relacionados coa secreción de insulina, incluíndo a piruvato carboxilase.[21][22] Ao mesmo tempo, o tecido adiposo desenvolve resistencia á insulina causando acumulación de triacilglicerois e ácidos graxos non esterificados circulantes; isto non só afecta á función das células β,[22][23] senón que tamén fai decrecer a expresión da piruvato carboxilase.[24][25] Estes cambios orixinan o declive do fenotipo de célula β na diabetes descompensada.
Unha deficiencia de piruvato carboxilase pode causar acidose láctica como resultado da acumulación de lactato.[26] Normalmente, o exceso de piruvato é desviado á gliconeoxénese por medio da conversión do piruvato en oxalacetato, pero debido á deficiencia do encima, o exceso de piruvato convértese nesa situación en lactato. Como un dos papeis fundamentais da gliconeoxénese é manter os niveis de azucre sanguíneo, a deficiencia de piruvato carboxilase pode tamén producir hipoglicemia.
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 1,2 PDB 2QF7; Jitrapakdee S, St Maurice M, Rayment I, Cleland WW, Wallace JC, Attwood PV (2008). "Structure, mechanism and regulation of pyruvate carboxylase". Biochem. J. 413 (3): 369–87. PMC 2859305. PMID 18613815. doi:10.1042/BJ20080709.
- ↑ Utter MF, Keech DB (1960). "Formation of oxaloacetate from pyruvate and carbon dioxide". J. Biol. Chem. 235: PC17–8. PMID 13840551.
- ↑ Cohen ND, Beegen H, Utter MF, Wrigley NG (1979). "A re-examination of the electron microscopic appearance of pyruvate carboxylase from chicken liver". J. Biol. Chem. 254 (5): 1740–7. PMID 762171. Arquivado dende o orixinal o 13 de setembro de 2019. Consultado o 07 de xaneiro de 2014.
- ↑ 4,0 4,1 4,2 Jitrapakdee S, Vidal-Puig A, Wallace JC (2006). "Anaplerotic roles of pyruvate carboxylase in mammalian tissues". Cell. Mol. Life Sci. 63 (7-8): 843–54. PMID 16505973. doi:10.1007/s00018-005-5410-y.
- ↑ 5,0 5,1 Jitrapakdee S, Nezic MG, Cassady AI, Khew-Goodall Y, Wallace JC (a 2002). "Molecular cloning and domain structure of chicken pyruvate carboxylase". Biochem. Biophys. Res. Commun. 295 (2): 387–93. PMID 12150961. doi:10.1016/S0006-291X(02)00651-4.
- ↑ 6,0 6,1 Jitrapakdee S, Walker ME, Wallace JC (1996). "Identification of novel alternatively spliced pyruvate carboxylase mRNAs with divergent 5'-untranslated regions which are expressed in a tissue-specific manner". Biochem. Biophys. Res. Commun. 223 (3): 695–700. PMID 8687459. doi:10.1006/bbrc.1996.0958.
- ↑ Kondo S, Nakajima Y, Sugio S, Yong-Biao J, Sueda S, Kondo H (2004). "Structure of the biotin carboxylase subunit of pyruvate carboxylase from Aquifex aeolicus at 2.2 A resolution". Acta Crystallogr. D Biol. Crystallogr. 60 (Pt 3): 486–92. PMID 14993673. doi:10.1107/S0907444904000423.
- ↑ 8,0 8,1 8,2 8,3 Yu LP, Xiang S, Lasso G, Gil D, Valle M, Tong L (2009). "A symmetrical tetramer for S. aureus pyruvate carboxylase in complex with coenzyme A". Structure 17 (6): 823–32. PMC 2731552. PMID 19523900. doi:10.1016/j.str.2009.04.008.
- ↑ 9,0 9,1 9,2 9,3 St Maurice M, Reinhardt L, Surinya KH, Attwood PV, Wallace JC, Cleland WW, Rayment I (2007). "Domain architecture of pyruvate carboxylase, a biotin-dependent multifunctional enzyme". Science 317 (5841): 1076–9. PMID 17717183. doi:10.1126/science.1144504.
- ↑ Stark R, Pasquel F, Turcu A; et al. (2009). "Phosphoenolpyruvate cycling via mitochondrial phosphoenolpyruvate carboxykinase links anaplerosis and mitochondrial GTP with insulin secretion.". Journal of Biological Chemistry 284 (39): 26578–26590. PMC 2785346. PMID 19635791. doi:10.1074/jbc.M109.011775.
- ↑ Rothman DL, Magnusson I, Katz LD, Shulman RG, Shulman GI (1991). "Quantitation of hepatic glycogenolysis and gluconeogenesis in fasting humans with 13C NMR". Science 254 (5031): 573–6. PMID 1948033. doi:10.1126/science.1948033.
- ↑ Bizeau ME, Short C, Thresher JS, Commerford SR, Willis WT, Pagliassotti MJ (2001). "Increased pyruvate flux capacities account for diet induced increase in gluconeogenesis in vitro". Am. J. Physiol. Regul. Integr. Comp. Physiol. 281 (2): R427–R433. PMID 11448844.
- ↑ Salto R, Sola M, Olicer F J, Vargas A M (1996). "Effects of starvation, diabetes, and carbon tetrachloride intoxication on rat kidney cortex and liver pyruvate carboxylase levels". Arch. Physiol. Biochem. 104 (7): 845–850. PMID 9127680. doi:10.1076/apab.104.7.845.13111.
- ↑ Large V, Beylot M (1999). "Modifications of citric acid cycle activity and gluconeogenesis in strepozotocin induced diabetes and effects of metformin". Diabetes 48 (6): 1251–1257. PMID 10342812. doi:10.2337/diabetes.48.6.1251.
- ↑ Greenfield RB, Cecava MJ, Donkin SS (2002). "Changes in mRNA expression for gluconeogenic enzymes in the liver of dairy cattle during transition to lactation". Journal of Dairy Science 82 (6): 1228–1236. PMID 10877388. doi:10.3168/jds.S0022-0302(00)74989-7.
- ↑ Liu YQ, Han J, Epstein PN, Long YS (2005). "Enhanced rat β-cell proliferation in 60% pancreatectomized islets by increased glucose metabolic flux through pyruvate carboxylase pathway". Am. J. Physiol. Endocrinol. Metab 288 (3): E471–E478. PMID 15507531. doi:10.1152/ajpendo.00427.2004.
- ↑ Desvergne B, Michalik L, Wahli W (2006). "Transcriptional regulation of metabolism". Physiol. Rev 86 (2): 465–514. PMID 16601267. doi:10.1152/physrev.00025.2005.
- ↑ Lynch CJ, McCall KM, Billingsley ML, Bohlen LM, Hreniuk SP, Martin LF, Witters LA, Vannucci SJ (1992). "Pyruvate carboxylase in genetic obesity". Am. J. Physiol 262 (5 Pt 1): E608–E618. PMID 1375435.
- ↑ MacDonald MJ, Tang J, Polonsky KS (1996). "Low mitochondrial glycerol phosphate dehydrogenase and pyruvate carboxylase in pancreatic islets of Zucker diabetic fatty rats". Diabetes 45 (11): 1626–1630. PMID 8866570. doi:10.2337/diabetes.45.11.1626.
- ↑ McDonald MJ, Efendic S, Ostenson CG (1996). "Normalization by insulin of low mitochondrial glycerol phosphate dehydrogenase and pyruvate carboxylase in pancreatic islets of the GK rat". Diabetes 45 (7): 886–890. PMID 8666138. doi:10.2337/diabetes.45.7.886.
- ↑ Laybutt DR, Glandt M, Xu G, Ahn YB, Trivedi N, Bonner-Weir S, Weir GC (2003). "Critical reduction in β-cell mass results in two distinct outcomes over time. Adaption with impaired glucose tolerance or decompensated diabetes". J. Biol. Chem. 278 (5): 2997–3005. PMID 12438314. doi:10.1074/jbc.M210581200.
- ↑ 22,0 22,1 Poitout V, Robertson R P (2002). "Secondary ß-cell failure in type 2 diabetes-a convergence of glucotoxicity and lipotoxicity". Endocrinology 143 (2): 339–342. PMID 11796484. doi:10.1210/en.143.2.339.
- ↑ Boucher A, Lu D, Burgess SC, Telamaque-Potts S, Jensen M V, Mulder H, Wang M Y, Unger R H, Sherry A D, Newgard C B (2004). "Biochemical mechanism of lipid-induced impairment of glucose-stimulated insulin secretion and reversal with a malate analogue". J. Biol. Chem. 279 (26): 27263–27271. PMID 15073188. doi:10.1074/jbc.M401167200.
- ↑ Busch AK, Cordery D, Denyer GS, Biden TJ (2002). "Expression profiling of palmitate- and oleate-regulated genes provides novel insights into the effects of chronic exposure on pancreatic β-cell function". Diabetes 51 (4): 977–987. PMID 11916915. doi:10.2337/diabetes.51.4.977.
- ↑ Iizuka K, Nakajima H, Namba M, Miyagawa J, Mijazaki J, Hanafusa T, Matsuzawa Y (2002). "Metabolic consequences of long-term exposure of pancreatic β-cells to free fatty acid with special reference to glucose insensitivity". Biochim. Biophys. Acta 1586 (1): 23–31. PMID 11781146.
- ↑ García-Cazorla A, Rabier D, Touati G, Chadefaux-Vekemans B, Marsac C, de Lonlay P, Saudubray JM (2006). "Pyruvate carboxylase deficiency: metabolic characteristics and new neurological aspects". Ann. Neurol. 59 (1): 121–7. PMID 16278852. doi:10.1002/ana.20709.