Periodontite
| Enfermidade periodontal | |
|---|---|
| Clasificación e recursos externos | |
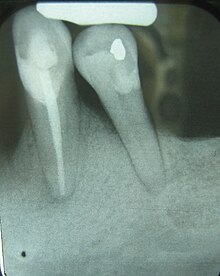
 Esta radiografía mostra unha significativa perda de óso entre as dúas raíces dun dente (rexión negra). O óso esponxoso retrocedeu debido a infeccións baixo o dente, reducindo o sostén óseo do dente. | |
| ICD-10 | K05.4 |
| DiseasesDB | 29362 |
| MedlinePlus | 001059 |
Se cre que pode requirir tratamento, por favor, consúltello ao médico. | |
A periodontite ou piorrea é o nome que se dá a un conxunto de enfermidades inflamatorias que afectan ao periodontio, é dicir, ao tecido que rodea e sostén os dentes. A periodontite implica a perda progresiva de óso alveolar arredor do dente, e se non se trata, pode orixinar o afrouxamento e finalmente a perda de pezas dentais. A periodontite está causada por microorganismos que se adhiren e crecen sobre a superficie dos dentes, xunto cunha resposta inmunitaria moi agresiva contra eles. A diagnose da periodontite realízase inspeccionando os tecidos brandos das enxivas que rodean os dentes por medio dunha sonda periodontal (exame clínico) e avaliando as radiografías do paciente (exame radiográfico), para determinar a cantidade de perda de óso arredor dos dentes.[1]
Etimoloxía
[editar | editar a fonte]A palabra periodontite procede do grego peri, "arredor de", e odous/odontos, "dente", e a terminación médica ite, que indica inflamación. A palabra piorrea tamén procede do grego pyon, "descarga dunha chaga", e rhoē, "fluír". Piorrea pode usarse en xeral para calquera descarga de pus, e non só nesta enfermidade dental. O termo piorrea caeu en desuso en favor de periodontite.[2][3]
Clasificación
[editar | editar a fonte]A periodontite é un tipo de enfermidade periodontal, das cales hai varias clasificacións. O sistema de clasificación de 1999 para as enfermidades e condicións periodontais considera sete categorías de enfermidades periodontais,[4] das cales da 2 á 6 considéranse destrutivas porque o dano é esencialmente irreversible. Estas sete categorías son:
- Xenxivite
- Periodontite crónica
- Periodontite agresiva
- Periodontite como manifestación dunha enfermidade sistémica
- Xenxivite/periodontite ulcerativa necrotizante
- Abscesos do periodontio
- Lesións periodónticas-endodónticas combinadas.
Ademais, engádese aos termos anteriores terminoloxía sobre a extensión e gravidade da enfermidade periodontal para indicar a diagnose específica dun determinado paciente ou grupo de pacientes.
Extensión
[editar | editar a fonte]A "extensión" da doenza refírese á proporción da dentición afectada pola enfermidade en termos de porcentaxe dos sitios afectados. Os sitios defínense como as posicións nas cales se fixeron medicións con sondas arredor de cada dente e, xeralmente, mídense seis sitios de sondaxe arredor de cada dente, e son os seguintes:
- mesiobucal
- mediobucal
- distobucal
- mesiolingual
- mediolingual
- distolingual.
Se están afectados o 30% dos sitios da boca, a manifestación clasifícase como "localizada"; cando son máis do 30%, denomínase "xeneralizada".
Gravidade
[editar | editar a fonte]A "gravidade" da doenza refírese á cantidade de fibras do ligamento periodontal que se perderon, o que se denomina "perda de inserción clínica". Un modo de clasificala é a seguinte:[5]
- Leve: 1–2 mm de adhesión/suxeición perdidos
- Moderada: 3–4 mm de adhesión perdidos
- Grave: ≥ 5 mm de adhesión perdidos.
Signos e síntomas
[editar | editar a fonte]
Nas etapas iniciais, a periodontite ten moi poucos síntomas; e en moitos individuos a enfermidade avanzou bastante antes de que empezasen a buscar un tratamento.
Entre os síntomas están:
- Enxivas avermelladas ou sangrantes durante o cepillado dos dentes, o uso de fío dental ou ao morder en comidas duras (por exemplo, mazás). Pero isto pode ocorrer tamén na xenxivite, na cal non hai perda de adhesión dental.
- Inchamento das enxivas recorrente.
- Cuspir sangue despois de cepillarse os dentes.
- Halitose, ou mal alento, e un sabor metálico persistente na boca.
- Recesión xenxival, o que dá lugar a un aparente alongamento dos dentes. Isto pode tamén ser causado por un cepillado demasiado enérxico ou con cepillos de sedas moi ríxidas.
- Bolsas profundas entre os dentes e as enxivas (estas bolsas son sitios nos que a adhesión foi gradualmente destruída por encimas que destrúen o coláxeno, chamadas colaxenases.
- Perda de pezas dentais, nas fases avanzadas (os dentes poden perderse por outras razóns tamén).
A inflamación xenxival e a perda de óso son en grande medida indoloros. Por tanto, ás veces a xente pode pensar que un sangrado indoloro cando lava os dentes non é significativo, cando podería ser un síntoma da progresión da periodontite.
Efectos fóra da boca
[editar | editar a fonte]A periodontite foi asociada cun incremento da inflamación no corpo, como indican os altos niveis de proteína C reactiva e interleucina 6.[6][7][8][9] Esta asociado por intermediación disto dun incremento do risco de accidente cerebrovascular,[10][11] infarto de miocardio,[12] e aterosclerose.[13][14][15][16][17][18][19] Tamén está asociado en persoas de máis de 60 anos con trastornos na memoria e habilidades de cálculo.[20][21] As persoas con niveis de glicosa en xaxún alterados e diabetes mellitus teñen maiores graos de inflamación periodontal, e a miúdo teñen dificultades para equilibrar o seu nivel de glicosa sanguíneo debido ao constante estado de inflamación sistémica causado pola inflamación periodontal.[22][23] Aínda que polo momento non hai unha conexión causal probada, un estudo recente indicou unha asociación epidemiolóxica entre a periodontite crónica e a disfunción eréctil.[24] Algúns estudos asociaron a enfermidade periodontal e a perda de dentes cun incremento do risco en pacientes masculinos de ter cancro.[25]
Causas
[editar | editar a fonte]A periodontite é unha inflamación do periodontio, é dicir, os tecidos que sosteñen os dentes. O periodontio está formado por catro tecidos:
- enxiva,
- cemento, ou capa máis externa da raíz dos dentes,
- óso alveolar, que forma os ocos no óso onde os dentes están inseridos, e
- ligamentos periodontais, que son as fibras de tecido conectivo que corren entre o cemento e o óso alveolar.
A etioloxía (causa) principal da xenxivite é unha hixiene oral mala ou ineficiente, o que leva a unha acumulación dunha matriz micótica[26][27][28][29] e bacteriana na liña da enxiva, chamada placa dental. Outras posibles causas son unha mala nutrición e problemas médicos subxacentes como a diabetes.[30] Os diabéticos deben ser meticulosos co coidado diario dos seus dentes para controlar unha posible enfermidade periodontal.[31]
Nalgunhas persoas a xenxivite progresa ata orixinar periodontite, con destrución das fibras xenxivais, separación dos tecidos xenxivais dos dentes e un suco profundizado, chamado bolsa periodontal. Os microorganismos subxenxivais (que viven por debaixo da liña das enxivas) colonizan as bolsas periodontais e causan máis inflamación nos tecidos da enxiva e a perda progresiva de óso. Exemplos de etioloxía secundaria son todas as que causan unha acumulación de placa, como partes sobresaíntes de restauracións dentais (empastes) e proximidade das raíces.

Fumar é outro factor que incrementa a aparición de periodontite, de forma directa ou indirecta,[32][33][34] e pode interferir ou afectar adversamente ao seu tratamento.[35][36][37]
A síndrome de Ehlers–Danlos é un factor de risco de periodontite e tamén a síndrome de Papillon-Lefèvre, tamén chamada queratoderma palmoplantar.
Se se deixa acumular, a placa microbiana calcifícase formando cálculos dentais, que se coñecen como sarrio ou tártaro. Os cálculos situados sobre ou debaixo da liña das enxivas deben ser retirados completamente polo hixienista dental ou dentista para tratar a xenxivite e a periodontite. Aínda que a causa principal tanto da xenxivite coma da periodontite é a placa microbiana que se adhire á superficie dos dentes, hai moitos outros factores modificadores. Un factor de risco moi forte é a susceptibilidade xenética de cada suxeito. Varias condicións e enfermidades, como a síndrome de Down, diabetes, e outras enfermidades que afectan a resistencia dunha persoa á infección, tamén incrementan a susceptibilidade á periodontite.
Outro factor que fai que a periodontite sexa unha enfermidade difícil de estudar é que a resposta do hóspede humano pode tamén afectar á reabsorción do óso alveolar. Aínda que a resposta do hóspede a ataques bacteriano-micóticos está principalmente determinada pola súa xenética, o desenvolvemento da resposta inmunitaria pode xogar tamén algún papel na susceptibilidade.
Segundo algúns investigadores a periodontite pode asociarse con altos niveis de estrés.[38]
Microscopia de biofilmes
[editar | editar a fonte]
Unha hipótese presentada xa ao inicio do século XX a partir de exames microscópicos dos biofilmes que se forman na boca, propón a existencia dunha correlación fundamental entre a presenza de amebas da especie Entamoeba gingivalis e a enfermidade periodontal activa, daquela chamada piorrea.[39] Esta noción foi recalcada medio século máis tarde e corroborada demostrando que un biofilme xenxival saudable consta principalmente de bacterias non móbiles, pero o da xenxivite presenta principalmente bacterias móbiles (bacilos, espirilos, vibrios), acompañados dun número significativo de leucocitos polimorfonucleares (PMN) e finalmente, que a periodontite progresa desde unha condición bacteriana similar pero co engadido da presenza do protozoo Entamoeba gingivalis, e menos frecuentemente de Trichomonas tenax e números moi significativos de granulocitos.[40] Esta teoría foi aplicada na década de 1980 por un odontólogo canadense e segundo os seus informes conseguíase a curación periodontal ao restablecer, por medio de hixiene, fármacos e monitorización por microscopio de contraste de fase, un biofilme comensal constituído por bacterias de varias formas cocoides, filamentos inmóbiles e ausencia de leucocitos.[41][42][43][44] Esta correlación microscópica foi practicamente confirmada recentemente por análises de bioloxía molecular de PCR que relacionaron a presenza deste protozoo nos casos de enfermidade periodontal activa e a súa ausencia durante a saúde xenxival, mesmo en zonas localizadas da boca.[45] Esta técnica de control antiparasitario propúxose como unha forma efectiva de superar a periodontite.[46] Os danos causados no tecido xenxival están baseados principalmente na fagocitose do núcleo dos leucocitos neutrófilos polimorfonucleares realizada pola ameba e a liberación pola célula resultante enucleada dos encimas proteolíticos que contén nos tecidos que o rodean, como se propón para os abscesos amébicos hepáticos de Entamoeba histolytica na disentería amebiana. A terapia enfocada a eliminar estas amebas ten a vantaxe de eliminar as bacterias patóxenas ao mesmo tempo que os protozoos, e é doada de visualizar ao microscopio. Este proceso de fagocitose agora chamado exonucleofaxia explicaría a deterioración local do sistema inmunitario nas bolsas periodontais profundas e tamén se produce en infeccións peri-implantite. A presenza sistemática de protozoos e as células fantasma sen núcleo alterarían aos PMN impedíndolles realizar a súa actividade de defensa de trampa extracelular de neutrófilos. Os primeiros datos sobre esta terapia antiparasitaria parecen efectivos para curar os sucos periodontais.[47]
Prevención
[editar | editar a fonte]A hixiene oral diaria prevén as enfermidades periodontais, e inclúe:
- Cepillado correcto e regular (polo menos dúas veces ao día), pasando tamén as sedas do cepillo por debaixo da liña das enxivas para dificultar o crecemento bacteriano-micótico e a formación de placa subxenxival.
- Limparse entre os dentes con uso de fío dental ou cepillos interdentais (se o espazo entre os dentes é grande dabondo), e limpar ben detrás do último molar.
- Usar unha enxaugadura ou colutorio bucal antiséptico. Os que están baseados no clorhexidina gluconato en combinación dunha hixiene bucal coidadosa poden curar a xenxivite, aínda que non poden inverter a perda de adhesión/suxeición dental na periodontite.
- Usar cubetas periodontais para manter as medicacións prescribidas polo dentista aplicadas sobre o foco da enfermidade: O uso destes produtos permite que a medicación permaneza no seu sitio o tempo suficienteto para penetrar nos biofilmes nos que se encontran os microorganismos
- Facer revisións dentais periódicas no dendista e limpezas profesionais: As revisións serven para controlar os métodos de hixiene oral da persoa e os niveis de suxeición dos dentes, identificando calquera signo inicial de periodontite, e monitorizar a resposta ao tratamento.
- Avaliación microscópica do biofilme, que serve de guía para recuperar a flora comensal saudable.[48]
Os hixienistas dentais ou os dentistas usan instrumentos especiais para limpar os dentes por debaixo da liña das enxivas e destruír as placas en crecemento debaixo da liña das enxivas. Este é un tratamento estándar para previr calquera progreso a peor dunha periodontite estabilizada. Os estudos indican que despois desta limpeza profesional, a placa microbiolóxica tende a crecer outra vez ata niveis preclínicos nuns tres ou catro meses. Non obstante, a continua estabilización do estado periodontal do paciente depende en grande medida ou principalmente da hixiene oral do paciente en casa ou onde vaia. Sen unha hixiene diaria, a enfermidade periodontal non se pode superar, especialmente se o paciente ten un historial de enfermidade periodontal extensiva.
Causas que contribúen poden ser o consumo de alcohol ou unha dieta baixa en antioxidantes.[49]
Xestión da doenza
[editar | editar a fonte]
A pedra angular dun tratamento exitoso periodontal é empezar por establecer unha hixiene oral excelente. Isto inclúe o cepillado dúas veces ao día e o uso diario do fío dental. Ademais, o uso dun cepillo interdental especial é útil se o espazo entre os dentes o permite. Para espazos máis pequenos, produtos como uns ganchos dentais estreitos con suaves sedas de goma proporcionan unha excelente limpeza manual. Ás persoas con problemas de mobilidade, como as que teñen artrite, a hixiene oral pode serlles difícil e poden requirir un coidado profesional máis frecuente e o uso de cepillos eléctricos. As persoas con periodontite deben darse conta que é unha enfermidade inflamatoria crónica e que son necesarios un réxime durante toda a vida de excelente hixiene oral e os coidados profesionais dun dentista/hixienista dental ou periodontista para manter os dentes afectados.
Terapia inicial
[editar | editar a fonte]Empézase pola eliminación da placa microbiana e os cálculos se é necesario para estabilizar a saúde periodontal. O primeiro paso no tratamento da periodontite implica a limpeza non cirúrxica debaixo da liña das enxivas cun procedemento chamado limpeza profunda e desbridamento. No pasado usábase a limpeza de raíces (eliminación da capa de cemento e os cálculos). Este procedemento implica o uso de curetas especializadas para eliminar mecanicamente a placa e os cálculos por debaixo da liña das enxivas, e pode requirir moitas visitas e anestesia local para completala axeitadamente. Ademais da limpeza inicial, pode ser necesario axustar a oclusión para previr que se exerza unha excesiva forza nos dentes que reduza o soporte óseo. Tamén, pode ser necesario completar outras operacións dentais que se crean necesarias, como a substitución de empastes que reteñan placa, pechar contactos abertos entre os dentes, e calquera outra cousa diagnosticada na avaliación inicial.
Reavaliación
[editar | editar a fonte]Moitos estudos clínicos mostran que a limpeza de dentes e raíces non cirúrxica é xeralmente exitosa se as bolsas periodontais son dunha profundidade menor a 4–5 mm.[50][51][52] O dentista ou hixienista debe realizar unha reavaliación de catro a seis meses despois da limpeza, para determinar se a hixiene oral do paciente mellorou e se a inflamación diminuíu. As sondaxes deberían evitarse entón, e unha análise polo índice xenxival debería determinar a presenza ou ausencia de inflamación. A reavaliación mensual da terapia periodontal debería implicar un historial periodontal como unha mellor indicación do éxito do tratamento, e ver se poden identificarse outros cursos de tratamento. As bolsas periodontais de máis de 5–6 mm que persisten despois da terapia inicial, con sangrado na sondaxe, indican unha enfermidade activa continuada e probablemente provocarán unha ulterior perda de óso co tempo. Isto é especialmente certo nos dentes molares onde hai furcacións (áreas entre as raíces) que foron expostas.
Cirurxía
[editar | editar a fonte]Se a terapia non cirúrxica non ten éxito en tratar os signos da actividade da enfermidade, pode ser necesaria a cirurxía periododontal para parar a progresiva perda de óso e rexenerar o óso perdido onde sexa posible. Utilízanse moitas estratexias cirúrxicas no tratamento da periodontite avanzada, como o desbridamento de colgallo (flap) aberto e cirurxía ósea, e a rexeneración de tecidos guiada e o enxerto de óso. O obxectivo da cirurxía periodontal é acceder aos cálculos para a súa definitiva eliminación e o tratamento cirúrxico de irregularidades óseas resultantes do proceso da doenza para reducir así as bolsas todo o posible. Nas periodontites moderadamente avanzadas, os estudos a longo prazo mostran que os casos tratados cirurxicamente a miúdo teñen unha menor descomposición posterior co tempo e, cando se complementan cun réxime de mantemento post-tratamento regular, teñen éxito en practicamente deter a perda de dentes en case o 85% dos pacientes.[53][54]
Mantemento
[editar | editar a fonte]Unha vez que se completou un tratamento periodontal exitoso, con ou sen cirurxía, requírese un réxime de "mantemento periodontal". Este implica revisións regulares e limpezas minuciosas cada tres meses para previr a repoboación por microorganismos causantes de periodontite, e monitorizar estreitamente os dentes afectados para aplicar un tratamento temperán se a enfermidade volve a aparecer. Normalmente, a enfermidade periodontal prodúcese debido a un mal control da placa, polo que se non se modifican as técnicas de cepillado é probable a recorrencia da enfermidade periodontal.
Tratamentos alternativos
[editar | editar a fonte]A periodontite ten unha relación directa cos cálculos (sarrio) subxenxivais. O primeiro paso en calquera procedemento é eliminar os cálculos baixo a liña das enxivas, xa que albergan os microorganismos anaerobios destrutivos que consomen o óso, enxivas e cemento (tecido conectivo).
A maioría dos tratamentos alternativos da enfermidades das enxivas “en casa” implican inxectar solucións antimicrobianas, como peróxido de hidróxeno, nas bolsas periodontais por medio de aplicadores delgados ou irrigadores bucais. Este proceso altera as colonias de microorganismos anaerobios e é efectiva na redución de infeccións e inflamacións cando se usa diariamente. Hai outros produtos, funcionalmente equivalentes ao peróxido de hidróxeno, dos que se dispón comercialmente, pero son moito máis caros. Porén, eses tratamentos non atacan a formación de cálculos, polo que son pouco duradeiros, xa que as colonias anaerobias se rexeneran rapidamente arredor dos cálculos.
Ademais, a periodontite pode tratarse de maneira non invasiva con doxiciclina, un antibiótico de administración oral que se viu que reduce a perda de óso. O seu mecanismo de acción implica en parte a inhibición das metaloproteinases de matriz (como as colaxenases), que degradan a matriz extracelular nas condicións inflamatorias. Isto leva finalmente á redución da perda de óso alveolar en pacientes con enfermidade periodontal (e noutros pacientes sen periodontite).
Prognose
[editar | editar a fonte]Os dentistas e hixienistas dentais miden a enfermidade periodontal utilizando un aparello chamado sonda periodontal, que é unha delgada "regra de medición" que se sitúa coidadosamente no espazo entre as enxivas e o dente, e se introduce debaixo da liña das enxivas. Se a sonda pode introducirse máis de 3 mm por debaixo da liña das enxivas, dise que o paciente ten unha bolsa xenxival se non houbo migración da adhesión epitelial ou unha bolsa periodontal se houbo migración apical. En certo modo este termo é un pouco inexacto, xa que calquera profundidade acadada indica en esencia unha bolsa, a cal á súa vez se define pola súa profundidade, é dicir, unha bolsa de 2 mm ou de 6 mm. Porén, considérase xeralmente que as bolsas as pode limpar un mesmo (o paciente en casa, cun cepillo de dentes) se son de 3 mm ou menores. Isto é importante porque se unha bolsa ten máis profundidade arredor dun dente, non será suficiente unha limpeza caseira, e deberá facela un profesional. Cando a profundidade da bolsa chega a 6–7 mm, os instrumentos manuais e cavitróns usados polos dentistas pode que non cheguen a suficiente profundidade na bolsa para limpar a placa microbiana que causa a inflamación xenxival. En tales situacións, o óso ou a xenxiva arredor do dente deberían ser alteradas cirurxicamente ou persistirá sempre a inflamación, que probablemente orixinará máis perda de óso arredor do dente. Unha forma adicional de parar a inflamación é administrar ao paciente antibióticos subxenxivais (como minociclina) ou sometelo a algún tipo de cirurxía xenxival para acceder ás partes profundas das bolsas e quizais mesmo cambiar a profundidade das bolsas para que pasen a ser de 3 mm ou menos e poidan outra vez ser limpadas axeitadamente en casa con cepillo de dentes.
Se os pacientes teñen bolsas de 7 mm ou máis profundas, están en risco de probablemente perder pezas dentais co paso dos anos. Se esta condición periodontal non se identifica e os pacientes non son conscientes da natureza progresiva da doenza, entón anos máis tarde, poden verse sorprendidos porque algúns dentes se van afrouxando progresivamente e poden ter que ser extraídos, e ás veces orixinan unha grave infección ou dor.
Segundo un estudo deito sobre os traballadores do té de Sri Lanka, en ausencia de calquera hixiene oral, aproximadamente o 10% sufrirá unha enfermidade periodontal grave con perda rápida de adhesión (>2 mm/ano). Un 80% sufrirá dunha perda moderada (1–2 mm/ano) e o restante 10% non sufrirá perdas.[55][56]
Epidemioloxía
[editar | editar a fonte]
A periodontite é moi común, e considérase a segunda enfermidade dental máis común en todo o mundo, despois da carie. En países desenvolvidos a incidencia é menor, pero non pequena. Por exemplo, nos Estados Unidos afecta ao 30-50% da poboación, pero só un 10% presenta as formas graves.
A periodontite crónica afecta a uns 750 millóns de persoas o que era o 10,8% da poboación mundial en 2010.[58]
Como outras condicións ligadas ao acceso á hixiene e a un seguimento e coidados médicos básicos, a periodontite tende a ser máis común en países, rexións ou poboacións economicamente desfavorecidas. A súa frecuencia diminúe ao aumentar o nivel de vida. Por exemplo, en Israel, os individuos de orixe iemenita, norteafricana, surasiática ou meditarránea teñen unha prevalencia maior que os individuos orixinarios doutras partes de Europa.[59]
Noutros animais
[editar | editar a fonte]A enfermidade periodontal é a enfermidade máis común dos cans e afecta a máis do 80% dos cans de tres anos ou máis vellos. A súa prevalencia nos cans increméntase coa idade, pero diminúe co aumento no peso corporal; é dicir, os cans de razas pequeniñas son os máis gravemente afectados. Poden orixinarse enfermidades sistémicas porque as enxivas están moi vascularizadas e a corrente sanguínea pode transportar os microorganismos anaeróbicos, e estes son filtrados polos riles e fígado, onde poden crear colonias e microabscesos. Os microorganismos que viaxan polo sangue poden tamén adherirse ás válvulas cardíacas, causando unha endocardite vexetativa. Outras doenzas que se poden orixinar son a bronquite crónica e a fibrose pulmonar.[60]
Notas
[editar | editar a fonte]- ↑ Savage, Amir; Eaton, Kenneth A.; Moles, David R.; Needleman, Ian (2009). "A systematic review of definitions of periodontitis and methods that have been used to identify this disease". Journal of Clinical Periodontology 36 (6): 458–467. PMID 19508246. doi:10.1111/j.1600-051X.2009.01408.x.
- ↑ Diccionario Terminológico de Ciencias Médicas. 13ª edición. Masson. Páxina 968. ISBN 84-458-0095-7.
- ↑ "pyorrhea". Merriam-Webster Online.
- ↑ Armitage, Gary C. (1999). "Development of a classification system for periodontal diseases and conditions". Annals of Periodontology 4 (1). pp. 1–6. doi:10.1902/annals.1999.4.1.1.
- ↑ The Periodontal Disease Classification System of the American Academy of Periodontology — An Update
- ↑ D'Aiuto, Francesco; Parkar, Mohammed; Andreou, Georgios; Suvan, Hannu; Brett, Peter M.; Ready, Derren; Tonetti, Maurizio S. (2004). "Periodontitis and systemic inflammation: control of the local infection is associated with a reduction in serum inflammatory markers". J Dent Res 83 (2): 156–160. PMID 14742655. doi:10.1177/154405910408300214.
- ↑ Nibali, Luigi; D'Aiuto, Francesco; Griffiths, Gareth; Patel, Kalpesh; Suvan, Jean; Tonetti, Maurizio S. (2007). "Severe periodontitis is associated with systemic inflammation and a dysmetabolic status: a case-control study". Journal of Clinical Periodontology 34 (11): 931–7. PMID 17877746. doi:10.1111/j.1600-051X.2007.01133.x.
- ↑ Paraskevas, Spiros; Huizinga, John D.; Loos, Bruno G. (2008). "A systematic review and meta-analyses on C-reactive protein in relation to periodontitis". Journal of Clinical Periodontology 35 (4): 277–290. PMID 18294231. doi:10.1111/j.1600-051X.2007.01173.x.
- ↑ D'Aiuto, Francesco; Ready, Derren; Tonetti, Maurizio S. (2004). "Periodontal disease and C-reactive protein-associated cardiovascular risk". Journal of Periodontal Research 39 (4): 236–241. PMID 15206916. doi:10.1111/j.1600-0765.2004.00731.x.
- ↑ Pussinen PJ, Alfthan G, Jousilahti P, Paju S, Tuomilehto J (2007). "Systemic exposure to Porphyromonas gingivalis predicts incident stroke". Atherosclerosis 193 (1): 222–8. PMID 16872615. doi:10.1016/j.atherosclerosis.2006.06.027.
- ↑ Pussinen PJ, Alfthan G, Rissanen H, Reunanen A, Asikainen S, Knekt P (September 2004). "Antibodies to periodontal pathogens and stroke risk". Stroke 35 (9): 2020–3. PMID 15232116. doi:10.1161/01.STR.0000136148.29490.fe.
- ↑ Pussinen PJ, Alfthan G, Tuomilehto J, Asikainen S, Jousilahti P (October 2004). "High serum antibody levels to Porphyromonas gingivalis predict myocardial infarction". European Journal of Cardiovascular Prevention & Rehabilitation 11 (5): 408–11. PMID 15616414. doi:10.1097/01.hjr.0000129745.38217.39.
- ↑ Ford PJ, Gemmell E, Timms P, Chan A, Preston FM, Seymour GJ (2007). "Anti-P. gingivalis response correlates with atherosclerosis". J Dent Res 86 (1): 35–40. PMID 17189460. doi:10.1177/154405910708600105.
- ↑ Beck, James D.; Eke, Paul; Heiss, Gerardo; Madianos, Phoebus; Couper, David; Lin, Dongming; Moss, Kevin; Elter, John; Offenbacher, Steven (2005-07-05). "Periodontal Disease and Coronary Heart Disease: A Reappraisal of the Exposure". Circulation (en inglés) 112 (1): 19–24. ISSN 0009-7322. doi:10.1161/CIRCULATIONAHA.104.511998.
- ↑ Scannapieco, Frank A.; Bush, Renee B.; Paju, Susanna (2003). "Associations Between Periodontal Disease and Risk for Atherosclerosis, Cardiovascular Disease, and Stroke. A Systematic Review". Annals of Periodontology 8 (1): 38–53. PMID 14971247. doi:10.1902/annals.2003.8.1.38.
- ↑ Wu, Tiejian; Trevisan, Maurizio; Genco, Robert J.; Dorn, Joan P.; Falkner, Karen L.; Sempos, Christopher T. (2000). "Periodontal Disease and Risk of Cerebrovascular Disease: The First National Health and Nutrition Examination Survey and Its Follow-up Study". Archives of International Medicine 160 (18): 2749–2755. PMID 11025784. doi:10.1001/archinte.160.18.2749. Arquivado dende o orixinal o 23 de marzo de 2012. Consultado o 26 de agosto de 2014.
- ↑ Beck, James D.; Elter, John R.; Heiss, Gerardo; Couper, David; Mauriello, Sally M.; Offenbacher, Steven (2001). "Relationship of Periodontal Disease to Carotid Artery Intima-Media Wall Thickness : The Atherosclerosis Risk in Communities (ARIC) Study". Arteriosclerosis, Thrombosis, and Vascular Biology 21 (21): 1816–1822. doi:10.1161/hq1101.097803. Arquivado dende o orixinal o 15/06/2011. Consultado o 26/08/2014.
- ↑ Elter, John R.; Champagne, Catherine M.E.; Beck, James D.; Offenbacher, Steven (2004). "Relationship of Periodontal Disease and Tooth Loss to Prevalence of Coronary Heart Disease". Journal of Periodontology 75 (6): 782–790. PMID 15295942. doi:10.1902/jop.2004.75.6.782.
- ↑ Humphrey, Linda L.; Fu, Rongwei; Buckley, David I.; Freeman, Michele; Helfand, Mark (2008). "Periodontal Disease and Coronary Heart Disease Incidence: A Systematic Review and Meta-analysis". Journal of General Internal Medicine 23 (12): 2079–2086. PMC 2596495. PMID 18807098. doi:10.1007/s11606-008-0787-. Arquivado dende o orixinal o 13 de setembro de 2019. Consultado o 26 de agosto de 2014.
- ↑ Noble JM, Borrell LN, Papapanou PN, Elkind MS, Scarmeas N, Wright CB (2009). "Periodontitis is associated with cognitive impairment among older adults: analysis of NHANES-III". J Neurol Neurosurg Psychiatry 80 (11): 1206–11. PMC 3073380. PMID 19419981. doi:10.1136/jnnp.2009.174029.
- ↑ Kaye, Elizabeth Krall; Valencia, Aileen; Baba, Nivine; Spiro III, Avron; Dietrich, Thomas; Garcia, Raul I. (2010). "Tooth Loss and Periodontal Disease Predict Poor Cognitive Function in Older Men". Journal of the American Geriatrics Society 58 (4): 713–718. PMID 20398152. doi:10.1111/j.1532-5415.2010.02788.x.
- ↑ Zadik Y, Bechor R, Galor S, Levin L (May 2010). "Periodontal disease might be associated even with impaired fasting glucose". Br Dent J 208 (10): e20. PMID 20339371. doi:10.1038/sj.bdj.2010.291.
- ↑ Soskolne WA, Klinger A (December 2001). "The relationship between periodontal diseases and diabetes: an overview". Ann Periodontol 6 (1): 91–8. PMID 11887477. doi:10.1902/annals.2001.6.1.91.
- ↑ Zadik Y, Bechor R, Galor S, Justo D, Heruti RJ (April 2009). "Erectile dysfunction might be associated with chronic periodontal disease: two ends of the cardiovascular spectrum". J Sex Med 6 (4): 1111–6. PMID 19170861. doi:10.1111/j.1743-6109.2008.01141.x.
- ↑ Michaud, Dominique S.; Liu, Yan; Meyer, Mara; Giovannucci, Edward; Joshipura, Kaumudi (2008). "Periodontal disease, tooth loss, and cancer risk in male health professionals: a prospective cohort study". Lancet Oncol. 9 (6): 550–8. PMC 2601530. PMID 18462995. doi:10.1016/S1470-2045(08)70106-2.
- ↑ Crich, Aubrey (1932). "Blastomycosis of the gingiva and jaw". Can Med Assoc J. 26 (6): 662–5. PMC 402380. PMID 20318753.
- ↑ Urzúa B, Hermosilla G, Gamonal J, Morales-Bozo I, Canals M, Barahona S, Cóccola C, Cifuentes V. (2008). "Yeast diversity in the oral microbiota of subjects with periodontitis: Candida albicans and Candida dubliniensis colonize the periodontal pockets". Med Mycol. 46 (8): 783–93. PMID 18608938. doi:10.1080/13693780802060899.
- ↑ Matsuo, Toshihiko; Nakagawa, Hideki; Matsuo, Nobuhiko; Matsuo, Nobuhiko (1995). "Endogenous Aspergillus endophthalmitis associated with periodontitis". Ophthalmologica 209 (2): 109–11. PMID 7746643. doi:10.1159/000310592.
- ↑ Migliari, Dante A.; Sugaya, Norberto N.; Mimura, Maria A.; Cucé, Luiz Carlos (1998). "Periodontal aspects of the juvenile form of paracoccidioidomycosis". Revista do Instituto de Medicina Tropical de São Paulo 40 (1). ISSN 0036-4665. doi:10.1590/S0036-46651998000100004.
- ↑ Lalla, Evanthia; Cheng, Bin; Lal, Shantanu; Kaplan, Selma; Softness, Barney; Greenberg, Ellen; Goland, Robin S.; Lamster, Ira B. (2007). "Diabetes mellitus promotes periodontal destruction in children". Journal of Clinical Periodontology 34 (4): 294–8. PMID 17378885. doi:10.1111/j.1600-051X.2007.01054.x.
- ↑ "Copia arquivada". Arquivado dende o orixinal o 16 de abril de 2016. Consultado o 26 de agosto de 2014.
- ↑ Obeid, Patrick; Bercy, P. (2000). "Effects of smoking on periodontal health: A review". Advances in Therapy 17 (5): 230–7. PMID 11186143. doi:10.1007/BF02853162. Arquivado dende o orixinal o 13 de setembro de 2019. Consultado o 26 de agosto de 2014.
- ↑ Tomar, Scott L.; Asma, Samira (2000). "Smoking-Attributable Periodontitis in the United States: Findings From NHANES III". Journal of Periodontology 71 (5): 743–751. PMID 10872955. doi:10.1902/jop.2000.71.5.743.
- ↑ Ryder, Mark I. (2007). "The influence of smoking on host responses in periodontal infections". Periodontology 2000 43 (1): 267–277. PMID 17214844. doi:10.1111/j.1600-0757.2006.00163.x.
- ↑ Pauletto, Nathalie C.; Liede, Kirsti; Nieminen, Anja; Larjava, Hannu; Uitto, Veli-Jukka (2000). "Effect of Cigarette Smoking on Oral Elastase Activity in Adult Periodontitis Patients". Journal of Periodontology 71 (1): 58–62. PMID 10695939. doi:10.1902/jop.2000.71.1.58.
- ↑ Persson, Lena; Bergström, Jan; Gustafsson, Anders (2003). "Effect of Tobacco Smoking on Neutrophil Activity Following Periodontal Surgery". Journal of Periodontology 74 (10): 1475–82. PMID 14653394. doi:10.1902/jop.2003.74.10.1475.
- ↑ Bergström, Jan; Boström, Lennart (2001). "Tobacco smoking and periodontal hemorrhagic responsiveness". Journal of Clinical Periodontology 28 (7): 680–5. PMID 11422590. doi:10.1034/j.1600-051x.2001.028007680.x.
- ↑ Peruzzo, Daiane C.; Benatti, Bruno B.; Ambrosano, Glaucia M.B.; Nogueira-Filho, Getúlio R.; Sallum, Enilson A.; Casati, Márcio Z.; Nociti Jr., Francisco H. (2007). "A Systematic Review of Stress and Psychological Factors as Possible Risk Factors for Periodontal Disease". Journal of Periodontology 78 (8): 1491–1504. PMID 17668968. doi:10.1902/jop.2007.060371.
- ↑ Kofoid CA, Hinshaw HC, Johnstone HG. Animal parasites of the mouth and their relation to dental disease. Journal of the American Dental Association 1929 Aug;1436-1455.
- ↑ Keyes PH, Rogosa M, RamsTH, Sarfatti DE. Diagnosis of Creviculoradicular Infections : Disease-Associated Bacterial Patterns in Periodontal Lesions. Host-Parasite Interactions in Periodontal Diseases. Genco and Mergenhagen 1982. ISBN 0-914826-37-9
- ↑ Lyons T, Sholten T, Palmer JC. Oral amoebiasis: a new approach for the general practitioner in the diagnosis and treatment of periodontal disease. Oral Health 1980 Oct; 70(10) : 39-41,108,110.
- ↑ Lyons T, Sholten T, Palmer JC, Stanfield E. Oral amoebiasis: alternatives in oral disease. Ontario dentist 1982 Feb;59(2):16-20.
- ↑ Lyons T, Sholten T, Palmer JC, Stanfield E. Oral amebiasis: the role of Entamoeba gingivalis in periodontal disease. Quintessence Int. 1983 Dec;14(12): 1245-8.
- ↑ Lyons T. Introduction to protozoa and fungi in periodontal infections. Trevor Lyons publications, Ontario, Canada 1989. ISBN 0-9693950-0-0 (disponible upon request at : http://www.parodontite.com)
- ↑ Trim RD, Skinner MA, Farone MB, Dubois JD, Newsome AL. Use of PCR to detect Entamoeba gingivalis in diseased gingival pockets and demonstrate its absence in healthy gingival sites. Parasitol Res. 2011 Sep;109(3):857-64.
- ↑ Bonner M. To Kiss or Not To Kiss. A Cure for Gum Disease. Editions Amyris 2013. EAN: 978-28755-2016-6
- ↑ Bonner M, Amard V, Amiot P, Ihler S, Marty M, Rochet JP, Verdy M. Antiparasitic treatment of periodontitis and peri-implantitis: 12-months multicentric follow-up. AOS Journal no 261 February 2013 (in French).
- ↑ Bonner M. To Kiss or Not to Kiss. A cure for gum disease. Amyris Editions, 2013 EAN : 978-28755-2016-6
- ↑ "First Evidence Found Of Link Between Gum Disease And High Alcohol Consumption, Low Dietary Antioxidants". Arquivado dende o orixinal o 29 de xuño de 2016. Consultado o 26 de agosto de 2014.
- ↑ Stambaugh RV, Dragoo M, Smith DM, Carasali L (1981). "The limits of subgingival scaling". Int J Periodontics Restorative Dent 1 (5): 30–41. PMID 7047434.
- ↑ Waerhaug J (January 1978). "Healing of the dento-epithelial junction following subgingival plaque control. I. As observed in human biopsy material". J Periodontol. 49 (1): 1–8. PMID 340634. doi:10.1902/jop.1978.49.1.1.
- ↑ Waerhaug J (March 1978). "Healing of the dento-epithelial junction following subgingival plaque control. II: As observed on extracted teeth". J Periodontol. 49 (3): 119–34. PMID 288899. doi:10.1902/jop.1978.49.3.119.
- ↑ Kaldahl WB, Kalkwarf KL, Patil KD, Molvar MP, Dyer JK (February 1996). "Long-term evaluation of periodontal therapy: II. Incidence of sites breaking down". J. Periodontol. 67 (2): 103–8. PMID 8667129. doi:10.1902/jop.1996.67.2.103.
- ↑ Hirschfeld L, Wasserman B (May 1978). "A long-term survey of tooth loss in 600 treated periodontal patients". J. Periodontol. 49 (5): 225–37. PMID 277674. doi:10.1902/jop.1978.49.5.225.
- ↑ Preus HR, Anerud A, Boysen H, Dunford RG, Zambon JJ, Loe H (1995). "The natural history of periodontal disease. The correlation of selected microbiological parameters with disease severity in Sri Lankan tea workers". J Clin Periodontol 22 (9): 674–8. PMID 7593696. doi:10.1111/j.1600-051X.1995.tb00825.x.
- ↑ Ekanayaka, Asoka (1984). "Tooth mortality in plantation workers and residents in Sri Lanka". Community Dent Oral Epidemiol 12 (2): 128–35. PMID 6584263. doi:10.1111/j.1600-0528.1984.tb01425.x.
- ↑ "Mortality and Burden of Disease Estimates for WHO Member States in 2002" (xls). World Health Organization. 2002.
- ↑ Vos, T; Flaxman, Abraham D; Naghavi, Mohsen; Lozano, Rafael; Michaud, Catherine; Ezzati, Majid; Shibuya, Kenji; Salomon, Joshua A; Abdalla, Safa; Aboyans, Victor; Abraham, Jerry; Ackerman, Ilana; Aggarwal, Rakesh; Ahn, Stephanie Y; Ali, Mohammed K; Almazroa, Mohammad A; Alvarado, Miriam; Anderson, H Ross; Anderson, Laurie M; Andrews, Kathryn G; Atkinson, Charles; Baddour, Larry M; Bahalim, Adil N; Barker-Collo, Suzanne; Barrero, Lope H; Bartels, David H; Basáñez, Maria-Gloria; Baxter, Amanda; Bell, Michelle L; et al. (Dec 15, 2012). "Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990-2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet 380 (9859): 2163–96. PMID 23245607. doi:10.1016/S0140-6736(12)61729-2.
- ↑ Zadik Y, Bechor R, Shochat Z, Galor S (April 2008). "Ethnic origin and alveolar bone loss in Israeli adults". Refuat Hapeh Vehashinayim (en Hebrew) 25 (2): 19–22, 72. PMID 18780541.
- ↑ Muller-Esnault, Susan, DVM. "Periodontal Disease in the Dog and Cat" (2009). http://www.critterology.com/articles/periodontal-disease-dog-and-cat Arquivado 27 de agosto de 2014 en Wayback Machine.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]- Actinomyces naeslundii
- Campylobacter
- Candida albicans
- Periodontite crónica
- Placa dental
- Xenxivite
- Microbioloxía oral
Bibliografía
[editar | editar a fonte]- Baelum, Vibeke; Lopez, Rodrigo (2003). "Defining and classifying periodontitis: need for a paradigm shift?". European Journal of Oral Sciences 111 (1): 2–6. PMID 12558801. doi:10.1034/j.1600-0722.2003.00014.x.
- Borrell, Luisa N.; Papapanou, Panos N. (2005). "Analytical epidemiology of periodontitis". Journal of Clinical Periodontology 32 (s6): 132–158. PMID 16128835. doi:10.1111/j.1600-051X.2005.00799.x.
- Javed, Fawad; Näsström, Karin; Benchimol, Daniel; Altamash, Mohammad; Klinge, Björn; Engström, Per-Erik (2005). "Comparison of periodontal and socioeconomic status between subjects with type 2 diabetes mellitus and non-diabetic controls". Journal of Periodontology 78 (11): 2112–9. PMID 17970677. doi:10.1902/jop.2007.070186.
- Kinane, Denis; and Bouchard, Phillippe on behalf of group E of the European Workshop on Periodontology; Group E of European Workshop on Periodontology (2008). "Periodontal diseases and health: Consensus Report of the Sixth European Workshop on Periodontology". Journal of Clinical Periodontology 35 (s8, Special Issue: The 6th European Workshop on Periodontology Contemporary Periodontics): 333–7. PMID 18724860. doi:10.1111/j.1600-051X.2008.01278.x.
- Kingman, Albert; Albandar, Jasim M. (2008). "Methodological aspects of epidemiological studies of periodontal diseases". Periodontology 2000 29 (1): 11–30. doi:10.1034/j.1600-0757.2002.290102.x.
- Lucarini, Guendalina; Zizzi, Antonio; Aspriello, Simone Domenico; Ferrante, Luigi; Tosco, Eugenio; Lo Muzio, Lorenzo; Foglini, Paolo; Mattioli-Belmonte, Monica; Di Primio, Roberto; Piemontese, Matteo; Mattioli-Belmonte, Monica; et al. (2009). "Involvement of vascular endothelial growth factor, CD44 and CD133 in periodontal disease and diabetes: an immunohistochemical study". Journal of Clinical Periodontology 36 (1): 3–10. PMID 19017033. doi:10.1111/j.1600-051X.2008.01338.x.
- Pihlstrom, Bruce L.; Michalowicz, Bryan S; Johnson, Newell W. (2005). "Periodontal diseases". Lancet 366 (9499): 1809–20. ISSN 0140-6736. PMID 16298220. doi:10.1016/S0140-6736(05)67728-8. Arquivado dende o orixinal o 20 de abril de 2019. Consultado o 18 de decembro de 2019.
- Williams, Ray C.; Offenbacher, Steven (2000). "Periodontal medicine: the emergence of a new branch of periodontology". Periodontology 2000 23 (1): 9–12. doi:10.1034/j.1600-0757.2000.2230101.x.
Ligazóns externas
[editar | editar a fonte]- O estado avanzdo da enfermidade das enxivas é a periodontite Causas e tratamento da enfermidade das enxivas
- Clínica Mayo
- Academia Canadense de Periodontite — Que é a periodontite?
- Os comportamentos saudables son igual a enxivas saudables — Artigo da Asociación Dental Americana
- Enfermidade das enxivas en cans, tratamento e síntomasArquivado 06 de decembro de 2011 en Wayback Machine.
- Enfermidade periodontal
- Enfermidade periodontal en cans e gatos do Hospital de Animais Cruz Azul.

