Candida albicans
| Candida albicans | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| |||||||||||||||
| Clasificación científica | |||||||||||||||
| |||||||||||||||
| Nome binomial | |||||||||||||||
| 'Candida albicans' (C.P.Robin) Berkhout (1923) | |||||||||||||||
| Sinonimia | |||||||||||||||
Candida albicans é unha especie de fungo diploide que pode crecer como un lévedo unicelular ou como fungo filamentoso multicelular, e é o axente causal de infeccións oportunistas orais e xenitais en humanos,[3][4] e da onicomicose candidal (infección na lámina ungueal da uña). As infeccións fúnxicas sistémicas por C. albicans (e outros fungos) son comúns en persoas inmunocomprometidas. Poden formarse biopelículas de C. albicans na superficie de aparellos médicos implantables. Ademais, as infeccións adquiridas en hospitais por C. albicans son un problema crecente.
C. albicans é un comensal e un constituínte da flora intestinal normal que comprende os microorganismos que viven na boca e no tracto gastrointestinal. C. albicans vive no 80% da poboación humana sen causarlle efectos nocivos, pero o sobrecrecemento do fungo dá lugar á candidíase. A candidíase é frecuente en individuos inmunocomprometidos, como os pacientes de SIDA ou os que foron sometidos a quimioterapia ou transplantes. Unha forma común de candidíase é a restrinxida ás membranas mucosas da boca ou vaxina, que se cura facilmente nas persoas cun sistema inmunitario en condicións normais. Informouse dunha elevada prevalencia da colonización por C. albicans en mozos con piercings na lingua, en comparación cos indivuduos que non os tiñan.[5] Para infectar os tecidos do hóspede, a forma usual unicelular de tipo lévedo de C. albicans reacciona a estímulos ambientais e cambia á forma invasiva multicelular filamentosa, un fenómeno chamado dimorfismo.[3]
Xenoma
[editar | editar a fonte]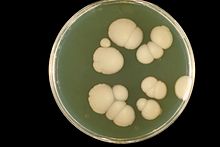
Unha das características máis importantes do xenoma de C. albicans é a presenza de rearranxos cromosómicos numéricos e estruturais que serven como medio para xerar diversidade xenética, denominados polimorfismos de lonxitude (contracción/expansión de repeticións), translocacións recíprocas, delecións xenéticas e trisomía de cromosomas individuais. Estas alteracións cariotípicas producen cambios no fenotipo, que son unha estratexia de adaptación deste fungo. Estes mecanismos serán entendidos mellor cando se complete a análise do xenoma de C. albicans.
Unha característica pouco usual do xénero Candida é que en moitas das súas especies (incluíndo C. albicans e C. tropicalis, pero non, por exemplo, C. glabrata) o codón CUG, que normalmente especifica a leucina, nestas especies codifica a serina. Este é un raro exemplo dunha desviación do código xenético estándar, e a maioría desas desviacións están localizadas nos codóns de inicio ou, en eucariotas, nos códigos xenéticos mitocondriais.[6][7][8] En certos ambientes, esta alteración pode axudar a estas especies de Candida a inducir unha resposta de estrés permanente, unha forma máis xeneralizada de resposta ao shock térmico.[9]
O xenoma de C. albicans é moi dinámico, e esta variabilidade foi utilizada ventaxosamente para estudos epidemiolóxicos moleculares e estudos de poboación nesta especie. A secuenciación do xenoma permitiu a identificación da presenza dun ciclo parasexual (división meiótica ata entón non detectada) en C. albicans.[10] Este estudo da evolución da reprodución sexual en seis especies de Candida atopou perdas recentes nos compoñentes da principal vía de formación dos sobrecruzamentos meióticos, pero a conservación dunha vía menor.[10] Os autores suxiren que se as especies de Candida sofren meiose utilizan unha maquinaria reducida ou unha maquinaria diferente da normal, e indican que poden existir ciclos meióticos non coñecidos en moitas especies. Noutro estudo evolutivo, a introdución dunha redefinición parcial da identidade do cocón CUG desde especies de Candida a clons de Saccharomyces cerevisiae causaba unha resposta ao estrés que afectaba negativamente á reprodución sexual. Esta redifinición do significado de CUG, que apareceu nos antepasados de especies de Candida, crese que deixou pechadas a estas especies nun estado diploide ou poliploide cun posible bloqueo da reprodución sexual.[11]
Dimorfismo
[editar | editar a fonte]Aínda que a miúido se fala de C. albicans como "dimórfica", de feito é polifénica. Cando se cultiva no medio estándar de laboratorio para lévedos, C. albicans crece como un "lévedo" de células ovoides. Porén, cambios ambientais suaves na temperatura e pH poden orixinar un cambio morfolóxico e as células pasan a un crecemento pseudohifal.[12] As pseudohifas comparten moitas semellanzas coas células de lévedos,[13] pero o seu papel durante a candidíase segue sendo descoñecido. Cando as células de C. albicans crecen nun medio que imita o ambiente fisiolóxico do corpo humano, crecen como hifas "verdadeiras". Propúxose que a súa capacidade de formar hifas é un factor de virulencia, xa que estas estruturas se observan frecuentemente nos tecidos invadidos, e as cepas que non poden formar hifas tampouco poden causar infeccións. C. albicans pode tamén formar clamidosporas, de función descoñecida.[14]
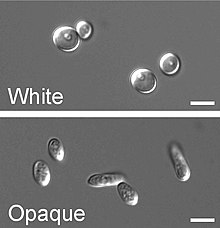
Nun proceso que superficialmente lembra o dimorfismo, C. albicans sofre un cambio fenotípico, no cal se xeran diferentes morfoloxías celulares espontaneamente. Entre as cepas normalmente estudadas, unha das que experimenta este cambio fenotípico é WO-1,[15] a cal presenta dúas fases: unha que crece formando células redondas e colonias brancas lisas, e outra con células de forma bacilar, que crece formando colonias grises planas. Outra cepa que se sabe que sofre cambio fenotípico é a 3153A; esta cepa produce polo menos sete morfoloxías de colonias diferentes. Tanto na cepa WO-1 coma na 3153A, cada fase convértese espontanemente na outra con baixa frecuencia. O cambio é reversible, e o tipo de colonias pode herdarse dunha xeración a outra. Identificaron varios xenes que se expresan de forma diferente en colonias con distintas morfoloxías, e algúns esforzos recentes céntranse en atopar que causa controla estes cambios. Ademais, unha tentadora cuestión é se hai ou non unha ligazón molecular entre o dimorfismo e o cambio fenotípico.[16]
Na cepa 3153A, atopouse un xene chamado SIR2 (ou "regulador da información silenciosa", do inglés silent information regulator), que parece ser importante para o cambio fenotípico. O SIR2 atopouse orixinalmente en Saccharomyces cerevisiae (lévedo de panadaría), no cal está implicado no silenciamento cromosómico, que é unha forma de regulación transcricional, na cal rexións do xenoma son inactivadas reversiblemente por cambios na estrutura da cromatina. Nos lévedos, os xenes implicados no control do tipo de apareamento están situados nestas rexións silenciadas, e SIR2 reprime a súa expresión ao manter nesa rexión unha estrutura da cromatina competente para o silenciamento. O descubrimento do C. albicans SIR2 implicado no cambio fenotípico tamén indica que ten rexións silenciadas controladas por SIR2, nas cales poden encontrarse os xenes específicos para o fenotipo.
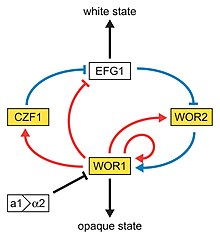
Outra molécula potencialmente reguladora é Efg1p, que é un factor de transcrición que se encontra na cepa WO-1 e que regula o dimorfismo, e máis recentemente suxeriuse que axuda a regular o cambio fenotípico. A Efg1p exprésase só no tipo celular branco e non no gris, e a sobreexpresión de Efg1p na forma gris causa unha rápida conversión á forma branca.[17][18]
Ata agora, hai moi poucos datos que indiquen que o dimorfismo e o cambio fenotípico utilicen compoñentes moleculares comúns. Con todo, non é inconcibible que o cambio fenotípico poida ocorrer en resposta a algúns cambios no contorno. Saber como se regula SIR2 en S. cerevisiae pode proporcionar pistas de como funcionan os mecanismos para o cambio fenotípico en C. albicans.
Heterocigosidade
[editar | editar a fonte]A heterocigosidade do xenoma de Candida excede ao que se atopa noutros xenomas e está xeneralizada entre os illados clínicos. Os polimorfismos dunha soa base non sinónimos orixinan dúas proteínas que difiren nun ou en varios aminoácidos, o que produce diferenzas funcionais para cada proteína. Esta situación aumenta considerablemente o número de proteínas diferentes que codifica un xenoma.[19]
Proteínas importantes para a patoxénese
[editar | editar a fonte]Hwp1
[editar | editar a fonte]A Hwp1, que significa Proteína da Parede da Hifa 1 (do inglés Hyphal Wall protein 1) é unha manoproteína localizada na superficie das hifas da forma filamentosa de C. albicans. A Hwp1 é o substrato da transglutaminase de mamífero. Este encima do hóspede permite que C. albicans se una de forma estable ás células epiteliais do hóspede.[20] A adhesión de C. albicans a células hóspede é un primeiro paso esencial no proceso de infección para a colonización e a subseguinte indución da enfermidade nas mucosas.
Slr1
[editar | editar a fonte]Descubriuse recentemente que a proteína de unión ao ARN Slr1 xoga un papel en promover a formación de hifas e na virulencia de C. albicans.[21]
Aplicación en enxeñaría
[editar | editar a fonte]C. albicans foi utilizada en combinación con nanotubos de carbono para producir materiais de tecidos de bio-nano-composite condutores electricamente, que se utilizaron como elementos sensibles á temperatura.[22]
Tratamento
[editar | editar a fonte]- Artigo principal: Candidíase.
O tratamento xeralmente inclúe o uso de:[23]
- nistatina
- anfotericina B, equinocandina, ou fluconazol para as infeccións sistémicas
- fluconazol ou equinocandinas para as infeccións orais e esofáxicas
- azol tópico para as infeccións vaxinais.
Notas
[editar | editar a fonte]- ↑ Candida albicans at NCBI Taxonomy browser, url accessed 2006-12-26
- ↑ "McClary, Dan Otho (May 1952). "Factors Affecting the Morphology of Candida Albicans". Annals of the Missouri Botanical Garden 39 (2): 137–164. JSTOR 2394509. doi:10.2307/2394509.
- ↑ 3,0 3,1 Ryan KJ, Ray CG (editors) (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. ISBN 0-8385-8529-9.
- ↑ dEnfert C; Hube B (editors) (2007). Candida: Comparative and Functional Genomics. Caister Academic Press. ISBN 978-1-904455-13-4.
- ↑ Zadik Yehuda, Burnstein Saar, Derazne Estella, Sandler Vadim, Ianculovici Clariel, Halperin Tamar (March 2010). "Colonization of Candida: prevalence among tongue-pierced and non-pierced immunocompetent adults". Oral Dis 16 (2): 172–5. PMID 19732353. doi:10.1111/j.1601-0825.2009.01618.x.
- ↑ Ohama, T; Suzuki, Tsutomu; Mori, Miki; Osawa, Syozo; Ueda, Takuya; Watanabe, Kimitsuna; Nakase, Takashi (August 1993). "Non-universal decoding of the leucine codon CUG in several Candida species". Nucleic Acids Research 21 (17): 1039–4045. PMC 309997. PMID 8371978. doi:10.1093/nar/21.17.4039.
- ↑ Arnaud, MB; Costanzo, MC; Inglis, DO; Skrzypek, MS; Binkley, J; Shah, P; Binkley, G; Miyasato, SR; Sherlock, G. "CGD Help: Non-standard Genetic Codes". Candida Genome Database. Consultado o 30 October 2011.
- ↑ Andrzej (Anjay) Elzanowski and Jim Ostell (7 July 2010). "The Alternative Yeast Nuclear Code". The Genetic Codes. Bethesda, Maryland, U.S.A.: National Center for Biotechnology Information (NCBI). Consultado o 30 October 2011.
- ↑ Santos, MA; Cheesman, C; Costa, V; Moradas-Ferreira, P; Tuite, MF (February 1999). "Selective advantages created by codon ambiguity allowed for the evolution of an alternative genetic code in Candida spp.". Molecular Microbiology 31 (3): 937–947. PMID 10048036. doi:10.1046/j.1365-2958.1999.01233.x.
- ↑ 10,0 10,1 Butler G, Rasmussen MD, Lin MF; et al. (June 2009). "Evolution of pathogenicity and sexual reproduction in eight Candida genomes". Nature 459 (7247): 657–62. PMC 2834264. PMID 19465905. doi:10.1038/nature08064.
- ↑ Silva RM, Paredes JA, Moura GR; et al. (October 2007). "Critical roles for a genetic code alteration in the evolution of the genus Candida". EMBO J. 26 (21): 4555–65. PMC 2063480. PMID 17932489. doi:10.1038/sj.emboj.7601876.
- ↑ Peter E. Sudbery (2011). "Growth of Candida albicans hyphae" (PDF). Nature Reviews Microbiology 9 (10): 737–748. PMID 21844880. doi:10.1038/nrmicro2636. Ver figure 2.
- ↑ Berman J, Sudbery PE (2002). "Candida Albicans: a molecular revolution built on lessons from budding yeast". Nature Reviews Genetics 3 (12): 918–930. PMID 12459722. doi:10.1038/nrg948.
- ↑ Staib P, Morschhäuser J (2007). "Chlamydospore formation in Candida albicans and Candida dubliniensis--an enigmatic developmental programme.". Mycoses 50 (1): 1–12. PMID 17302741. doi:10.1111/j.1439-0507.2006.01308.x.
- ↑ Rikkerrink E, Magee B, Magee P (1988). "Opaque-white phenotype transition: a programmed morphological transition in Candida albicans". J. Bact. 170 (2): 895–899. PMC 210739. PMID 2828333.
- ↑ Soll D.R. (2012). Signal Transduction Pathways Regulating Switching, Mating and Biofilm Formation in Candida Albicans and Related Species. In: G. Witzany (ed). Biocommunication of Fungi. Springer, 85-102. ISBN 978-94-007-4263-5.
- ↑ Sonneborn A, Tebarth B, Ernst J (1999). "Control of white-opaque phenotypic switching in Candida albicans by the Efg1p morphogenetic regulator". Infection and Immunity 67 (9): 4655–4660. PMC 96790. PMID 10456912.
- ↑ Srikantha T, Tsai L, Daniels K, Soll D (2000). "EFG1 Null Mutants of Candida albicans Switch but Cannot Express the Complete Phenotype of White-Phase Budding Cells". J. Bact. 182 (6): 1580–1591. PMC 94455. PMID 10692363. doi:10.1128/JB.182.6.1580-1591.2000.
- ↑ Larriba G; Calderone RA (2008). "Heterozygosity and Loss of Heterozygosity in Candida albicans". Pathogenic Fungi: Insights in Molecular Biology. Caister Academic Press. ISBN 978-1-904455-32-5.
- ↑ Staab, J. F. (1999). "Adhesive and Mammalian Transglutaminase Substrate Properties of Candida albicans Hwp1". Science 283 (5407): 1535–1538. ISSN 0036-8075. doi:10.1126/science.283.5407.1535.
- ↑ Ariyachet, C.; Solis, N. V.; Liu, Y.; Prasadarao, N. V.; Filler, S. G.; McBride, A. E. (2013). "SR-like RNA-binding protein Slr1 affects Candida albicans filamentation and virulence". Infection and Immunity 81 (4): 1267–1276. ISSN 0019-9567. doi:10.1128/IAI.00864-12.
- ↑ Di Giacomo, Raffaele; Maresca, Bruno; Porta, Amalia; Sabatino, Paolo; Carapella, Giovanni; Neitzert, Heinz-Christoph (2013). "Candida albicans/MWCNTs: A Stable Conductive Bio-Nanocomposite and Its Temperature-Sensing Properties". IEEE Transactions on Nanotechnology 12 (2): 111. doi:10.1109/TNANO.2013.2239308.
- ↑ Rambach, G; Oberhauser, H; Speth, C; Lass-Flörl, C (2011). "Susceptibility of Candida species and various moulds to antimycotic drugs: Use of epidemiological cutoff values according to EUCAST and CLSI in an 8-year survey". Medical mycology : official publication of the International Society for Human and Animal Mycology 49 (8): 856–63. PMID 21619497. doi:10.3109/13693786.2011.583943.
Véxase tamén
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Waldman A, Gilhar A, Duek L, Berdicevsky I (May 2001). "Incidence of Candida in psoriasis—a study on the fungal flora of psoriatic patients". Mycoses 44 (3–4): 77–81. PMID 11413927. doi:10.1046/j.1439-0507.2001.00608.x.
- Zordan RE, Miller MG, Galgoczy DJ, Tuch BB, Johnson AD (October 2007). "Interlocking Transcriptional Feedback Loops Control White-Opaque Switching in Candida albicans". PLoS Biology 5 (10): e256. PMC 1976629. PMID 17880264. doi:10.1371/journal.pbio.0050256. Consultado o 21 de marzo de 2022.
- Rossignol T, Lechat P, Cuomo C, Zeng Q, Moszer I, d'Enfert C (January 2008). "CandidaDB: a multi-genome database for Candida species and related Saccharomycotina". Nucleic Acids Research 36 (Database issue): D557–61. PMC 2238939. PMID 18039716. doi:10.1093/nar/gkm1010.
- "How Candida albicans switches phenotype – and back again: the SIR2 silencing gene has a say in Candida's colony type". NCBI Coffeebreak. 1999-11-24. Consultado o 2008-11-02.
Ligazóns externas
[editar | editar a fonte]| Commons ten máis contidos multimedia sobre: Candida albicans |
