Acetilcolina
Número CAS: 51-84-3
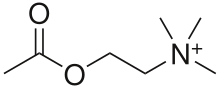
Nome IUPAC: 2-Acetoxi-N,N,N-trimetiletanaminio [1].

A acetilcolina [2] (ás veces abreviada como ACh) é un ión poliatómico orgánico formado por unha molécula de colina unida a un grupo acetilo por enlace éster [3], que actúa como neurotransmisor dos sistemas nerviosos central e periférico do home e moitos organismos. A acetilcolina é un dos moitos neurotransmisores do sistema nervioso autónomo e o único neurotransmisor que se usa na división motora do sistema nervioso somático (as neuronas sensoriais utilizan o glutamato e varios péptidos nas súas sinapses). A acetilcolina é tamén o principal neurotransmisor en todos os ganglios autónomos.
No tecido cardíaco a neurotransmisión con acetilcolina ten efecto inhibitorio, polo que baixa a frecuencia cardíaca. Porén, a acetilcolina tamén se comporta como un neurotransmisor excitatorio nas unións neuromusculares do músculo esquelético.[4]
Historia[editar | editar a fonte]
A acetilcolina foi identificada en 1914 por Henry Hallett Dale polas súas accións sobre o tecido cardíaco. Foi confirmada como neurotransmisor por Otto Loewi, que inicialmente lle dera a esta substancia o nome de Vagusstoff porque a liberaba o nervio vago. Ambos os dous recibiron o premio Nobel de Medicina de 1936 polo seu traballo. A acetilcolina foi o primeiro neurotransmisor que foi identificado.
Química[editar | editar a fonte]
A acetilcolina pode describirse quimicamente como un éster do ácido acético e a colina coa fórmula CH3COOCH2CH2N+(CH3)3. Esta estrutura reflíctese no seu nome sistemático, 2-acetoxi-N,N,N-trimetiletanaminio. Os seus receptores teñen unhas constantes elevadas de unión.
Función[editar | editar a fonte]
A acetilcolina ten funcións como neuromodulador tanto no sistema nervioso periférico coma no central.
No sistema nervioso periférico, a acetilocolina activa os músculos, e é un neurotransmisor importante no sistema nervioso autónomo.
No sistema nervioso central, a acetilcolina e as neuronas asociadas forman o sistema neurotransmisor, chamado sistema colinérxico, que tende a causar accións antiexcitatorias.
No sistema nervioso periférico[editar | editar a fonte]
No sistema nervioso periférico, a acetilcolina activa os músculos, e é un neurotransmisor importante do sistema nervioso autónomo. Cando a acetilcolina se une aos receptores de acetilcolina nas fibras do músculo esquelético, abre as canles de sodio reguladas por ligando na membrana celular. Os ións sodio entran despois na célula muscular, iniciando unha secuencia de pasos que finalmente producen a contracción muscular. Aínda que a acetilcolina induce a contracción do músculo esquelético, actúa por medio de varios tipos de receptores (muscarínicos) para inhibir a contracción das fibras do músculo cardíaco.
No sistema nervioso autónomo, a acetilcolina libérase nos seguintes lugares:
- en todas as neuronas pre- e postganglionares do sistema nervioso parasimpático,
- en todas as neuronas preganglionares do sistema nervioso simpático,
- fibras simpáticas preganglionares da medula suprarrenal, que se considera un ganglio simpático modificado; coa estimulación da acetilcolina, a medula suprarrenal libera adrenalina (epinefrina) e noradrenalina (norepinefrina),
- nalgunhas fibras simpáticas postganglionares,
- neuronas pseudomotoras das glándulas sudoríparas.
No sistema nervioso central[editar | editar a fonte]
No sistema nervioso central, a acetilcolina ten varios efectos como neuromodulador sobre a plasticidade, excitación e sistema de recompensa. A acetilocolina ten un importante papel no reforzamento das percepcións sensoriais cando se desperta [5] e para manter a atención.[6]
Danos no sistema colinérxico (produtor de acetilcolina) do cerebro foron asociados con déficits de memoria asociados coa enfermidade de Alzheimer.[7] A acetilcolina promove os movementos oculares rápidos no sono.[8]
Estrutura[editar | editar a fonte]
A acetilcolina e as neuronas asociadas forman un sistema neurotransmisor, o sistema colinérxico do tronco cerebral e prosencéfalo basal que proxecta axóns a moitas áreas do cerebro. No tronco cerebral orixínase no núcleo pedunculopontino e núcleos tegmentais dorsolaterais coñecidos conxuntamente como a área do tegmento mesopontino ou complexo pontomesencefalotegmental.[9][10] No prosencéfalo basal, orixínase no núcleo óptico basal de Meynert e núcleo septal medial:
- O complexo pontomesencefalotegmental actúa principalmente sobre os receptoreds M1 do tronco cerebral, núcleos cerebelares profundos, núcleos pontinos, locus ceruleus, núcleo do rafe, núcleo reticular lateral e oliva inferior.[10] Tamén envía proxeccións ao tálamo, tectum, ganglios basais e prosencéfalo basal.[9]
- Núcleo óptico basal de Meynert actúa principalmente sobre os receptores M1 no neocórtex.
- Núcleo septal medial actúa principalmente sobre os receptores M1 do hipocampo e neocórtex.
Además, a acetilcolina actúa como un importante transmisor "interno" no corpo estriado, que é parte dos ganglios basais. Está relacionado por un gran conxunto de interneuronas con dendritas lisas coñecidas como neuronas activas tónicas ou TANs.
Plasticidade[editar | editar a fonte]
A acetilcolina está implicada na plasticidade sináptica, especificamente na aprendizaxe e memoria a curto prazo.
A acetilcolina potencia a amplitude dos potenciais sinápticos seguindo a potenciación a longo prazo en moitas rexións, como a circunvolución dentada, CA1, córtex piriforme, e neocórtex. Este efecto ocorre moi probablemente por correntes potenciadores a través dos receptores de NMDA ou indirectamente suprimindo a adaptación neural.[11]
Excitabilidade e inhibición[editar | editar a fonte]
A acetilcolina tamén ten o efecto sobre as neuronas de causar unha lenta despolarización [12] ao bloquear as correntes tonicamente activas de K+, que incrementan a excitabilidade neuronal. Alternativamente, a acetilcolina pode activar condutancias non específicas de catións para excitar directamente ás neuronas.[12] Un efecto sobre os receptores muscarínicos de acetilcolina M4 postsinápticos é abrir unha canle de potasio rectificante entrante (inward-rectifier potassium ion channel ou Kir) e causar inhibición.[13] A influencia da acetilcolina sobre tipos específicos de neuronas pode depender da duración da estimulación colinérxica. Por exemplo, a exposición transitoria á acetilcolina (ata de varios segundos) pode inhibir as neuronas piramidais corticais por medio dos receptores muscarínicos M1 que están ligados ás subunidades alfa da proteína G do tipo Gq. A activación do receptor M1 pode inducir a liberación de calcio dos seus depósitos intracelulares, o cal despois activa unha condutancia de potasio activada por calcio, que inhibe o disparo de impulsos nerviosos nas neuronas piramidais.[14] Por outra parte, a activación dos receptores M1 tónicos é fortemente excitatoria. Así, a acetilcolina que actúa nun tipo de receptor pode ter múltiples efectos sobre a mesma neurona postsináptica, dependendo da duración da activación do receptor.[15] Experimentos recentes en comportamento animal demostraron que as neuronas corticais experimentan cambios tanto transitorios coma permanentes nos niveis locais de acetilcolina durante o comportamento por detección de sinal (cue-detection).[16]
No córtex cerebral, a cetilcolina tónica inhibe a capa 4 de neuronas espiñosas medias, as principais dianas dos impulsos talamocorticais mentres se excitan as células piramidais nas capas 2/3 e 5.[13] Isto elimina os impulsos sensoriais febles na capa 4 e amplifica os impulsos que chegan ás capas 2/3 e L5 dos microcircuítos excitatorios. Como resultado, estes efectos específicos de capa da acetilcolina poderían funcionar mellorando a proporción de sinal de ruído do procesamento cortical.[13] Ao mesmo tempo, a acetilcolina actúa a través dos receptores nicotínicos excitando certos grupos de interneuronas inhibitorias no córtex, que posteriormente moderan a actividade cortical.[17]
Papel na toma de decisións[editar | editar a fonte]
Unha función ben coñecida da acetilcolina no córtex é incrementar a sensibilidade aos estímulos sensoriais, unha forma de aumentar a atención. Os incrementos fásicos de acetilcolina durante a estimulación visual,[18] auditivos [19] e somatosensoriais [20] incrementan a frecuencia de "disparo" das neuronas nos correspondentes córtex sensoriais primarios. Cando as neuronas colinérxicas no prosencéfalo basal se lesionan, a capacidade dos animais de detectaren os sinais visuais vese afectada de forma intensa e persistente.[21] Nese mesmo estudo, a capacidade dos animais de rexeitaren correctamente ensaios sen obxectivo (non-target) non era afectada, o que apoia a interpretación de que a acetilcolina fásica facilita a sensibilidade aos estímulos. Observando os efectos da acetilcoina nas conexións talamocorticais, que son unha vía coñecida de información sensorial, comprobouse que a aplicación in vitro do agonista colinérxico carbacol no córtex auditivo dos ratos aumentaba a actividade talamocortical.[22] Ademais, Gil et al. (1997) aplicarun un agonista colinérxico diferente, a nicotina, e encontraron que a actividade aumentaba nas sinapses talamocorticais.[23] Este descubrimento proporciona máis evidencias do papel facilitador da acetilcolina na transmisión de información sensorial desde o tálamo a rexións selectivas do córtex.
Unha función adicional suxerida para a acetilcolina no córtex é a supresión da transmisión da información intracortical. Gil et al. (1997) aplicaron o agonista colinérxico muscarina a capas neocorticais e encontraron que se deprimían os potenciais possinápticos excitatorios entre as sinapses intracorticais.[23] A aplicación in vitro do agonista colinérxico carbacol ao córtex auditivo do rato suprimía tamén a actividade intracortical.[22] O rexistro óptico cunha tinguidura sensible á voltaxe en preparacións de córtex visual de ratas demostraron unha supresión significativa na extensión intracortical da excitación en presenza de acetilcolina.[24]
Algunhas formas de aprendizaxe e plasticidade no córtex parecen depender da presenza da acetilcolina. Bear et al. (1986) encontraron que o típico remapeo sináptico no córtex estriado (visual) que ocorre durante a deprivación monocular reducíase cando hai unha diminución das proxeccións colinérxicas a esa rexión do córtex.[25] Kilgard et al. (1998) encontraron que a estimulación repetida do prosencéfalo basal, que é unha fonte primaria de neuronas de acetilcolina, acompañado coa presentación dun ton a unha frecuencia específica, orixinaba o remapeo do córtex auditivo para axeitarse mellor ao procesamento dese ton.[26] Baskerville et al. (1996) investigaron o papel da acetilcolina na plasticidade dependente da experiencia ao deprimir os impulsos colinérxicos en certas zonas da capa catro do córtex somatosensorial das ratas.[27] Os animais con diminución colinérxica tiñan unha cantidade significativamente reducida de plasticidade de emparellar as sensacións dos seus bigotes. Ademais das áreas corticais, Crespo et al. (2006) encontraron que a activación de receptores nicotínicos e muscarínicos no núcleo accumbens é necesario para a adquisición de determinadas tarefas.[11]
A acetilcolina tamén inflúe nos resultados de ensaios sobre inseguridade esperada no ambiente (expected uncertainty in the environment) realizados en primates con niveis alterados farmacoloxicamente (por exemplo en Witte et al., 1997) e cirurxicamente (por exemplo en Voytko et al., 1994) de acetilcolina.[28][29][30] O resultado foi atopado tamén na enfermidade de Alzheimer (Parasuraman et al., 1992) e en fumadores despois do consumo de nicotina (un agonista da acetilcolina).[31][32].
Síntese e degradación[editar | editar a fonte]
A acetilcolina sintetízase en certas neuronas polos encimas colina acetiltransferase a partir dos compostos colina e acetil-CoA. As neuronas colinérxicas poden producir acetilcolina e almacenala en vesículas.[33] Un exemplo de área central colinérxica é o núcleo basal de Meynert no prosencéfalo.
O encima acetilcolinesterase converte a acetilcolina nos metabolitos inactivos colina e acetato. Este encima é abundante na fenda sináptica, e o seu papel na rapidez da eliminación (aclaramento) da acetilcolina libre na sinapse é esencial para a correcta función muscular. Certas neurotoxinas funcionan inhibindo a acetilcolinesterase, orixinando un exceso de acetilcolina na unión neuromuscular, causando a parálise dos músculos necesarios para a respiración e parando o latexo cardíaco.
Receptores[editar | editar a fonte]
- Artigo principal: Receptor da acetilcolina.
Hai dúas clases de receptores de acetilcolina, os receptores nicotínicos da acetilcolina (nAChR) e os receptores muscarínicos da acetilcoina (mAChR). Foron nomeados polo ligando usado para activar os receptores.
Nicotínicos[editar | editar a fonte]
Os receptores nicotínicos da acetilcolina son receptores ionotrópicos permeables ao ións sodio, potasio, e calcio. Son estimulados pola nicotina e a acetilcolina. Hai dous grandes tipos, o de tipo muscular e o de tipo neuronal. O primeiro pode ser bloqueado selectivamente polo curare e o último polo hexametonio. A principal localización dos receptores nicotínicos son as placas motoras terminais do músculo, ganglios autónomos simpáticos e parasimpáticos, e no sistema nervioso central.[34]
Miastenia gravis[editar | editar a fonte]
A doenza miastenia gravis, caracterizada por debilidade muscular e fatiga, ocorre cando o corpo produce de forma inapropiada anticorpos contra os receptores nicotínicos da acetilcolina, e deste modo inhibe a correcta transmisión de sinais por acetilcolina. Co tempo, a placa motora terminal queda destruída. As drogas que inhiben competitivamente a acetilcolinesterase (como neostigmina, fisostigmina, ou a piridostigmina) son efectivas no tratamento deste trastorno, xa que permiten que a acetilcolina liberada endoxenamente teña máis tempo para interaccionar cos seus respectivos receptores antes de ser inactivada pola acetilcolinesterase na unión comunicante.
Muscarínicos[editar | editar a fonte]
Os receptores muscarínicos son metabotrópicos, e afectan ás neuronas durante un longo lapso de tempo. Están estimulados por muscarina e acetilcolina, e bloqueados por atropina. Os receptores muscarínicos encóntranse no sistema nervioso central e no periférico, no corazón, pulmóns, tracto xenitourinario superior e glándulas sudoríparas. Os extractos da planta Atropa belladonna conteñen atropina, e este bloqueante dos receptores muscarínicos da acetilcolina dilata as pupilas. Agora, a acetilcolina utilízase ás veces na cirurxía das cataratas para producir unha rápida constrición da pupila. Debe ser administrada intraocularmente porque a colinesterase corneal metaboliza a acetilcolina administrada topicamente antes de que difunda no ollo. Drogas similares utilízanse para inducir a midríase (dilatación pupilar), na resucitación cardiopulmonar e en moitas outras situacións.
Drogas que actúan sobre o sistema colinérxico[editar | editar a fonte]
Bloquear, dificultar ou imitar a acción da acetilcolina ten moitos usos en medicina. As drogas que actúan sobre o sistema da acetilcolina son agonistas dos receptores, que estimulan o sistema, ou antagonistas, que o inhiben.
| Droga | Nm | Nn | M1 | M2 | M3 |
|---|---|---|---|---|---|
| Acetilcolina, Carbacol, AChEi (Psisostigmina, Galantamina, Neostigmina, Piridostigmina) | + | + | + | + | + |
| Nicotina, Vareniclina | + | + | |||
| Succinilcolina | +/- | ||||
| Atracurio, Vecuronio, Tubocurarina, Pancuronio | - | ||||
| Epibatidina, DMPP | + | ||||
| Trimetafán, Mecamilamina, Bupropion, Dextrometofán, Hexametonio | - | ||||
| Muscarina, Metacolina, Oxotremorina, Betanecol, Pilocarpina | + | + | + | ||
| Atropina, Tolterodina, Oxibutinina | - | - | - | ||
| Vedaclidina, Talsaclidina, Xanomelina, Ipatropio | + | ||||
| Pirenzepina, Telenzepina | - | ||||
| Metoctramina | - | ||||
| Darifenacina, 4-DAMP, Solifenacina | - |
Agonistas/antagonistas dos receptores de acetilcolina[editar | editar a fonte]
Os agonistas e antagonistas dos rceptores de acetilcolina poden tamén ter un efecto directo sobre os receptores ou exerceren os seus efectos indirectamente; por exemplo, afectando ao encima acetilcolinesterase, que degrada o ligando do receptor. Os agonistas incrementan o nivel de activación do receptor, e os antagonistas redúceno.
Trastornos asociados[editar | editar a fonte]
Os agonistas dos receptores de acetilcolina utilízanse para tratar a miastenia gravis e a enfermidade de Alzheimer.
Enfermidade de Alzheimer[editar | editar a fonte]
Como os receptores de acetilcolina α4β2 están reducidos no Alzheimer, as drogas que inhiben a acetilcolinesterase, como a galantamina hidrobromuro (un inhibidor da colinesterase reversible e competitivo), utilízanse comunmente no seu tratamento.
Acción directa[editar | editar a fonte]
Son drogas que imitan á acetilcolina no receptor. En doses baixas, estimulan os receptores, en doses altas adormécenos debido ao bloqueo da despolarización.
|
Inhibidores da colinesterase[editar | editar a fonte]
- Artigo principal: Inhibidor da colinesterase.
A maioría dos agonistas dos receptores da acetilcolina que actúan indirectamente funcionan inhibindo o encima acetilcolinesterase. A acumulación resultante de acetilcolina causa a continua estimulación dos músculos, glándulas, e sistema nerviosos central.
Son bos exemplos de inhibidores encimáticos, e incrementan a acción da acetilcolina atrasando a súa degradación; algúns foron usados como axentes nerviosos (Sarín e o gas nervioso axente VX) ou pesticidas (organofosfatos e os carbamatos). No uso clínico, adminístranse para reverter a acción dos relaxantes musculares, para tratar a miastenia gravis, e para tratar os síntomas da enfermidade de Alzheimer (rivastigmina, que incrementa a actividade colinérxica no cerebro).
Reversible[editar | editar a fonte]
As seguintes substancias inhiben reversiblemente o encima acetilcolinesterase (que degrada a acetilcolina), e deste modo incrementan os niveis de acetilcolina.
- Moitos medicamentos para a enfermidade de Alzheimer
- Edrofonio (atrasa as crises miasténicas e colinérxicas)
- Neostigmina (xeralmente usada para reverter o efecto de bloqueantes neuromusculares utilizados na anestesia, ou menos ferecuentemente na mistenia gravis)
- Fisostigmina (no glaucoma e sobredoses de drogas anticolinérxicas)
- Piridostigmina (na miastenia gravis)
- Insecticidas carbamatos (como o Aldicarb)
- Huperzina A
Irreversible[editar | editar a fonte]
Inhiben semipermanentemente o encima acetilcolinesterase.
- Ecotiofato
- Isofluorofato
- Insecticidas organofosfatos (Malation, Paration, Azinfos metilo, Clorpirifos, entre outros)
- Axentes nerviosos que conteñpen organofosfatos (como Sarín, axente nervioso VX)
As vítimas dos axentes nerviosos que conteñen organofosfatos xeralmente morren de asfixia, xa que non poden relaxar o seu músculo diafragma.
Reactivación da acetilcolinesterase[editar | editar a fonte]
Antagonists dos receptores da acetilcolina[editar | editar a fonte]
Axentes antimuscarínicos[editar | editar a fonte]
Bloqueantes ganglionares[editar | editar a fonte]
Bloqueantes neuromusculares[editar | editar a fonte]
Inhibidores da síntese[editar | editar a fonte]
- Compostos orgánicos mercuriais, como o metilmercurio, teñen unha grande afinidade por grupos sulfhidrilo, que causa a disfunción do encima colina acetiltransferase. Esta inhibición pode causar deficiencia de acetilcolina, e pode ter consecuencias sobre a función motora.
Liberación de ihibidores[editar | editar a fonte]
- A toxina botulínica actúa suprimindo a liberación de acetilcolina; e o veleno da araña viúva negra (Latrodectus) (alfa-latrotoxina) ten os efectos contrarios. A inhibición da acetilcolina causa a parálise. Cando nos pica a viúva negra, experimentamos unha perda das reservas de acetilcolina. Cando as reservas están case esgotadas, os músculos empezan a contraerse, e ocorre a parálise.
Outras/non categorizadas/descoñecidas[editar | editar a fonte]
Notas[editar | editar a fonte]
- ↑ ChemSpider Acetylcholine
- ↑ PubChem compound Acetylcholine
- ↑ CHEBI Acetylcholine
- ↑ Campbell, N. A.; Reece, J. B. (2002). "48". Biology (6th ed.). San Francisco, CA: Pearson Education, Inc. pp. 1037. ISBN 0-8053-6624-5.
- ↑ Jones, BE (2005). "From waking to sleeping: neuronal and chemical substrates". Trends in pharmacological sciences 26 (11): 578–86. PMID 16183137. doi:10.1016/j.tips.2005.09.009.
- ↑ Himmelheber, AM; Sarter, M; Bruno, JP (2000). "Increases in cortical acetylcholine release during sustained attention performance in rats". Brain research. Cognitive brain research 9 (3): 313–25. PMID 10808142. doi:10.1016/S0926-6410(00)00012-4.
- ↑ http://www.biopsychiatry.com/alzheim.htm
- ↑ Platt, Bettina; Riedel, Gernot (2011). "The cholinergic system, EEG and sleep". Behavioural Brain Research 221 (2): 499–504. PMID 21238497. doi:10.1016/j.bbr.2011.01.017.
- ↑ 9,0 9,1 Woolf, NJ; Butcher, LL (1986). "Cholinergic systems in the rat brain: III. Projections from the pontomesencephalic tegmentum to the thalamus, tectum, basal ganglia, and basal forebrain". Brain Research Bulletin 16 (5): 603–37. PMID 3742247. doi:10.1016/0361-9230(86)90134-6.
- ↑ 10,0 10,1 Woolf, NJ; Butcher, LL (1989). "Cholinergic systems in the rat brain: IV. Descending projections of the pontomesencephalic tegmentum". Brain Research Bulletin 23 (6): 519–40. PMID 2611694. doi:10.1016/0361-9230(89)90197-4.
- ↑ 11,0 11,1 Crespo JA, Sturm K, Saria A, Zernig G (2006). "Activation of muscarinic and nicotinic acetylcholine receptors in the nucleus accumbens core is necessary for the acquisition of drug reinforcement". J. Neurosci. 26 (22): 6004–10. PMID 16738243. doi:10.1523/JNEUROSCI.4494-05.2006.
- ↑ 12,0 12,1 Haj-Dahmane, S; Andrade, R (1996). "Muscarinic activation of a voltage-dependent cation nonselective current in rat association cortex". Journal of Neuroscience 16 (12): 3848–61. PMID 8656279.
- ↑ 13,0 13,1 13,2 Eggermann, E; Feldmeyer, D (2009). "Cholinergic filtering in the recurrent excitatory microcircuit of cortical layer 4". Proceedings of the National Academy of Sciences of the United States of America 106 (28): 11753–8. PMC 2710689. PMID 19564614. doi:10.1073/pnas.0810062106.
- ↑ Gulledge, AT; Stuart, GJ (2005). "Cholinergic inhibition of neocortical pyramidal neurons". Journal of Neuroscience 25 (44): 10308–20. PMID 16267239. doi:10.1523/JNEUROSCI.2697-05.2005.
- ↑ Gulledge, AT; Bucci, DJ; Zhang, SS; Matsui, M; Yeh, HH (2009). "M1 Receptors Mediate Cholinergic Modulation of Excitability in Neocortical Pyramidal Neurons". Journal of Neuroscience 29 (31): 9888–902. PMC 2745329. PMID 19657040. doi:10.1523/JNEUROSCI.1366-09.2009.
- ↑ Parikh, V; Kozak, R; Martinez, V; Sarter, M (2007). "Prefrontal acetylcholine release controls cue detection on multiple time scales". Neuron 56 (1): 141–54. PMC 2084212. PMID 17920021. doi:10.1016/j.neuron.2007.08.025.
- ↑ Gulledge, AT; Park, SB; Kawaguchi, Y; Stuart, GJ (2007). "Heterogeneity of phasic cholinergic signaling in neocortical neurons". Journal of neurophysiology 97 (3): 2215–29. PMID 17122323. doi:10.1152/jn.00493.2006.
- ↑ Spehlmann R, Daniels JC, Smathers CC (1971). "Acetylcholine and the synaptic transmission of specific impulses to the visual cortex". Brain 94 (1): 125–38. PMID 4324030.
- ↑ Foote SL, Freedman R, Oliver AP (1975). "Effects of putative neurotransmitters on neuronal activity in monkey auditory cortex". Brain Res. 86 (2): 229–42. PMID 234774. doi:10.1016/0006-8993(75)90699-X.
- ↑ Stone, T. W. (1972-09-01). "Cholinergic mechanisms in the rat somatosensory cerebral cortex". The Journal of Physiology (en inglés) 225 (2): 485–499. PMC 1331117. PMID 5074408. doi:10.1113/jphysiol.1972.sp009951.
- ↑ McGaughy J, Kaiser T, Sarter M (1996). "Behavioral vigilance following infusions of 192 IgG-saporin into the basal forebrain: selectivity of the behavioral impairment and relation to cortical AChE-positive fiber density". Behav. Neurosci. 110 (2): 247–65. PMID 8731052.
- ↑ 22,0 22,1 Hsieh CY, Cruikshank SJ, Metherate R (2000). "Differential modulation of auditory thalamocortical and intracortical synaptic transmission by cholinergic agonist". Brain Res. 880 (1-2): 51–64. PMID 11032989. doi:10.1016/S0006-8993(00)02766-9.
- ↑ 23,0 23,1 Gil Z, Connors BW, Amitai Y (1997). "Differential regulation of neocortical synapses by neuromodulators and activity". Neuron 19 (3): 679–86. PMID 9331357. doi:10.1016/S0896-6273(00)80380-3.
- ↑ Kimura F, Fukuda M, Tsumoto T (1999). "Acetylcholine suppresses the spread of excitation in the visual cortex revealed by optical recording: possible differential effect depending on the source of input". Eur. J. Neurosci. 11 (10): 3597–609. PMID 10564367.
- ↑ Bear MF, Singer W (1986). "Modulation of visual cortical plasticity by acetylcholine and noradrenaline". Nature 320 (6058): 172–6. PMID 3005879. doi:10.1038/320172a0.
- ↑ Kilgard MP, Merzenich MM (1998). "Cortical map reorganization enabled by nucleus basalis activity". Science 279 (5357): 1714–8. PMID 9497289. doi:10.1126/science.279.5357.1714.
- ↑ Baskerville KA, Schweitzer JB, Herron P (1997). "Effects of cholinergic depletion on experience-dependent plasticity in the cortex of the rat". Neuroscience 80 (4): 1159–69. PMID 9284068. doi:10.1016/S0306-4522(97)00064-X.
- ↑ Yu, AJ; Dayan, P (May 2005). "Uncertainty, neuromodulation, and attention". Neuron 46 (4): 681–92. doi:10.1016/j.neuron.2005.04.026. PMID 15944135. http://linkinghub.elsevier.com/retrieve/pii/S0896-6273(05)00362-4. as PDF
- ↑ Witte EA, Marrocco RT (1997). "Alteration of brain noradrenergic activity in rhesus monkeys affects the alerting component of covert orienting". Psychopharmacology (Berl.) 132 (4): 315–23. PMID 9298508. doi:10.1007/s002130050351.
- ↑ Voytko ML, Olton DS, Richardson RT, Gorman LK, Tobin JR, Price DL (1994). "Basal forebrain lesions in monkeys disrupt attention but not learning and memory". J. Neurosci. 14 (1): 167–86. PMID 8283232.
- ↑ Parasuraman R, Greenwood PM, Haxby JV, Grady CL (1992). "Visuospatial attention in dementia of the Alzheimer type". Brain 115 (Pt 3): 711–33. PMID 1628198.
- ↑ Witte EA, Davidson MC, Marrocco RT (1997). "Effects of altering brain cholinergic activity on covert orienting of attention: comparison of monkey and human performance". Psychopharmacology (Berl.) 132 (4): 324–34. PMID 9298509. Arquivado dende o orixinal o 12 de xaneiro de 2002. Consultado o 04 de agosto de 2012.
- ↑ Acetylcholine as a neurotransmitter. University of Washington - School of Medicine [1]
- ↑ Katzung, B.G. (2003). Basic and Clinical Pharmacology (9th ed.). McGraw-Hill Medical. ISBN 0-07-141092-9.
- ↑ Nałecz, Ka; Miecz, D; Berezowski, V; Cecchelli, R (2004). "Carnitine: transport and physiological functions in the brain". Molecular aspects of medicine 25 (5–6): 551–67. ISSN 0098-2997. PMID 15363641. doi:10.1016/j.mam.2004.06.001.
Véxase tamén[editar | editar a fonte]
Bibliografía[editar | editar a fonte]
- Brenner, G.M.; Stevens, C.W. (2006). Pharmacology (2nd ed.). Philadelphia PA: W.B. Saunders. ISBN 1-4160-2984-2.
- Canadian Pharmacists Association (2000). Compendium of Pharmaceuticals and Specialties (25th ed.). Toronto ON: Webcom. ISBN 0-919115-76-4.
- Carlson, NR (2001). Physiology of Behavior (7th ed.). Needham Heights MA: Allyn and Bacon. ISBN 0-205-30840-6.
- Gershon, Michael D. (1998). The Second Brain. New York NY: HarperCollins. ISBN 0-06-018252-0.
- Siegal, A.; Sapru, H.N. (2006). "Ch. 15". Essential Neuroscience (Revised 1st ed.). Philadelphia: Lippincott, Williams & Wilkins. pp. 255–267.
- Hasselmo ME (1995). "Neuromodulation and cortical function: modeling the physiological basis of behavior". Behav. Brain Res. 67 (1): 1–27. PMID 7748496. doi:10.1016/0166-4328(94)00113-T. as PDF
