ARN transferente
O ARN transferente, ARN de transferencia ou ARNt (tRNA en inglés) é un tipo de ácido ribonucleico encargado de transportar os aminoácidos aos ribosomas para incorporalos ás proteínas que se están formando alí durante a síntese proteica. Os ARNt representan aproximadamente o 15% do ARN total da célula.[1]
Estrutura[editar | editar a fonte]
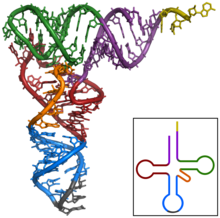

Un ARNt ten unha lonxitude de entre 65 e 110 nucleótidos, e unha masa molecular de 22.000 a 37.000 daltons.[1] Está disolvido no citoplasma celular. Os ARNt poden presentar nucleótidos pouco usuais como o ácido pseudouridílico, ácido inosínico e mesmo nucleótidos con bases características do ADN como a timina.
O ARNt presenta zonas de complementariedade intracatenaria, é dicir, zonas con bases complementarias dentro da mesma cadea, o que determina que a molécula se dobre sobre si mesma e esas zonas se coloquen unhas en fronte das outras, e as bases se emparellen dando unha estrutura característica semellante á dun trevo coas súas tres follas e o talo, coñecida como estrutura secundaria en "folla de trevo".
Na estrutura secundaria dos ARNt distínguense as seguintes partes:
- Brazo aceptor ou brazo aminoácido, formado polos extremos 5' e 3'. O extremo 3' en todos os ARNt posúe a secuencia CCA, cuxo grupo 3'-OH terminal serve de lugar de unión co aminoácido. O extremo 5' case sempre acaba cun GMP ou ácido guanílico (pG). O brazo ten emparellamento intracatenario de bases entre as bases complementarias, excepto no extremo final, onde se une o aminoácido, xa que alí o extremo 3' sobresae máis ca o 5'.
- O bucle ou brazo T, tamén chamado TΨC, que actúa como lugar de recoñecemento do ribosoma. Ten emparellamento de bases no tramo inicial, pero non na asa final. Contén pseudouridina (Ψ) e ribotimidina (coa timina típica do ADN).
- O bucle ou brazo D, tamén chamado brazo DHU porque con frecuencia ten a base rara dihidrouridina. Presenta emparellamento de bases ao principio e sen emparellamentos ao final.
- O brazo anticodón, que despois dun tramo con emparellamentos ten un bucle que contén unha secuencia de tres bases chamada anticodón. O nucleótido 5' do anticodón pode ter bases nitroxenads raras como a inosina ou pseudouridina e nel poden darse emparellamentos de bases non estándar (é dicir, non A-U ou G-C) co codón. Cada ARNt "cargado" co seu correspondente aminoácido únese no ribosoma ao ARNm pola rexión do anticodón, emparellándose con tripletes de bases do ARNm ou codóns, no proceso da tradución da información xenética durante a síntese das proteínas. Codón e anticodón teñen bases complementarias. O ARNt levará o aminoácido que segundo o código xenético corresponde ao codón co cal se vai unir.
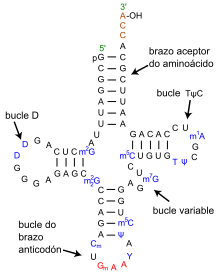
Poden ter ademais un 5º brazo pequeno entre o T e o brazo anticodón.
Estes catro brazos da estrutura secundaria en "folla de trevo" non están estendidos en cruz na célula, senón que se dobran sobre si mesmos, orixinando unha estrutura terciaria con forma de L retorto.
Nas células como mínimo hai 31 ARNt distintos (máis que os 20 aminoácidos estándar) e cada un deles recoñece un só aminoácido, pero o normal é que haxa máis, pero non é necesario que haxa tantos coma codóns codificantes (61) debido ao cambaleo no emparellamento de bases. Outra característica dos ARNt é que ademais das catro bases fundamentaies presentan outras bases púricas e pirimidínicas menos frecuentes. Os encimas aminoacil ARNt sintetases catalizan a unión de cada aminoácido á súa molécula de ARNt específica. Cada aminoacil ARNt sintetase ten a capacidade de distinguir un aminoácido en particular dos restantes 19, a pesar de que algúns deles son moi similares quimicamente. De igual modo, estes encimas recoñecen con precisión a molécula correcta de ARNt para emparellalo co correspondente aminoácido. A reacción que une ao aminoácido co seu ARNt é a mesma para cada aminoácido, o cal, unha vez enlazado no ARNt terá a suficiente enerxía no enlace aminoácido:ARNt para catalizar a reacción que máis adiante unirá un aminoácido con outro por enlace peptídico durante a síntese de proteínas.
Función[editar | editar a fonte]
Os ARNt son intermediarios esenciais entre o ADN e as proteínas. Cada ARNt só pode transferir un único aminoácido. Un ARNt que acepta a alanina escríbese ARNtAla, e un que transporte a lisina sería ARNtLys.
A unión do aminoácido específico co extremo 3' do ARNt require a intervención dun encima aminoacil ARNt sintetase. O recoñecemento do ARNt apropiado polas sintetases non só está mediado polo anticodón, senón que o brazo aceptor xoga tamén un importante papel [2].
As reaccións que se producen son:
Ás veces, certos organismos poden carecer dunha ou de máis aminoacil ARNt sintetases. Isto orixina que o ARNt cargue un aminoácido incorrecto. Nese caso outro encima debe corrixir o aminoácido errado e modificalo para que sexa o correcto. Por exemplo, a bacteria Helicobacter pylori carece da glutaminil-ARNt sintetase (que carga glutamina no ARNt), e, por tanto, a glutamato-ARNt sintetase (da que non carece) carga incorrectamente no ARNt glutamato en lugar de glutamina. Posteriormente o encima amidotransferase converte a cadea lateral do glutamato na cadea lateral da glutamina, desfacendo o erro e formando o correcto ARNtGln.
Unha vez unido o aminoácido, o ARNt diríxese ao ribosoma onde o anticodón do ARNt se une ao codón do ARN mensaxeiro por emparellamento de bases complementarias (A=U, C=G). Deste modo, os ARNt van achegando, un a un, levando os aminoácidos, os cales son ensamblados no ribosoma para formar a cadea polipeptídica segundo a secuencia de codóns do ARNm e as correspondencias do código xenético.
Unión ao ribosoma[editar | editar a fonte]

O ribosoma ten tres sitios ou centros de unión para os ARNt que ocupan o espazo entre as dúas subunidades do ribosoma. Son os seguintes: sitio A (aminoacil), P (peptidil), e E (de expulsión ou saída). No sitio A entra un ARNt co novo aminoácido que se vai incorporar á proteína. No sitio P está o ARNt que leva a cadea polipeptídica en crecemento. O sitio E é un centro desde onde se expulsan os ARNt que xa deixaron o seu aminoácido no ribosoma e acabaron a súa misión.
Ademais, o ribosoma ten outros dous sitios de unión para os ARNt que se usan durante a descodificación do ARNm ou durante a iniciación da tradución de proteínas. Son o sitio T (para o chamado factor de elongación Tu) e o sitio I (de iniciación).[3][4] Por convención, os sitios de unión do ARNt denótanse con dúas letras, xa que ás veces están formados por partes distintas, e sempre se pon primeiro a parte que está na subunidade menor do ribosoma e despois a que está na maior; por exemplo, o sitio A escríbese a miúdo como A/A, o P como P/P etc.[3]
Unha vez que se inicia a tradución, o primeiro aminoacil ARNt colócase no sitio P/P, listo para iniciar un ciclo de elongación. Durante a elongación da proteína, o ARNt únese primeiro ao ribosoma formando parte dun complexo co factor de elongación Tu (EF-Tu) bacteriano ou o seu equivalente eucariótico (eEF-1). Este sitio de unión inicial chámase sitio A/T porque a el se unen o ARNt e o factor Tu. No sitio A/T, a parte A está situada na subunidade menor do ribosoma, onde tamén está localizado o sitio de descodificación do ARNm, que é o sitio onde se le o codón do ARNm durante a tradución. A parte T do sitio está situada principalmente na subunidade maior do ribosoma, onde o factor EF-Tu bacteriano (ou o eEF-1 eucariótico) interacciona co ribosoma.
Unha vez que a descodificación dese codón do ARNm está completa, o aminoacil-ARNt está unido no sitio A/A e está listo para establecer o seguinte enlace peptídico con outro aminoácido. No sitio P/P atópase o peptidil-ARNt que vai transferir o polipéptido en crecemento ao aminoacil-ARNt do sitio A/A (é dicir, todo o polipéptido en crecemento únese ao novo aminoácido acabado de chegar). Cando se forma o enlace peptídico, o ARNt do sitio P/P é perde o polipéptido, e quédalle o extremo 3’ libre, mentres que o ARNt do sitio A/A recolle toda a cadea poplipeptídica en formación, que agora é un aminoácido máis longa, xa que se establece un enlace peptídico entre o polipéptido e o aminoácido que levaba dito ARNt. Para permitir que comece un novo ciclo de elongación, os ARNt móvense a través do sitio híbrido A/P e P/E, e acaban situándose nos sitios P/P e E/E. O ARNm tamén se move un codón e o sitio A/T queda baleiro e preparado para que entre nel un novo ARNt nun novo ciclo de elongación. Finalmente, o ARNt situado no sitio E/E abandona o ribosoma.
En realidade, o primeiro sitio que recibe o aminoacil ARNt nas bacterias é o sitio P/I do ribosoma, no cal se sitúa o factor de iniciación chamado IF2 en bacterias, que trae o ARNt.[4] Non obstante, a existencia deste sitio P/I nos ribosomas de eucariotas e arqueas non foi aínda confirmado.
Xenes dos ARNt[editar | editar a fonte]
O número de xenes dos ARNt nos distintos organismos varía. O verme nematodo Caenorhabditis elegans, que ten un total de 29.647 xenes no seu xenoma nuclear [5], presenta 620 xenes que codifican ARNt.[6][7] O lévedo Saccharomyces cerevisiae ten 275 destes xenes. No xenoma humano unha estimación é que hai en total uns 27.161 xenes [8], e deles uns 4.421 son xenes de ARN que non codifica proteínas, entre os que se inclúen os xenes de ARNt. Hai 22 xenes mitocondriais de ARNt;[9] 497 xenes nucleares que codifican moléculas de ARNt citoplasmático e 324 pseudoxenes relacionados cos ARNt.[10]
Os xenes do ARNt citoplasmático poden agruparse en 49 familias de acordo coas características dos seus anticodóns. Estes xenes atópanse en todos os cromosomas, excepto o 22 e o Y. Un enorme agrupamento de 140 xenes de ARNt está situado en 6p, e no cromosoma 1.[10]
Bioxénese do ARNt[editar | editar a fonte]
En eucariotas os ARNt son transcritos pola ARN polimerase III en forma de pre-ARNt no núcleo.[11] A ARN polimerase III recoñece nos xenes de ARNt dúas secuencias promotoras internas (A-box e o promotor interno B).[12] O primeiro promotor empeza no nucleótido 8 do ARNt maduro e o segundo promotor está situado a 30-60 nucleótidos do anterior. A transcrición termina despois de chegar a un tramo de catro ou máis timidinas seguidas.[12]
Os pre-ARNt sofren grandes modificacións no núcleo. Algúns pre-ARNt conteñen intróns; en bacterias sofren un auto-splicing, e en eucariotas e arqueas son eliminados por unha endonuclease.[13] A secuencia inicial 5' é eliminada por unha ARNase P,[14] e a do extremo 3' é eliminada pola ARNtase Z.[15] Unha notable excepción é a arquea Nanoarchaeum equitans, a cal non posúe ARNase P e ten un promotor situado de maneira que a transcrición empeza no extremo 5' do ARNt maduro.[16] O extremo 3' CCA non está codificado e engádese despois da transcrición por unha nucleotidil transferase.[17]
Antes de que os ARNt sexan exportados do núcleo ao citoplasma polo Los1/Xpo-t,[18][19] os ARNt son aminoacilados (únese o aminoácido).[20] A orde dos eventos de procesamento non foi conservado nas liñas filoxenéticas. Por exemplo nos lévedos, o splicing non se leva a cabo no núcleo senón no lado citoplásmico das membranas das mitocondrias.[21]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 Devlin, T. M. 2004. Bioquímica, 4ª edición. Reverté, Barcelona. ISBN 84-291-7208-4
- ↑ Schimmel P, Giege R, Moras D, Yokoyama S (1993). "An operational RNA code for amino acids and possible relationship to genetic code". Proc Natl Acad Sci 90 (19): 8763–876. doi:10.1073/pnas.90.19.8763.
- ↑ 3,0 3,1 Agirrezabala X, Frank J (2009). "Elongation in translation as a dynamic interaction among the ribosome, tRNA, and elongation factors EF-G and EF-Tu". Q Rev Biophys 42 (3): 159–200. PMC 2832932. PMID 20025795. doi:10.1017/S0033583509990060.
- ↑ 4,0 4,1 Allen GS, Zavialov A, Gursky R, Ehrenberg M, Frank J (2005). "The cryo-EM structure of a translation initiation complex from Escherichia coli". Cell 121 (5): 703–712. PMID 15935757. doi:10.1016/j.cell.2005.03.023.
- ↑ WormBase web site, http://www.wormbase.org Arquivado 20 de abril de 2017 en Wayback Machine., release WS187, date 25-Jan-2008.
- ↑ Spieth, J; Lawson, D (2006). "Overview of gene structure". WormBook : the online review of C. Elegans biology: 1–10. PMID 18023127. doi:10.1895/wormbook.1.65.1.
- ↑ Hartwell LH, Hood L, Goldberg ML, Reynolds AE, Silver LM, Veres RC. (2004). Genetics: From Genes to Genomes 2nd ed. McGraw-Hill: New York, NY. p 264.
- ↑ Ensembl release 48 - Dec 2007 http://www.ensembl.org
- ↑ Ibid. p 529.
- ↑ 10,0 10,1 Lander E.; et al. (2001). "Initial sequencing and analysis of the human genome". Nature 409 (6822): 860–921. PMID 11237011. doi:10.1038/35057062.
- ↑ White RJ (1997). "Regulation of RNA polymerases I and III by the retinoblastoma protein: a mechanism for growth control?". Trends in Biochemical Sciences 22 (3): 77–80. PMID 9066256. doi:10.1016/S0968-0004(96)10067-0.
- ↑ 12,0 12,1 Dieci G, Fiorino G, Castelnuovo M, Teichmann M, Pagano A (2007). "The expanding RNA polymerase III transcriptome". Trends Genet. 23 (12): 614–22. PMID 17977614. doi:10.1016/j.tig.2007.09.001.
- ↑ Abelson J, Trotta CR, Li H (1998). "tRNA Splicing". J Biol Chem 273 (21): 12685–12688. PMID 9582290. doi:10.1074/jbc.273.21.12685.
- ↑ Frank DN, Pace NR (1998). "Ribonuclease P: unity and diversity in a tRNA processing ribozyme". Annu. Rev. Biochem. 67 (1): 153–80. PMID 9759486. doi:10.1146/annurev.biochem.67.1.153.
- ↑ Ceballos M, Vioque A (2007). "tRNase Z". Protein Pept. Lett. 14 (2): 137–45. PMID 17305600. doi:10.2174/092986607779816050.
- ↑ Randau L, Schröder I, Söll D (2008). "Life without RNase P". Nature 453 (7191): 120–3. PMID 18451863. doi:10.1038/nature06833.
- ↑ Weiner AM (2004). "tRNA maturation: RNA polymerization without a nucleic acid template". Curr. Biol. 14 (20): R883–5. PMID 15498478. doi:10.1016/j.cub.2004.09.069.
- ↑ Kutay, U. .; Lipowsky, G. .; Izaurralde, E. .; Bischoff, F. .; Schwarzmaier, P. .; Hartmann, E. .; Görlich, D. . (1998). "Identification of a tRNA-Specific Nuclear Export Receptor". Molecular Cell 1 (3): 359–369. doi:10.1016/S1097-2765(00)80036-2. PMID 9660920.
- ↑ Arts, G. J.; Fornerod, M. .; Mattaj, L. W. (1998). "Identification of a nuclear export receptor for tRNA". Current Biology 8 (6): 305–314. doi:10.1016/S0960-9822(98)70130-7. PMID 9512417.
- ↑ Arts, G. .; Kuersten, S. .; Romby, P. .; Ehresmann, B. .; Mattaj, I. . (1998). "The role of exportin-t in selective nuclear export of mature tRNAs". The EMBO journal 17 (24): 7430–7441. doi:10.1093/emboj/17.24.7430. PMC 1171087. PMID 9857198. http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pmcentrez&artid=1171087.
- ↑ Yoshihisa, T.; Yunoki-Esaki, K.; Ohshima, C.; Tanaka, N.; Endo, T. (2003). "Possibility of cytoplasmic pre-tRNA splicing: the yeast tRNA splicing endonuclease mainly localizes on the mitochondria". Molecular biology of the cell 14 (8): 3266–3279. doi:10.1091/mbc.E02-11-0757. PMC 181566. PMID 12925762. http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pmcentrez&artid=181566.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- tRNAdb (updated and completely restructured version of Spritzls tRNA compilation) Arquivado 19 de xullo de 2011 en Wayback Machine.
- tRNA link to heart disease and stroke
- GtRNAdb: Collection of tRNAs identified from complete genomes
- Molecule of the MonthArquivado 27 de outubro de 2009 en Wayback Machine. © RCSB Protein Data Bank:
- Transfer RNAArquivado 12 de novembro de 2010 en Wayback Machine.
- Aminoacyl-tRNA SynthetasesArquivado 16 de xaneiro de 2010 en Wayback Machine.
- Elongation FactorsArquivado 16 de marzo de 2011 en Wayback Machine.
- Rfam entry for tRNA
