Aminoacil ARNt sintetase

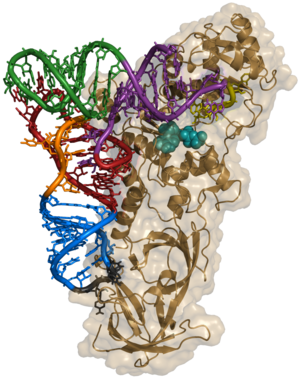
Unha aminoacil ARNt sintetase é un encima que cataliza o enlace por esterificación dun aminoácido específico ou o seu precursor a un dos seus varios ARNt compatibles, para formar así un aminoacil-ARNt. A esta unión chámaselle ás veces "cargar" o ARNt co aminoácido. Unha vez que o ARNt está cargado, vai a un ribosoma onde o aminoácido que leva pode ser transferido á cadea polipeptídica en crecemento durante a síntese de proteínas, de acordo coas correspondencias do código xenético.
Na maior parte dos organismos vivos, existe unha aminoacil ARNt sintetase para cada un dos 20 aminoácidos presentes nas proteínas normais. A selenocisteína, considerada o aminoácido 21, incorpórase por un mecanismo diferente e non ten unha aminoacil ARNt sintetase asociada. Cada un destes encimas recoñece un aminoácido e un ou varios ARNt aceptores. A súa función é esencial para a exactitude da tradución do código xenético, xa que son eles os que garanten que o aminoácido que foi esterificado no extremo 3' do ARNt se corresponda co anticodón axeitado. No ribosoma non se realiza ningunha verificación posterior.
Mecanismo[editar | editar a fonte]
A reacción require unha fase inicial na que a sintetase se une a un ATP e ao correspondente aminoácido (ou ao seu precursor) para formar un aminoacil-adenilato (co aminoácido unido ao fosfato polo seu grupo carboxilo) e liberar un pirofosfato inorgánico (PPi). O complexo AMP-aminoácido no encima únese despois a unha molécula apropiada de ARNt, e o aminoácido é transferido dese complexo a un OH da ribosa do último nucleótido do extremo 3' do ARNt (a A76), que pode ser o OH situado na posición 2' ou 3' de dito nucleótido. O enlace faise polo grupo carboxilo do aminoácido. Algunhas sintetases tamén median unha reacción de comprobación para asegurar unha alta eficiencia na carga, e se durante a comprobación se ve que o ARNt foi incorrectamente cargado, o enlace ARNt-aminoácido é hidrolizado.
Reacción[editar | editar a fonte]
Reaccións:
- aminoácido + ATP → aminoacil-AMP + PPi
- aminoacil-AMP + ARNt → aminoacil-ARNt + AMP
Suma de 1 e 2:
aminoácido + ARNt + ATP → aminoacil-ARNt + AMP + PPi
Clases[editar | editar a fonte]
| Dominio de unión ao anticodón do ARNt | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 a leucil-ARNt sintetase de Thermus thermophilus en complexo cun análogo do substrato | |||||||||
| Identificadores | |||||||||
| Símbolo | Anticodon_1 | ||||||||
| Pfam | PF08264 | ||||||||
| InterPro | IPR013155 | ||||||||
| SCOPe | 1ivs / SUPFAM | ||||||||
| |||||||||
| dominio 1 de unión ao anticodón DALR | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 arxinil-ARNt sintetase de Thermus thermophilus | |||||||||
| Identificadores | |||||||||
| Símbolo | DALR_1 | ||||||||
| Pfam | PF05746 | ||||||||
| Pfam clan | CL0258 | ||||||||
| InterPro | IPR008909 | ||||||||
| SCOPe | 1bs2 / SUPFAM | ||||||||
| |||||||||
| Dominio 2 de unión ao anticodón DALR | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 estrutura cristalina da cisteinil-ARNt sintetase en complexo binario co ATNtcys | |||||||||
| Identificadores | |||||||||
| Símbolo | DALR_2 | ||||||||
| Pfam | PF09190 | ||||||||
| Pfam clan | CL0258 | ||||||||
| InterPro | IPR015273 | ||||||||
| |||||||||
Hai dúas clases de aminoacil ARNt sintetases:[1]
- Aminoacil ARNt sintetases da clase I, que teñen na súa secuencia dous motivos estruturais moi conservados. Unen o aminoácido na posición 2'-OH do nucleótido adenosina-fosfato, e son normalmente proteínas monoméricas ou diméricas.
- Aminoacil ARNt sintetases da clase II, que teñen tres motivos na súa secuencia moi conservados. Unen o aminoácido na posición 3'-OH do nucleótido adenosina-fosfato, e xeralmente son diméricas ou tetraméricas. Unha excepción é a Phe-ARNt sintetase, que estruturalmente é da clase II, pero une o aminoácido na posición 2'-OH.
Os aminoácidos únense polo seu grupo carboxilo (-COOH) ao OH da adenosina.
En calquera caso, cando o aminoácido se une inicialmente á posición 2'-OH do nucleótido, despois sempre migra á posición 3'-OH por transesterificación.
Estruturas[editar | editar a fonte]
Ambas as clases de aminoacil ARNt sintetases son proteínas multidominio. No caso máis típico unha aminocil ARNt sintetase consta dun dominio catalítico (onde teñen lugar ambas as reaccións indicadas antes) e un dominio de unión ao anticodón (que interacciona principalmente coa rexión anticodón do ARNt e asegura a unión do ARNt correcto ao aminoácido). Ademais, algunhas teñen dominios de unión ao ARN adicionais e dominios de edición[2] que separan moléculas de aminoacil-ARNt incorrectamente emparelladas.
Os dominios catalíticos de todas as aminoacil ARNt sintetases da mesma clase son homólogos, pero os das clases I e II non están relacionados. As sintetases da clase I teñen o moi común pregamento de Rossmann e teñen unha arquitectura de cadeas β antiparalelas, entanto que as da clase II teñen un único pregamento feito de cadeas β antiparalelas.
Evolución[editar | editar a fonte]
A maioría das aminoacil ARNt sintetases que teñen unha determinada especificidade están evolutivamente máis próximas ca as que teñen outra especificidade. Porén, a Asn-ARNt sintetase e a Gln-ARNt sintetase hai que agrupalas coa Asp-ARNt sintetase e a Glu-ARNt sintetase, respectivamente. A maioría destes encimas que teñen unha determinada especificidade tamén pertencen a unha mesma clase, aínda que hai dúas versións distintas da Lys-ARNt sintetase, unha da clase I e outra da clase II.
Ademais, as filoxenias moleculares destes encimas son a miúdo pouco consistentes coas filoxenias aceptadas para os organismos, é dicir, violan o patrón filoxenético seguido pola maioría dos encimas, que se corresponde ben coa filoxenia dos tres grandes dominios da vida, Archaea, Bacteria, e Eukarya. E aínda máis, as filoxenias das aminoacil ARNt sintetases de diferentes aminoácidos con frecuencia non coinciden. Estes son dous claros sinais de que na historia evolutiva destes encimas ten sucedido varias veces unha transferencia horizontal [3].
Expansión do código xenético por medio de aminoacil ARNt sintetases mutantes[editar | editar a fonte]
Nalgunhas aminoacil ARNt sintetases a cavidade na que se encontra o aminoácido pode ser mutada e modificada para que leve aminoácidos non naturais artificiais sintetizados no laboratorio, e o unan a ARNt específicos. Isto xera unha expansión do código xenético alén dos 20 aminoácidos universais naturais, e inclúe un novo aminoácido non natural. O aminoácido non natural está codificado por un triplete normalmente non codificante como o codón ámbar (codón de parada). O organismo que expresa a sintetase mutante pode entón programarse xeneticamente para incorporar o aminoácido non natural en calquera posición desexada de calquera proteína que interese, o que permite aos químicos investigar ou facer cambios nas funcións da proteína. Por exemplo, pode empezarse co xene dunha proteína que se une a certas secuencias do ADN, e, dirixindo un aminoácido non natural cunha cadea lateral reactiva ao sitio de unión, crear unha nova proteína que corte o ADN na secuencia diana en lugar de unirse a dita secuencia.
Provocando mutacións nas aminoacil ARNt sintetases os investigadores expandiron os códigos xenéticos de varios organismos para incluír neles aminoácidos sintetizados no laboratorio con toda clase de propiedades útiles: aminoácidos fotoreactivos, con quelación de metais ou de xenon, con enlaces cruzados, cambios de cor, resonancia de spin, fluorescencia, unidos á biotina, ou con propiedades redox.[4]
Notas[editar | editar a fonte]
- ↑ "tRNA Synthetases". Arquivado dende o orixinal o 04 de agosto de 2012. Consultado o 2007-08-18.
- ↑ "High Fidelity". Arquivado dende o orixinal o 08 de xuño de 2011. Consultado o 2007-08-18.
- ↑ Carl R. Woese, Gary J. Olsen, Michael Ibba, and Dieter Söll. Microbiology and Molecular Biology Reviews, March 2000, p. 202-236, Vol. 64, No. 1: Aminoacyl-tRNA Synthetases, the Genetic Code, and the Evolutionary Process)
- ↑ Wang, Lei; Schultz, Peter G. (2005). "Expanding the Genetic Code". Angewandte Chemie International Edition (en inglés) 44 (1): 34–66. ISSN 1521-3773. doi:10.1002/anie.200460627.
