Ácido alxínico
O Ácido alxínico, tamén chamado alxina ou alxinato, é un polisacárido aniónico abondoso na parede celular das algas pardas, onde desempeña unha función estrutural, xa que por medio da absorción de auga forma unha goma natural viscosa. En forma de extracto absorbe a auga rapidamente: é capaz de absorber 200-300 veces o seu propio peso en auga.[1]
Tamén é producido por dous xéneros de bacterias, as Pseudomonas e as Azotobacter, nas que xoga un rol principal no desenvolvemento da súa vía anabólica. Os alxinatos bacterianos son útiles para a produción de micro- ou nano-estruturas para aplicacións médicas.[2]
Estrutura
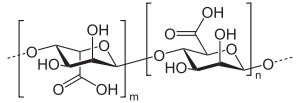
[editar | editar a fonte]É un copolímero lineal con bloques homopoliméricos ligados entres si por ligazóns covalentes glucosídicas entre os seus carbonos de números 1 e 4. Os monómeros básicos son o β-D-manuronato (M) e o seu epímero α-L-guluronato (G).
Os monómeros poden aparecer en bloques homopoliméricos de (G) consecutivos, bloques M consecutivos ou alternando M e G (bloques MG).

Extracción e formas comerciais
[editar | editar a fonte]As variedades comerciais do alxinato extráense das algas pardas, incluíndo os argazos xigantes (Macrocystis pyrifera), bucho bravo (Ascophyllum nodosum), e varios tipos de laminarias. Véndense en forma de sales (de aí a denominación alxinatos) principalmente de sodio; preparadas en grans, filamentos ou po. A súa cor vai do branco ao castaño-amarelado.
No medio acuoso, estas substancias poden formar unha solución coloidal sol (química) viscosa, un xel ou un precipitado, segundo a forza iónica e o pH do medio. A xelificación, en particular, ocorre cando certos catións divalentes están presentes, especialmente o calcio (Ca2+), ou cando o polímero é acidificado (transformado en ácido alxínico). As solucións coloidais de alxinatos compórtanse como fluídos non-newtonianos, exhibindo pseudoplasticidade e, baixo certas condicións, tixotropía (variación da viscosidade no tempo ao seren sometidos a tensión cortante).
Alxinato sódico
[editar | editar a fonte]O composto químico chamado alxinato de sodio é o sal sódico do ácido alxínico. A súa fórmula empírica é NaC6H7O6. Extraese das paredes celulares das algas pardas.
Usos
[editar | editar a fonte]É unha goma natural sen cheiro, usada na industria alimentaria para aumentar a viscosidade e como emulsionante. Úsase na produción de alimentos con aparencia de xel, como espesante de bebidas, de xeados, de sopas e xelatinas. Ten o Número E-401.
É usado na fabricación de papel, téxtiles e cosméticos. Tamén para impermeabilizar as teas e facelas resistentes ao lume. Outra aplicación importante é o uso como aditivo para tinturas reactivas na industria téxtil. O alxinato non reacciona con esas tinturas e pode eliminarse por lavado, ao contrario doutros espesantes baseados no amidón.
Úsase en odontoloxía para facer impresións dentais.
En farmacoloxía como compoñente de varias preparacións farmacéuticas, como pílulas para a indixestión e dado que absorbe auga rapidamente, deshidratado ou liofilizado serve como supresor do apetito.
O alxinato de sodio é un bo quelante para eliminar do corpo as toxinas radioactivas como o Iodo-131 e Estroncio-90 que ocuparon o lugar dos seus isótopos non radioactivos.[3][4]
En marzo do 2010 investigadores da Universidade de Newcastle anunciaron que os alxinatos dietéticos poden reducir a absorción de graxa en humanos en máis do 75%[5]
Tamén, dada a súa biocompatibilidade e fácil xelificación con catións divalentes como o Ca2+, é abondosamente usado en sistemas biotecnolóxicos de inmobilización celular e inmobilización enzimática, para a obtención de produtos como alcohois, ácidos orgánicos etc.
Nas artes culinarias, Ferran Adrià usouno por vez primeira para facer esferificacións, é dicir encapsulación de zumes de froitas ou verduras de xeito que estouren na boca ao tomalos. Combinouno con lactato de calcio para crear esferas de líquido arrodeadas dunha fina membrana xelatinosa. Por exemplo, o seu caviar de mazá.[6]
Alxinato de calcio
[editar | editar a fonte]O alxinato de calcio é o sal cálcico do ácido alxínico
Usos
[editar | editar a fonte]É usado en vendas para queimaduras que favorecen a curación e se poden retirar con menos dor que as convencionais.
Alxinato de potasio
[editar | editar a fonte]O alxinato de potasio é o sal potásico do ácido alxínico. Extráese das algas. A súa fórmula empírica é KC6H7O6.
Usos
[editar | editar a fonte]Amplamente usado en alimentos como estabilizador, espesante e emulsionante.
O seu uso como excipiente farmacéutico actualmente se limita a hidroxeles experimentais. As súas propiedades de viscosidade, adhesividade, elasticidade, rixidez e cohesividade foron estudadas e comparadas coas doutros hidroxeles. Asemade foi estudado o efecto dos ións de calcio sobre as súas propiedades reolóxicas (de comportamento fluído) para a administración oral.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- Algas que son fontes de alxinatos Arquivado 17 de setembro de 2013 en Wayback Machine.(en inglés)
- Propiedades dos alxinatos Arquivado 17 de setembro de 2013 en Wayback Machine.(en inglés)
Notas
[editar | editar a fonte]- ↑ Roew, Raymond (2009). Handbook of Pharmaceutical Excipients (en inglés).
- ↑ Remminghorst e Rehm (2009). Microbial Production of Biopolymers and Polymer Precursors. Microbial Production of Alginate: Biosynthesis and Applications. Caister Academic Press (en inglés). isbn 978-1-904455-36-3.
- ↑ Sutton, A., Harrison, G. E., Carr, T. E., and Barltrop, D. Reduction in the absorption of dietary strontium in children by an alginate derivative. Br.J.Radiol. 44[523], 567. 1971
- ↑ Sutton, A., Harrison, B. E., Carr, T. E., and Barltrop, D. Reduction in the absorption of dietary strontium in children by an alginate derivative. Int.J.Radiat.Biol.Relat Stud.Phys.Chem.Med. 19[1], 79-85. 1971
- ↑ "Seaweed to tackle rising tide of obesity". Newcastle University. Arquivado dende o orixinal o 25 de marzo de 2010. Consultado o 2010-03-22. Arquivado 25 de marzo de 2010 en Wayback Machine.
- ↑ "Lo Mejor de la Gastronomia". StarChefs.com. Arquivado dende o orixinal o 01 de decembro de 2007. Consultado o 2007-11-14. (en inglés).
