Metabolismo de fármacos

O metabolismo de fármacos tamén chamado metabolismo xenobiótico é a modificación bioquímica de substancias farmacéuticas ou xenobióticos polos organismos vivos, xeralmente mediante sistemas encimáticos especializados. O metabolismo de fármacos a miúdo converte os compostos químicos lipófilos en produtos hidrófilos máis fáciles de excretar. A taxa do metabolismo determina a duración e intensidade da acción dos fármacos.
O metabolismo xenobiótico está constituído polo conxunto de rutas metabólicas que modifican a estrutura química de substancias estrañas á bioquímica normal do organismo (xenobióticos), como fármacos e velenos. Estas rutas son unha forma de biotransformación presente en todos os grupos principais de organismos, e considérase que é de orixe antiga. Estas reaccións xeralmente actúan detoxificando compostos velenosos; porén, nalgúns casos, os propios intermediarios do metabolismo xenobiótico poden causar efectos tóxicos.
As reaccións destas rutas son de especial interese para a medicina como parte do metabolismo de fármacos e como un factor que contribúe á resistenca a multidrogas en enfermidades infecciosas e quimioterapia do cancro. As accións dalgúns fármacos como substratos ou inhibidores de encimas implicados no metabolismo xenobiótico son unha causa común de interaccións de fármacos perigosas. Estas vías metabólicas son tamén importantes en ciencias ambientais, e o metabolismo xenobiótico de microorganismos determina se un contaminante será degradado durante a biorremediación, ou persista no ambiente. Os encimas do metabolismo xenobiótico, particularmente as glutatión S-transferases son tamén importantes en agricultura, xa que poden producir resistencia a pesticidas e herbicidas.
O metabolismo de fármacos está dividido en tres fases. Na fase I, encimas como as citocromo P450 oxidases introducen grupos reactivos ou polares nos xenobióticos. Estes compostos modificados son despois conxugados a compostos polares nas reaccións da fase II. Estas reaccións están catalizadas por encimas transferases como as glutatión S-transferases. Finalmente, na fase III, os xenobióticos conxugados poden sufrir aínda ou maior procesamento, antes de seren recoñecidos por transportadores de efluxo e bombeados fóra das células.
Barreiras de permeabilidade e detoxificación
[editar | editar a fonte]Os compostos exactos aos que está exposto un organismo son en gran medida impredicibles e poden diferir grandemente co tempo; estas son as principais características do estrés xenobiótico tóxico.[1] O principal reto ao que se teñen que enfrontar os sistema de detoxificación xenobiótica é que deben poder eliminar un número case ilimitado de compostos xenobióticos na comlexa mestura de compostos químicos implicados no metabolismo normal. A solución que evolucionou para afrontar este problema é unha elegante combinación de barreiras físicas e sistemas encimáticos de baixa especificidade.
Todos os organismos usan as membranas plasmáticas como barreiras de permeabilidade hidrofóbicas para controlar o acceso ao seu ambiente interno. Os compostos polares non poden difundir a través desas membranas, e a captación de moléculas útiles é mediada por proteínas de transporte que seleccionan especificamente substratos da mestura extracelular. Esta captación selectiva significa que a maioría das moléculas hidrófilas non poden entrar nas células, xa que non son recoñecidos por ningún transportador específico.[2] En contraste, a difusión de compostos hidrófobos a través destas barreiras non pode ser controlada, e os organismos, por tanto, non poden excluír xenobióticos liposolubles usando as barreiras de membrana.
Porén, a existencia dunha barreira de permeabilidade significa que os organismos teñen a capacidade de facer evolucionar sistemas de detoxificación que explotan a hidrofobicidade común a xenobióticos permeables á membrana. Estes sistemas resolven o problema da especificidade ao posuíren unhas especificidades de substrato amplas coas que poden metabolizar case calquera composto non polar.[1] Os metabolitos útiles son excluídos xa que son polares, e en xeral conteñen un ou máis grupos cargados.
A detoxificación dos subprodutos reactivos do metabolismo normal non poden conseguirse polos sistemas indicados antes, porque estas especies son derivadas dos constituíntes celulares normais e xeralmente teñen tamén as súas mesmas características polares. Porén, como estes compostos son poucos en número, os encimas específicos poden recoñecelos e eliminalos. Exemplos destes sitemas de detoxificación específica son o sistema da glioxalase, que elimina o aldehido metilglioxal reactivo,[3] e os diversos sistemas antioxidantes que eliminan especies reactivas do oxíxeno.[4]
Fases da detoxificación
[editar | editar a fonte]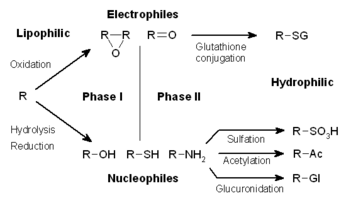
O metabolismo de xenobióticos é a miúdo dividido en tres fases: modificación, conxugación e excreción. Estas reaccións actúan concertadamente para detoxificar xenobióticos e eliminalos das células.
Fase I. Modificación
[editar | editar a fonte]Na fase I, diversos encimas actúan introducindo grupos polares e reactivos nos seus substratos. unha das modificacións máis comúns é a hidroxilación catalizada polo sistema de oxidases de función mixta dependente do citocromo P450. Este complexo de encimas actúa incorporando un átomo de oxíxeno en hidrocarburos non activados, que pode ter como resultado a introdución de grupos hidroxilo ou ben a N-, O- ou S-desalquilación de substratos.[5] O mecanismo de reacción das oxidases dependendtes do P-450 é a redución do oxíxeno unido ao citocromo e a xeración de especies oxiferril altamente reactivas, segundo o seguinte esquema:[6]
- O2 + NADPH + H+ + RH → NADP+ + H2O + ROH
As reacción de fase I (tamén chamadas reaccións non sintéticas) poden ocorer por oxidación, redución, hidrólise, ciclación, desciclación, e adición dun oxíxeno ou retirada dun hidróxeno, levadas a cabo polas oxidases defunción mixta, xeralmente no fígado. Nestas reaccións oxidativas normalmente intervén unha citocromo P450 monooxixenase (xeralmente abreviada CYP), o NADPH e oxíxeno. Entre as clases de fármacos que utilizan este método para o seu metabolismo están as fenotiazinas, o paracetamol, e os esteroides. Se os metabolitos das reaccións de fase I son suficientemente polares, poden ser doadamente excretados neste momento. Porén, moitos produtos da fase I non son eliminados rapidamente e sofren máis reaccións nas cales un substrato endóxeno se combina con grupos químicos novos acabados de incorporar para formar un conxugado moi polar.
Unha oxidación común da fase I supón a conversión dun enlace C-H noutro C-OH. Esta reacción ás veces converte un composto farmacoloxicamente inactivo (un profármaco ou prodroga) noutro farmacoloxicamente activo. Igualmente, na fase I poden converterse moléculas non tóxicas en velenosas (toxifición). A hidrólise simple no estómago é normalmente unha reacción inocua, mais hai excepcións. Por exemplo, o metabolismo da fase I converte o acetonitrilo en HOCH2CN, que é rapidamente disociado en formaldehido e cianuro de hidróxeno, e ambos os dous son tóxicos.
O metabolismo da fase I de fármacos candidatos pode ser simulado no laboratorio usando catalizadores non encimáticos.[7] Este exemplo dunha reacción biomimética tende a dar produtos que a miúdo conteñen os metabolitos da fase I. Como exemplo, o principal metabolito do composto farmacéutico trimebutina, que é a desmetiltrimebutina (nor-trimebutina), pode producirse eficazmente por oxidación in vitro do fármaco dispoñible comercialmente. A hidroxilación dun grupo N-metilo leva á expulsión dunha molécula de formaldehido, mentres que a oxidación dos grupos O-metilo ten lugar en menor medida.
Oxidación
[editar | editar a fonte]- Sistema da citocromo P450 monooxixenase
- Sistema da monooxixenase que contén flavina
- Alcohol deshidroxenase e aldehido deshidroxenase
- Monoamino oxidase
- Cooxidación por peroxidases
Redución
[editar | editar a fonte]A citocromo P450 redutase, tamén chamada NADPH:ferrihemoproteína oxidorredutase, NADPH:hemoproteína oxidorredutase, NADPH:P450 oxidorredutase, P450 redutase, POR, CPR, e CYPOR, é un encima unido a membranas necesario para a transferencia de electróns ao citocromo P450 nos microsomas da célula eucariota desde un encima NADPH:citocromo P450 redutase que contén FAD ou FMN. O esquema xeral do fluxo de electróns no sistema POR/P450 é: NADPH → FAD → FMN → P450 → O2
Durante as reaccións de redución, un coposto químico pode entrar nun ciclo fútil, no cal gaña un electrón de radical libre, despois pérdeo inmediatamente ao oxíxeno (para formar un anión superóxido).
Hidrólise
[editar | editar a fonte]Fase II. Conxugación
[editar | editar a fonte]Nas subseguintes reacciñóns da fase II, estes metabolitos xenobióticos activados son conxugados con especies cargadas comoo glutatión (GSH), sulfato, glicina, ou ácido glicurónico. Os sitios dos fármacos nos que ocorren as reaccións de conxugación poden ser grupos carboxilos (-COOH), hidroxilos (-OH), aminos (NH2), e sulfhidrilos (-SH). Os produtos das reaccións de conxugación incrementaron o seu peso molecular e tenden a ser menos activos que os seus substratos, a diferenza do que pasaba nas reaccións da fase I que a miúdo producían metabolitos activos. A adición de grandes grupos aniónicos (como o GSH) detoxifica electrófilos reactivos e produce máis metabolitos polares que non poden difundir a través das membranas, e poden, por tanto, ser transportados activamente.
Estas reaccións son catalizadas por un gran grupo de transferases de ampla especificidade, que en combinación poden metabolizar case calquera composto hidrófobo que conteña grupos nucleofílicos ou electrofílicos.[1] Unha das clases máis importantes deste grupo é a das glutatión S-transferases (GSTs).
| Mecanismo | Encima implicado[8] | Cofactor[8] | Localización[8] |
|---|---|---|---|
| metilación | metiltransferase | S-adenosil-L-metionina | fígado, riles, pulmóns, SNC |
| sulfación | sulfotransferases | 3'-fosfoadenosina-5'-fosfosulfato | fígado, riles, intestino |
| acetilación | acetil coencima A | fígado, pulmóns, bazo, mucosa gástrica, eritrocitos, linfocitos | |
| glicuronidación | UDP-glicuronosiltransferases | UDP-ácido glicurónico | fígado, riles, intestino, pulmóns, pel, próstata, cerebro |
| conxugación de glutatión | glutatión S-transferases | glutatión | fígado, riles |
| conxugación de glicina | acetil coencima A-encima | glicina | fígado, riles |
Fase III. Modificacións finais e excreción
[editar | editar a fonte]Despois das reaccións da fase II, os conxugados xenobióticos deben ser ulteriormente metabolizados. Un exemplo común é o procesamento de conxugados de glutatión a conxugados de acetilcisteína (ácido mercaptúrico).[9] Aquí, os residuos de γ-glutamato e glicina na molécula de glutatión son retirados por unha gamma-glutamil transpeptidase e dipeptidases. No paso final, o residuo de cistina no conxugado é acetilado.
Os conxugados e os seus metabolitos poden ser excretados das células na fase III do seu metabolismo, e os grupos aniónicos actúan como marcas de afinidade para unha variedade de transportadores de membrana da familia da proteína de resistencia a multidrogas (MRP).[10] Estas proteínas son membros da familia do transportador de casete que se une ao ATP e poden catalizar o transporte dependente de ATP dunha enorme variedade de anións hidrofóbicos,[11] e así actúan eliminando os produtos da fase II ao medio extracelular, onde poden sufrir unha maior metabolización ou ser excretados.[12]
Toxinas endóxenas
[editar | editar a fonte]A detoxificación de metabolitos reactivos endóxenos como os peróxidos e aldehidos reactivos xeralmente non pode realizarse polo sistema descrito antes. Isto débese a que estas especies químicas derivan de constituíntes celulares normais e xeralmente teñen tamén características polares. Porén, como estes compostos son poucos, é posible que os sistemas encimáticos utilicen un recoñecemento molecular específico para detectalos e eliminalos. A semellanza destas moléculas con metabolitos útiles significa que cómpren diferentes encimas de detoxificación para cada grupo de toxinas endóxenas. Exemplos destes sistemas de detoxificación específicos son o sistema da glioxalase, que actúa eliminando o aldehido reactivo metilglioxal, e os diversos sistemas antioxidantes que destrúen as especies reactivas do oxíxeno.
Sitios
[editar | editar a fonte]Cuantitativamente, o retículo endoplasmático liso das células do fígado é o principal lugar onde se produce o metabolismo de fármacos, aínda que cada tecido ten certa capacidade de metabolizar fármacos. Os factores responsables da contribución do fígado ao metabolismo de fármacos son que é un órgano grande, que é o primeiro órgano ao que chegan os produtos químicos absorbidos no intestino, e que ha nel moi altas concentracións da maioría dos sistemas que metabolizan fármacos en comparación con outros órganos. Se un fármaco é absorbido no tracto gastrointestinal, chega á circulación hepática a través da vea porta, e será ben metabolizado e mostrará o chamado efecto de primeiro paso.
Outros sitios importantes de metabolización de fármacos son as células epiteliais do tracto gastrointestinal, pulmóns, riles, e a pel. Estes sitios son xeralmente responsables de certas reaccións de toxicidade localizadas.
Factores que afectan ao metabolismo de fármacos
[editar | editar a fonte]A duración e intensidade da acción farmacolóxica da maioría dos fármacos lipófilos está determinada pola velocidade con que son metabolizados a produtos inactivos. O sistema da citocromo P450 monooxixenase é a vía máis importante nesta tarefa. En xeral, calquera cousa que incremente a velocidade do metabolismo (por exemplo indución de encimas) dun metabolito farmacoloxicamene activo diminuirá a duración e intensidade da acción do fármaco. O oposto é tamén certo (por exemplo a inhibición de encimas). Porén, en casos nos que un encima é responsable de metabolizar un profármaco a un fármaco, a indución de encimas pode acelerar esta conversión e incrementar os niveis de fármaco, potencialmente ata causar toxicidade.
Varios factores fisiolóxicos e patolóxicos poden tamén afectar ao metabolismo de fármacos. Factores fisiolóxicos que poden influenciar o metabolismo de fármacos son a idade, variación individual (por exemplo a farmacoxenética), a circulación enterohepática, a nutrición, a flora intestinal ou as diferenzas entre sexos.
En xeral, os fármacos son metabolizados máis lentamente nas etapas fetal, neonatal e na ancianidade que na etapa adulta tanto en humanos coma noutros animais.
As variacións xenéticas (polimorfismos) explican parte da variabilidade no efecto dos fármacos. Nas N-acetiltransferases (implicadas nas reaccións da fase II), as variacións individuais fan que algunhas persoas acetilen lentamente (acetiladores lentos) e outras o fagan rapidamente, e nun estudo feito no Canadá os dous grupos eran o 50% da poboación. Esta variación pode ter drásticas consecuencias, xa que os acetiladores lentos son máis propensos a sufrir unha toxicidade dependente de dose.
O sistema da citocromo P450 monooxenase pode tamén variar entre individuos, e aparecen deficiencias en do 1 ao 30% dos casos, dependendo da súa ascendencia étnica.
Os factores patolóxicos poden tamén influír no metabolismo de fármacos, como as doenzas do fígado, riles ou corazón.
Os modelos in silico (computacionais) e métodos de simulación permiten predicir o metabolismo de fármacos en poboacións de pacientes virtuais antes de realizar estudos clínicos en suxeitos humanos.[13] Isto pode utilizarse tamén para identificar individuos que están en maior risco de sufrir unha reacción adversa.
Historia
[editar | editar a fonte]Os estudos de como as persoas transforman as substancias que inxiren empezaron a mediados do século XIX, cando os químicos descubriron que os compostos orgánicos como o benzaldehido podían ser oxidados e conxugados a aminoácidos no corpo humano.[14] Durante o resto do século XIX, descubríronse outras reaccións de detoxificación básicas, como a metilación, acetilación e a sulfonación.
A inicios do século XX, os traballos centráronse en investigar os encimas e as rutas que eran responsables da produción destes metabolitos. Este campo foi definido como unha área separada de estudo coa publicación por Richard Williams do libro Detoxication mechanisms (Mecanismos de detoxificación) en 1947.[15] Esta moderna investigación bioquímica tivo como resultado a identificación das glutatión S-transferases en 1961,[16] seguido do descubrimento dos citocromos P450 en 1962,[17] e a comprensión do seu papel central no metabolismo xenobiótico en 1963.[18][19]
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 1,2 Jakoby WB, Ziegler DM (December 1990). "The enzymes of detoxication". J. Biol. Chem. 265 (34): 20715–8. PMID 2249981. Arquivado dende o orixinal o 21 de xuño de 2009. Consultado o 06 de xullo de 2016.
- ↑ Mizuno N, Niwa T, Yotsumoto Y, Sugiyama Y (September 2003). "Impact of drug transporter studies on drug discovery and development". Pharmacol. Rev. 55 (3): 425–61. PMID 12869659. doi:10.1124/pr.55.3.1.
- ↑ Thornalley PJ (July 1990). "The glyoxalase system: new developments towards functional characterization of a metabolic pathway fundamental to biological life". Biochem. J. 269 (1): 1–11. PMC 1131522. PMID 2198020.
- ↑ Sies H (March 1997). "Oxidative stress: oxidants and antioxidants" (PDF). Exp. Physiol. 82 (2): 291–5. PMID 9129943. doi:10.1113/expphysiol.1997.sp004024. Arquivado dende o orixinal (PDF) o 25 de marzo de 2009. Consultado o 06 de xullo de 2016.
- ↑ Guengerich FP (June 2001). "Common and uncommon cytochrome P450 reactions related to metabolism and chemical toxicity". Chem. Res. Toxicol. 14 (6): 611–50. PMID 11409933. doi:10.1021/tx0002583.
- ↑ Schlichting I, Berendzen J, Chu K, Stock AM, Maves SA, Benson DE, Sweet RM, Ringe D, Petsko GA, Sligar SG (March 2000). "The catalytic pathway of cytochrome p450cam at atomic resolution". Science 287 (5458): 1615–22. PMID 10698731. doi:10.1126/science.287.5458.1615.
- ↑ Akagah B, Lormier AT, Fournet A, Figadère B (December 2008). "Oxidation of antiparasitic 2-substituted quinolines using metalloporphyrin catalysts: scale-up of a biomimetic reaction for metabolite production of drug candidates". Org. Biomol. Chem. 6 (24): 4494–7. PMID 19039354. doi:10.1039/b815963g.
- ↑ 8,0 8,1 8,2 Liston HL, Markowitz JS, DeVane CL (October 2001). "Drug glucuronidation in clinical psychopharmacology". J Clin Psychopharmacol 21 (5): 500–15. PMID 11593076. doi:10.1097/00004714-200110000-00008.
- ↑ Boyland E, Chasseaud LF (1969). "The role of glutathione and glutathione S-transferases in mercapturic acid biosynthesis". Adv. Enzymol. Relat. Areas Mol. Biol. Advances in Enzymology – and Related Areas of Molecular Biology 32: 173–219. ISBN 9780470122778. PMID 4892500. doi:10.1002/9780470122778.ch5.
- ↑ Homolya L, Váradi A, Sarkadi B (2003). "Multidrug resistance-associated proteins: Export pumps for conjugates with glutathione, glucuronate or sulfate". BioFactors 17 (1–4): 103–14. PMID 12897433. doi:10.1002/biof.5520170111.
- ↑ König J, Nies AT, Cui Y, Leier I, Keppler D (December 1999). "Conjugate export pumps of the multidrug resistance protein (MRP) family: localization, substrate specificity, and MRP2-mediated drug resistance". Biochim. Biophys. Acta 1461 (2): 377–94. PMID 10581368. doi:10.1016/S0005-2736(99)00169-8.
- ↑ Commandeur JN, Stijntjes GJ, Vermeulen NP (June 1995). "Enzymes and transport systems involved in the formation and disposition of glutathione S-conjugates. Role in bioactivation and detoxication mechanisms of xenobiotics". Pharmacol. Rev. 47 (2): 271–330. PMID 7568330.
- ↑ Rostami-Hodjegan A, Tucker GT (February 2007). "Simulation and prediction of in vivo drug metabolism in human populations from in vitro data". Nat Rev Drug Discov 6 (2): 140–8. PMID 17268485. doi:10.1038/nrd2173.
- ↑ Murphy PJ (June 2001). "Xenobiotic metabolism: a look from the past to the future". Drug Metab. Dispos. 29 (6): 779–80. PMID 11353742. Arquivado dende o orixinal o 21 de xuño de 2009. Consultado o 06 de xullo de 2016.
- ↑ Neuberger A, Smith RL (1983). "Richard Tecwyn Williams: the man, his work, his impact". Drug Metab. Rev. 14 (3): 559–607. PMID 6347595. doi:10.3109/03602538308991399.
- ↑ Booth J, Boyland E, Sims P (June 1961). "An enzyme from rat liver catalysing conjugations with glutathione". Biochem. J. 79 (3): 516–24. PMC 1205680. PMID 16748905.
- ↑ Omura T, Sato R (April 1962). "A new cytochrome in liver microsomes". J. Biol. Chem. 237: 1375–6. PMID 14482007. Arquivado dende o orixinal o 21 de xuño de 2009. Consultado o 06 de xullo de 2016.
- ↑ Estabrook RW (December 2003). "A passion for P450s (remembrances of the early history of research on cytochrome P450)". Drug Metab. Dispos. 31 (12): 1461–73. PMID 14625342. doi:10.1124/dmd.31.12.1461.
- ↑ Estabrook RW, Cooper DY, Rosenthal O (1963). "The light reversible carbon monoxide inhibition of steroid C-21 hydroxylase system in adrenal cortex". Biochem Z 338: 741–55. PMID 14087340.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Parvez H, Reiss C (2001). Molecular Responses to Xenobiotics. Elsevier. ISBN 0-345-42277-5.
- Ioannides C (2001). Enzyme Systems That Metabolise Drugs and Other Xenobiotics. John Wiley and Sons. ISBN 0-471-89466-4.
- Richardson M (1996). Environmental Xenobiotics. Taylor & Francis Ltd. ISBN 0-7484-0399-X.
- Ioannides C (1996). Cytochromes P450: Metabolic and Toxicological Aspects. CRC Press Inc. ISBN 0-8493-9224-1.
- Awasthi YC (2006). Toxicology of Glutathionine S-transferses. CRC Press Inc. ISBN 0-8493-2983-3.
Ligazóns externas
[editar | editar a fonte]- Bases de datos
- Metabolismo de fármacos
- Biodegradación microbiana
- Historia
