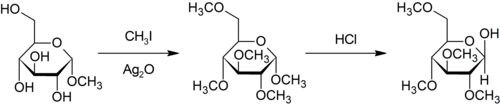Metilación
En química, a metilación é a adición dun grupo metilo (CH3) a un substrato ou a substitución dun átomo ou grupo por un grupo metilo. A metilación é unha forma de alquilación cun grupo metilo, en lugar de por unha cadea carbonada grande como ocorre noutras alquilacións, que substitúe a un átomo de hidróxeno. Este termo utilízase en química, bioquímica, edafoloxía, e bioloxía.
Nos sistemas biolóxicos a metilación é catalizada por encimas; ditas metilacións poden estar implicadas en modificacións de metais pesados, a regulación da expresión xénica, a regulación da función proteica, e o procesamento do ARN. A metilación de metais pesados pode ocorrer tamén fóra dos sistemas biolóxicos. A metilación química de mostras de tecidos é tamén un método para reducir certos artefactos histolóxicos de tinguidura.
En bioloxía
[editar | editar a fonte]- Véxase tamén: Metilación do ADN.
Epixenética
[editar | editar a fonte]A metilación que contribúe á herdanza epixenética pode ocorrer por metilación do ADN ou por metilación das proteínas.
A metilación do ADN en vertebrados ocorre tipicamente en sitios CpG (sitios citosina-fosfato-guanina, que son sitios onde unha citosina está seguida por unha guanina na secuencia de ADN). Esta metilación orixina a conversión da citosina en 5-metilcitosina. A formación de Me-CpG está catalizada polo encima ADN metiltransferase. O ADN humano ten do 80 ao 90% dos sitios CpG metilados, pero hai certas áreas, chamadas illas CpG, que son ricas en GC (teñen un alto contido en guanina e citosina, e comprenden o 65% dos residuos CG), nos que non está metilada ningunha. Estas illas están asociadas cos promotores do 56% dos xenes de mamíferos, incluíndo todos os xenes que se expresan ubicuamente. Do 1 ao 2 % do xenoma humano son grupos CpG, e hai unha relación inversa entre a metilación CpG e a actividade transcricional.
A metilación de proteínas é un tipo de modificación postraducional que ten lugar normalmente nos residuos de aminoácidos arxinina ou lisina da secuencia da proteína.[1] A arxinina pode ser metilada unha vez (arxinina monometilada) ou dúas (arxinina dimetilada), e nese caso pode ter ambos os grupos metilo situados nun nitróxeno terminal (arxinina dimetilada asimétrica) ou un en cada nitróxeno terminal (arxinina dimetilada simétrica). A reacción catalízana peptidilarxinina metiltransferases (PRMTs). A lisina pode ser metilada unha, dúas ou tres veces polas lisina metiltransferases. A metilación de proteínas foi máis estudada nas histonas. A transferencia de grupos metilo desde a S-adenosil metionina a histonas é catalizada por encimas chamados histona metiltransferases. As histonas que son metiladas en certos residuos poden actuar epixeneticamente para reprimir ou activar a expresión xénica.[2][3]
Desenvolvemento embrionario
[editar | editar a fonte]Aínda que os cromosomas das células somáticas reteñen os patróns de metilación parentais, durante o desenvolvemento das células xerminais os seus xenomas son desmetilatdos. Despois diso, ten lugar unha metilación de novo das células xerminais, modificando e engadindo información epixenética ao xenoma que depende do sexo do individuo.[4]
Despois da fertilización dun ovocito e a formación do cigoto, o seu xenoma combinado é desmetilado e remetilatdo outra vez (coa excepción dos chamados xenes impresos). No estado de blástula, a metilación das células embrionarias é completa.
O proceso de desmetilación/remetilación denomínase "reprogramación".[5] A importancia da metilación pode verse nos mutantes obtidos por knockout de xenes que carecen de ADN metiltransferase, que morren todos no estado de mórula.[6]
A conversión da 5-metilcitosina en 5-hidroximetilcitosina asóciase ás veces con nucleosomas inestables lábiles, que son con frecuencia reposicionados durante a diferenciación das células nai.[7]
Desenvolvemento posnatal
[editar | editar a fonte]Hai crecentes evidencias de que a metilación exerce un papel na interacción de factores ambientais coa expresión xenética. As diferenzas en coidados maternos durante os primeiros 6 días de vida nas ratas inducen patróns de metilación diferencial nalgunhas rexións promotoras dos xenes, influíndo deste modo na expresión xénica.[8] Ademais, os procesos que son aínda máis dinámicos, como a sinalización por interleucinas, están regulados por metilación.[9]
A investigación en humanos mostrou que niveis altos repetidos de activación do sistema de estrés do corpo, especialmente na infancia temperá, poden alterar os procesos de metilación e orixinan cambios na química do ADN dun individuo. Os cambios químicos poden inutilizar xenes e impedir que o cerebro regule correctamente a súa resposta ao estrés. Os investigadores e clínicos atoparon unha ligazón entre esta desregulación neuroquímica e o desenvolvemento de problemas de saúde crónicos como a depresión, obesidade, diabetes, hipertensión, e enfermidades coronarias.[10][11][12][13][14]
Cancro
[editar | editar a fonte]O patrón de metilación converteuse nun importante tema de investigación. Diversos estudos atoparon que en tecidos normais, a metilación dun xene está principalmente localizada na rexión codificante, que é pobre en CpG. Ao contrario, a rexión promotora do xene non está metilada, a pesar da gran densidade de illas CpG nesa rexión.
A neoplasia caracterízase por presentar un "desequilibrio de metilación" no que a hipometilación no conxunto do xenoma está acompañada por unha hipermetilación localizada e un incremento da expresión xénica da ADN metiltransferase.[15] Tipicamente, hai hipermetilación de xenes supresores de tumores e hipometilación de oncoxenes.[16] O estado de metilación global nunha célula podería tamén ser un factor que precipita a carcinoxénese, xa que as probas suxiren que a hipometilación no conxunto do xenoma pode levar a unha inestabilidade cromosómica e a un aumento das taxas de mutación.[17] O estado de metilación dalgúns xenes pode usarse como un biomarcador indicador da xénese de tumores. Por exemplo, a hipermetilación do xene da glutatión S-transferase de clase pi (GSTP1) parece ser un indicador diagnóstico prometedor do cancro de próstata.[18]
No cancro, as dinámicas xenética e epixenética do silenciamento de xenes son moi diferentes. A mutación xenética somática produce un bloqueo da produción de proteínas funcionais no alelo mutante. Se a célula obtén unha vantaxe selectiva, as células expándense clonalmente dando lugar a un tumor no cal todas as células carecen da capacidade de producir proteínas. Ao contrario, o silenciamento de xenes mediado pola epixenética prodúcese gradualmente. Empeza cunha diminución sutil na transcrición, que promove unha diminución na protección das illas CpG da expansión da heterocromatina dos flancos e a metilación nas illas. Esta perda dá lugar a un incremento gradual de sitios CpG individuais, o cal varía entre copias do mesmo xene en diferentes células.[19]
Defensa en bacterias
[editar | editar a fonte]A metilación de adenosina ou citosina é parte do sistema de restrición-modificación de moitas bacterias. Os ADNs bacterianos son metilados periodicamente por todo o xenoma. Unha metilase recoñece unha secuencia específica e metila unha das bases nese secuencia ou preto dela. Os ADN estraños (que non están metilados da mesma maneira) que se introducen na célula bacteriana son degradados por encimas de restrición específicos de secuencia. O ADN xenómico bacteriano non é recoñecido por estes encimas de restrición. A metilación do ADN nativo actúa como un tipo de sistema inmunitario primitivo, o que permite á bacteria protexerse das infeccións por bacteriófagos. Estes enicmas de restrición son a base das probas de polimorfismo de lonxitude de fragmentos de restrición (RFLP), usadas para detectar os polimorfismos de ADN.
Aplicación na diagnose prenatal
[editar | editar a fonte]Técnicas recentes de diagnóstico analizan o ADN fetal libre de células (ffDNA) que se encontra no sangue materno; porén, o ffDNA encóntrase en moi pequenas cantidades e é difícil de distinguir da maioría do ADN materno libre de células.[20] Rexións específicas do xenoma están diferencialmente metiladas se comparamos o ADN fetal co ADN materno. Por exemplo, o promotor do xene do regulador autoinmune (AIRE) está moi metilado no ADN fetal pero está submetilado no ADN materno.[21] Utilizouse a inmunoprecipitación de ADN metilado (MeDIP) para purificar o ffDNA do soro materno co propósito de facer unha diagnose prenatal da síndrome de Down.[22]
En química
[editar | editar a fonte]O termo metilación en química orgánica refírese ao proceso de alquilación usado para describir a cesión de grupos CH3.[23] Isto realízase normalmente utilizando forntes de metilos electrófilas, como iodometano, dimetil sulfato, dimetil carbonato, ou menos comunmente cos máis potentes (e perigosos) reactivos metilantes de metil triflato, diazometano ou metil fluorosulfonato (metilo máxico), que reaccionan por medio de substitución nucleofílica SN2. Por exemplo un carboxilato pode ser metilado nun oxíxeno para dar un metil éster, un sal alcóxido RO− pode ser igualmente metilado para dar un éter, ROCH3, ou unha cetona enolato pode sufrir metilación no carbono para producir unha cetona distinta.
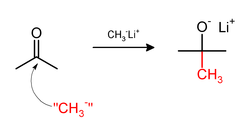
Por outra parte, a metilación pode implicar o uso de compostos de metilo nucleófilos como o metillitio (CH3Li) ou reactivos de Grignard (CH3MgX). Por exemplo, o CH3Li metilará a acetona, engadindo o metilo a través do carbonilo (C=O) para dar o alcóxido de litio do ter-butanol:
Metilación de Purdie
[editar | editar a fonte]A metilación de Purdie é un método específico de metilación en oxíxenos de carbohidratos usando iodometano e óxido de prata.[24]
5-O-metilacións
[editar | editar a fonte]- 5-O-Metilxenisteína
- 5-O-Metilmiricetina
- 5-O-Metilquercetina, tamén chamada azaleatina.
Notas
[editar | editar a fonte]- ↑ Walsh, Christopher (2006). "Chapter 5 – Protein Methylation" (PDF). Posttranslational modification of proteins: expanding nature's inventory. Roberts and Co. Publishers. ISBN 0-9747077-3-2. Arquivado dende o orixinal (PDF) o 28 de setembro de 2007. Consultado o 13 de marzo de 2015.
- ↑ Grewal, S. I.; Rice, J. C. (2004). "Regulation of heterochromatin by histone methylation and small RNAs". Current Opinion in Cell Biology 16 (3): 230–238. doi:10.1016/j.ceb.2004.04.002. PMID 15145346.
- ↑ Nakayama, J. -I.; Rice, J. C.; Strahl, B. D.; Allis, C. D.; Grewal, S. I. (2001). "Role of Histone H3 Lysine 9 Methylation in Epigenetic Control of Heterochromatin Assembly". Science 292 (5514): 110–113. doi:10.1126/science.1060118. PMID 11283354.
- ↑ Carroll, Sean B; Wessler, Susan R; Griffiths, Anthony J. F; Lewontin, Richard C (2008). Introduction to genetic analysis (9th ed.). New York: W.H. Freeman and CO. p. 403. ISBN 0-7167-6887-9.
- ↑ Mann, M. R.; Bartolomei, M. S. (2002). "Epigenetic reprogramming in the mammalian embryo: struggle of the clones". Genome Biology 3 (2): reviews1003.reviews1001. doi:10.1186/gb-2002-3-2-reviews1003.
- ↑ Woroniecki, R.; Gaikwad, A. B.; Susztak, K. (2010). "Fetal environment, epigenetics, and pediatric renal disease". Pediatric Nephrology 26 (5): 705–711. doi:10.1007/s00467-010-1714-8. PMC 3063864. PMID 21174217.
- ↑ Teif, Vladimir; Beshnova, Daria A.; Vainshtein, Yevhen; Marth, Caroline; Mallm, Jan-Philipp; Höfer, Thomas; Rippe, Karsten (8 May 2014). "Nucleosome repositioning links DNA (de)methylation and differential CTCF binding during stem cell development". Genome Research 24 (8): 1285–1295. PMID 24812327. doi:10.1101/gr.164418.113.
- ↑ Weaver, I. C. G. (2007). "Epigenetic Programming by Maternal Behavior and Pharmacological InterventionNature Versus Nurture: Let's Call the Whole Thing off". Epigenetics 2 (1): 22–28. doi:10.4161/epi.2.1.3881. PMID 17965624.
- ↑ Bird, A. (2003). "Il2 transcription unleashed by active DNA demethylation". Nature Immunology 4 (3): 208–209. doi:10.1038/ni0303-208. PMID 12605226.
- ↑ Caldji, C.; Hellstrom, I. C.; Zhang, T. Y.; Diorio, J.; Meaney, M. J. (2011). "Environmental regulation of the neural epigenome". FEBS Letters 585 (13): 2049–2058. doi:10.1016/j.febslet.2011.03.032. PMID 21420958.
- ↑ Champagne, F. A.; Curley, J. P. (2005). "How social experiences influence the brain". Current Opinion in Neurobiology 15 (6): 704–709. doi:10.1016/j.conb.2005.10.001. PMID 16260130.
- ↑ Champagne, F. A.; Weaver, I. C.; Diorio, J.; Dymov, S.; Szyf, M.; Meaney, M. J. (2006). "Maternal Care Associated with Methylation of the Estrogen Receptor- 1b Promoter and Estrogen Receptor- Expression in the Medial Preoptic Area of Female Offspring". Endocrinology 147 (6): 2909–2915. doi:10.1210/en.2005-1119. PMID 16513834.
- ↑ Felitti, V. J.; Anda, R. F.; Nordenberg, D.; Williamson, D. F.; Spitz, A. M.; Edwards, V.; Koss, M. P.; Marks, J. S. (1998). "Relationship of Childhood Abuse and Household Dysfunction to Many of the Leading Causes of Death in Adults". American Journal of Preventive Medicine 14 (4): 245–258. doi:10.1016/S0749-3797(98)00017-8. PMID 9635069.
- ↑ McEwen, B. S.; Gianaros, P. J. (2010). "Central role of the brain in stress and adaptation: Links to socioeconomic status, health, and disease". Annals of the New York Academy of Sciences 1186: 190–222. doi:10.1111/j.1749-6632.2009.05331.x. PMC 2864527. PMID 20201874.
- ↑ Baylln, S. B.; Herman, J. G.; Graff, J. R.; Vertino, P. M.; Issa, J. P. (1997). "Alterations in DNA Methylation: A Fundamental Aspect of Neoplasia". Advances in Cancer Research Volume 72. Advances in Cancer Research 72. p. 141. doi 10.1016/S0065-230X(08)60702-2. ISBN 978-0-12-006672-8.
- ↑ Gonzalo S (2010). "Epigenetic alterations in aging". Journal of Applied Physiology 109 (2): 586–597. PMC 2928596. PMID 20448029. doi:10.1152/japplphysiol.00238.2010. Arquivado dende o orixinal o 13 de agosto de 2014. Consultado o 13 de marzo de 2015.
- ↑ Jaenisch, R.; Pettersson, R. Z.; Beard, U.; Jackson-Grusby, C.; Jaenisch, L. (1998). "DNA hypomethylation leads to elevated mutation rates". Nature 395 (6697): 89–93. doi:10.1038/25779. PMID 9738504.
- ↑ Nakayama, M.; Gonzalgo, M. L.; Yegnasubramanian, S.; Lin, X.; De Marzo, A. M.; Nelson, W. G. (2004). "GSTP1 CpG island hypermethylation as a molecular biomarker for prostate cancer". Journal of Cellular Biochemistry 91 (3): 540–552. doi:10.1002/jcb.10740. PMID 14755684.
- ↑ Jones, Peter A.; Baylin, Stephen B. (2002). "The fundamental role of epigenetic events in cancer". Nature Reviews Genetics 3: 415–428. doi:10.1038/nrg816. PMID 12042769.
- ↑ Papageorgiou, E. A.; Karagrigoriou, A.; Tsaliki, E.; Velissariou, V.; Carter, N. P.; Patsalis, P. C. (2011). "Fetal-specific DNA methylation ratio permits noninvasive prenatal diagnosis of trisomy 21". Nature Medicine 17 (4): 510–513. doi:10.1038/nm.2312. PMID 21378977.
- ↑ Old, R. W.; Crea, F.; Puszyk, W.; Hultén, M. A. (2007). "Candidate epigenetic biomarkers for non-invasive prenatal diagnosis of Down syndrome". Reproductive BioMedicine Online 15 (2): 227–235. doi:10.1016/S1472-6483(10)60713-4. PMID 17697502.
- ↑ Kyriakou, S.; Kypri, E.; Spyrou, C.; Tsaliki, E.; Velissariou, V.; Papageorgiou, E. A.; Patsalis, P. C. (2013). "Variability of ffDNA in maternal plasma does not prevent correct classification of trisomy 21 using MeDIP-qPCR methodology". Prenatal Diagnosis 33 (7): 650–655. doi:10.1002/pd.4140. PMID 23619923.
- ↑ March, Jerry; Smith, Michael W (2001). March's advanced organic chemistry: reactions, mechanisms, and structure. New York: Wiley. ISBN 0-471-58589-0.
- ↑ Purdie, T.; Irvine, J. C. (1903). "C.?The alkylation of sugars". Journal of the Chemical Society, Transactions 83: 1021. doi:10.1039/CT9038301021.
Véxase tamén
[editar | editar a fonte]| Commons ten máis contidos multimedia sobre: Metilación |
Outros artigos
[editar | editar a fonte]- Alquilación
- Secuenciación de bisulfito – o método bioquímico usado para determinat a presenza ou ausencia de grupos metilo nunha secuencias de ADN
- MethDB Base de datos de metilación do ADN
- Termoforese de microescala – un método biofísico para determinar o estado de metilación do ADN[1]
Ligazóns externas
[editar | editar a fonte]- deltaMasses Detección de metilacións e espectrometría de masas
- ↑ Wienken CJ, Baaske P, Duhr S, Braun D (2011). "Thermophoretic melting curves quantify the conformation and stability of RNA and DNA". Nucleic Acids Research 39 (8): e52–e52. doi:10.1093/nar/gkr035.