Bioloxía do desenvolvemento

A bioloxía do desenvolvemento é o estudo do proceso polo cal os animais e plantas crecen e se desenvolven desde as súas etapas embrionarias, e é sinónimo de ontoxenia. Nos animais a maioría do desenvolvemento ten lugar na vida embrionaria, pero tamén se produce en procesos como a rexeneración, reprodución asexual e metamorfose, e no crecemento e diferenciación de células nai no organismo adulto. Nas plantas o desenvolvemento ocorre no embrión, durante a reprodución vexetativa, e no crcemento normal das raíces, talos e flores, gromos. Os resultados prácticos do estudo da bioloxía do desenvolvemento animal inclúen a fecundación in vitro, moi usada hoxe nos tratamentos de fertilidade, a comprensión dos riscos das substancias que poden danar ao feto (teratóxenos), e a creación de varios modelos animais para doenzas humanas, que son útiles en investigación. A bioloxía do desenvolvemento tamén axudou a xerar a moderna bioloxía das células nai, que promete ter moitos beneficios prácticos no campo da saúde humana.
Perspectivas[editar | editar a fonte]
Os principais procesos implicados no desenvolvemento embrionario dos animais son: especificación rexional, morfoxénese, diferenciación celular, crecemento, e o control global da temporalización dos procesos. A especificación rexional refírese a procesos que crean patróns espaciais nunha bóla ou capa de células inicialmente similares. Para isto xeralmene cómpre a acción de determinantes citoplásmicos, localizados en partes do ovo fertilizado, e de sinais indutivos emitidos desde os centros de sinalización do embrión. Os estadios iniciais da especificación rexional non xeran células diferenciadas funcionais, senón as poboacións celulares destinadas a desenvolver unha rexión específica ou parte do organismo. Estas son definidas pola expresión de combinacións específicas de factores de transcrición. A morfoxénese relaciónase coa formación da forma tridimensional. Implica principalmente os movementos orquestrados das follas ou capas celulares e de células individuais. A morfoxénese é importante para crear as tres capas xerminais do embrión temperán (ectoderma, mesoderma e endoderma) e para construír estruturas complexas durante o desenvolvemento de órganos. A diferenciación celular relaciónase especificamente coa formación de tipos de células funcionais como nervios, músculo, epitelio secretor etc. As células diferenciadas conteñen grandes cantidades de proteínas específicas asociadas coa función celular. O crecemento implica tanto un incremento no tamaño global, coma tamén o crecemento diferencial de partes (alometría) que contribúe á morfoxénese. O crecemento ocorre principalmente por medio de división celular pero tamén por medio de cambios no tamaño celular e a deposición de materiais extracelulares. O control da temporalización de eventos e a integración de varios procesos é a área menos coñecida do asunto. Segue sen aclararse se os embriósn animais conteñen un mecanismo de reloxo mestre ou non. O desenvolvemento das plantas implica procesos similares aos dos animais. Aínda que as células de plantas son normalmente inmóbiles, a súa morfoxénese realízase por crecemento diferencial, sen que haxa movementos celulares. Ademais, os sinais indutivos e os xenes implicados no desenvolvemento das plantas son diferentes dos que controlan o desenvolvemeno animal.
Organismos modelo para o desenvolvemento[editar | editar a fonte]
Gran parte da investigación en bioloxía do desenvolvemento das últimas décadas fíxose utilizando un pequeno número de organismos modelo. Os resultados indicaron que hai moita máis conservación de mecanismos de desenvolvemento no reino animal. Nas etapas iniciais do desenvolvemento as diferentes especies de vertebrados usan os mesmos sinais indutivos e os mesmos xenes que codifican a identidade rexional. Mesmo os invertebrados usan un repertorio similar de sinais e xenes aínda que as partes do corpo formadas son significativamente diferentes. Cada organismo modelo ten determinadas vantaxes experimentais que fixeron que moitos investigadores recorresen a eles. En certo sentido son "modelos" para todo o reino animal, e noutro sentido son "modelos" para o desenvolvemento humano, que é difícil de estudar directamente por razóns éticas e prácticas. Os organismos modelos foron máis útiles para esclarecer a natureza xeral dos mecanismos do desenvolvemento. Canto máis detalles se buscan, máis difiren uns dos outros e dos humanos.
Vertebrados:
- Ras: Xenopus (X. laevis e X. tropicalis).[1][2] Boa subministración de embrións. Especialmente axeitado para microcirurxía.
- Peixe cebra: Danio rerio.[3] Boa subministración de embrións. Xenética ben desenvolvida.
- Polos: Gallus gallus.[4] Estadios iniciais similares aos dos mamíferos, pero a microcirurxía é máis doada de facer. Baratos.
- Rato: Mus musculus.[5] Mamífero cunha xenética ben desenvolvida.
Invertebrados:
- Mosca do vinagre: Drosophila melanogaster.[6] Boa subministración de embrións. Xenética ben desenvolvida.
- Nematodos: Caenorhabditis elegans.[7] Boa subministración de embrións. Xenética ben desenvolvida. Baratos.
O ourizo de mar é tamén bastante usado para algúns propósitos,[8] igual que as ascidias.[9] Para estudos de rexeneración utilízanse anfibios urodelos como o axolote Ambystoma mexicanum,[10] e tamén vermes planarias como Schmidtea mediterranea.[11] O estudo do desenvolvemento das plantas enfocouse na especie Arabidopsis thaliana como organismo modelo.[12]
Procesos de desenvolvemento[editar | editar a fonte]
Desenvolvemento embrionario en animais[editar | editar a fonte]
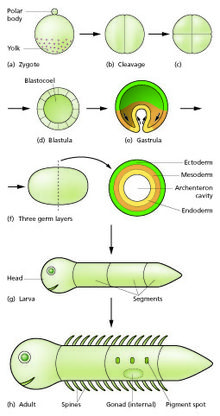

O espermatozoide e o óvulo fusiónanse no proceso de fertilización para formar un ovo fertilizado ou cigoto.[13] Ese experimenta un período de divisións para formar unha bóla ou lámina de células similares chamado blástula ou blastoderma. Estas divisións celulares son normalmente rápidas e sen crecemento do tamaño celular, polo que as células fillas son da metade do tamaño da célula nai e o embrión no seu conxunto mentense inicialmente co mesmo tamaño. Estas dividións denomínanse divisións de segmentación ou clivaxe. Os movementos morfoxenéticos converten a masa de células nunha estrutura de tres capas que consta de capas multicelulars chamadas ectoderma, mesoderma e endoderma, que se coñecen como capas xerminais. Este é o proceso de gastrulación. Durante a segmentación e a gastrulación ocorren os primeiros eventos de especificación rexional. Ademais da formación das tres capas xerminais, estas a miúdo xeran estruturas extraembrionais, como a placenta dos mamíferos, necesaria para o sostén e nutrición do embrión,[14] e tamén establecen diferenzas no destino das células ao longo do eixe anteroposterior (cabeza, tronco e cola).[15]
A especificación rexional iníciase pola presenza de determinantes citoplasmáticos nunha parte do cigoto. As células que conteñen o determinante convértense nun centro sinalizador e emiten un factor indutor. Como o factor indutor se produce nun lugar, difunde desde alí, e vai diminuíndo, formando un gradiente de concentración, alto cerca das fontes que son a fonte do factor e baixo máis lonxe.[16][17] As células restantes do embrión, que non conteñen o determinante, son competentes para responder a diferentes concentracións pola regulación á alza de xenes de control do desenvolvemento específicos. Isto ten como resultado unha serie de zonas que se van establecendo, situadas a distancias progresivamente maiores do centro sinalizador. En cada zona está regulada á alza unha diferente combinación de xenes de control do desenvolvemento.[18] Estes xenes codifican factores de trranscrición que regulan á alza novas combinacións de actividades de xenes en cada rexión. Entre outras funcións, estes factores de transcrición controlan a expresión de xenes que confiren propiedades específicas de adhesión e motilidade nas células nas que son activos. Debido a estas propiedades morfoxenéticas diferentes, as células de cada capa xerminal móvense para formar láminas ou follas como o ectoderma, que acaba por fóra, o mesoderma, que queda no medio, e o endoderma, que queda no interior.[19][20] Os movementos morfoxenéticos non só cambian a forma e estrutura do embrión, senón que ao poñeren capas de células en novas relacións espaciais tamén fan posibles novas fases de sinalización e resposta entre elas.
O crecemento dos embrións é principalmente autónomo.[21] Para cada territorio de células a taxa de crecemento está controlada pola combinación de xenes que están activos. Os embrións de vida libre non crecen en masa, xa que non teñen unha fonte externa que lles subministre nutrición. Pero os embrións alimentados a través dunha placenta ou por unha subministración de xema extraembrionaria poden crecer moi rápido, e neses organismos os cambios nas taxas de crecemento relativo entre distintas partes contribúen a producir a anatomía global final.
O proceso completo ten que ser coordinado no tempo e non se coñece como se produce ese control. Pode haber un reloxo mestre con capacidade de comunicarse con todas as partes do embrión que controle o curso do que vai ocorrendo, ou a temporalización pode depender simplemente de secuencias de eventos locais causais.[22]
Diferenciación celular[editar | editar a fonte]
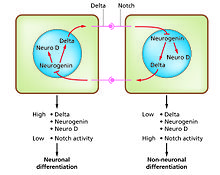
A diferenciación celular é o proceso no que se orixinan tipos de células funcional e/ou morfoloxicamente diferentes no desenvolvemento. Por exemplo, as neuronas, fibras musculares e hepatocitos son tipos de células diferenciadas. As células diferenciadas xeralmente producen grandes cantidades dunhas poucas proteínas que son necesarias polas súas específicas funcións, e isto dálles a aparencia característica que permite recoñecelas ao microscopio óptico. Os xenes que codifican estas proteínas son moi activos. A súa estrutura cromatínica é moi aberta, dando libre acceso a encimas de transcrición, e a factores de transcrición específicos unidos a secuencias reguladoras no ADN para activar a súa expresión.[23][24] Por exemplo, NeuroD é un factor de transcrición clave para a diferenciación neuronal, a mioxenina éo para a diferenciación muscuar, e o HNF4 para a diferenciación dos hepatocitos. A diferenciación celular é xeralmente o estadio final do desenvolvemento, precedido por varios estadios nos que as células quedan comprometidas a un destino e que non están visiblemente diferenciados. Un só tecido, formado a partir dun só tipo de células proxenitoras ou céllas nais, a miúdo consiste en varios tipos de células diferenciadas. O control da súa formación implica un proceso de inhibición lateral,[25] baseado nas propiedades do sistema de sinalización Notch-Delta.[26] Por exemplo, na placa neural do embrión este sistema opera xerando unha poboación de células precursoras neuronais nas cales NeuroD ten unha alta expresión.
Rexeneración[editar | editar a fonte]
A rexeneración indica a capacidade de volver facer crecer unha parte do corpo perdida.[27] Isto é moi patente nas plantas, que presentan un crecemento continuo, e tamén en animais coloniais como os hidroides e as ascidias. Pero o maior interese para a bioloxía do desenvolvemento é a rexeneración de partes en animais de vida libre. En particular catro modelos foron os máis investigados. Dous destes modelos teñen a capacidade de rexenerar o corpo completo: a Hydra, que pode rexenerar calquera parte do pólipo a partir dun pequeno fragmento,[28] e os vermes planarias, que poden xeralmente rexenerar tanto as "cabezas" coma as colas.[11] Ambos os exemplos destes exemplos teñen un continuo recambio celular a partir de células nai e, polo menos nas planarias, sábese que algunhas das células nai son pluripotentes.[29] Os outros dous modelos mostran só a rexeneración distal dos apéndices, e son os apéndices de insectos, xeralmene as patas dos insectos hemimetábolos como o grilo,[30] e as patas de anfibios urodelos.[31] Disponse dunha considerable cantidade de información sobre a rexeneración de patas de anfibios e cada tipo celular rexenérase a si mesmo, agás no caso dos tecidos conectivos, onde hai unha considerable interconversión entre cartilaxes, derma e tendóns. En termos do patrón de estruturas, isto é controlado por unha reactivación de sinais activa no embrión. Aínda se debate sobre a vella cuestión de se a rexeneración é unha propiedade "prístina" ou "adaptiva".[32] Se é certo o primeiro caso, coñecendo mellor os procesos, podería esperarse conseguir mellorar a capacidade rexenerativa en humanos. Se é correcto o segundo caso, entón cada exemplo de rexeneración teríase orixinado por selección natural en circunstancias particulares de cada especie, polo que non se esperaría que houbese regras xerais para o proceso.
Metamorfose[editar | editar a fonte]
Os procesos de desenvolvemento son moi evidentes durante o proceso da metamorfose. Isto ocorre en varios tipos de animais. Son ben coñecidos os exemplos das ras, que normalmente eclosionan en forma de cágados e sofren unha metamorfose para converterse en ras adultas, e a de certos insectos que eclosionan como larvas e despois son remodeladas á forma adulta durante o estadio pupal.
Todos os procesos de desenvolvemento mencionados ata agora ocorren durante a metamorfose. Exemplos que foron estudados en detalle inclúen a perda da cola e outros cambios nos cágados da ra Xenopus,[33][34] e a bioloxía dos discos imaxinais, que xeran as partes do corpo adulto da mosca Drosophila melanogaster.[35][36]
Notas[editar | editar a fonte]
- ↑ Nieuwkoop, P.D. and Faber, J. (1967) Normal table of Xenopus laevis (Daudin). North-Holland, Amsterdam.
- ↑ Harland, R.M. and Grainger, R.M. (2011) Xenopus research: metamorphosed by genetics and genomics. Trends in Genetics 27, 507-515.
- ↑ Lawson, N. D. and Wolfe, S. A. (2011) Forward and Reverse Genetic Approaches for the Analysis of Vertebrate Development in the Zebrafish. Developmental Cell 21, 48-64.
- ↑ Hassan Rashidi, V.S. (2009) The chick embryo: hatching a model for contemporary biomedical research. BioEssays 31, 459-465.
- ↑ Behringer, R., Gertsenstein, M, Vintersten, K. and Nagy, M. (2014) Manipulating the Mouse Embryo. A Laboratory Manual, Fourth Edition. Cold Spring Harbor, NY: Cold Spring Harbor Laboratory Press.
- ↑ St Johnston, D. (2002) The art and design of genetic screens: Drosophila melanogaster. Nat Rev Genet 3, 176-188.
- ↑ Riddle, D.L., Blumenthal, T., Meyer, B.J. and Priess, J.R. (1997) C.elegans II. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY.
- ↑ Ettensohn, C.A. and Sweet, H.C. (2000) Patterning the early sea urchin embryo. Curr. Top. Dev. Biol. 50, 1-44.
- ↑ Lemaire, P. (2011) Evolutionary crossroads in developmental biology: the tunicates. Development 138, 2143-2152.
- ↑ Nacu, E. and Tanaka, E.M. (2011) Limb Regeneration: A New Development? Annual Review of Cell and Developmental Biology 27, 409-440.
- ↑ 11,0 11,1 Reddien, P.W. and Alvarado, A.S. (2004) Fundamentals of planarian regeneration. Annual Review of Cell and Developmental Biology 20, 725-757.
- ↑ Weigel, D. and Glazebrook, J. (2002) Arabidopsis. A Laboratory Manual. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY.
- ↑ Jungnickel, M.K., Sutton, K.A. and Florman, H.M. (2003) In the beginning: lessons from fertilization in mice and worms. Cell 114, 401-404
- ↑ Steven, D.H.(ed.) (1975) Comparative Placentation. Academic Press, London
- ↑ Kimelman, D. and Martin, B.L. (2012) Anterior-posterior patterning in early development: three strategies. Wiley Interdisciplinary Reviews-Developmental Biology 1, 253-266.
- ↑ Slack, J.M.W. (1987). Morphogenetic gradients - past and present. Trends in Biochemical Sciences 12, 200-204
- ↑ Rogers, K. W. and Schier, A. F. (2011). Morphogen Gradients: From Generation to Interpretation. Annual Review of Cell and Developmental Biology 27, 377-407
- ↑ Dahmann, C., Oates, A. C. and Brand, M. (2011). Boundary formation and maintenance in tissue development. Nat Rev Genet 12, 43-55
- ↑ Hardin, J. and Walston, T. (2004) Models of morphogenesis: the mechanisms and mechanics of cell rearrangement. Current Opinion in Genetics and Development 14, 399-406
- ↑ Hammerschmidt, M. and Wedlich, D. (2008). Regulated adhesion as a driving force of gastrulation movements. Development 135, 3625-3641
- ↑ O'Farrell, P. H. (2003). How metazoans reach their full size: the natural history of bigness. In Cell Growth: Control of Cell Size, (ed. M. N. Hall, Raff, M., and Thomas, G. (eds)), pp. 1-21: Cold Spring Harbor Laboratory Press
- ↑ Moss, E.G. and Romer-Seibert, J. (2014) Cell-intrinsic timing in animal development. Wiley Interdisciplinary Reviews-Developmental Biology 3, 365-377.
- ↑ Li, B., Carey, M. and Workman, J.L. (2007) The role of chromatin during transcription. Cell 128, 707-719.
- ↑ Heintzman, N.D., et al. (2007) Distinct and predictive chromatin signatures of transcriptional promoters and enhancers in the human genome. Nat Genet 39, 311-318.
- ↑ Meinhardt, H. and Gierer, A. (2000) Pattern formation by local self-activation and lateral inhibition. Bioessays 22, 753-760.
- ↑ Sprinzak, D., et al. (2010) Cis-interactions between Notch and Delta generate mutually exclusive signalling states. Nature 465, 86-90.
- ↑ Carlson, B.M. (2007) Principles of Regenerative Biology. Academic Press, Burlington MA.
- ↑ Bosch, T.C.G. (2007) Why polyps regenerate and we don't: Towards a cellular and molecular framework for Hydra regeneration. Developmental Biology 303, 421-433.
- ↑ Wagner, D.E., Wang, I.E. and Reddien, P.W. (2011) Clonogenic Neoblasts Are Pluripotent Adult Stem Cells That Underlie Planarian Regeneration. Science 332, 811-816.
- ↑ Nakamura, T., et al. (2008). Dissecting insect leg regeneration through RNA interference. Cellular and Molecular Life Sciences 65, 64-72.
- ↑ Simon, A. and Tanaka, E.M. (2013) Limb regeneration. Wiley Interdisciplinary Reviews-Developmental Biology 2, 291-300.
- ↑ Slack, J.M.W. (2013) Essential Developmental Biology. Chapter 20. Wiley-Blackwell, Oxford.
- ↑ Tata, J.R. (1996) Amphibian metamorphosis: an exquisite model for hormonal regulation of postembryonic development in vertebrates. Dev. Growth Diffn. 38, 223-231
- ↑ Brown, D.D. and Cai, L. (2007) Amphibian metamorphosis. Developmental Biology 306, 20-33
- ↑ Cohen, S.M. (1993) Imaginal Disc Development. In Bate and Martinez-Arias (eds.), The Development of Drosophila melanogaster, Cold Spring Harbor Press
- ↑ Maves, L. and Schubiger, G. (2003) Transdetermination in Drosophila imaginal discs: a model for understanding pluripotency and selector gene maintenance. Current Opinion in Genetics & Development 13, 472-479
Véxase tamén[editar | editar a fonte]
Bibliografía[editar | editar a fonte]
- Gilbert, S. F. (2013). Developmental Biology. Sunderland, Mass.: Sinauer Associates Inc.
- Slack, J. M. W. (2013). Essential Developmental Biology. Oxford: Wiley-Blackwell.
- Wolpert, L. e Tickle, C. (2011). Principles of Development. Oxford e Nova York: Oxford University Press.
Outros artigos[editar | editar a fonte]
- Embrioxénese
- Embrioloxía
- Bioloxía evolutiva do desenvolvemento
- Ontoxenia
- Bioloxía evolutiva do desenvolvemento das plantas
