Lactato deshidroxenase
| Lactato deshidroxenase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Número EC | 1.1.1.27 | ||||||||
| Número CAS | 9001-60-9 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| Gene Ontology | AmiGO / EGO | ||||||||
| |||||||||

| |
| Lactato deshidroxenase M4 humana (o isoencima que se encontra no músculo esquelético). De PDB 1I10. | |
lactato deshidroxenase A (subunidade M)
| |
| Identificadores | |
| Símbolo | LDHA |
| Símbolos alt. | LDHM |
| Entrez | 3939 |
| HUGO | 6535 |
| OMIM | |
| RefSeq | NM_005566 |
| UniProt | P00338 |
| Outros datos | |
| Número EC | 1.1.1.27 |
| Locus | Cr. 11 p15.4 |
lactato deshidroxenase B (subunidade H)
| |
| Identificadores | |
| Símbolo | LDHB |
| Símbolos alt. | LDHL |
| Entrez | 3945 |
| HUGO | 6541 |
| OMIM | |
| RefSeq | NM_002300 |
| UniProt | P07195 |
| Outros datos | |
| Número EC | 1.1.1.27 |
| Locus | Cr. 12 p12.2-12.1 |
lactato deshidroxenase C
| |
| Identificadores | |
| Símbolo | LDHC |
| Entrez | 3948 |
| HUGO | 6544 |
| OMIM | |
| RefSeq | NM_002301 |
| UniProt | P07864 |
| Outros datos | |
| Número EC | 1.1.1.27 |
| Locus | Cr. 11 p15.5-15.3 |
| Lactato deshidroxenase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
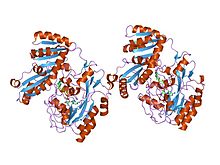 Estrutura cristalina da D-lactato deshidroxenase, un encima respiratorio de membrana periférico. | |||||||||
| Identificadores | |||||||||
| Símbolo | Lact-deh-memb | ||||||||
| Pfam | PF09330 | ||||||||
| Pfam clan | CL0277 | ||||||||
| InterPro | IPR015409 | ||||||||
| SCOPe | 1f0x / SUPFAM | ||||||||
| |||||||||
A lactato deshidroxenase ou L-lactato deshidroxenase (LDH ou LD) é un encima que se encontra en animais, plantas e procariotas, que intervén na fermentación homoláctica. Como deshidroxenase que é transfire un hidróxeno dunha molécula a outra. En concreto, a lactato deshidroxenase cataliza a conversiónn reversible do piruvato en lactato e á vez converte o coencima NADH na súa forma oxidada NAD+.
A lactato deshidroxenase ten importancia médica porque se encontra abundantemente nos tecidos corporais, como o músculo e células do sangue. Como se libera cando hai danos nos tecidos, serve como marcador de lesións e doenzas comúns.
O coencima que actúa con este encima é normalmente o NADH, pero pode actuar tamén o NADP, aínda que máis lentamente, no encima animal, pero non no bacteriano.[1]
Este artigo trata sobre a L-lactato deshidroxenase dependente de NAD(P) (EC1.1.1.27, e nome sistemático (S)-lactato:NAD+ oxidorredutase), pero existen outras clases de lactato deshidroxenase, que poden actuar sobre o D-lactato ou o L-lactato e ser dependentes do citocromo c ou do NAD(P), entre as que están: D-lactato deshidroxenase (citrocromo) (EC: 1.1.2.4), D-lactato deshidroxenase dependente de NAD(P) (EC: 1.1.1.28), e L-lactato deshidroxenase (citocromo) (EC: 1.1.2.3).
Reaccións[editar | editar a fonte]

A lactato deshidroxenase cataliza a interconversión reversible do piruvato e o lactato á vez que se interconverten o NADH e o NAD+. O piruvato é o produto final da glicólise, que cando non hai oxíxeno ou é moi escaso, fermenta a lactato. Despois, realízase a reacción inversa durante o ciclo de Cori no fígado. A altas concentracións de lactato, o encima mostra inhibición por retroalimentación, e a velocidade de conversión do piruvato en lactato diminúe.
Tamén pode catalizar a deshidroxenación do 2-hidroxibutirato, pero é un substrato moito peor que o lactato para o encima. Ten moi pouca ou ningunha actividade co beta-hidroxibutirato.
Regulación do encima[editar | editar a fonte]
Esta proteína pode usar o modelo da morfeeína de regulación alostérica.[2]
Hipoglicemia inducida por etanol[editar | editar a fonte]
O etanol pode afectar indirectamente á actividade deste encima. O etanol é deshidroxenado a acetaldehido pola alcohol deshidroxenase, e despois este é transformado en acetato pola acetaldehido deshidroxenase. Durante esta reacción prodúcense 2 NADH. Se están presentes grandes cantidades de etanol, prodúcense grandes cantidades de NADH, o que orixina unha depleción do NAD+ celular. Deste xeito, a conversión de piruvato en lactato increméntase debido á rexeneración asociada do NAD+ que se produce. Por tanto, pode ocorrer unha acidose láctica metabólica no envelenamento por etanol.
O incremento da proporción NADH/NAD+ tamén pode causar hipoglicemia nun individuo en xaxún que estivo bebendo e é dependente da gliconeoxénese para manter os niveis de glicosa sanguínea. A alanina e o lactato son importantes precursores gliconeoxénicos que entran na gliconeoxénese en forma de piruvato. A proporción alta NADH/NAD+ cambia o equilibrio da lactato deshidroxenase cara ao lactato, para que se forme menos piruvato e, por tanto, diminúa a gliconeoxénese.
Isoencimas[editar | editar a fonte]
A lactato deshidroxenase funcional é un homo ou heterotetrámero composto polas subunidades M e H codificadas polos xenes LDHA do cromosoma 11 e LDHB do cromosoma 12, respectivamente. As posibles isoencimas son:
- LDH-1 (4H) — presente no corazón e glóbulos vermellos do sangue
- LDH-2 (3H1M) — no sistema reticuloendotelial
- LDH-3 (2H2M) — nos pulmóns
- LDH-4 (1H3M) — nos riles, placenta, e páncreas
- LDH-5 (4M) — no fígado e músculo esquelético[3]
O principal isoencima presentes no fígado e músculo esquelético é o M4, que ten catro subunidades M (M do inglés muscle), mentres que o isoencima H4 é o principal na maioría das especies no corazón, con 4 subunidades H (H de heart). As outras variantes conteñen as dúas subunidades en diferentes proporcións, polo que son heterotetrámeras.
Xeralmente a LDH-2 é a forma predominante no soro sanguíneo. Un nivel de LDH-1 máis alto que o de LDH-2 (un "patrón invertido" con respecto ao normal) suxire infarto de miocardio (as lesións cardíacas liberan a LDH cardíaca LDH-1, no torrente sanguíneo).
Xenética en humanos[editar | editar a fonte]
As subunidades M e H están codificadas en dous xenes diferentes:
- A subunidade M está codificada polo xene LDHA, localizado no cromosoma 11 na posición 11p15.4 (OMIM 150000)
- A subunidade H está codificada no xene LDHB, localizado no cromosoma 12 na posición 12p12.2-p12.1 (OMIM 150100)
- Coñécese unha trerceira isoforma chamada LDHC ou LDHX, que se expresa só nos testículos (OMIM 150150). O seu xene é probablemente un duplicado do LDHA e está tamén localizado no cromosoma 11 na posición 11p15.5-p15.3.
As mutacións na subunidade M foron asociadas á rara enfermidade chamada mioglobinuria do esforzo, e describíronse mutacións da subunidade H, pero non parecen producir doenzas.
Uso médico[editar | editar a fonte]
A LDH é unha proteína que normalmente aparece en todo o corpo en pequenas cantidades. Moitos cancros poden aumentar os niveis de LDH, polo que a LDH pode utilizarse como un marcador de tumores, pero ao mesmo tempo, non é útil para identificar o tipo de cancro. A medida dos niveis de LDH pode ser útil para monitorizar o tratamento dun cancro. Condicións non cancerosas que tamén elevan os niveis de LDH son a insuficiencia cardíaca, hipotiroidismo, anemia, e enfermidades pulmonares ou hepáticas.[4]
A descomposición dos tecidos libera LDH, e, por tanto, pode medirse a LDH para coñecer o grao de descomposición do tecido, por exemplo hemólise. Outros trastornos indicados por niveis elevados de LDH son cancro, meninxite, encefalite, pancreatite aguda, e infección por VIH. A LDH mídese polo test da lactato deshidroxenase (LDH). A comparación dos valores de LDH medidos cos normais axuda á diagnose.[5]
Hemólise[editar | editar a fonte]
En medicina, a LDH utilízase a miúdo como marcador da descomposición de tecidos, e como a LDH é abundante nos glóbulos vermellos pode funcionar como marcador para a hemólise. Unha mostra de sangue que foi manipulada incorrectamente pode dar un falso positivo indicando altos niveis de LDH debido ao dano sufrido polos glóbulos vermellos pola mala manipulación.
Pode utilizarse tamén como marcador para o infarto de miocardio. Despois dun infarto, os niveis de LDH chegan a un máximo aos 3–4 días e permanecen elevados durante 10 días. Deste modo, os niveis elevados de LDH (nos que o nivel de LDH1 é máis alto que o de LDH2) poden ser útiles para determinar se un paciencte tivo un infarto de miocardio se o examinan os doutores días despois do episodio de dor de peito.
Renovación de tecidos[editar | editar a fonte]
Outros usos son a avaliación da necrose nos tecidos en xeral; isto pódese aplicar cando non hai outros indicadores de hemólise. Utilízase para facer un seguimento do cancro (especialmente en pacientes de linfoma), xa que as células cancerosas teñen un alto grao de renovación e as células destruídas orixinan un nivel elevado de LDH.
Exsudados e transudados[editar | editar a fonte]
A medida da LDH en fluídos aspirados dun derramamento pleural ou pericárdico poden axudar a distinguir entre exsudados (fluídos segregados activamente, por exemplo, debido á inflamación) ou transudados (fluídos segregados pasivamente, debido a unha alta presión hidrostática ou a unha baixa presión oncótica). O criterio usual é que unha proporción de LDH no fluído con respecto ao límite superior de LDH normal no soro de máis de 0,6[6] ou 2/3[7] indica un exsudado, mentres que unha proporción menor indica un transudado. Os distintos laboratorios teñen diferentes valores como límite superiro de LDH no soro, pero son exemplos 200[8] e 300[8] IU/L.[9] Nun empiema (pus nunha cavidade anatómica natural), os niveis de LDH, en xeral, exceden as 1000 IU/L.
Meninxite e encefalite[editar | editar a fonte]
Niveis altos de LDH no líquido cefalorraquídeo están asociados a miúdo coa meninxite bacteriana.[10] En casos de meninxite vírica, uns niveis altos de LDH, en xeral, indican a presenza de encefalite e un mal prognóstico.
VIH[editar | editar a fonte]
A LDH mídese con frecuencia en pacientes de VIH como un marcador non específico para a pneumonía por Pneumocystis (PCP), causada por Pneumocystis jirovecii. Unha elevada LDH no marco de síntomas respiratorios das vías superiores nun paciente de VIH suxiren unha PCP (pero non a diagnostican con certeza). Porén, nos pacientes VIH positivos con síntomas respiratorios, un nivel moi alto de LDH (>600 IU/L) indicou histoplasmose nun estudo de 120 pacientes de PCP e 30 de histoplasmose.[11]
Notas[editar | editar a fonte]
- ↑ BRENDA EC 1.1.1.27 L-lactate dehydrogenase
- ↑ Selwood T, Jaffe EK (2012). "Dynamic dissociating homo-oligomers and the control of protein function". Arch. Biochem. Biophys. 519 (2): 131–43. PMC 3298769. PMID 22182754. doi:10.1016/j.abb.2011.11.020.
- ↑ Van Eerd, J. P. F. M.; Kreutzer, E. K. J. (1996). Klinische Chemie voor Analisten deel 2. pp. 138–139. ISBN 978-90-313-2003-5.
- ↑ Stanford Cancer Center. "Cancer Diagnosis - Understanding Cancer". Understanding Cancer. Stanford Medicine.
- ↑ "Lactate dehydrogenase test: MedlinePlus Medical Encyclopedia". MedlinePlus. U.S. National Library of Medicine.
- ↑ Heffner JE, Brown LK, Barbieri CA (1997). "Diagnostic value of tests that discriminate between exudative and transudative pleural effusions. Primary Study Investigators". Chest 111 (4): 970–80. PMID 9106577. doi:10.1378/chest.111.4.970.
- ↑ Light RW, Macgregor MI, Luchsinger PC, Ball WC (1972). "Pleural effusions: the diagnostic separation of transudates and exudates". Ann. Intern. Med. 77 (4): 507–13. PMID 4642731. doi:10.7326/0003-4819-77-4-507.
- ↑ 8,0 8,1 Joseph J, Badrinath P, Basran GS, Sahn SA (2001). "Is the pleural fluid transudate or exudate? A revisit of the diagnostic criteria". Thorax 56 (11): 867–70. PMC 1745948. PMID 11641512. doi:10.1136/thorax.56.11.867.
- ↑ Joseph J, Badrinath P, Basran GS, Sahn SA (2002). "Is albumin gradient or fluid to serum albumin ratio better than the pleural fluid lactate dehydroginase in the diagnostic of separation of pleural effusion?". BMC Pulm Med 2: 1. PMC 101409. PMID 11914151. doi:10.1186/1471-2466-2-1.
- ↑ Stein JH (1998). Internal Medicine. Elsevier Health Sciences. pp. 1408–. ISBN 978-0-8151-8698-4. Consultado o 12 August 2013.
- ↑ Butt AA, Michaels S, Greer D, Clark R, Kissinger P, Martin DH (2002). "Serum LDH level as a clue to the diagnosis of histoplasmosis". AIDS Read 12 (7): 317–21. PMID 12161854.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
- Deshidroxenase
- Oxidorredutase
- D-lactato deshidroxenase
- L-lactato deshidroxenase (citocromo)
- D-lactato deshidroxenase (citrocromo)
Este artigo incorpora contidos en dominio público de Pfam e InterPro IPR015409
