Cloruro de hidróxeno
| |
|
Xeral | |
|---|---|
| Nome | Cloruro de hidróxeno |
| Outros nomes | (disolto en auga)Ácido clorhídrico |
| Fórmula química | HCl |
| Aparencia | Gas incoloro, higroscópico. |
| Número CAS | [7647-01-0] |
|
Físicas | |
| Masa molecular | 36,4606 uma |
| Punto de fusión | 158,8 K (-114,2 °C). |
| Punto de ebulición | 187,9 K (-85,1 °C). |
| Densidade | 1,477 kg/m3. 1,477 g/L. |
| Solubilidade | 38 g/100 mL (20 °C) . |
| Forma molecular | Lineal. |
| Momento dipolar | 1,05 D |
| pKa | -8,0 |
| Compostos relacionados. | HF, HBr , HI |
|
Termoquímica | |
| ΔfH0gas | -92,3 kJ/mol.. |
| S0gas, 1 bar | 186,7 J/mol•K . |
| ΔfG0gas | -95,3 kJ/mol . |
|
Seguridade | |
| MSDS | External MSDS |
| Inxestión | A disolución acuosa pode producir gastrite, queimaduras, gastrite hemorráxica, edema, necrose. Recomendase beber auga ou leite e NON inducir o vómito. |
| Inhalación | Pode producir irritación, edema e corrosión do tracto respiratorio, bronquite crónica. Recomendase levar a persoa a un lugar con aire fresco, mantela quente e quieta. Se se detén a respiración practicar reanimación cardiopulmonar. |
| Pel | Pode producir queimaduras, úlceras, irritación. Quitar da zona afectada toda a vestimenta e calzado e facer correr auga durante 20 minutos polo menos. |
| Ollos | Pode producir necrose na córnea, inflamación no ollo, irritación ocular e nasal, úlcera nasal. Lavar os ollos expostos con abundante auga durante 15 minutos polo menos. |
| Máis información | Hazardous Chemical Database (En inglés)[Ligazón morta] |
|
As propiedades sen referencia veñen dadas en condicións estándar(100 kPa, 25 °C), a non ser que se indique outra cousa. | |
O cloruro de hidróxeno, tamén coñecido como HCl, é un gas incoloro altamente corrosivo e tóxico que forma unha especie de fume branco en contacto coa humidade. Estes fumes están constituídos por ácido clorhídrico, que se forma cando o cloruro de hidróxeno se disolve en auga. O gas cloruro de hidróxeno, así como o ácido clorhídrico, son compostos químicos importantes na Química, na ciencia en xeral, na tecnoloxía e na industria. Moitas veces a denominación de cloruro de hidróxeno aplícase ó ácido clorhídrico e non especificamente ó composto gasoso.
Química[editar | editar a fonte]
A molécula de cloruro de hidróxeno é unha molécula diatómica que consiste nun átomo de hidróxeno unido a un átomo de cloro por un enlace covalente sinxelo. Posto que o átomo de cloro é moito máis electronegativo que o átomo de hidróxeno o enlace entre estes átomos presenta polaridade. A molécula é un dipolo no que o átomo de cloro acumula unha fracción de carga negativa, δ-, e o átomo de hidróxeno acumula unha fracción de carga positiva, δ+ . Esta polaridade posibilita a elevada solubilidade do cloruro de hidróxeno en auga. Na auga pura disólvense ata 38 g/100 mL aínda que a baixa temperatura pódense formar cristais de HCl•H2O cun contido do 68% de HCl. A disolución forma un azeótropo cun contido do 20,2% de HCl en masa e un punto de ebulición de 108,6 °C.
En contacto coa auga ionízase inmediatamente formando o catión hidronio, H3O+, e o anión cloruro, Cl-.
- HCl + H2O → H3O+ + Cl−
A disolución resultante recibe o nome de ácido clorhídrico e é un ácido forte. A constante de ionización do ácido correspondente ó clorhídrico, [[Ka]], é moi grande o que indica que o ácido clorhídrico disóciase en auga de maneira practicamente total.
Incluso en ausencia de auga o cloruro de hidróxeno pode actuar como ácido. Por exemplo o cloruro de hidróxeno pode disolverse noutros disolventes como o metanol e as moléculas protonadas resultantes, ou ións, actúan como catalizadores ácidos en reaccións químicas que deben realizarse en condicións anhidras.
- HCl + CH3OH → CH3O+H2 + Cl−
HCl protonizando a molécula de metanol (CH3OH)
Debido a súa natureza ácida, o cloruro de hidróxeno é un gas corrosivo, particularmente en presenza de humidade.

Efectos na saúde[editar | editar a fonte]
O cloruro de hidróxeno forma o ácido clorhídrico, que resulta corrosivo por contacto cos tecidos corporais. A inhalación dos fumes pode causar tose, respiración arfante, inflamación do nariz, da gorxa e das vías respiratorias superiores e, en casos máis graves, edema pulmonar, fallo do sistema circulatorio e morte. O contacto coa pel pode causar enroxecemento, dor, e graves queimaduras. Nos ollos pode causar queimaduras graves e dano permanente nos mesmos.
Historia[editar | editar a fonte]
Os alquimistas da Idade Media coñeceron o ácido clorhídrico (para eles alcohol do sal ou acido do sal), que emite vapores de cloruro de hidróxeno, e que foi chamado aire marino ácido.
No século XVII Johann Rudolf Glauber empregou sal (cloruro de sodio) e ácido sulfúrico para a preparación de sulfato de sodio, reacción na que se desprende cloruro de hidróxeno gas.
- 2NaCl + H2SO4 → 2HCl + Na2SO4
En 1772, Carl Wilhelm Scheele tamén levou a cabo esa reacción polo que é igualmente é considerado o seu descubridor. Joseph Priestley preparou cloruro de hidróxeno puro en 1772, e en 1818 Humphry Davy demostróu que estaba composto quimicamente por hidróxeno e cloro.
Durante a Revoluciónn Industrial, a demanda de substancias alcalinas como a sosa incrementouse, o que deu lugar a que Nicolas Leblanc desenvolvera un novo proceso a escala industrial polo que convertía o sal, cloruro de sodio, en carbonato de sodio, (sosa), empregando para iso ácido sulfúrico, pedra calcaria e carbón, dando cloruro de hidróxeno como produto de refugallo. Unha lei de 1863 prohibiu as emisións de HCl, polo que os fabricantes de sosa absorberon o HCl, por entón un produto inútil, en auga, producindo ácido clorhídrico a escala industrial. Máis tarde, desenvolveuse o proceso de Hargreaves, similar ó de Leblanc salvo que en vez de empregar ácido sulfúrico empregaba dióxido de xofre, auga e aire. A principio do século XX o proceso de Leblanc foi substituído polo proceso de Solvay, que non produce HCl, pero para entón a utilidade e o uso do HCl estaban tan asentados que se continuou coa produción do mesmo por outros métodos.
As aplicacións históricas do cloruro de hidróxeno no século XX inclúen hidrocloracións de alquinos para producir monómeros clorados, como o cloropreno e o cloruro de vinilo, que se polimerizan posteriormente para producir policloropreno (neopreno) e pilicloruro de vinilo, PVC, respectivamente. Na produción do cloruro de vinilo, o acetileno, HC≡CH (C2H2) é hidroclorado pola adición de HCl ó triplo enlace da molécula de HC≡CH, pasando o triplo enlace a dobre e converténdose en cloruro de vinilo, H2C=CHCl.
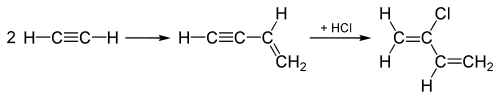
O "proceso do acetileno", usado ata os anos 60 para facer cloropreno, comenza unindo dúas moléculas de acetileno, e incorporando a continuación unha molécula de HCl ó triplo enlace, para dar lugar ó cloropreno:
O "proceso do acetileno" foi substituído por un proceso que agrega Cl2 a un dos dobres enlaces do 1,3-butadieno para, a continuación, eliminar HCl, co que se obtén o cloropreno.
Produción[editar | editar a fonte]
A meirande parte do cloruro de hidróxeno obtido a escala industrial destínase á produción do ácido clorhídrico. O método de obtención de HCl a partir de cloruro de sodio e do ácido sulfúrico tamén se emprega a escala industrial.
Unha maneira habitual de producir cloruro de hidróxeno é utilizando os chamados fornos de HCl, onde a reacción exotérmica entre o cloro e o hidróxeno dá lugar ó HCl gas.
- Cl2 + H2 → 2HCl
Esta reacción pode ser usada para dar un produto de elevada pureza, válido para ser empregado na industria alimentaria.
O cloruro de hidróxeno pode producirse tamén a partir de cloro e de compostos que conteñan hidróxeno, como é o caso dos hidrocarburos:
- R–H + Cl2 → R–Cl + HCl
A reacción posterior destas substancias cloradas con fluoruro de hidróxeno dá lugar a compostos fluorados e novo desprendemento de HCl:
- R–Cl + HF → R–F + HCl
Cando estas reaccións teñen lugar en condicións anhidras prodúcese HCl gas. Os produtos orgánicos resultantes inclúen derivados clorados, derivados fluorados e clorofluorocarbonos, CFCs.
Síntese[editar | editar a fonte]
Un desprendemento continuado e gradual de cloruro de hidróxeno pode conseguirse agregando auga de xeito gradual a un exceso de certos compostos reactivos que conteñen cloro, como é o caso dos cloruros de fósforo, cloruros de tionilo (SOCl2) e cloruros de acilo. A adición de máis auga absorbería o gas HCl formando ácido clorhídrico. Por exemplo, podemos facer gotear auga fría sobre pentacloruro de fósforo (PCl5) para dar HCl segundo a reacción: [4]
- PCl5 + H2O → POCl3 + 2HCl
Con auga quente aínda poderíamos obter máis HCl do PCl5 pois a hidrólise chegaría ata o final obténdose ácido orto- fosfórico.[4]
A reacción da auga co tricloruro de fósforo (PCl3) tamén rende HCl.[4]
A reacción do cloruro de tionilo con auga daría dióxido de xofre, gas(SO2), e HCl.
Outra maneira de sintetizar HCl gas é usando un xerador como os que se describen deseguida.
Xerador de HCl[editar | editar a fonte]
As cantidades pequenas de HCl gas para uso no laboratorio poden producirse empregando un xerador de HCl usando diferentes procesos químicos:
- Liberación a partir de ácido clorhídrico concentrado usando ácido sulfúrico concentrado.
- Liberación a partir de ácido clorhídrico concentrado usando cloruro de calcio seco.
- Por reacción do ácido sulfúrico co cloruro de sodio: NaCl + H2SO4 → NaHSO4 + HCl↑
Tipicamente o ácido clorhídrico ou o ácido sulfúrico déixanse caer, dende un funil, pinga a pinga nun frasco que contén o outro reactivo ou un desecante remexido mediante un axitador magnético. O HCl gas sécase facéndoo pasar a través de ácido sulfúrico concentrado, que é un poderoso deshidratante.
Aplicacións[editar | editar a fonte]
As que seguen son algunhas das aplicacións do gas cloruro de hidróxeno:
- A meirande parte do cloruro de hidróxeno emprégase na produción de ácido clorhídrico.
- Hidrocloración do caucho.
- Produción dos cloruros de vinilo e alquilo.
- Intermedio químico noutra produción química.
- Uso como decapante.
- Tratamento do algodón.
- Uso, con elevado grao de pureza, na industria dos semicondutores.
- Gravado, tipo augaforte, de circuítos en cristais de semicondutores
- Converter o silicio, vía SiHCl3 , en silicio de elevada pureza.
O cloruro de hidróxeno, habitualmente, ven en bombonas que son vermellas e marróns ou grises cunha banda amarela.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Chemical and laboratory data
- MSDS safety data
- Chemical data Arquivado 02 de febreiro de 2007 en Wayback Machine.
- Hydrogen Chloride
- Computational Chemistry Wiki