Alfa-sinucleína
| Alfa-sinucleína | |||
|---|---|---|---|
 | |||
| Estruturas dispoñibles | |||
| PDB | Buscar ortólogos: PDBe, RCSB
Lista de códigos PDB
| ||
| Identificadores | |||
| Nomenclatura | Outros nomes
| ||
| Identificadores externos | |||
| Locus | Cr. 4 q22.1 | ||
| Padrón de expresión de ARNm | |||
 | |||
 | |||
| Máis información | |||
| Ortólogos | |||
| Especies |
| ||
| Entrez |
| ||
| Ensembl |
| ||
| UniProt |
| ||
| RefSeq (ARNm) |
| ||
| RefSeq (proteína) NCBI |
| ||
| Localización (UCSC) |
| ||
| PubMed (Busca) |
| ||
A alfa-sinucleína (α-sinucleína) é unha proteína que nos humanos está codificada polo xene SNCA do cromosoma 4.[1] Abunda no cerebro, e aparece en pequenas cantidades no corazón, músculo e outros tecidos. No cerebro, a alfa-sinucleína encóntrase principalmente nos extremos das neuronas en estruturas especializadas chamadas terminais presinápticos.[1] Dentro destas estruturas, a alfa-sinucleína interacciona cos fosfolípidos[2] e proteínas.[1][3][4] Os terminais presinápticos liberan mensaxeiros químicos chamados neurotransmisores, almacenados en vesículas sinápticas. A liberación de neurotransmisores envía sinais entre as neuronas e é fundamental para o funcionamento normal do cerebro.[1]
Aínda que a función da alfa-sinucleína aínda non se comprende ben, os estudos realizados suxiren que exerce un papel na restrición da mobilidade de vesículas sinápticas, atenuando en consecuencia a reciclaxe de vesículas sinápticas e a liberación de neurotransmisores.[5][6][7][8][9][10][3] Unha idea alternativa é que a alfa-sinuceína se une á VAMP2 (unha sinaptobrevina) e estabiliza os complexos SNARE;[11][12][13][14][15] aínda que recentes estudos indican que a unión alfa-sinucleína–VAMP2 é esencial para a atenuación mediada pola alfa-sinucleína da reciclaxe de vesículas sinápticas, o que conecta estás dúas visións do seu funcionamento, aparentemente diverxentes.[3] Pode tamén axudar a regular a liberación de dopamina, un tipo de neurotransmisor que é esencial para controlar o comezo e a detención dos movementos voluntarios e involuntarios.[1]
A proteína alfa-sinucleína humana está formada por 140 aminoácidos.[16][17][18] Un fragmento de alfa-sinucleína, coñecido como compoñente non Abeta (NAC) do amiloide da enfermidade de Alzheimer, atopado orixinalmente nunha fracción enriquecida de amiloide, resultou seu un fragmento da súa proteína precursora, NACP.[16] Posteriormente, determinouse que a NACP era o homólogo humano da sinucleína da raia Torpedo. Por tanto, a NACP denomínase agora alfa-sinucleína humana.
Expresión nos tecidos[editar | editar a fonte]
A alfa-sinucleína é unha proteína sinucleína de función descoñecida que se encontra principalmente no tecido nervioso, constituíndo o 1% de todas as proteínas do citosol das células cerebrais.[19] Exprésase predominantemente no neocórtex, hipocampo, substancia negra, tálamo e cerebelo. É predominantemente unha proteína neuronal, mais pode tamén encontrarse en células da neuroglía.[20] En células melanocíticas, a expresión da proteína SNCA pode ser regulada polo MITF.[21]
Está establecido que a alfa-sinucleína está extensamente localizada no núcleo de neuronas do cerebro de mamíferos, o que suxire un papel da alfa-sinucleína no núcleo.[22] Porén, a sinucleína atópase predominantemente nas terminais presinápticas, tanto en forma libre coma unida a membranas,[23] e aproximadamente o 15% da sinucleína está unida a membranas nas neuronas.[24]
Tamén se demostrou que a alfa-sinucleína está localizada nas mitocondrias neuronais.[25][26] A alfa-sinucleína exprésase abundantemente nas mitocondrias do bulbo olfactorio, o hipocampo, corpo estriado e tálamo, onde tamén abunda a alfa-sinucleína citosólica. Porén, o córtex cerebral e o cerebelo son dúas excepcións, que conteñen moita alfa-sinucleína citosólica pero niveis moi baixos da alfa-sinucleína mitocondrial. Demostrouse que a alfa-sinucleína está localizada na membrana interna das mitocondrias, e que os efectos inhibitorios da alfa-sinucleína na actividade do complexo I da cadea respiratoria mitocondrial é dependente de dose. Así, suxeriuse que a alfa sinucleína nas mitocondrias exprésase diferencialmente en diferenetes rexións do cerebro e os niveis de fondo da alfa-sinucleína mitocondrial pode ser un factor potencial que afecta á función mitocondrial e predispón algunhas neuronas á dexeneración.[26]
Prodúcense polo menos tres isoformas de sinucleína por empalme alternativo.[27] A forma maioritaria da proteína e a máis investigada é a proteína de lonxitude completa de 140 aminoácidos. Outras isoformas son a alfa-sinucleína-126, que carece dos residuos 41-54 debido á perda do exón 3; e a alfa-sinucleína-112,[28] á que lle faltan os residuos 103-130 debido á perda do exón 5.[27]
Estrutura[editar | editar a fonte]
A alfa-sinucleína en solución é considerada unha proteína intrinsecamente desordenada, é dicir, non ten unha soa estrutura tridimensional estable.[29][30] Porén, en 2014, un crecente número de informes suxiren, a presenza de estruturas parciais ou estados oligoméricos bastante estruturados na estrutura en solución da alfa-sinucleína mesmo en ausencia de lípidos. Esta tendencia é tamén apoiada por un gran número de medidas de moléculas individuais (pinzas ópticas) feitas en copias únicas da alfa-sinucleína monomérica así como dímeros ou tetrámeros reforzados covalentemente da alfa-sinucleína.[31]
A alfa-sinucleína está especificamente regulada á alza nunha poboación discreta de terminais presinápticos do cerebro durante un período de rearranxos sinápticos relacionados coa adquisición.[32] A alfa-sinucleína interacciona significativamente coa tubulina,[33] e a alfa-sinucleína pode ter actividade como unha potencial proteína asociada aos microtúbulos, como a tau.[34]
Recentes evidencias suxiren que a alfa-sinucleína funciona como unha chaperona molecular na formación de complexos SNARE.[35][36] En particular, únese simultaneamente a fosfolípidos da membrana plasmática por medio do seu dominio N-terminal e á sinaptobrevina-2 polo seu dominio C-terminal, cunha importancia maior durante a actividade sináptica.[11] Hai crecentes probas de que a alfa-sinucleína está implicada no funcionamento do aparato de Golgi neuronal e o tráfico de vesículas.[37]
Aparentemente, a alfa-sinucleína é esencial para o desenvolvemento normal de funcións cognitivas. Os ratos knockout con inactivación da expresión da alfa-sinucleína mostran unha alteración da aprendizaxe espacial e da memoria de traballo.[38]
Interacción coas membranas lipídicas[editar | editar a fonte]
Realizáronse moitas experiencias sobre a interacción da alfa-sinucleína coa membrana plasmática e a súa implicación coa composición e recambio da membrana. No cribado do xenoma do lévedo Saccharomyces cerevisiae atopouse que varios xenes que teñen que ver co metabolismo de lípidos exercen un papel na toxicidade da alfa-sinucleína.[39] Inversamente, a expresión dos niveis de alfa-sinucleína pode afectar a viscosidade e a cantidade relativa de ácidos graxos na bicapa lipídica.[40]
A alfa sinucleína únese directamente a membranas lipídicas, asociándose con superficies cargadas negativamente de fosfolípidos.[40] A alfa-sinucleína forma unha estrutura helicoidal estendida en pequenas vesículas unilamelares.[41] Atopouse que ten unha preferencia por unirse a pequenas vesículas.[42] A unión da alfa-sinucleína ás membranas lipídicas ten complexos efectos sobre estas, alterando a estrutura da bicapa ao que orixina a formación de pequenas vesículas.[43] A alfa-sinucleína fai que se dobren as membranas de vesículas fosfolipídicas cargadas negativamente e transforma as vesículas en túbulos membranosos.[44] Usando criomicrografía electrónica de transmisión demostrouse que estes son tubos micelares de ~5-6 nm de diámetro.[45] A alfa-sinucleína forma tamén partículas lipídicas discoidais similares a apolipoproteínas.[46] Os estudos de resonancia paramagnética electrónica mostraron que a estrutura da alfa-sinucleína depende da superficie á que se une.[47] A proteína adopta unha conformación helicoidal rota sobre partículas lipoproteicas, mentres que forma unha estrutura helicoidal estendida sobre vesículas lipídicas e tubos membranosos.[47] Tamén se suxeriu que hai unha posible actividade antioxidante da alfa-sinucleína na membrana.[48]
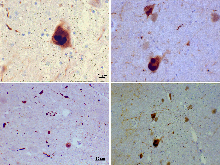
A interacción coa membrana da alfa-sinucleína modula ou afecta a súa taxa de agregación.[49] A modulación da agregación mediada por membranas é moi similar á observada noutras proteínas amiloides como IAPP e abeta.[49] Os estados agregados da alfa-sinucleína permean a membrana das vesículas lipídicas.[50] Fórmanse pola interacción con ácidos graxos poliinsaturados tendentes á peroxidación pero non con ácidos graxos monoinsaturados[51] e a unión a metais de transición que promoven a autoxidación de lípidos, como ferro ou cobre provocn a oligomerización da alfa-sinucleína.[52] A alfa-sinucleína agregada ten unha actividade específica sobre lípidos peroxidados e induce a autoxidación de lípidos en membranas con abundantes ácidos graxos poliinsaturados de neuronas e astrocitos, diminuíndo a resistencia á apoptose.[53] A autooxidación de lípidos é inhibida se as células son preincubadas con ácidos graxos poliinsaturados con isótopos de deuterio.[54]
Función na reparación do ADN[editar | editar a fonte]
A alfa-sinucleína modula os procesos de reparación do ADN, como a reparación de roturas de dobre febra do ADN.[55] Os marcadores de resposta aos danos ao ADN colocalízanse coa alfa-sinucleína para formar focos discretos en células do cerebro humanas e de rato. A depleción da alfa-sinucleína en células humanas causa un incremento na introdución de roturas de dobre febra no ADN despois da exposción á bleomicina e unha redución da capacidade de reparar estas roturas de dobre febra. Ademais, os ratos knocout para a alfa-sinucleína mostran un maior nivel de roturas de dobre febra e este problema pode ser aliviado pola reintrodución transxénica da alfa-sinucleína humana. A alfa-sinucleína promove a vía de reparación das roturas de dobre febra denominada unión de extremos non homólogos.[55] A función na reparación do ADN da alfa-sinucleína parece estar comprometida en neuronas que teñen inclusións de corpos de Lewy e isto pode desencadear a morte celular.
Secuencia[editar | editar a fonte]
A estrutura primaria da alfa-sinucleína está xeralmente divida en tres dominios:
- Residuos 1-60: unha rexión anfipática N-terminal dominada por catro repeticións de 11 residuos incluíndo a secuencia consenso KTKEGV. Esta secuencia ten unha propensión estrutural a hélice alfa similar aos dominios de unión a apolipoproteínas.[56] É un terminal altamente conservado que interacciona con membranas lipídicas ácidas, e todas as mutacións puntuais descubertas do xene SNCA están localizadas dentro deste terminal.[57]
- Residuos 61-95: unha rexión hidrófoba central, que inclúe a rexión do compoñente non amiloide-β (NAC), implicada na agregación de proteínas.[16] Este dominio é único da alfa-sinucleína dentro da familia da sinucleína.[58]
- Residuos 96-140: unha rexión moi ácida e rica en prolina, que non ten unha propensión estrutural clara. Este dominio xoga un importante papel na función, solubilidade e interacción da alfa-sinucleína con outras proteínas.[11]
Actividade autoproteolítica[editar | editar a fonte]
O uso de espectrometría de masas de mobilidade de ións (IMS-MS) de alta resolución sobre alfa-sinnucleína purificada por HPLC in vitro mostrou que a alfa-sinucleína é autoproteolítca, xerando cando se incuba unha variedade de fragmentos de pequeno peso molecular.[59] A proteína de 14,46 kDa xera numerosos pequenos fragmentos, incluíndo fragmentos de 12,16 kDa (aminoácidos 14-133) e 10,44 kDa (40-140) formados por truncamento C-terminal ou N-terminal e un fragmento de 7,27 kDa C-terminal (72-140). O fragmento de 7,27 kDa, que contén a maioría da rexión NAC (rexión do compoñente non amiloide), agregábase considerablemente máis rápido que a alfa-sinucleína de lonxitude completa. É posible que estes produtos autoproteolíticos xoguen un papel como intermediarios ou cofactores na agregación da alfa-sinucleína in vivo.
Importancia clínica[editar | editar a fonte]

Clasicamente foi considerada unha proteína non estruturada soluble, pero a α-sinucleína non mutada forma un tetrámero pregado de forma estable que resiste a agregación.[60] Esta observación, aínda que reproducida por varios laboratorios,[61][62][63] é aínda un asunto moi debatido debido á existencia de informes contraditorios.[64][65][66] Non obstante, a alfa-sinucleína agrégase para formar fibrilas insolubles en condicións patolóxicas caracterizadas pola presenza de corpos de Lewy, como na enfermidade de Parkinson, demencia con corpos de Lewy e atrofia multisistémica.[67][68] Estes trastornos coñécense como sinucleinopatías. Os modelos in vitro das sinucleinopatías revelaron que a agregación da alfa-sinucleína pode conducir á aparición de varios trastornos celulares, como a alteración dos microtúbulos, disfuncións sinápticas e mitocondriais, estrés oxidativo e desregulación da sinalización por calcio, ou das vías proteasómica e lisosómica.[69] A alfa-sinucleína é o principal compoñente estrutural das fibrilas dos corpos de Lewy. Ocasionalmente, os corpos de Lewy conteñen a proteína tau;[70] con todo, a alfa-sinucleína e a tau constitúen dous subconxuntos distintos de filamentos situados nos mesmos corpos de inclusión.[71] A patoloxía da alfa-sinucleína tamén se atopa en casos de alzhéimer esporádico ou familiar.[72]
O mecanismo de agregación da alfa-sinucleína é descoñecido. Hai evidencias dun intermediario estruturado rico en estrutura beta que pode ser o precursosr da agregación e, finalmente, dos corpos de Lewy.[73] Un estudo dunha soa molécula en 2008 suxire que a alfa-sinucleína existe en forma de mestura de confórmeros non estruturados, e ricos en hélice alfa e folla beta en equilibrio. As mutacións ou condicións de tamponamento que melloran a agregación incrementan grandemente a poboación do confórmero beta, o que indica que esta podería ser unha conformación relacionada coa agregación patoxénica.[74] Unha teoría di que a maioría dos agregados de alfa-sinucleína están localizados na presinapse en forma de pequenos depósitos que causan disfunción sináptica.[75] Entre as estratexias para tratar as sinucleinopatías está o uso de compostos que inhiben a agregación da alfa-sinucleína. A pequena molécula cuminaldehido inhibe a fibrilación da alfa-sinucleína.[76] O virus de Epstein-Barr foi implicado nestes trastornos.[77]
En raros casos de formas familiares da enfermidade de Parkinson, hai unha mutación no xene que codifica a alfa-sinucleína. Identificáronse ata agora cinco mutacións puntuais, que son: A53T,[78] A30P,[79] E46K,[80] H50Q,[81] e G51D.[82] Informouse de que algunhas mutacións inflúen nos pasos de iniciación e amplificación do proceso de agregación.[83] A duplicación e triplicación xenómica do xene parece ser unha rara causa do párkinson noutras liñaxes, aínda que máis común que as mutacións puntuais.[84][85] Por tanto, certas mutacións da alfa-sinucleína poden causar que esta forme fibrilas similares ás amiloides que contribúen á enfermidade de Parkinson. A sobreexpresión da alfa-sinucleína de tipo silvestre humana ou a da mutante A53T en primates orixina a deposición de alfa-sinucleína no mesencéfalo ventral, a dexeneración do sistema dopaminérxico e a alteración da acción motora.[86]
Certas seccións da proteína alfa-sinucleína poden xogar un papel nas tauopatías.[87]
Unha forma prión da proteína alfa-sinucleína pode ser un axente causal da enfermidade atrofia multisistémica.[88][89][90]

Os anticorpos contra a alfa-sinucleína substituíron os anticorpos contra a ubiquitina como estándar para a inmunotinguidura de corpos de Lewy.[92] Na figura, o panel central mostra as principais vías para a agregación da proteína. A α-sinucleína monomérica nativa está en estado despregado en solución pero pode unirse a membranas nunha forma α-helicoidal. Á esquerda móstranse algúns modificadores deste proceso. Á dereita móstranse algunhas dianas celulares propostas para a toxicidade mediada pola α-sinucleína, como o transporte RE-Golgi, as vesículas sinápticas, as mitocondrias e lisosomas e outra maquinaria proteólítica.[91]
Interaccións proteína-proteína[editar | editar a fonte]
A alfa-sinucleína presenta interaccións con:
- Transportador de dopamina,[93][94]
- Parkin (ligase),[95][96]
- Fosfolipase D1,[97]
- SNCAIP,[98][99][100][101]
- Proteína tau.[102][103]
- Beta amiloide[104]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 1,2 1,3 1,4 "Genetics Home Reference: SNCA". U.S. National Library of Medicine. 12 Nov 2013. Consultado o 14 Nov 2013.
- ↑ Chandra S, Chen X, Rizo J, Jahn R, Südhof TC (abril de 2003). "A broken alpha -helix in folded alpha -Synuclein". The Journal of Biological Chemistry 278 (17): 15313–8. PMID 12586824. doi:10.1074/jbc.M213128200.
- ↑ 3,0 3,1 3,2 Sun J, Wang L, Bao H, Premi S, Das U, Chapman ER, Roy S (xuño de 2019). "Functional cooperation of α-synuclein and VAMP2 in synaptic vesicle recycling". Proceedings of the National Academy of Sciences of the United States of America 116 (23): 11113–11115. PMC 6561242. PMID 31110017. doi:10.1073/pnas.1903049116.
- ↑ Atias M, Tevet Y, Sun J, Stavsky A, Tal S, Kahn J, et al. (xuño de 2019). "Synapsins regulate α-synuclein functions". Proceedings of the National Academy of Sciences of the United States of America 116 (23): 11116–11118. PMC 6561288. PMID 31110014. doi:10.1073/pnas.1903054116.
- ↑ Larsen KE, Schmitz Y, Troyer MD, Mosharov E, Dietrich P, Quazi AZ, et al. (novembro de 2006). "Alpha-synuclein overexpression in PC12 and chromaffin cells impairs catecholamine release by interfering with a late step in exocytosis". The Journal of Neuroscience 26 (46): 11915–22. PMC 6674868. PMID 17108165. doi:10.1523/JNEUROSCI.3821-06.2006.
- ↑ Nemani VM, Lu W, Berge V, Nakamura K, Onoa B, Lee MK, et al. (xaneiro de 2010). "Increased expression of alpha-synuclein reduces neurotransmitter release by inhibiting synaptic vesicle reclustering after endocytosis". Neuron 65 (1): 66–79. PMC 3119527. PMID 20152114. doi:10.1016/j.neuron.2009.12.023.
- ↑ Scott DA, Tabarean I, Tang Y, Cartier A, Masliah E, Roy S (xuño de 2010). "A pathologic cascade leading to synaptic dysfunction in alpha-synuclein-induced neurodegeneration". The Journal of Neuroscience 30 (24): 8083–95. PMC 2901533. PMID 20554859. doi:10.1523/JNEUROSCI.1091-10.2010.
- ↑ Scott D, Roy S (xullo de 2012). "α-Synuclein inhibits intersynaptic vesicle mobility and maintains recycling-pool homeostasis". The Journal of Neuroscience 32 (30): 10129–35. PMC 3426499. PMID 22836248. doi:10.1523/JNEUROSCI.0535-12.2012.
- ↑ Vargas KJ, Makani S, Davis T, Westphal CH, Castillo PE, Chandra SS (xullo de 2014). "Synucleins regulate the kinetics of synaptic vesicle endocytosis". The Journal of Neuroscience 34 (28): 9364–76. PMC 4087213. PMID 25009269. doi:10.1523/JNEUROSCI.4787-13.2014.
- ↑ Wang L, Das U, Scott DA, Tang Y, McLean PJ, Roy S (outubro de 2014). "α-synuclein multimers cluster synaptic vesicles and attenuate recycling". Current Biology 24 (19): 2319–26. PMC 4190006. PMID 25264250. doi:10.1016/j.cub.2014.08.027.
- ↑ 11,0 11,1 11,2 Burré J, Sharma M, Tsetsenis T, Buchman V, Etherton MR, Südhof TC (setembro de 2010). "Alpha-synuclein promotes SNARE-complex assembly in vivo and in vitro". Science 329 (5999): 1663–7. Bibcode:2010Sci...329.1663B. PMC 3235365. PMID 20798282. doi:10.1126/science.1195227.
- ↑ Burré J, Sharma M, Südhof TC (marzo de 2018). "Cell Biology and Pathophysiology of α-Synuclein". Cold Spring Harbor Perspectives in Medicine 8 (3): a024091. PMC 5519445. PMID 28108534. doi:10.1101/cshperspect.a024091.
- ↑ Burré J, Sharma M, Südhof TC (outubro de 2012). "Systematic mutagenesis of α-synuclein reveals distinct sequence requirements for physiological and pathological activities". The Journal of Neuroscience 32 (43): 15227–42. PMC 3506191. PMID 23100443. doi:10.1523/JNEUROSCI.3545-12.2012.
- ↑ Burré J, Sharma M, Südhof TC (outubro de 2014). "α-Synuclein assembles into higher-order multimers upon membrane binding to promote SNARE complex formation". Proceedings of the National Academy of Sciences of the United States of America 111 (40): E4274–83. Bibcode:2014PNAS..111E4274B. PMC 4210039. PMID 25246573. doi:10.1073/pnas.1416598111.
- ↑ Diao J, Burré J, Vivona S, Cipriano DJ, Sharma M, Kyoung M, et al. (abril de 2013). "Native α-synuclein induces clustering of synaptic-vesicle mimics via binding to phospholipids and synaptobrevin-2/VAMP2". eLife 2: e00592. PMC 3639508. PMID 23638301. doi:10.7554/eLife.00592.
- ↑ 16,0 16,1 16,2 Uéda K, Fukushima H, Masliah E, Xia Y, Iwai A, Yoshimoto M, et al. (decembro de 1993). "Molecular cloning of cDNA encoding an unrecognized component of amyloid in Alzheimer disease". Proceedings of the National Academy of Sciences of the United States of America 90 (23): 11282–6. Bibcode:1993PNAS...9011282U. PMC 47966. PMID 8248242. doi:10.1073/pnas.90.23.11282.
- ↑ Xia Y, Saitoh T, Uéda K, Tanaka S, Chen X, Hashimoto M, et al. (outubro de 2001). "Characterization of the human alpha-synuclein gene: Genomic structure, transcription start site, promoter region and polymorphisms". Journal of Alzheimer's Disease 3 (5): 485–494. PMID 12214035. doi:10.3233/JAD-2001-3508. Arquivado dende o orixinal o 14 de maio de 2016. Consultado o 03 de maio de 2020.
- ↑ Xia Y, Saitoh T, Uéda K, Tanaka S, Chen X, Hashimoto M, Hsu L, Conrad C, Sundsmo M, Yoshimoto M, Thal L, Katzman R, Masliah E (2002). "Characterization of the human alpha-synuclein gene: Genomic structure, transcription start site, promoter region and polymorphisms: Erratum p489 Fig 3". J. Alzheimers Dis. 4 (4): 337. Arquivado dende o orixinal o 14 de maio de 2016. Consultado o 03 de maio de 2020.
- ↑ Iwai A, Masliah E, Yoshimoto M, Ge N, Flanagan L, de Silva HA, et al. (febreiro de 1995). "The precursor protein of non-A beta component of Alzheimer's disease amyloid is a presynaptic protein of the central nervous system". Neuron 14 (2): 467–75. PMID 7857654. doi:10.1016/0896-6273(95)90302-X.
- ↑ Dominik Brück, Gregor K. Wenning, [...], and Lisa Fellner. Glia and alpha-synuclein in neurodegeneration: a complex interaction. Neurobiology of disease. [https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4730552/ ]
- ↑ Hoek KS, Schlegel NC, Eichhoff OM, Widmer DS, Praetorius C, Einarsson SO, et al. (decembro de 2008). "Novel MITF targets identified using a two-step DNA microarray strategy". Pigment Cell & Melanoma Research 21 (6): 665–76. PMID 19067971. doi:10.1111/j.1755-148X.2008.00505.x.
- ↑ Yu S, Li X, Liu G, Han J, Zhang C, Li Y, et al. (marzo de 2007). "Extensive nuclear localization of alpha-synuclein in normal rat brain neurons revealed by a novel monoclonal antibody". Neuroscience 145 (2): 539–55. PMID 17275196. doi:10.1016/j.neuroscience.2006.12.028.
- ↑ McLean PJ, Kawamata H, Ribich S, Hyman BT (marzo de 2000). "Membrane association and protein conformation of alpha-synuclein in intact neurons. Effect of Parkinson's disease-linked mutations". The Journal of Biological Chemistry 275 (12): 8812–6. PMID 10722726. doi:10.1074/jbc.275.12.8812.
- ↑ Lee HJ, Choi C, Lee SJ (xaneiro de 2002). "Membrane-bound alpha-synuclein has a high aggregation propensity and the ability to seed the aggregation of the cytosolic form". The Journal of Biological Chemistry 277 (1): 671–8. PMID 11679584. doi:10.1074/jbc.M107045200.
- ↑ Zhang L, Zhang C, Zhu Y, Cai Q, Chan P, Uéda K, et al. (decembro de 2008). "Semi-quantitative analysis of alpha-synuclein in subcellular pools of rat brain neurons: an immunogold electron microscopic study using a C-terminal specific monoclonal antibody". Brain Research 1244: 40–52. PMID 18817762. doi:10.1016/j.brainres.2008.08.067.
- ↑ 26,0 26,1 Liu G, Zhang C, Yin J, Li X, Cheng F, Li Y, et al. (maio de 2009). "alpha-Synuclein is differentially expressed in mitochondria from different rat brain regions and dose-dependently down-regulates complex I activity". Neuroscience Letters 454 (3): 187–92. PMID 19429081. doi:10.1016/j.neulet.2009.02.056.
- ↑ 27,0 27,1 Beyer K (setembro de 2006). "Alpha-synuclein structure, posttranslational modification and alternative splicing as aggregation enhancers". Acta Neuropathologica 112 (3): 237–51. PMID 16845533. doi:10.1007/s00401-006-0104-6.
- ↑ Uéda K, Saitoh T, Mori H (decembro de 1994). "Tissue-dependent alternative splicing of mRNA for NACP, the precursor of non-A beta component of Alzheimer's disease amyloid". Biochemical and Biophysical Research Communications 205 (2): 1366–72. PMID 7802671. doi:10.1006/bbrc.1994.2816.
- ↑ van Rooijen BD, van Leijenhorst-Groener KA, Claessens MM, Subramaniam V (decembro de 2009). "Tryptophan fluorescence reveals structural features of alpha-synuclein oligomers". Journal of Molecular Biology 394 (5): 826–33. PMID 19837084. doi:10.1016/j.jmb.2009.10.021.
- ↑ Weinreb PH, Zhen W, Poon AW, Conway KA, Lansbury PT (outubro de 1996). "NACP, a protein implicated in Alzheimer's disease and learning, is natively unfolded". Biochemistry 35 (43): 13709–15. PMID 8901511. doi:10.1021/bi961799n.
- ↑ Neupane K, Solanki A, Sosova I, Belov M, Woodside MT (xaneiro de 2014). "Diverse metastable structures formed by small oligomers of α-synuclein probed by force spectroscopy". PLOS ONE 9 (1): e86495. Bibcode:2014PLoSO...986495N. PMC 3901707. PMID 24475132. doi:10.1371/journal.pone.0086495.
- ↑ George JM, Jin H, Woods WS, Clayton DF (agosto de 1995). "Characterization of a novel protein regulated during the critical period for song learning in the zebra finch". Neuron 15 (2): 361–72. PMID 7646890. doi:10.1016/0896-6273(95)90040-3.
- ↑ Alim MA, Hossain MS, Arima K, Takeda K, Izumiyama Y, Nakamura M, et al. (xaneiro de 2002). "Tubulin seeds alpha-synuclein fibril formation". The Journal of Biological Chemistry 277 (3): 2112–7. PMID 11698390. doi:10.1074/jbc.M102981200.
- ↑ Alim MA, Ma QL, Takeda K, Aizawa T, Matsubara M, Nakamura M, et al. (agosto de 2004). "Demonstration of a role for alpha-synuclein as a functional microtubule-associated protein". Journal of Alzheimer's Disease 6 (4): 435–42; discussion 443–9. PMID 15345814. doi:10.3233/JAD-2004-6412.
- ↑ Bonini NM, Giasson BI (novembro de 2005). "Snaring the function of alpha-synuclein". Cell 123 (3): 359–61. PMID 16269324. doi:10.1016/j.cell.2005.10.017.
- ↑ Chandra S, Gallardo G, Fernández-Chacón R, Schlüter OM, Südhof TC (novembro de 2005). "Alpha-synuclein cooperates with CSPalpha in preventing neurodegeneration". Cell 123 (3): 383–96. PMID 16269331. doi:10.1016/j.cell.2005.09.028.
- ↑ Cooper AA, Gitler AD, Cashikar A, Haynes CM, Hill KJ, Bhullar B, et al. (xullo de 2006). "Alpha-synuclein blocks ER-Golgi traffic and Rab1 rescues neuron loss in Parkinson's models". Science 313 (5785): 324–8. Bibcode:2006Sci...313..324C. PMC 1983366. PMID 16794039. doi:10.1126/science.1129462.
- ↑ Kokhan VS, Afanasyeva MA, Van'kin GI (maio de 2012). "α-Synuclein knockout mice have cognitive impairments". Behavioural Brain Research 231 (1): 226–30. PMID 22469626. doi:10.1016/j.bbr.2012.03.026.
- ↑ Willingham S, Outeiro TF, DeVit MJ, Lindquist SL, Muchowski PJ (decembro de 2003). "Yeast genes that enhance the toxicity of a mutant huntingtin fragment or alpha-synuclein". Science 302 (5651): 1769–72. Bibcode:2003Sci...302.1769W. PMID 14657499. doi:10.1126/science.1090389.
- ↑ 40,0 40,1 Uversky VN (outubro de 2007). "Neuropathology, biochemistry, and biophysics of alpha-synuclein aggregation". Journal of Neurochemistry 103 (1): 17–37. PMID 17623039. doi:10.1111/j.1471-4159.2007.04764.x.
- ↑ Jao CC, Hegde BG, Chen J, Haworth IS, Langen R (decembro de 2008). "Structure of membrane-bound alpha-synuclein from site-directed spin labeling and computational refinement". Proceedings of the National Academy of Sciences of the United States of America 105 (50): 19666–71. Bibcode:2008PNAS..10519666J. PMC 2605001. PMID 19066219. doi:10.1073/pnas.0807826105.
- ↑ Zhu M, Li J, Fink AL (outubro de 2003). "The association of alpha-synuclein with membranes affects bilayer structure, stability, and fibril formation". The Journal of Biological Chemistry 278 (41): 40186–97. PMID 12885775. doi:10.1074/jbc.M305326200.
- ↑ Madine J, Doig AJ, Middleton DA (maio de 2006). "A study of the regional effects of alpha-synuclein on the organization and stability of phospholipid bilayers". Biochemistry 45 (18): 5783–92. PMID 16669622. doi:10.1021/bi052151q.
- ↑ Varkey J, Isas JM, Mizuno N, Jensen MB, Bhatia VK, Jao CC, et al. (outubro de 2010). "Membrane curvature induction and tubulation are common features of synucleins and apolipoproteins". The Journal of Biological Chemistry 285 (42): 32486–93. PMC 2952250. PMID 20693280. doi:10.1074/jbc.M110.139576.
- ↑ Mizuno N, Varkey J, Kegulian NC, Hegde BG, Cheng N, Langen R, Steven AC (agosto de 2012). "Remodeling of lipid vesicles into cylindrical micelles by α-synuclein in an extended α-helical conformation". The Journal of Biological Chemistry 287 (35): 29301–11. PMC 3436199. PMID 22767608. doi:10.1074/jbc.M112.365817.
- ↑ Varkey J, Mizuno N, Hegde BG, Cheng N, Steven AC, Langen R (xuño de 2013). "α-Synuclein oligomers with broken helical conformation form lipoprotein nanoparticles". The Journal of Biological Chemistry 288 (24): 17620–30. PMC 3682563. PMID 23609437. doi:10.1074/jbc.M113.476697.
- ↑ 47,0 47,1 Varkey J, Langen R (xullo de 2017). "Membrane remodeling by amyloidogenic and non-amyloidogenic proteins studied by EPR". Journal of Magnetic Resonance 280: 127–139. Bibcode:2017JMagR.280..127V. PMC 5461824. PMID 28579098. doi:10.1016/j.jmr.2017.02.014.
- ↑ Zhu M, Qin ZJ, Hu D, Munishkina LA, Fink AL (xullo de 2006). "Alpha-synuclein can function as an antioxidant preventing oxidation of unsaturated lipid in vesicles". Biochemistry 45 (26): 8135–42. PMID 16800638. doi:10.1021/bi052584t.
- ↑ 49,0 49,1 Rawat A, Langen R, Varkey J (abril de 2018). "Membranes as modulators of amyloid protein misfolding and target of toxicity". Biochimica et Biophysica Acta (BBA) - Biomembranes 1860 (9): 1863–1875. PMC 6203680. PMID 29702073. doi:10.1016/j.bbamem.2018.04.011.
- ↑ Flagmeier P, De S, Wirthensohn DC, Lee SF, Vincke C, Muyldermans S, et al. (xuño de 2017). "2+ Influx into Lipid Vesicles Induced by Protein Aggregates". Angewandte Chemie 56 (27): 7750–7754. PMC 5615231. PMID 28474754. doi:10.1002/anie.201700966.
- ↑ Sharon R, Bar-Joseph I, Frosch MP, Walsh DM, Hamilton JA, Selkoe DJ (febreiro de 2003). "The formation of highly soluble oligomers of alpha-synuclein is regulated by fatty acids and enhanced in Parkinson's disease". Neuron 37 (4): 583–95. PMID 12597857. doi:10.1016/s0896-6273(03)00024-2.
- ↑ Amer DA, Irvine GB, El-Agnaf OM (agosto de 2006). "Inhibitors of alpha-synuclein oligomerization and toxicity: a future therapeutic strategy for Parkinson's disease and related disorders". Experimental Brain Research 173 (2): 223–33. PMID 16733698. doi:10.1007/s00221-006-0539-y.
- ↑ Ruipérez V, Darios F, Davletov B (outubro de 2010). "Alpha-synuclein, lipids and Parkinson's disease". Progress in Lipid Research 49 (4): 420–8. PMID 20580911. doi:10.1016/j.plipres.2010.05.004.
- ↑ Angelova PR, Horrocks MH, Klenerman D, Gandhi S, Abramov AY, Shchepinov MS (maio de 2015). "Lipid peroxidation is essential for α-synuclein-induced cell death". Journal of Neurochemistry 133 (4): 582–9. PMC 4471127. PMID 25580849. doi:10.1111/jnc.13024.
- ↑ 55,0 55,1 Schaser AJ, Osterberg VR, Dent SE, Stackhouse TL, Wakeham CM, Boutros SW, Weston LJ, Owen N, Weissman TA, Luna E, Raber J, Luk KC, McCullough AK, Woltjer RL, Unni VK (Jul 2019). "Alpha-synuclein is a DNA binding protein that modulates DNA repair with implications for Lewy body disorders". Sci Rep 9 (1): 10919. PMC 6662836. PMID 31358782. doi:10.1038/s41598-019-47227-z.
- ↑ Clayton DF, George JM (1998). "The synucleins: a family of proteins involved in synaptic function, plasticity, neurodegeneration and disease". Trends in Neurosciences 21 (6): 249–254. PMID 9641537. doi:10.1016/S0166-2236(97)01213-7.
- ↑ Bussell R, Eliezer D (xuño de 2003). "A structural and functional role for 11-mer repeats in alpha-synuclein and other exchangeable lipid binding proteins". Journal of Molecular Biology 329 (4): 763–78. PMID 12787676. doi:10.1016/S0022-2836(03)00520-5.
- ↑ Uchihara T, Giasson BI (xaneiro de 2016). "Propagation of alpha-synuclein pathology: hypotheses, discoveries, and yet unresolved questions from experimental and human brain studies". Acta Neuropathologica 131 (1): 49–73. PMC 4698305. PMID 26446103. doi:10.1007/s00401-015-1485-1.
- ↑ Vlad C, Lindner K, Karreman C, Schildknecht S, Leist M, Tomczyk N, et al. (decembro de 2011). "Autoproteolytic fragments are intermediates in the oligomerization/aggregation of the Parkinson's disease protein alpha-synuclein as revealed by ion mobility mass spectrometry". ChemBioChem 12 (18): 2740–4. PMC 3461308. PMID 22162214. doi:10.1002/cbic.201100569.
- ↑ Bartels T, Choi JG, Selkoe DJ (agosto de 2011). "α-Synuclein occurs physiologically as a helically folded tetramer that resists aggregation". Nature 477 (7362): 107–10. Bibcode:2011Natur.477..107B. PMC 3166366. PMID 21841800. doi:10.1038/nature10324. Arquivado dende o orixinal o 03 de outubro de 2020. Consultado o 03 de maio de 2020. Resumo divulgativo – Harvard Medical School New Focus.
- ↑ Dettmer U, Newman AJ, Luth ES, Bartels T, Selkoe D (marzo de 2013). "In vivo cross-linking reveals principally oligomeric forms of α-synuclein and β-synuclein in neurons and non-neural cells". The Journal of Biological Chemistry 288 (9): 6371–85. PMC 3585072. PMID 23319586. doi:10.1074/jbc.M112.403311.
- ↑ Westphal CH, Chandra SS (xaneiro de 2013). "Monomeric synucleins generate membrane curvature". The Journal of Biological Chemistry 288 (3): 1829–40. PMC 3548493. PMID 23184946. doi:10.1074/jbc.M112.418871.
- ↑ Trexler AJ, Rhoades E (maio de 2012). "N-Terminal acetylation is critical for forming α-helical oligomer of α-synuclein". Protein Science 21 (5): 601–5. PMC 3403458. PMID 22407793. doi:10.1002/pro.2056.
- ↑ Fauvet B, Mbefo MK, Fares MB, Desobry C, Michael S, Ardah MT, et al. (maio de 2012). "α-Synuclein in central nervous system and from erythrocytes, mammalian cells, and Escherichia coli exists predominantly as disordered monomer". The Journal of Biological Chemistry 287 (19): 15345–64. PMC 3346117. PMID 22315227. doi:10.1074/jbc.M111.318949.
- ↑ Burré J, Vivona S, Diao J, Sharma M, Brunger AT, Südhof TC (xuño de 2013). "Properties of native brain α-synuclein". Nature 498 (7453): E4–6; discussion E6–7. Bibcode:2013Natur.498E...4B. PMC 4255827. PMID 23765500. doi:10.1038/nature12125.
- ↑ Theillet FX, Binolfi A, Bekei B, Martorana A, Rose HM, Stuiver M, et al. (febreiro de 2016). "Structural disorder of monomeric α-synuclein persists in mammalian cells". Nature 530 (7588): 45–50. Bibcode:2016Natur.530...45T. PMID 26808899. doi:10.1038/nature16531. hdl:11336/53199.
- ↑ Spillantini MG, Schmidt ML, Lee VM, Trojanowski JQ, Jakes R, Goedert M (agosto de 1997). "Alpha-synuclein in Lewy bodies". Nature 388 (6645): 839–40. Bibcode:1997Natur.388..839G. PMID 9278044. doi:10.1038/42166.
- ↑ Mezey E, Dehejia A, Harta G, Papp MI, Polymeropoulos MH, Brownstein MJ (xullo de 1998). "Alpha synuclein in neurodegenerative disorders: murderer or accomplice?". Nature Medicine 4 (7): 755–7. PMID 9662355. doi:10.1038/nm0798-755.
- ↑ Marvian AT, Koss DJ, Aliakbari F, Morshedi D, Outeiro TF (setembro de 2019). "In vitro models of synucleinopathies: informing on molecular mechanisms and protective strategies". Journal of Neurochemistry 150 (5): 535–565. PMID 31004503. doi:10.1111/jnc.14707.
- ↑ Arima K, Hirai S, Sunohara N, Aoto K, Izumiyama Y, Uéda K, et al. (outubro de 1999). "Cellular co-localization of phosphorylated tau- and NACP/alpha-synuclein-epitopes in lewy bodies in sporadic Parkinson's disease and in dementia with Lewy bodies". Brain Research 843 (1–2): 53–61. PMID 10528110. doi:10.1016/S0006-8993(99)01848-X.
- ↑ Arima K, Mizutani T, Alim MA, Tonozuka-Uehara H, Izumiyama Y, Hirai S, Uéda K (agosto de 2000). "NACP/alpha-synuclein and tau constitute two distinctive subsets of filaments in the same neuronal inclusions in brains from a family of parkinsonism and dementia with Lewy bodies: double-immunolabeling fluorescence and electron microscopic studies". Acta Neuropathologica 100 (2): 115–21. PMID 10963357. doi:10.1007/s004010050002.
- ↑ Yokota O, Terada S, Ishizu H, Ujike H, Ishihara T, Nakashima H, et al. (decembro de 2002). "NACP/alpha-synuclein, NAC, and beta-amyloid pathology of familial Alzheimer's disease with the E184D presenilin-1 mutation: a clinicopathological study of two autopsy cases". Acta Neuropathologica 104 (6): 637–48. PMID 12410385. doi:10.1007/s00401-002-0596-7.
- ↑ Kim HY, Heise H, Fernandez CO, Baldus M, Zweckstetter M (setembro de 2007). "Correlation of amyloid fibril beta-structure with the unfolded state of alpha-synuclein". ChemBioChem 8 (14): 1671–4. PMID 17722123. doi:10.1002/cbic.200700366.
- ↑ Sandal M, Valle F, Tessari I, Mammi S, Bergantino E, Musiani F, et al. (xaneiro de 2008). "Conformational equilibria in monomeric alpha-synuclein at the single-molecule level". PLoS Biology 6 (1): e6. PMC 2174973. PMID 18198943. doi:10.1371/journal.pbio.0060006.
- ↑ Schulz-Schaeffer WJ (agosto de 2010). "The synaptic pathology of alpha-synuclein aggregation in dementia with Lewy bodies, Parkinson's disease and Parkinson's disease dementia". Acta Neuropathologica 120 (2): 131–43. PMC 2892607. PMID 20563819. doi:10.1007/s00401-010-0711-0.
- ↑ Morshedi D, Aliakbari F (Spring 2012). "The Inhibitory Effects of Cuminaldehyde on Amyloid Fibrillation and Cytotoxicity of Alpha-synuclein". Modares Journal of Medical Sciences: Pathobiology 15 (1): 45–60.
- ↑ Woulfe J, Hoogendoorn H, Tarnopolsky M, Muñoz DG (novembro de 2000). "Monoclonal antibodies against Epstein-Barr virus cross-react with alpha-synuclein in human brain". Neurology 55 (9): 1398–401. PMID 11087792. doi:10.1212/WNL.55.9.1398.
- ↑ Polymeropoulos MH, Lavedan C, Leroy E, Ide SE, Dehejia A, Dutra A, et al. (xuño de 1997). "Mutation in the alpha-synuclein gene identified in families with Parkinson's disease". Science 276 (5321): 2045–7. PMID 9197268. doi:10.1126/science.276.5321.2045.
- ↑ Krüger R, Kuhn W, Müller T, Woitalla D, Graeber M, Kösel S, et al. (febreiro de 1998). "Ala30Pro mutation in the gene encoding alpha-synuclein in Parkinson's disease". Nature Genetics 18 (2): 106–8. PMID 9462735. doi:10.1038/ng0298-106.
- ↑ Zarranz JJ, Alegre J, Gómez-Esteban JC, Lezcano E, Ros R, Ampuero I, et al. (febreiro de 2004). "The new mutation, E46K, of alpha-synuclein causes Parkinson and Lewy body dementia". Annals of Neurology 55 (2): 164–73. PMID 14755719. doi:10.1002/ana.10795.
- ↑ Appel-Cresswell S, Vilarino-Guell C, Encarnacion M, Sherman H, Yu I, Shah B, et al. (xuño de 2013). "Alpha-synuclein p.H50Q, a novel pathogenic mutation for Parkinson's disease". Movement Disorders 28 (6): 811–3. PMID 23457019. doi:10.1002/mds.25421.
- ↑ Lesage S, Anheim M, Letournel F, Bousset L, Honoré A, Rozas N, et al. (abril de 2013). "G51D α-synuclein mutation causes a novel parkinsonian-pyramidal syndrome". Annals of Neurology 73 (4): 459–71. PMID 23526723. doi:10.1002/ana.23894.
- ↑ Flagmeier P, Meisl G, Vendruscolo M, Knowles TP, Dobson CM, Buell AK, Galvagnion C (setembro de 2016). "Mutations associated with familial Parkinson's disease alter the initiation and amplification steps of α-synuclein aggregation". Proceedings of the National Academy of Sciences of the United States of America 113 (37): 10328–33. PMC 5027465. PMID 27573854. doi:10.1073/pnas.1604645113.
- ↑ Singleton AB, Farrer M, Johnson J, Singleton A, Hague S, Kachergus J, et al. (outubro de 2003). "alpha-Synuclein locus triplication causes Parkinson's disease". Science 302 (5646): 841. PMID 14593171. doi:10.1126/science.1090278.
- ↑ Chartier-Harlin MC, Kachergus J, Roumier C, Mouroux V, Douay X, Lincoln S, Levecque C, Larvor L, Andrieux J, Hulihan M, Waucquier N, Defebvre L, Amouyel P, Farrer M, Destée A (2004). "Alpha-synuclein locus duplication as a cause of familial Parkinson's disease". Lancet 364 (9440): 1167–9. PMID 15451224. doi:10.1016/S0140-6736(04)17103-1.
- ↑ Eslamboli, A., Romero-Ramos, M., Burger, C., Bjorklund, T., Muzyczka, N. Mandel, R.J., Baker, H.F., Ridley, R.M., and Kirik, D. (2007). "Long-term consequences of human alpha-synuclein over-expression in the primate ventral midbrain.". Brain 130 (3): 799–815. PMID 17303591. doi:10.1093/brain/awl382.
- ↑ Takeda A, Hashimoto M, Mallory M, Sundsumo M, Hansen L, Masliah E (marzo de 2000). "C-terminal alpha-synuclein immunoreactivity in structures other than Lewy bodies in neurodegenerative disorders". Acta Neuropathologica 99 (3): 296–304. PMID 10663973. doi:10.1007/PL00007441.
- ↑ Prusiner SB, Woerman AL, Mordes DA, Watts JC, Rampersaud R, Berry DB, et al. (setembro de 2015). "Evidence for α-synuclein prions causing multiple system atrophy in humans with parkinsonism". Proceedings of the National Academy of Sciences of the United States of America 112 (38): E5308–17. Bibcode:2015PNAS..112E5308P. PMC 4586853. PMID 26324905. doi:10.1073/pnas.1514475112.
- ↑ Weiler N (31 de agosto de 2015). "New Type of Prion May Cause, Transmit Neurodegeneration".
- ↑ Rettner R (31 de agosto de 2015). "Another Fatal Brain Disease May Come from the Spread of 'Prion' Proteins". Wired Science.
- ↑ 91,0 91,1 Cookson MR (febreiro de 2009). "alpha-Synuclein and neuronal cell death". Molecular Neurodegeneration 4 (1): 9. PMC 2646729. PMID 19193223. doi:10.1186/1750-1326-4-9.
- ↑ Fujiwara H, Hasegawa M, Dohmae N, Kawashima A, Masliah E, Goldberg MS, et al. (febreiro de 2002). "alpha-Synuclein is phosphorylated in synucleinopathy lesions". Nature Cell Biology 4 (2): 160–4. PMID 11813001. doi:10.1038/ncb748.
- ↑ Wersinger C, Sidhu A (abril de 2003). "Attenuation of dopamine transporter activity by alpha-synuclein". Neuroscience Letters 340 (3): 189–92. PMID 12672538. doi:10.1016/S0304-3940(03)00097-1.
- ↑ Lee FJ, Liu F, Pristupa ZB, Niznik HB (abril de 2001). "Direct binding and functional coupling of alpha-synuclein to the dopamine transporters accelerate dopamine-induced apoptosis". FASEB Journal 15 (6): 916–26. PMID 11292651. doi:10.1096/fj.00-0334com.
- ↑ Choi P, Golts N, Snyder H, Chong M, Petrucelli L, Hardy J, et al. (setembro de 2001). "Co-association of parkin and alpha-synuclein". NeuroReport 12 (13): 2839–43. PMID 11588587. doi:10.1097/00001756-200109170-00017.
- ↑ Kawahara K, Hashimoto M, Bar-On P, Ho GJ, Crews L, Mizuno H, et al. (marzo de 2008). "alpha-Synuclein aggregates interfere with Parkin solubility and distribution: role in the pathogenesis of Parkinson disease". The Journal of Biological Chemistry 283 (11): 6979–87. PMID 18195004. doi:10.1074/jbc.M710418200.
- ↑ Ahn BH, Rhim H, Kim SY, Sung YM, Lee MY, Choi JY, et al. (abril de 2002). "alpha-Synuclein interacts with phospholipase D isozymes and inhibits pervanadate-induced phospholipase D activation in human embryonic kidney-293 cells" (PDF). The Journal of Biological Chemistry 277 (14): 12334–42. PMID 11821392. doi:10.1074/jbc.M110414200.
- ↑ Neystat M, Rzhetskaya M, Kholodilov N, Burke RE (xuño de 2002). "Analysis of synphilin-1 and synuclein interactions by yeast two-hybrid beta-galactosidase liquid assay". Neuroscience Letters 325 (2): 119–23. PMID 12044636. doi:10.1016/S0304-3940(02)00253-7.
- ↑ Reed JC, Meister L, Tanaka S, Cuddy M, Yum S, Geyer C, Pleasure D (decembro de 1991). "Differential expression of bcl2 protooncogene in neuroblastoma and other human tumor cell lines of neural origin". Cancer Research 51 (24): 6529–38. PMID 1742726.
- ↑ Kawamata H, McLean PJ, Sharma N, Hyman BT (maio de 2001). "Interaction of alpha-synuclein and synphilin-1: effect of Parkinson's disease-associated mutations". Journal of Neurochemistry 77 (3): 929–34. PMID 11331421. doi:10.1046/j.1471-4159.2001.00301.x.
- ↑ Engelender S, Kaminsky Z, Guo X, Sharp AH, Amaravi RK, Kleiderlein JJ, et al. (maio de 1999). "Synphilin-1 associates with alpha-synuclein and promotes the formation of cytosolic inclusions". Nature Genetics 22 (1): 110–4. PMID 10319874. doi:10.1038/8820.
- ↑ Jensen PH, Hager H, Nielsen MS, Hojrup P, Gliemann J, Jakes R (setembro de 1999). "alpha-synuclein binds to Tau and stimulates the protein kinase A-catalyzed tau phosphorylation of serine residues 262 and 356". The Journal of Biological Chemistry 274 (36): 25481–9. PMID 10464279. doi:10.1074/jbc.274.36.25481.
- ↑ Giasson BI, Lee VM, Trojanowski JQ (2003). "Interactions of amyloidogenic proteins". Neuromolecular Medicine 4 (1–2): 49–58. PMID 14528052. doi:10.1385/NMM:4:1-2:49.
- ↑ Ono K, Takahashi R, Ikeda T, Yamada M (setembro de 2012). "Cross-seeding effects of amyloid β-protein and α-synuclein". Journal of Neurochemistry 122 (5): 883–90. PMID 22734715. doi:10.1111/j.1471-4159.2012.07847.x. hdl:2297/34736.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Bibliografía[editar | editar a fonte]
- Blakeslee S (2002-05-27). "In Folding Proteins, Clues to Many Diseases -". New York Times.
- Polymeropoulos MH, Lavedan C, Leroy E, Ide SE, Dehejia A, Dutra A, et al. (xuño de 1997). "Mutation in the alpha-synuclein gene identified in families with Parkinson's disease". Science 276 (5321): 2045–7. PMID 9197268. doi:10.1126/science.276.5321.2045.
- Neumann M, Kahle PJ, Giasson BI, Ozmen L, Borroni E, Spooren W, et al. (novembro de 2002). "Misfolded proteinase K-resistant hyperphosphorylated alpha-synuclein in aged transgenic mice with locomotor deterioration and in human alpha-synucleinopathies". The Journal of Clinical Investigation 110 (10): 1429–39. PMC 151810. PMID 12438441. doi:10.1172/JCI15777.
- George JM (2001). "The synucleins". Genome Biology 3 (1): REVIEWS3002. PMC 150459. PMID 11806835. doi:10.1186/gb-2001-3-1-reviews3002.
- Lavedan C (setembro de 1998). "The synuclein family". Genome Research 8 (9): 871–80. PMID 9750188. doi:10.1101/gr.8.9.871.
- Ozawa T, Wakabayashi K, Oyanagi K (febreiro de 2002). "[Recent progress in the research of multiple system atrophy with special references to alpha-synuclein and suprachiasmatic nucleus]". No to Shinkei = Brain and Nerve 54 (2): 111–7. PMID 11889756.
- Cole NB, Murphy DD (2002). "The cell biology of alpha-synuclein: a sticky problem?". Neuromolecular Medicine 1 (2): 95–109. PMID 12025860. doi:10.1385/NMM:1:2:95.
- Iwatsubo T (xuño de 2002). "[alpha-synuclein and Parkinson's disease]". Seikagaku. The Journal of Japanese Biochemical Society 74 (6): 477–82. PMID 12138709.
- Trojanowski JQ, Lee VM (outubro de 2002). "Parkinson's disease and related synucleinopathies are a new class of nervous system amyloidoses". Neurotoxicology 23 (4–5): 457–60. PMID 12428717. doi:10.1016/S0161-813X(02)00065-7.
- Alves da Costa C (febreiro de 2003). "Recent advances on alpha-synuclein cell biology: functions and dysfunctions". Current Molecular Medicine 3 (1): 17–24. PMID 12558071. doi:10.2174/1566524033361690.
- Ma QL, Chan P, Yoshii M, Uéda K (abril de 2003). "Alpha-synuclein aggregation and neurodegenerative diseases". Journal of Alzheimer's Disease 5 (2): 139–48. PMID 12719631. doi:10.3233/JAD-2003-5208.
- Di Rosa G, Puzzo D, Sant'Angelo A, Trinchese F, Arancio O (outubro de 2003). "Alpha-synuclein: between synaptic function and dysfunction". Histology and Histopathology 18 (4): 1257–66. PMID 12973692. doi:10.14670/HH-18.1257.
- Baptista MJ, Cookson MR, Miller DW (febreiro de 2004). "Parkin and alpha-synuclein: opponent actions in the pathogenesis of Parkinson's disease". The Neuroscientist 10 (1): 63–72. PMID 14987449. doi:10.1177/1073858403260392.
- Kim S, Seo JH, Suh YH (maio de 2004). "Alpha-synuclein, Parkinson's disease, and Alzheimer's disease". Parkinsonism & Related Disorders. 10 Suppl 1: S9–13. PMID 15109581. doi:10.1016/j.parkreldis.2003.11.005.
- Sidhu A, Wersinger C, Vernier P (maio de 2004). "alpha-Synuclein regulation of the dopaminergic transporter: a possible role in the pathogenesis of Parkinson's disease". FEBS Letters 565 (1–3): 1–5. PMID 15135042. doi:10.1016/j.febslet.2004.03.063.
- Vekrellis K, Rideout HJ, Stefanis L (agosto de 2004). "Neurobiology of alpha-synuclein". Molecular Neurobiology 30 (1): 001–022. PMID 15247485. doi:10.1385/MN:30:1:001.
- Chiba-Falek O, Nussbaum RL (2004). "Regulation of alpha-synuclein expression: implications for Parkinson's disease". Cold Spring Harbor Symposia on Quantitative Biology 68: 409–15. PMID 15338643. doi:10.1101/sqb.2003.68.409.
- Pankratz N, Foroud T (abril de 2004). "Genetics of Parkinson disease". NeuroRx 1 (2): 235–42. PMC 534935. PMID 15717024. doi:10.1602/neurorx.1.2.235.
- Singleton AB (agosto de 2005). "Altered alpha-synuclein homeostasis causing Parkinson's disease: the potential roles of dardarin". Trends in Neurosciences 28 (8): 416–21. PMID 15955578. doi:10.1016/j.tins.2005.05.009.
- Yu S, Uéda K, Chan P (2005). "Alpha-synuclein and dopamine metabolism". Molecular Neurobiology 31 (1–3): 243–54. PMID 15953825. doi:10.1385/MN:31:1-3:243.
- Lee HG, Zhu X, Takeda A, Perry G, Smith MA (xullo de 2006). "Emerging evidence for the neuroprotective role of alpha-synuclein". Experimental Neurology 200 (1): 1–7. PMID 16780837. doi:10.1016/j.expneurol.2006.04.024.
- Giorgi FS, Bandettini di Poggio A, Battaglia G, Pellegrini A, Murri L, Ruggieri S, et al. (2006). "A short overview on the role of alpha-synuclein and proteasome in experimental models of Parkinson's disease". Journal of Neural Transmission. Supplementum 70 (70): 105–9. ISBN 978-3-211-28927-3. PMID 17017516. doi:10.1007/978-3-211-45295-0_17.
Ligazóns externas[editar | editar a fonte]
- alpha-Synuclein Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- Localización no xenoma humano de SNCA e páxina con detalles sobre o xene SNCA no UCSC Genome Browser.
