Tripsina
| Tripsina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Número EC | 3.4.21.4 | ||||||||
| Número CAS | 9002-07-7 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| Gene Ontology | AmiGO / EGO | ||||||||
| |||||||||
| Tripsina | |||||||||
|---|---|---|---|---|---|---|---|---|---|
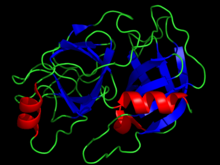 | |||||||||
| Identificadores | |||||||||
| Símbolo | Trypsin | ||||||||
| Pfam | PF00089 | ||||||||
| InterPro | IPR001254 | ||||||||
| SMART | SM00020 | ||||||||
| PROSITE | PDOC00124 | ||||||||
| MEROPS | S1 | ||||||||
| SCOPe | 1c2g / SUPFAM | ||||||||
| CDD | cd00190 | ||||||||
| |||||||||
A tripsina é un encima (co número EC 3.4.21.4) do grupo das serina proteases, que se encontra no aparato dixestivo de moitos vertebrados, onde intervén na hidrólise dixestiva de proteínas.[2][3] A tripsina prodúcese no páncreas en forma do proencima inactivo tripsinóxeno. A tripsina cliva as cadeas de péptidos principalmente polo grupo carboxilo dos aminoácidos lisina ou arxinina, excepto cando calquera deles vai seguido de prolina. Utilízase tamén en moitos procesos biotecnolóxicos. A súa acción denomínase xeralmente proteólise por tripsina ou tripsinización, e as proteínas que foron dixeridas/tratadas con tripsina dise que foron tripsinizadas.
Tripsinóxeno[editar | editar a fonte]
O tripsinóxeno (EC 3.4.23.18/20/21/23/24/26) é a forma precursora ou cimóxeno da tripsina e funciona como unha forma de almacenamento da tripsina no páncreas, que pode ser liberada en cantidades significativas durante a dixestión. Encóntrase no zume pancreático xunto coa amilase, a lipase, e o quimotripsinóxeno. O tripsinóxeno almacénase en vesículas intracelulares chamadas gránulos de cimóxeno, que teñen membranas que se cre son resistentes á degradación encimática.
Función da tripsina[editar | editar a fonte]
A tripsina no duodeno cataliza a hidrólise de enlaces peptídicos para que as proteínas poidan ser divididas en péptidos máis pequenos. Estes péptidos poden despois ser hidrolizados a aminoácidos por outras proteases antes de entraren na corrente sanguínea. A dixestión por tripsina é un paso necesario para a absorción das proteínas, porque as proteínas xeralmente son demasiado grandes para ser absorbidas a través do revestimento interno do intestino delgado.
Activación[editar | editar a fonte]
A tripsina prodúcese no páncreas en forma do cimóxeno inactivo tripsinóxeno. Cando o páncreas é estimulado pola colecistoquinina, o cimóxeno é despois segregado na primeira parte do intestino delgado (o duodeno) a través do conduto pancreático. Unha vez que está no intestino delgado, o encima enteropeptidase actívaa ao transformar o tripsinóxeno en tripsina por medio de clivaxe proteolítica. A propia tripsina pode despois activar a máis tripsinóxeno (autocatálise), polo que só cómpre unha pequena cantidade de enteropeptidase para que se inicie a reacción. Este mecanismo de activación é común para a maioría das serina proteases, e serve para impedir a autodegradación do páncreas (o páncreas podería autodixerirse se a tripsina estivese activa alí). A tripsina pode activar tamén a outras proteases como o precursor da quimotripsina.
A enteropeptidase, tamén chamada enteroquinase, producida pola mucosa do duodeno, cliva o enlace peptídico do tripsinóxeno situado detrás do residuo 15, que é unha lisina. Elimínase o péptido N-terminal de 15 aminoácidos, e prodúcese un lixeiro rearranxo no pregamento da proteína. O novo residuo N-terminal orixinado (o que era o residuo 16) insírese nunha fenda onde o seu grupo α-amino forma un par iónico co aspartato situado preto do sitio activo serina, e isto causa o rearranxo conformacional doutros residuos. O grupo amino da glicina 193 oriéntase na correcta posición, o cal completa o burato de oxianión no sitio activo, e a proteína queda activada.[4].
Nun páncreas normal, chega a activarse arredor do 5% do tripsinóxeno, polo que hai defensas contra esta inapropiada activación, como a presenza de inhibidores da tripsina. A activación autocatalítica do tripsinóxeno pola tripsina é tamén un proceso lento debido á presenza de carga negativa no hexapéptido N-terminal do tripsinóxeno, que repele o aspartato situado na parte de atrás do peto (pocket) de especificidade da tripsina.[5] A tripsina pode inactivar a outras tripsinas por clivaxe.
Mecanismo de acción[editar | editar a fonte]
O mecanismo encimático é similar ao doutras serina proteases. Estes encimas conteñen unha tríade catalítica que consta de histidina-57, aspartato-102 e serina-195 (os números son as posicións na cadea polipeptídica).[6] Estes tres residuos forman un relevo de carga (charge relay) que serve para facer nucleofílico o sitio activo serina. Isto conséguese modificando o ambiente electrostático arredor da serina. A reacción encimática que cataliza a tripsina é termodinamicamente favorable pero require unha enerxía de activación significativa (é "cineticamente desfavorable"). Ademais, a tripsina contén un "burato de oxianión" formado polo esqueleto de átomos de hidróxeno da amida da Gly-193 e a Ser-195, que serve para estabilizar a carga negativa que se desenvolve no átomo de oxíxeno carbonílico das amidas clivadas.
O residuo aspartato (Asp 189) localizado no peto (pocket) catalítico (S1) das tripsinas é responsable da atracción e estabilización das lisina e/ou arxinina cargadas positivamente, e, deste xeito, é responsable da especificidade do encima. Isto significa que a tripsina cliva predominantemente proteínas no lado carboxilo (ou "lado C-terminal") dos aminoácidos lisina e arxinina excepto cando calquera delas está unida a unha prolina N-terminal.[7], aínda que os datos de espectrometría de masas a grande escala suxiren que a clivaxe ocorre mesmo en presenza de prolina.[8] As tripsinas considéranse endopeptidases, é dicir, a clivaxe (corte) que realizan ocorre no interior da cadea polipeptídica en vez de nos extremos da mesma.
Propiedades da tripsina[editar | editar a fonte]
As tripsinas teñen un pH óptimo de funcionamento de 7,5-8,5 e unha temperatura óptima de arredor de 37 °C.[7]
A actividade das tripsinas non está afectada polo inhibidor tosil fenilalanil clorometil cetona (TPCK), que desactiva a quimotripsina. Isto é importante porque, nalgunhas aplicacións, como na espectrometría de masas, a especificidade de clivaxe é importante.
As tripsinas deberían almacenarse a temperaturas moi frías (entre −20 °C e −80 °C) para impedir a autólise, a cal pode impedirse tamén almacenándoas a pH 3 ou usando tripsina modificada por metilación redutiva. Cando o pH se axusta de novo a pH 8, recuperan a actividade.
Isoencimas[editar | editar a fonte]
Os seguintes xenes humanos codifican proteínas con actividade encimática de tripsina:
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Noutros organismos poden encontrarse outras isoformas da tripsina.
Estes tipos de tripsina están en correspondencia coas tres isoformas de tripsinóxeno que poden encontrarse no zume pancreático humano. Son os tripsinóxenos catiónico (dá a tripsina 1), aniónico (tripsina 2) e meso (mesotripsina), que supoñen respectivamente o 23,1%, 16% e 0,5% do total das proteínas de secreción pancreáticas.[9]
Importancia médica[editar | editar a fonte]
A activación da tripsina por clivaxe (corte) proteolítica do tripsinóxeno no páncreas pode dar lugar a unha serie de eventos que causan a autodixestión do páncreas, o que orixina pancreatite. Unha consecuencia da enfermidade autosómica recesiva fibrose quística é a deficiencia no transporte de tripsina e outros encimas dixestivos desde o páncreas. Isto causa un trastorno denominado meconium ileus. O meconio son as feces producidas polos neonatos. Este trastorno implica a obstrución intestinal debido á formación de meconio demasiado mesto, o cal en condicións normais sería degradado polas tripsinas e outras proteases, e despois evacuado coas feces.[10]
No soro sanguíneo pode medirse a cantidade de tripsinóxeno por medio dunha análise de sangue. Aparecen niveis altos en casos de pancreatite e fibrose quística.
Algúns tipos de pancreatite poden estar asociadas con formas mutantes do tripsinóxeno. Unha mutación na arxinina 117, un sitio sensible á clivaxe por tripsina, no tripsinóxeno catiónico foi implicado na heredabilidade da pancreatite, un trastorno xenético raro de inicio temperá. A arxinina 117 pode funcionar como un mecanismo a proba de fallos polo cal a tripsina que está está inapropiadamente activa no páncreas, pode ser inactivada, e ao perder ese sitio de clivaxe pérdese tamén ese sitio de control, o que pode causar a autodixestión que dá lugar á pancreatite.[11] Atopáronse outras mutacións que foron ligadas á pancreatite.[12]
Aplicacións[editar | editar a fonte]
A tripsina está presente no páncreas en grandes cantidades (en forma do seu precursor) e pode ser purificada doadamente, polo que se usa moito en diversos procesos biotecnolóxicos.
Nos laboratorios de cultivo de tecidos, as tripsinas utilízanse para resuspender células adheridas ás paredes da placa de cultivo celular durante o proceso de colleita de células.[13] Algúns tipos celulares teñen a tendencia a adheririse ás paredes laterais ou ao fondo da placa de cultivo cando se cultivan in vitro. A tripsina utilízase para clivar as proteínas que unen as células cultivadas á placa, para que as células se poidan suspender en novas solucións e transferirse a novas placas.
A tripsina pode tamén usarse para disociar células disecadas (por exemplo, antes de fixar e seleccionar as células).
As tripsinas poden usarse para degradar a caseína no leite humano. Se se engade tripsina a unha solución de leite en po, a rotura das moléculas de caseína fai que o leite se faga translúcido. O grao de reacción pode medirse vendo a cantidade de tempo que o leite tarda en poñerse translúcido.
A tripsina utilízase comunmente na investigación biolóxica durante experimentos de proteómica para dixerir proteínas a péptidos para a análise de espectrometría de masas, por exemplo na dixestión en xel. A tripsina é especialmente axeitada para iso, xa que ten unha especificade moi ben definida ao hidrolizar só os enlaces peptídicos nos cales o grupo carbonilo pertence a unha arxinina ou a unha lisina.
A tripsina pode tamén utilizarse para disolver certos coágulos de sangue e tratar a inflamación na súa forma pancreática.
En alimentación[editar | editar a fonte]
As preparacións comerciais de proteases xeralmente constan dunha mestura de varias proteases entre as que a miúdo está a tripsina. Estas preparacións son amplamente utilizadas no procesamento de alimentos:[14]
- como encima de enfornado para mellorar a traballabilidade das masas (de bolaría ou panadaría);
- na extracción de condimentos e aromas de proteínas vexetais ou animais e na elaboración de prebes;
- para controlar a formación do aroma nos queixos e nos produtos lácteos;
- para melorar a textura dos produtos de peixe;
- para abrandar a carne;
- durante a estabilización en frío da cervexa;
- na produción de alimentos hipoalerxénicos, nos que as proteases degradan proteínas específicas alerxénicas orixinando péptidos non alerxénicos. Por exemplo, as proteases úsanse para producir alimentos hipoalerxénicos para bebés a partir de leite de vaca, o que diminúe o risco de que os meniños desenvolvan alerxia ao leite.
Inhibidores da tripsina[editar | editar a fonte]
Para evitar a acción da tripsina activa no páncreas, que podería ser moi daniña, están presentes no páncreas inhibidores como BPTI e SPINK1 e no soro sanguíno a α1-antitripsina como parte da defensa contra a súa activación inadecuada. O inhibidor unirase a calquera tripsina formada prematuramente a partir do tripsinóxeno inactivo. A interacción proteína-proteína entre a tripsina e os seus inhibidores é unha das máis fortes coñecidas, e a tripsina únese a algúns dos seus inhibidores pancreáticos de modo esencialmente irreversible.[15] A diferenza do que ocorre con case todas as ensamblaxes coñecidas de proteínas, algúns complexos que forma a tripsina cos seus inhibidores non se disocian doadamente despois do tratamento con urea 8M.[16]
Notas[editar | editar a fonte]
- ↑ PDB|1UTN; Leiros HK, Brandsdal BO, Andersen OA, Os V, Leiros I, Helland R, Otlewski J, Willassen NP, Smalås AO (2004). "Trypsin specificity as elucidated by LIE calculations, X-ray structures, and association constant measurements". Protein Sci. 13 (4): 1056–70. PMC 2280040. PMID 15044735. doi:10.1110/ps.03498604.
- ↑ Rawlings ND, Barrett AJ (1994). "Families of serine peptidases". Meth. Enzymol. Methods in Enzymology 244: 19–61. ISBN 978-0-12-182145-6. PMID 7845208. doi:10.1016/0076-6879(94)44004-2.
- ↑ The German physiologist Wilhelm Kühne (1837-1900) discovered trypsin in 1876. See: W. Kühne (1877) "Über das Trypsin (Enzym des Pankreas)", Verhandlungen des naturhistorisch-medicinischen Vereins zu Heidelberg, new series, vol. 1, no. 3, pages 194-198.
- ↑ Thomas E Creighton (1993). Proteins: Structures and Molecular Properties (2nd ed.). W H Freeman and Company. pp. 434. ISBN 0-7167-2317-4.
- ↑ Voet & Voet (1995). Biochemisty (2nd ed.). John Wiley & Sons. pp. 399-400. ISBN 0-471-58651-X.
- ↑ Polgár L (2005). "The catalytic triad of serine peptidases". Cell. Mol. Life Sci. 62 (19–20): 2161–72. PMID 16003488. doi:10.1007/s00018-005-5160-x.
- ↑ 7,0 7,1 "Sequencing Grade Modified Trypsin" (PDF). www.promega.com. 2007-04-01. Arquivado dende o orixinal (PDF) o 19 de maio de 2003. Consultado o 2009-02-08.
- ↑ Rodriguez J, Gupta N, Smith RD, Pevzner PA (2008). "Does trypsin cut before proline?". J. Proteome Res. 7 (1): 300–305. PMID 18067249. doi:10.1021/pr0705035.
- ↑ Scheele G, Bartelt D, Bieger W (March 1981). "Characterization of human exocrine pancreatic proteins by two-dimensional isoelectric focusing/sodium dodecyl sulfate gel electrophoresis". Gastroenterology 80 (3): 461–73. PMID 6969677.
- ↑ Noone PG, Zhou Z, Silverman LM, Jowell PS, Knowles MR, Cohn JA (2001). "Cystic fibrosis gene mutations and pancreatitis risk: relation to epithelial ion transport and trypsin inhibitor gene mutations". Gastroenterology 121 (6): 1310–9. PMID 11729110. doi:10.1053/gast.2001.29673.
- ↑ Whitcomb DC, Gorry MC, Preston RA, Furey W, Sossenheimer MJ, Ulrich CD, Martin SP, Gates LK Jr, Amann ST, Toskes PP, Liddle R, McGrath K, Uomo G, Post JC, Ehrlich GD (1996). "Hereditary pancreatitis is caused by a mutation in the cationic trypsinogen gene". Nature Genetics 14 (2): 141–5. PMID 8841182. doi:10.1038/ng1096-141.
- ↑ Rebours V, Lévy P, Ruszniewski P (2011). "An overview of hereditary pancreatitiss". Digestive and Liver Disease 44 (1): 8–15. PMID 21907651. doi:10.1016/j.dld.2011.08.003.
- ↑ "Trypsin-EDTA (0.25%)". Stem Cell Technologies. Consultado o 2012-02-23.
- ↑ "Protease - GMO Database". GMO Compass. European Union. 2010-07-10. Arquivado dende o orixinal o 24 de febreiro de 2015. Consultado o 2012-01-01.
- ↑ Voet & Voet (1995). Biochemisty (2nd ed.). John Wiley & Sons. pp. 396-400. ISBN 0-471-58651-X.
- ↑ N. Levilliers, M. Péron, B. Arrio, J. Pudles (1970). "On the mechanism of action of proteolyticinhibitors: IV. Effect of 8murea on the stability of trypsin in trypsin-lnhibitor complexes". Archives of Biochemistry and Biophysics 140 (2): 474–483. PMID 5528741.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Base de datos en liña MEROPS para as peptidases e os seus inhibidores: Tripsina 1 S01.151 Arquivado 05 de abril de 2008 en Wayback Machine., Tripsina 2 S01.258 Arquivado 19 de setembro de 2019 en Wayback Machine., Tripsina 3 S01.174 Arquivado 19 de setembro de 2019 en Wayback Machine.
- Inhibidores da tripsina Arquivado 23 de abril de 2008 en Wayback Machine. e Trypsin Assay Method en Sigma-Aldrich
- MeshName - Trypsin
- MeshName - Trypsinogen
