Telómero
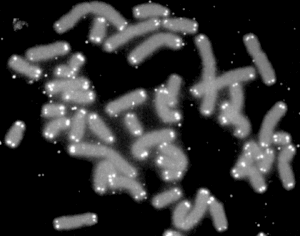
O telómero (do grego τέλος telos 'final' e μέρος meros 'parte') é a rexión terminal do cromosoma, composta por ADN moi repetitivo, que non codifica proteínas. Xoga un papel fundamental para evitar a perda de información durante a duplicación do cromosoma. O encima que replica o ADN, a ADN polimerase, non pode replicar o cromosoma ata o seu extremo, polo que se perde unha parte dese extremo en cada replicación; pero a parte que se perde é a dos telómeros, que non son codificantes, e que por iso se fan máis curtos en cada replicación. Se non fose por eles a parte que se perdería sería codificante, o que supoñería unha perda significativa de información xenética en cada replicación. Hai probas de que este acurtamento dos telómeros está asociado co envellecemento da célula e do organismo.
Historia
[editar | editar a fonte]Os telómeros foron descubertos por Hermann Joseph Muller na década de 1930, o cal, xunto con Barbara McClintock, recibiu o Premio Nobel. Propoñían que os telómeros, situados nos extremos dos cromosomas, tiñan a función de impedir que estes se fusionasen ao poñerse en contacto polos seus extremos. Desde entón, avanzouse moito no coñecemento dos telómeros, grazas ás técnicas de xenética molecular.
Os científicos Elizabeth Blackburn, Carol Greider e Jack Szostak foron galardoados co Premio Nobel de Medicina en 2009 pola descrición molecular dos telómeros, a demostración da súa conservación evolutiva e o descubrimento do encima telomerase, elaborando un modelo moi consistente que explica o "problema da terminación da replicación" e o mecanismo molecular de protección dos extremos cromosómicos.
Natureza e función dos telómeros
[editar | editar a fonte]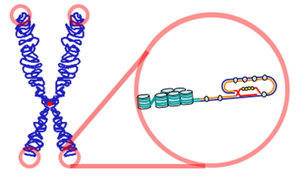

O telómero está composto por secuencias repetidas de ADN que adoptan unha disposición característica e dalgunhas proteínas, e ten a función de protexer as terminacións dos cromosomas. Isto impide por unha parte a degradación progresiva con risco de perda de información, e por outra que ditas rexións, que non presentan unha estrutura correcta en dobre hélice, sexan procesadas como extremos de filamento roto, e impide a fusión entre dúas rexións teloméricas de cromosomas distintos.
Partes dun telómero. Un telómero humano consta de tres partes, que desde que empeza o tramo terminal do cromosoma (zona proximal do telómero) ao extremo final (zona distal) son as seguintes:
- Zona de 100–300 kb con repeticións de bases asociadas aos telómeros. É a zona que conecta o telómero co resto do cromosoma (parte proximal do telómero).
- Zona de 3 a 20 kb situada despois da anterior cunha secuencia repetida de bases, que no home é de seis nucleótidos: TTAGGG. A secuencia repítese moitas veces ata abranguer a lonxitude indicada e forma unha estrutura chamada cuádruplex.
- 5'-TTAGGG TTAGGG TTAGGG TTAGGG...3'
- 3'-AATCCC AATCCC AATCCC AATCCC...5'
- Zona distal final de 300 pb, onde o telómero acaba. É monocatenaria e forma un bucle pregado sobre si mesmo, chamado bucle T, mantido nesa posición por proteínas.
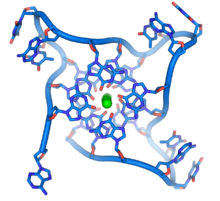
No home a secuencia repetida dos telómeros está composta por seis nucleótidos TTAGGG, que se repiten ata ocupar unha lonxitude de 3 a 20 kb, pero a secuencia telomérica varía entre especies (véxase a táboa do apartado secuencias teloméricas), e xeralmente unha das cadeas é rica en G e pobre en C. Estas secuencias ricas en G poden dispoñerse formando estruturas de catro cadeas chamadas G-cuadrúplex, que constan de conxuntos de catro bases situadas no mesmo plano e amoreadas unhas enriba das outras con ións sodio ou potasio entre cada plano do cuádruplex. Se o telómero é moi curto non pode formar estas estruturas, a célula pode detectar este incorrecto pregamento e considérao como un dano do ADN, polo que detén o crecemento celular ou pon en marcha a vía da apoptose por medio de moléculas como a p53. Tal proceso de morte celular pode tamén ser iniciado por unha fusión entre cromosomas.
A zona distal dos telómeros está formada por unha zona de 300 pb dunha soa cadea (aquí o ADN non é bicatenario), que forma o chamado bucle T. Este bucle é análogo a un nó que estabiliza o telómero, impedindo que os extremos do telómero sexan recoñecidos pola maquinaria de reparación do ADN como puntos de rotura do ADN. Se estas zonas monocatenarias estivesen despregadas e se producise a unión dos extremos de dous cromosomas non homólogos, os cromosomas poderían acabar fusionándose. O bucle T mantense dobrado pola acción de sete proteínas coñecidas, as máis importantes forman un complexo (shelterin complex), e son TRF1, TRF2, POT1, TIN1, e TIN2.
Os telómeros pode agrandalos o encima telomerase, que é unha clase de retrotrascritase ou reversotranscriptase especializada, presente en numerosos organismos (entre eles o home), mais non en todos nin en todas as fases do desenvolvemento. No caso humano e na maior parte dos eucariotas multicelulares as telomerases están activas só nas células da liña xerminal. Como nas demais células non está activa, en cada replicación os telómeros humanos se acurtan nun certo número de pares de bases.
Existen teorías que asocian o continuo acurtamento dos telómeros coa senescencia das células da liña somática e coa prevención do cancro. Os telómeros funcionarían como unha especie de reloxo biolóxico, que determinaría un número máximo posible de mitoses (e de replicacións do ADN), ao final das cales a célula sería demasiado vella para ser mantida con vida e tomaría a vía da apoptose. Para garantir un eficaz recambio celular, en moitos tecidos do organismo están presentes células troncais ou nais, que manteñen a lonxitude correcta dos telómeros por medio de mecanismos diversos, xa que, como se dixo, as telomerases exprésanse só na liña xerminal. Elaborouse unha teoría aplicable ás células troncais, a teoría do filamento immortal, segundo a cal, estas, por medio dunha anafase especial, conservan para elas os dous filamentos de ADN cromosómico orixinais (non acurtados), deixando os filamentos acurtados pola replicación para as células fillas non troncais.
Na maior parte dos procariotas, os cromosomas son circulares, o que implica que non teñen ningún tipo de telómero. Porén, unha pequena parte das especies bacterianas poden ter cromosomas lineares e posúen rexións teloméricas, que son moi diferentes das eucariotas, tanto en estrutura coma en función. Este é o caso de Streptomyces e Borrelia.
Acurtamento dos telómeros
[editar | editar a fonte]
Os telómeros acórtanse a causa do mecanismo de replicación do filamento ou fibra retardada ou descontinua do ADN. O ADN en replicación presenta unha fibra líder ou condutora e unha fibra retardada ou descontinua. Isto débese a que a replicación do ADN non comeza polo seu extremo senón en varias rexións máis centrais á vez (orixes de replicación) e todas as ADN polimerases polimerizan en dirección 5'→3' (movéndose sobre o ADN en dirección 3'→5').
Na fibra líder a ADN polimerase pode producir un filamento complementario sen atopar obstáculos, porque avanza de 5' a 3' conforme os encimas desenredadores da dobre hélice van desenredando o ADN. Polo contrario, na outra fibra, que é antiparalela, a replicación orixina a fibra retardada, porque o encima debe avanzar pola fibra no sentido contrario en que esta se desenreda, polo que a replicación se fai por fragmentos, chamados fragmentos de Okazaki, xa que despois de sintetizar cada fragmento hai que esperar a que se desenrede outro tramo para facer o seguinte (de aí o retardo). Cada fragmento de Okazaki empézase sintetizando por un primer ou cebador de ARN feito por unha ARN polimerase, porque a ADN polimerase só pode colocar os nucleótidos sobre unha cadea xa existente (non pode colocar o primeiro nucleótido dunha cadea, empezándoa); pero unha vez feito o primer despois a ADN polimerase fai a replicación colocando nucleótidos de ADN a partir do primer.
Os fragmentos de Okazaki teñen pois, inicialmente, unha parte de ARN e outra de ADN. A parte de ARN é substituída por ADN encimaticamente en cada fragmento (os cebadores desaparecen) e seguidamente unha ADN ligase une por enlace fosfodiéster os fragmentos de Okazaki separados, convertendo a fibra retardada ou descontinua nunha fibra continua. Isto sucede sen problemas en todos os fragmentos de Okazaki, pero non onde aparece o último cebador de ARN. Nesta rexión o ARN do fragmento é destruído por ARNases, pero non se substitúe por ADN coma nos outros, polo que se perde ese cacho de ADN. Isto xera un continuo proceso de acurtamento nesta rexión terminal próxima ao telómero.
A telomerase
[editar | editar a fonte]A telomerase (TERT) é unha ribonucleoproteína que contén na súa molécula a secuencia AAUCCC, que ten a capacidade de crear e inserir os fragmentos TTAGGG que se perden en cada división e funciona como unha transcriptase inversa ou reversotranscriptase, que sintetiza ADN a partir dun molde de ARN. En 1998, Bodnar e col. introduciron en dous tipos de células humanas normais, telomerase-negativas, o xene que codifica a telomerase. A diferenza das células normais que mostraban senescencia e un acurtamento dos telómeros, os clons que expresaban a telomerase mostraron ter telómeros elongados, dividíanse vigorosamente e presentaban unha redución da beta-galactosidase, un biomarcador da senescencia. As células transformadas para expresar a telomerase tiñan un cariotipo normal e a súa lonxevidade superou a normal en máis de 20 divisións celulares.
Moitas células cancerosas derivan de células somáticas, e comprobouse a presenza de telomerase no 75-80% das liñas tumorais. Isto non quere dicir que a telomerase induza o cáncer. É máis, Kathleen Collins da Universidade de Berkeley en Califormia encontrou que doentes que padecían unha enfermidade conxénita moi pouco frecuente, a disqueratose conxénita, tiñan niveis de telomerase anormalmente baixos, e en moitos casos morrían a pesar de todo de cáncer gastrointestinal. Malia esta incongruencia, sábese que a agresividade das células tumorais está relacionada cos seus niveis de telomerase e que niveis altos deste encima son indicativos da malignidade do tumor. Recentemente a FDA autorizou dous estudos clínicos con telomerase, un deles encamiñado a obter un mellor diagnóstico do cáncer cervical e o outro para avaliar un fármaco contra a leucemia mieloide.
No Xapón, está utilizándose en nenos con neuroblastoma 4S. Parece que estes rapaces teñen un cáncer metastásico, pero os tumores son telomerase-negativos e aproximadamente o 80% chegan a unha remisión espontánea unha vez que o tumor foi eliminado cirurxicamente. O estudo identifica os que son telomerase-positivos, de maneira que poidan ser tratados dunha maneira máis agresiva.
Extensión dos telómeros e cancro
[editar | editar a fonte]A presenza dun límite no número de divisións celulares, debido ao acurtamento dos telómeros, foi descuberto por primeira vez por Leonard Hayflick. As súas observacións levárono a hipotizar un número máximo preciso de división mitóticas posibles, coñecido como límite de Hayflick.
A correlación entre senescencia celular e o número de Hayflick non foi probada ata 1998, cando a Compañía Geron puxo a punto técnicas que podían ampliar os telómeros, que orixinaban unha notable ralentización da senescenza da célula. O alongamento dos telómeros recibiu moita atención desde entón pola posibilidade de idear técnicas que aumenten a duración da vida. Isto podería facerse coa indución temporal (por vía farmacolóxica) ou permanente (por terapia xénica) da telomerase. En 2006 a Compañía Geron anunciou o descubrimento de dous fármacos que poderían activar a telomerase, pero isto non foi confirmado por estudos independentes.[1]
En 2003 os investigadores identificaron por primeira vez un organismo cuxos telómeros se estenden aumentando gradualmente co envellecemento do organismo. Tal organismo é a ave Oceanodroma leucorhoa (paíño gallado), que, de feito, pode vivir moito tempo.
Tamén un estudo feito no verme nematodo Caenorhabditis elegans indica que a extensión dos telómeros pode alongar a vida. Estudáronse dous grupos de vermes distintos, que tiñan como única diferenza a lonxitude dos telómeros. O verme cos telómeros máis longos mostrou, como media, unha esperanza de vida un 20% superior ca a do que non tiña os telómeros modificados. Un efecto colateral mostrado neste experimento en C. elegans é o incremento da resistencia á calor, do que non se sabe a razón [2].
A principal prevención que mostra a comunidade científica con respecto a este tipo de estratexias é que tales fármacos poderían supoñer un risco canceríxeno. O alongamento da vida dunha célula está, de feito, intrinsecamente correlacionado cun aumento da vulnerabilidade ao cancro [3].
Por outra parte, o mantemento da lonxitude dos telómeros é un signo distintivo de moitos tipos de cancro nos mamíferos. No home por exemplo, numerosos tumores teñen a capacidade de aumentar a actividade da teomerase, conseguindo unha capacidade de replicación case infinita. Outros tipos de carcinoma, polo contrario, teñen a capacidade de iniciar vías alternativas de alongamento dos telómeros, coñecidas como ALT (do inglés alternative lengthening of telomeres), que implican a transferencia de repeticións teloméricas en tándem entre cromátides irmás. O mecanismo de activación de ALT non está aínda ben definido.
As técnicas seguras de extensión dos telómeros serán útiles sobre todo no campo da enxeñaría de tecidos, xa que permitirían producir grandes cantidades de células sás e non canceríxenas para utilizalas como substitutas de tecidos danados, como, por exemplo, tecidos danados por queimadurras.
Porén, segundo outros investigadores os telómeros non serían un índice do potencial replicativo celular. Entre eles están:
Elizabeth H. Blackburn (co artigo en Nature 408,53,2000), Vincent Cristofalo[4], James Smith, Malcolm H. Goyns[5] e Harry Rubin[6].
Por exemplo, Goyns criou ratos privados do xene da telomerase, e comprobou que nas dúas xeracións observadas non había envellecemento precoz a pesar dos seus curtos telómeros; ademais hai que salientar que os telómeros dos ratos teñen unha lonxitude comprendida entre 20 e 250 kb, mentres que os humanos, especie que vive como media 40 veces máis, son de entre 15 e 25 kb.
Se a lonxitude dos telómeros fose unha especie de contador marcha atrás para a senescencia, e a Oceanodroma leucorhoa pode incrementalos, entón ese organismo debería tender á inmortalidae.
Secuencias teloméricas
[editar | editar a fonte]Notas
[editar | editar a fonte]- ↑ "human embryonic stem cell-based therapeutics. biopharmaceuticals". Geron. Arquivado dende o orixinal o 23 de maio de 2006. Consultado o 14 de xullo de 2011.
- ↑ * (en inglés) Joeng KS, Song EJ, Lee KJ, Lee J, Long lifespan in worms with long telomeric DNA, 2004
- ↑ * (en inglés) Weinstein B, Ciszek D, The Reserve Capacity Hypothesis, 2002
- ↑ PNAS,95,10614,1998
- ↑ Mech.Agein dev 114,69,2000
- ↑ Nature Biotech 16,396,1998
Véxase tamén
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Joeng KS, Song EJ, Lee KJ, Lee J, Long lifespan in worms with long telomeric DNA(en inglés)
- Weinstein B, Ciszek D, The Reserve Capacity Hypothesis(en inglés)
- Yu-Sheng Cong, Woodring E. Wright, and Jerry W. Shay (2002). "Human Telomerase and Its Regulation". Microbiology and Molecular Biology Reviews (en inglés) 66 (3): 407–25. PMID 12208997. doi:10.1128/MMBR.66.3.407-425.2002.
- Susan Bassham, Aaron Beam, and Janis Shampay (1998). "Telomere Variation in Xenopus laevis". Molecular and Cellular Biology: (en inglés) 18 (1): 269–275. PMC 121490. PMID 9418874. doi:10.1128/MMBR.66.3.407-425.2002.
- N Crumet, RL Carlson, SB Drutman, and Janis Shampay; A truncated acidic domain in Xenopus TRF1(en inglés)
Ligazóns externas
[editar | editar a fonte]- Senescence.info: Colección de datos sobre o papel dos telómeros no envellecemento celular.(en inglés)
- O encima telomerase na leucemia.(en inglés)
- Telomerase.org - banco de datos de artigos referentes á telomerase.(en inglés)
- Telomere.netArquivado 11 de agosto de 2011 en Wayback Machine.(en inglés)
- Telomere.org(en inglés)
