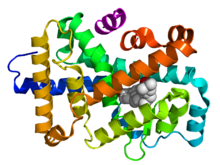
Receptor nuclear

En bioloxía molecular, os receptores nucleares son un tipo de proteínas que se encontran dentro das células que son responsables de detectar certas moléculas, como por exemplo as hormonas esteroides e tiroides. Como resposta á unión a estas moléculas, os receptores traballan conxuntamente con outras proteínas regulando a expresión de xenes específicos, controlando así o desenvolvemento, homeostase, e metabolismo do organismo.
Os receptores nucleares teñen a capacidade de unirse directamente ao ADN e regular a expresión de xenes adxacentes, polo que estes receptores se clasifican como factores de transcrición.[2][3] A regulación da expresión xénica feita polos receptores nucleares xeralmente só ocorre cando está presente un ligando (unha molécula que afecta ao comportamento do receptor). Máis especificamente, a unión do ligando a un receptor nuclear dá lugar a un cambio conformacional no receptor, o cal, á súa vez, activa o receptor, o que ten como resultado a regulación da expresión xénica á alza ou á baixa.
Unha característica peculiar dos receptores nucleares, que os diferencia doutras clases de receptores, é a súa capacidade de interaccionar directamente co ADN e controlar a expresión do ADN xenómico. Como consecuencia, os receptores nucleares xogan un papel clave no desenvolvemento embrionario e na homeostase do adulto. Como se discute máis abaixo, os receptores nucleares poden clasificarsse de acordo co seu mecanismo de acción[4][5] ou segundo a súa homoloxía.[6][7]
Distribución entre as especies[editar | editar a fonte]
Os receptores nucleares son específicos dos animais e non se encontran en protistas, algas, fungos, ou plantas.[8] Entre as primeiras liñas animais que apareceron na evolución con xenomas secuenciados, informouse da presenza de dous destes receptores na esponxa Amphimedon queenslandica, outros dous no ctenóforo Mnemiopsis leidyi[9] catro no placozoo Trichoplax adhaerens e 17 no cnidario Nematostella vectensis.[10] Atopáronse 270 receptores nucleares no nematodo C. elegans.[11] Os humanos, ratos e ratas teñen respectivamente 48, 49, e 47 receptores nucleares.[12]
Ligandos[editar | editar a fonte]

Entre os ligandos que se unen e activan os recptores nucleares están substancias lipófilas como as hormonas endóxenas, as vitaminas A e D, e perturbadores endócrinos xenobióticos. Como a expresión dun gran número de xenes está regulada por receptores nucleares, os ligandos que activan estes receptores poden ter profundos efectos sobre o organismo. Moitos destes xenes regulados están asociados con varias doenzas, o que explica por que as dianas moleculares de moitos fármacos son receptores nucleares (por exemplo nos Estados Unidos son o 13% dos fármacos aprobados pola FDA).[13]
Certos receptores nucleares, denominados receptores orfos,[14] non teñen ligandos endóxenos coñecidos (ou polo menos aceptados xeneralizadamente). Algúns destes receptores, como o FXR, LXR, e o PPAR únense a varios intermediarios metabólicos, como ácidos graxos, ácidos biliares e esterois con afinidade relativamente baixa. Estes receptores poden, por tanto, funcionar como sensores metabólicos. Outros receptores nuceares, como o CAR e o PXR parecen funcionar como sensores xenobióticos que regulan á alza a expresión de encimas citocromo P450 que metabolizan estes xenobióticos.[15]
Estrutura[editar | editar a fonte]
A maioría dos receptores nucleares teñen unha masa molecular entre 50.000 e 100.000 daltons.
Os receptores nucleares son de estrutura modular e conteñen os seguintes dominios estruturais:[16][17]
- (A-B) Dominio regulador N-terminal: Contén a función de activación 1 (AF-1) cuxa acción é independente da presenza do ligando.[18] A activación transcricional de AF-1 é normalmente moi feble, pero non se sinerxiza con AF-2 no dominio E (véxase máis abaixo) para producir unha regulación á alza máis robusta da expresión xénica. O dominio A-B é moi variable en secuencia entre varios receptores nucleares.
- (C) Dominio de unión ao ADN (DBD): Un dominio moi conservado que contén dous dedos de zinc que se unen a secuencias específicas de ADN chamadas elementos de resposta a hormonas (HRE, do inglés hormone response element).
- (D) Rexión bisagra: Crese que é un dominio flexible que conecta o dominio de unión ao ADN (DBD) co dominio de unión ao ligando (LBD). Inflúe no tráfico intracelular e na distribución subcelular.
- (E) Dominio de unión ao ligando (LBD): Un dominio de secuencia moderadamente conservada e de estrutura moi conservada entre os diversos receptores nucleares. A estrutura do dominio de unión ao ligando (LBD) é un pregamento en sándwich de hélices alfa no cal hai tres helices alfa antiparalelas (o "recheo" do sándwich) que están flanqueadas por dúas hélices alfa nun dos lados e tres no outro lado (o "pan" do sándwich). A cavidade para a unión do ligando está no interior do LBD e xusto debaixo das tres hélices alfa antiparalelas do "recheo" do sándwich. Xunto co dominio de unión ao ADN, o dominio de unión ao ligando contribúe á interface de dimerización do receptor, e ademais, a el únense proteínas coactivatoras e correpresoras. O dominio de unión ao ligando tamén contén a función de activación 2 (AF-2), cuxa acción depende de que haxa un ligando unido.[18]
- (F) Dominio C-terminal: Moi variable en secuencia entre diversos receptores nucleares.
Os dominios N-terminal (A/B), de unión ao ADN (C), e de unión ao ligando (E) están ben pregados independentemente e son estruturalmente estables, mentres que a rexión bisagra (D) e os dominios opcionais C-terminais (F) poden ser conformacionalmente flexibles e desordenados.[19] As orientacións relativas dos dominios son moi diferentes se comparamos as tres estruturas cristalinas multidominio coñecidas; dous deles únense en DR1,[1][20] e un únese en DR4.[21]
 Arriba – Secuencia de aminoácidos esquemática en 1D dun receptor nuclear. Abaixo – Estruturas 3D das rexións do dominio de unión ao ADN (unido ao ADN) e do dominio de unión ao ligando (unido a unha hormona) do receptor nuclear. As estruturas ilustradas son do receptor de estróxenos. As estruturas experimentais do dominio N-terminal (A/B), rexión bisagra (D), e dominio C-terminal (F) non foron determinados e están representados en liñas descontinuas en vermello, púrpura e laranxa, respectivamente. |
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Mecanismo de acción[editar | editar a fonte]


Os receptores nucleares (RN, ou, en inglés, NR) son proteínas multifuncionais que transducen sinais dos seus ligandos correspondentes. Os receptores nucleares poden clasificarse en dúas grandes clases segundo o seu mecanismo de acción e a distribución subcelular en ausencia de ligando.
As pequenas substancias lipófilas, como moitas hormonas naturais, poden difundir a través da membrana plasmática e únense a receptores nucleares localizados no citosol (os receptores nucleares de tipo I) ou no núcleo (os receptores nucleares de tipo II) da célula. A unión causa un cambio conformacional no receptor, o cal, dependendo da clase de receptor que sexa, desencadea unha fervenza de eventos augas abaixo da súa ruta, que dirixe os receptores nucleares aos sitios de regulación da transcrición do ADN, o que ten como resultado a regulación á alza ou á baixa da expresión xénica. Ademais, identificáronse outras dúas clases de receptores nucleares, que son os de tipo III, que son unha variante do tipo I, e os de tipo IV, que se poden unir ao ADN como monómeros.[4]
En consecuencia, os receptores nucleares poden subdividirse nas seguintes clases segundo o seu mecanismo:[4][5]
Tipo I[editar | editar a fonte]
A unión do ligando aos receptores nucleares de tipo I no citosol causa a disociación das proteínas de shock térmico, a homodimerización, a translocación (por transporte activo) desde o citoplasma ao núcleo celular, e a unión a secuencias específicas do ADN chamadas elementos de resposta a hormonas (HREs). Os receptores nucleares de tipo I únense a HREs que consisten en dúas rexións (dous "medios sitios") separados por un tramo de lonxitude variable de ADN, e o segundo destes medios sitios ten unha secuencia invertida con respecto ao primeiro (repetición invertida). Os receptores nucleares de tipo I inclúen os membros da subfamilia 3, como o receptor de andróxenos, receptores de estróxenos, receptor de glicocorticoides, e receptor de proxesterona.[24]
Algúns dos receptores nucleares da subfamilia 2 poden unirse a HREs con repeticións directas en vez de con repeticións invertidas. Ademais, algúns receptores nucleares únense tanto a monómeros coma a dímeros, de maneira que só un único dominio de unión ao ADN do receptor se une a un único medio sitio do HRE. Estes receptores nucleares son considerados receptores orfos, dado que os seus ligandos endóxenos son aínda descoñecidos.
Despois, O complexo receptor/ADN recruta outras proteínas que transcriben o ADN augas abaixo a partir do HRE orixinando ARN mensaxeiros e finalmente proteínas, o que causa un cambio no funcionamento celular.
Tipo II[editar | editar a fonte]
Os receptores de tipo II, a diferenza dos de tipo I, quedan retidos no núcleo independentemente do estado de unión co ligando e ademais únense como heterodímeros (xeralmente co RXR) ao ADN. En ausencia de ligando, os receptores nucleares de tipo II están a miúdo en complexo con proteínas correpresoras. A unión de ligandos ao receptor nuclear causa a disociación do correpresor e o recrutamento de proteínas coactivadoras. As proteínas adicionais como a ARN polimerase recrútanse despois e únense ao complexo receptor nuclear/ADN que transcribe o ADN en ARNm.
Os receptores nucleares de tipo II inclúen principalmente á subfamilia 1, por exemplo o receptor do ácido retinoico, o receptor X retinoide e o receptor de hormonas tiroides.[25]
Tipo III[editar | editar a fonte]
Os receptores nucleares de tipo III (principalmenre da subfamilia 2) parécense aos receptores de tipo I en que ambas as clases se unen ao ADN como homodímeros. Porén, os receptores nucleares de tipo III, a diferenza dos de tipo I, únense a HREs con repeticións directas en vez de a HREs con repeticións invertidas.
Tipo IV[editar | editar a fonte]
Os receptores nucleares de tipo IV únense tanto a monómeros coma a dímeros, pero de maneira que só un único dominio de unión ao ADN do receptor se une a un único medio sitio de HRE. Exemplos de receptores de tipo IV poden atoparse na maioría das subfamilias de receptores nucleares.
Proteínas correguladoras[editar | editar a fonte]
- Artigo principal: Corregulador de receptor nuclear.
Os receptores nucleares que se unen a elementos de resposta a hormonas recrutan un significativo número doutras proteínas (denominadas correguladores da transcrición) que facilitan ou inhiben a transcrición do xene diana asociado a ARNm.[26][27] As funcións destes correguladores son variadas e inclúen a remodelación da cromatina (facendo que o xene diana sexa máis accesible ou menos á transcrición) ou unha función de ponte para estabilizar a unión doutras proteínas correguladoras. Os receptores nucleares poden unirse especificamente a varias proteínas correguladoras, e deste xeito inflúen nos mecanismos celulares de transdución de sinais de forma directa ou indirecta.[28]
Coactivatores[editar | editar a fonte]
A unión de ligandos agonistas (véxase máis abaixo) a receptores nucleares induce unha conformación do receptor que se une preferencialmente a proteínas coactivadoras. Estas proteínas con frecuencia teñen unha actividade intrínseca de histona acetiltransferase (HAT), que debilita a asociación das histonas co ADN, e promove así a transcrición dos xenes.
Correpresores[editar | editar a fonte]
Ao contrario, a unión de ligandos antagonistas aos receptores nucleares induce unha conformación do receptor que favorece a unión preferencial de proteínas correpresoras. Estas proteínas, á súa vez, recrutan histona desacetilases (HDACs), que fan máis forte a asociación das histonas co ADN, o que reprime a transcrición xénica.
Agonismo e antagonismo[editar | editar a fonte]

Dependendo do receptor implicado, a estrutura química do ligando e o tecido que é afectado, os ligandos dos receoptores nucleares poden mostrar diversos efectos que van desde o agonismo ao antagonismo e ao agonismo inverso.[31]
Agonistas[editar | editar a fonte]
A actividade dos ligandos endóxenos (como as hormonas estradiol e testosterona) cando se unen aos seus correspondentes receptores nucleares é normalmente regular á alza a expresión xénica. Esta estimulación da expresión xénica polo ligando denomínase resposta agonista. Os efectos agonistas das hormonas endóxenas poden tamén ser imitados por certos ligandos sintéticos, por exemplo, o fármaco antiinflamatorio receptor de glicocorticoides dexametasona. Os ligandos agonistas funcionan inducindo unha conformación do receptor que favorece a unión do coactivador (ver a parte superior da figura da dereita).
Antagonistas[editar | editar a fonte]
Outros ligandos sintéticos de receptores nucleares non teñen un efecto aparente sobre a transcrición xénica en ausencia de ligando endóxeno. Porén, bloquean o efecto do agonista por medio da unión competitiva no mesmo sitio de unión no receptor nuclear. Estes ligandos denomínanse antagonistas. Un exemplo de fármaco antagonista de receptor nuclear é a mifepristona, que se une a receptores de glicocorticoides e de proxesterona e, por tanto, bloquea a actividade das hormonas endóxenas cortisol e proxesterona respectivamente. Os ligandos antagonistas funcionan inducindo unha conformación do receptor, o cal impide a unión do coactivador e promove a unión do correpresor (ver a metade inferior da figura da dereita).
Agonistas inversos[editar | editar a fonte]
Finalmente, algúns receptores nucleares promoven un baixo nivel de transcrición xénica en ausencia de agonistas (tamén denominada actividade constitutiva ou basal). Os ligandos sintéticos, que reducen este nivel basal de actividade en receptores nucleares denomínanse agonistas inversos.[32]
Moduladores de receptor selectivos[editar | editar a fonte]
Varios fármacos que funcionan por medio de receptores nucleares mostran unha resposta agonista nalgúns tecidos e antagonista noutros. Este comportamento pode ter vantaxes substanciais xa que permite manter os efectos terapéuticos beneficiosos desexados dun fármaco á vez que se minimizan os efectos indesexados. Os fármacos que teñen este perfil de acción mixto agonista/antagonista denomínanse moduladores de receptor selectivos (SRMs). Exemplos son os Moduladores do Receptor de Andróxenos Selectivos (SARMs), os Moduladores do Receptor de Estróxenos Selectivos (SERMs) e os Moduladores do Receptor de Proxesterona Selectivos (SPRMs). O mecanismo de accíón dos SRMs pode variar dependendo da estrutura química do ligando e do receptor implicado, aínda que se cre que moitos SRMs funcionan promovendo unha conformación do receptor que está estreitamente equilibrada entre o agonismo e o antagonismo. En tecidos nos que a concentración de proteínas coactivadoras é máis alta que a de correpresores, o equilibrio está inclinado en dirección ao agonista. Inversamente, en tecidos onde domina o correpresor, o ligando compórtase como un antagonista.[33]
Mecanismos alternativos[editar | editar a fonte]

Transrepresión[editar | editar a fonte]
O mecanismo de acción máis común dos receptores nucleares supón a unión directa do receptor nuclear a un elemento de resposta a hormonas do ADN. Este mecanismo chámase transactivación. Non obstante, algúns receptores nucleares non só teñen a capacidade de unirse directamente ao ADN, senón tamén a outros factores de transcrición. Esta unión adoita orixinar a desactivación dun segundo factor de transcrición nun proceso coñecido como transrepresión.[34] Un exemplo de receptor nuclear con capacidade de transreprimir é o receptor de glicocorticoides (GR). Ademais, certos ligandos do receptor de glicocorticoides chamados Agonistas do Receptor de Glicocorticoides Selectivos (SEGRAs) poden activar ao receptor de glicocorticoides dun modo tal que dito receptor fai con máis forza a transrepresión que a transactivación. Esta selectividade incrementa a separación entre os efectos antiinflamatorios desexados e os efectos laterais metabólicos non desexados destes glicocorticoides selectivos.
Non xenómica[editar | editar a fonte]
Os efectos directos clásicos dos receptores nucleares sobre a regulación xénica normalmente son lentos e tárdase horas en poder apreciar un efecto funcional nas células debido ao gran número de pasos intermedios entre a activación do receptor nuclear e os cambios nos niveis de expresión das proteínas. Con todo, observouse que algúns efectos da aplicación de hormonas como o estróxeno aparecen en cuestión de minutos, o cal non está en concordancia co mecanismo clásico da acción dos receptores nucleares. Aínda que a diana molecular para estes efectos non xenómicos dos receptores nucleares non foi claramente demostrada, hipotetízase que hai variantes dos receptores nucleares que están asociados á membrana en vez de estaren localizados no citosol ou no núcleo. Ademais, estes receptores asociados á membrana funcionarían por medio de mecanismos de transdución de sinais alternativos, que non implican a regulación xénica.[35][36]
Membros da familia[editar | editar a fonte]
A seguinte lista de 48 receptores nucleares humanos coñecidos xunto con algúns receptores non humanos seleccionados[12] clasifícaos segundo a homoloxía de secuencias entre eles.[6][7]
| Subfamilia | Grupo | Membro | ||||||
|---|---|---|---|---|---|---|---|---|
| Símbolo NRNC[6] | Abreviatura | Nome | Xene | Ligando(s) | ||||
| 1 | similar ao receptor de hormonas tiroides | A | receptor de hormonas tiroides | NR1A1 | TRα | Receptor de hormonas tiroides α | THRA | Hormona tiroide |
| NR1A2 | TRβ | Receptor de hormonas tiroides β | THRB | |||||
| B | Receptor de ácido retinoico | NR1B1 | RARα | Receptor de ácido retinoico α | RARA | vitamina A e compostos relacionados | ||
| NR1B2 | RARβ | Receptor de ácido retinoico β | RARB | |||||
| NR1B3 | RARγ | Receptor de ácido retinoico γ | RARG | |||||
| C | Receptor activado polo proliferador do peroxisoma | NR1C1 | PPARα | Receptor activado polo proliferador do peroxisoma α | PPARA | ácidos graxos, prostaglandinas | ||
| NR1C2 | PPAR-β/δ | Receptor activado polo proliferador do peroxisoma β/δ | PPARD | |||||
| NR1C3 | PPARγ | Receptor activado polo proliferador do peroxisoma γ | PPARG | |||||
| D | Rev-ErbA | NR1D1 | Rev-ErbAα | Rev-ErbAα | NR1D1 | hemo | ||
| NR1D2 | Rev-ErbAβ | Rev-ErbAα | NR1D2 | |||||
| F | receptor orfo relacionado con RAR | NR1F1 | RORα | Receptor orfo relacionado con RAR α | RORA | colesterol, ATRA | ||
| NR1F2 | RORβ | Receptor orfo relacionado con RAR β | RORB | |||||
| NR1F3 | RORγ | Receptor relacionado con RAR γ | RORC | |||||
| H | similar ao receptor X hepático | NR1H3 | LXRα | Receptor X hepático α | NR1H3 | oxiesterois | ||
| NR1H2 | LXRβ | Receptor X hepático β | NR1H2 | |||||
| NR1H4 | FXR | Receptor X farnesoide | NR1H4 | |||||
| NR1H5[37] | FXR-β | Receptor X farnesoide β | NR1H5P | |||||
| I | similar ao receptor de vitamina D | NR1I1 | VDR | Receptor de vitamina D | VDR | vitamina D | ||
| NR1I2 | PXR | Receptor X de pregnano | NR1I2 | xenobioticos | ||||
| NR1I3 | CAR | Receptor de androstano constitutivo | NR1I3 | androstano | ||||
| X | Receptores nucleares con dous dominios de unión ao ADN[38][39] | NR1X1 | 2DBD-NRα | |||||
| NR1X2 | 2DBD-NRβ | |||||||
| NR1X3 | 2DBD-NRγ | |||||||
| 2 | similar ao receptor X retinoide | A | factor nuclear do hepatocito 4 | NR2A1 | HNF4α | Factor nuclear do hepatocito 4 α | HNF4A | ácidos graxos |
| NR2A2 | HNF4γ | Factor nuclear do hepatocito 4 γ | HNF4G | |||||
| B | Receptor X retinoide | NR2B1 | RXRα | Receptor X retinoide α | RXRA | retinoides | ||
| NR2B2 | RXRβ | Receptor X retinoide β | RXRB | |||||
| NR2B3 | RXRγ | Receptor X retinoide γ | RXRG | |||||
| C | Receptor testicular | NR2C1 | TR2 | Receptor testicular 2 | NR2C1 | |||
| NR2C2 | TR4 | Receptor testicular 4 | NR2C2 | |||||
| E | TLX/PNR | NR2E1 | TLX | Homólogo do xene tailless de Drosophila | NR2E1 | |||
| NR2E3 | PNR | Receptor nuclear específico de célula fotorreceptora | NR2E3 | |||||
| F | COUP/EAR | NR2F1 | COUP-TFI | Factor de transcrición do promotor de augas arriba da ovoalbumina de polo I | NR2F1 | |||
| NR2F2 | COUP-TFII | Factor de transcrición do promotor de augas arriba da ovoalbumina de polo II | NR2F2 | |||||
| NR2F6 | EAR-2 | relacionado con V-erbA | NR2F6 | |||||
| 3 | similar ao receptor de estróxenos | A | Receptor de estróxenos | NR3A1 | ERα | Receptor de estróxenos α | ESR1 | estróxenos |
| NR3A2 | ERβ | Receptor de estróxenos β | ESR2 | |||||
| B | receptor relacionado con estróxenos | NR3B1 | ERRα | Receptor relacionado con estróxenos α | ESRRA | |||
| NR3B2 | ERRβ | Receptor relacionado con estróxenos β | ESRRB | |||||
| NR3B3 | ERRγ | Receptor relacionado con estróxenos γ | ESRRG | |||||
| C | Receptores de 3-cetoesteroides | NR3C1 | GR | Receptor de glicocorticoides | NR3C1 | cortisol | ||
| NR3C2 | MR | Receptor de mineralocorticoides | NR3C2 | aldosterona | ||||
| NR3C3 | PR | Receptor de proxesterona | PGR | proxesterona | ||||
| NR3C4 | AR | Receptor de andróxenos | AR | testosterona | ||||
| 4 | similar ao factor de crecemento dos nervios IB | A | NGFIB/NURR1/NOR1 | NR4A1 | NGFIB | Factor de crecemento dos nervios IB | NR4A1 | |
| NR4A2 | NURR1 | Relacionado co receptor nuclear 1 | NR4A2 | |||||
| NR4A3 | NOR1 | Receptor 1 orfo derivado de neuronas | NR4A3 | |||||
| 5 | similar ao factor esteroidoxénico | A | SF1/LRH1 | NR5A1 | SF1 | Factor esteroidoxénico 1 | NR5A1 | fosfatidilinositois |
| NR5A2 | LRH-1 | Homólogo 1 do receptor hepático | NR5A2 | fosfatidilinositois | ||||
| 6 | similar ao factor nuclear de célula xerminal | A | GCNF | NR6A1 | GCNF | Factor nuclear de célula xerminal | NR6A1 | |
| 0 | Miscelánea | B | DAX/SHP | NR0B1 | DAX1 | reversión sexual sensible á dose, rexión crítica de hipoplasia adrenal, no cromosoma X, xene 1 | NR0B1 | |
| NR0B2 | SHP | Partner heterodímero pequeno | NR0B2 | |||||
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 PDB 3E00; Chandra V, Huang P, Hamuro Y, Raghuram S, Wang Y, Burris TP, Rastinejad F (October 2008). "Structure of the intact PPAR-gamma-RXR-alpha nuclear receptor complex on DNA". Nature 456 (7220): 350–356. PMC 2743566. PMID 19043829. doi:10.1038/nature07413.
- ↑ Evans RM (1988). "The steroid and thyroid hormone receptor superfamily". Science 240 (4854): 889–95. PMID 3283939. doi:10.1126/science.3283939.
- ↑ Olefsky JM (2001). "Nuclear receptor minireview series". J. Biol. Chem. 276 (40): 36863–4. PMID 11459855. doi:10.1074/jbc.R100047200.
- ↑ 4,0 4,1 4,2 Mangelsdorf DJ, Thummel C, Beato M, Herrlich P, Schutz G, Umesono K, Blumberg B, Kastner P, Mark M, Chambon P, Evans RM (1995). "The nuclear receptor superfamily: the second decade". Cell 83 (6): 835–9. PMID 8521507. doi:10.1016/0092-8674(95)90199-X.
- ↑ 5,0 5,1 Novac N, Heinzel T (2004). "Nuclear receptors: overview and classification". Curr Drug Targets Inflamm Allergy 3 (4): 335–46. PMID 15584884. doi:10.2174/1568010042634541.
- ↑ 6,0 6,1 6,2 Nuclear Receptors Nomenclature Committee (1999). "A unified nomenclature system for the nuclear receptor superfamily". Cell 97 (2): 161–3. PMID 10219237. doi:10.1016/S0092-8674(00)80726-6.
- ↑ 7,0 7,1 Laudet V (1997). "Evolution of the nuclear receptor superfamily: early diversification from an ancestral orphan receptor". J. Mol. Endocrinol. 19 (3): 207–26. PMID 9460643. doi:10.1677/jme.0.0190207.
- ↑ Escriva H, Langlois MC, Mendonça RL, Pierce R, Laudet V (May 1998). "Evolution and diversification of the nuclear receptor superfamily". Annals of the New York Academy of Sciences 839: 143–6. PMID 9629140. doi:10.1111/j.1749-6632.1998.tb10747.x.
- ↑ Reitzel AM, Pang K, Ryan JF, Mullikin JC, Martindale MQ, Baxevanis AD, Tarrant AM (2011). "Nuclear receptors from the ctenophore Mnemiopsis leidyi lack a zinc-finger DNA-binding domain: lineage-specific loss or ancestral condition in the emergence of the nuclear receptor superfamily?". Evodevo 2 (1): 3. PMC 3038971. PMID 21291545. doi:10.1186/2041-9139-2-3.
- ↑ Bridgham JT, Eick GN, Larroux C, Deshpande K, Harms MJ, Gauthier ME, Ortlund EA, Degnan BM, Thornton JW (2010). "Protein evolution by molecular tinkering: diversification of the nuclear receptor superfamily from a ligand-dependent ancestor". PLoS Biol. 8 (10): e1000497. PMC 2950128. PMID 20957188. doi:10.1371/journal.pbio.1000497.
- ↑ Sluder AE, Maina CV (April 2001). "Nuclear receptors in nematodes: themes and variations". Trends in Genetics : TIG 17 (4): 206–13. PMID 11275326. doi:10.1016/S0168-9525(01)02242-9.
- ↑ 12,0 12,1 Zhang Z, Burch PE, Cooney AJ, Lanz RB, Pereira FA, Wu J, Gibbs RA, Weinstock G, Wheeler DA (2004). "Genomic analysis of the nuclear receptor family: new insights into structure, regulation, and evolution from the rat genome". Genome Res 14 (4): 580–90. PMC 383302. PMID 15059999. doi:10.1101/gr.2160004.
- ↑ Overington JP, Al-Lazikani B, Hopkins AL (2006). "How many drug targets are there?". Nature reviews. Drug discovery 5 (12): 993–6. PMID 17139284. doi:10.1038/nrd2199.
- ↑ Benoit G, Cooney A, Giguere V, Ingraham H, Lazar M, Muscat G, Perlmann T, Renaud JP, Schwabe J, Sladek F, Tsai MJ, Laudet V (2006). "International Union of Pharmacology. LXVI. Orphan nuclear receptors". Pharmacol. Rev. 58 (4): 798–836. PMID 17132856. doi:10.1124/pr.58.4.10.
- ↑ Mohan R, Heyman RA (2003). "Orphan nuclear receptor modulators". Curr Top Med Chem 3 (14): 1637–47. PMID 14683519. doi:10.2174/1568026033451709.
- ↑ Kumar R, Thompson EB (1999). "The structure of the nuclear hormone receptors". Steroids 64 (5): 310–9. PMID 10406480. doi:10.1016/S0039-128X(99)00014-8.
- ↑ Klinge CM (2000). "Estrogen receptor interaction with co-activators and co-repressors". Steroids 65 (5): 227–51. PMID 10751636. doi:10.1016/S0039-128X(99)00107-5.
- ↑ 18,0 18,1 Wärnmark A, Treuter E, Wright AP, Gustafsson J-Å (2003). "Activation functions 1 and 2 of nuclear receptors: molecular strategies for transcriptional activation". Mol. Endocrinol. 17 (10): 1901–9. PMID 12893880. doi:10.1210/me.2002-0384.
- ↑ Weatherman RV, Fletterick RJ, Scanlan TS (1999). "Nuclear-receptor ligands and ligand-binding domains". Annu. Rev. Biochem. 68: 559–81. PMID 10872460. doi:10.1146/annurev.biochem.68.1.559.
- ↑ Chandra V, Huang P, Potluri N, Wu D, Kim Y, Rastinejad F (March 2013). "Multidomain integration in the structure of the HNF-4α nuclear receptor complex". Nature 495 (7441): 394–398. PMID 23485969. doi:10.1038/nature11966.
- ↑ Lou X, Toresson G, Benod C, Suh JH, Philips KJ, Webb P, Gustafsson JA (February 2014). "Structure of the retinoid X receptor α-liver X receptor β (RXRα-LXRβ) heterodimer on DNA". Nat. Struct. Mol. Biol. 21 (3): 277–281. PMID 24561505. doi:10.1038/nsmb.2778.
- ↑ PDB 2C7A; Roemer SC, Donham DC, Sherman L, Pon VH, Edwards DP, Churchill ME (December 2006). "Structure of the progesterone receptor-deoxyribonucleic acid complex: novel interactions required for binding to half-site response elements". Mol. Endocrinol. 20 (12): 3042–52. PMC 2532839. PMID 16931575. doi:10.1210/me.2005-0511.
- ↑ PDB 3L0L; Jin L, Martynowski D, Zheng S, Wada T, Xie W, Li Y (May 2010). "Structural basis for hydroxycholesterols as natural ligands of orphan nuclear receptor RORgamma". Mol. Endocrinol. 24 (5): 923–9. PMC 2870936. PMID 20203100. doi:10.1210/me.2009-0507.
- ↑ Linja MJ, Porkka KP, Kang Z, Savinainen KJ, Jänne OA, Tammela TL, Vessella RL, Palvimo JJ, Visakorpi T (February 2004). "Expression of androgen receptor coregulators in prostate cancer". Clin. Cancer Res. 10 (3): 1032–40. PMID 14871982. doi:10.1158/1078-0432.CCR-0990-3.
- ↑ Klinge CM, Bodenner DL, Desai D, Niles RM, Traish AM (May 1997). "Binding of type II nuclear receptors and estrogen receptor to full and half-site estrogen response elements in vitro". Nucleic Acids Res. 25 (10): 1903–12. PMC 146682. PMID 9115356. doi:10.1093/nar/25.10.1903.
- ↑ Glass CK, Rosenfeld MG (2000). "The coregulator exchange in transcriptional functions of nuclear receptors". Genes Dev 14 (2): 121–41. PMID 10652267. doi:10.1101/gad.14.2.121.
- ↑ Aranda A, Pascual A (2001). "Nuclear hormone receptors and gene expression" (abstract). Physiol. Rev. 81 (3): 1269–304. PMID 11427696.
- ↑ Copland JA, Sheffield-Moore M, Koldzic-Zivanovic N, Gentry S, Lamprou G, Tzortzatou-Stathopoulou F, Zoumpourlis V, Urban RJ, Vlahopoulos SA (June 2009). "Sex steroid receptors in skeletal differentiation and epithelial neoplasia: is tissue-specific intervention possible?". BioEssays 31 (6): 629–41. PMID 19382224. doi:10.1002/bies.200800138.
- ↑ Brzozowski AM, Pike AC, Dauter Z, Hubbard RE, Bonn T, Engström O, Öhman L, Greene GL, Gustafsson J-Å, Carlquist M (1997). "Molecular basis of agonism and antagonism in the oestrogen receptor". Nature 389 (6652): 753–8. PMID 9338790. doi:10.1038/39645.
- ↑ Shiau AK, Barstad D, Loria PM, Cheng L, Kushner PJ, Agard DA, Greene GL (1998). "The structural basis of estrogen receptor/coactivator recognition and the antagonism of this interaction by tamoxifen". Cell 95 (7): 927–37. PMID 9875847. doi:10.1016/S0092-8674(00)81717-1.
- ↑ Gronemeyer H, Gustafsson JA, Laudet V (2004). "Principles for modulation of the nuclear receptor superfamily". Nature reviews. Drug discovery 3 (11): 950–64. PMID 15520817. doi:10.1038/nrd1551.
- ↑ Busch BB, Stevens WC Jr, Martin R, Ordentlich P, Zhou S, Sapp DW, Horlick RA, Mohan R (2004). "Identification of a selective inverse agonist for the orphan nuclear receptor estrogen-related receptor alpha". J. Med. Chem. 47 (23): 5593–6. PMID 15509154. doi:10.1021/jm049334f.
- ↑ Smith CL, O'Malley BW (2004). "Coregulator function: a key to understanding tissue specificity of selective receptor modulators". Endocr Rev 25 (1): 45–71. PMID 14769827. doi:10.1210/er.2003-0023.
- ↑ Pascual G, Glass CK (2006). "Nuclear receptors versus inflammation: mechanisms of transrepression". Trends Endocrinol Metab 17 (8): 321–7. PMID 16942889. doi:10.1016/j.tem.2006.08.005.
- ↑ Björnström L, Sjöberg M (2004). "Estrogen receptor-dependent activation of AP-1 via non-genomic signalling". Nucl Recept 2 (1): 3. PMC 434532. PMID 15196329. doi:10.1186/1478-1336-2-3.
- ↑ Zivadinovic D, Gametchu B, Watson CS (2005). "Membrane estrogen receptor-alpha levels in MCF-7 breast cancer cells predict cAMP and proliferation responses". Breast Cancer Res. 7 (1): R101–12. PMC 1064104. PMID 15642158. doi:10.1186/bcr958.
- ↑ Otte K, Kranz H, Kober I, Thompson P, Hoefer M, Haubold B, Remmel B, Voss H, Kaiser C, Albers M, Cheruvallath Z, Jackson D, Casari G, Koegl M, Pääbo S, Mous J, Kremoser C, Deuschle U (2003). "Identification of farnesoid X receptor beta as a novel mammalian nuclear receptor sensing lanosterol". Mol. Cell. Biol. 23 (3): 864–72. PMC 140718. PMID 12529392. doi:10.1128/mcb.23.3.864-872.2003.
- ↑ Wu W, Niles EG, El-Sayed N, Berriman M, LoVerde PT (2006). "Schistosoma mansoni (Platyhelminthes, Trematoda) nuclear receptors: sixteen new members and a novel subfamily". Gene 366 (2): 303–15. PMID 16406405. doi:10.1016/j.gene.2005.09.013.
- ↑ Wu W, Niles EG, Hirai H, LoVerde PT (2007). "Evolution of a novel subfamily of nuclear receptors with members that each contain two DNA binding domains". BMC Evol Biol 7: 27. PMC 1810520. PMID 17319953. doi:10.1186/1471-2148-7-27.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Eukaryotic Linear Motif LIG_CORNRBOX
- Eukaryotic Linear Motif LIG_NRBOX
- Nuclear Receptors Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- Vincent Laudet (2006). "The IUPHAR Compendium of the Pharmacology and Classification of the Nuclear Receptor Superfamily 2006E". Nuclear Receptor Compendium. The International Union of Basic and Clinical Pharmacology. Arquivado dende o orixinal o 02 de abril de 2015. Consultado o 2015-05-02.
- "Nuclear Receptor Signaling Atlas (Receptors, Coactivators, Corepressors and Ligands)". The NURSA Consortium. Consultado o 2015-05-02.
un consorcio de investigación do NIH e base de datos; inclúe a revista Nuclear Receptor Signaling
- "Nuclear Receptor Resource". Jack Vanden Heuvel. Consultado o 2015-05-02.