Microsporidios
| Microsporidios | |||||
|---|---|---|---|---|---|
 Esporoblasto de Fibrillanosema crangonycis | |||||
| Clasificación científica | |||||
| |||||
| Clases e ordes | |||||
| Sinonimia | |||||
Os microsporidios (Microsporidia) son un grupo de parasitos unicelulares formadores de esporas relacionados cos fungos. Estas esporas conteñen un aparato extrusor que ten un extremo enroscado tubular polar nun disco de ancoraxe na parte apical da espora. [6] Tradicionalmente foran considerados protozoos ou protistas, pero agora sábese que son fungos,[7] ou un grupo irmán dos fungos.[8] Este tipo de fungos son parasitos eucariotas obrigados que usan un mecanismo exclusivo para infectar as células hóspedes. [9] Descubriuse recentemente que infectan coleópteros a grande escala, grazas a un estudo de 2017 de Cornell. Están nomeadas unhas 1500 das probablemente máis dun millón[10] de especies que se cre existen. Os Microsporidia están restrinxidos a hóspedes animais, e todos os grandes grupos de animais son hóspedes de microsporidios. A maioría infectan insectos, mais son tamén responsables de doenzas comúns en crustáceos e peixes. As especies con nome de microsporidios xeralmente infectan unha especie hóspede ou un grupo de taxons estreitamente relaconados. Aproximadamente o 10 % das especies son parasitas de vertebrados; varias especies, a maioría das cales son oportunistas, poden infectar humanos, nos cales poden causar microsporidiose.
Despois da infección inflúen nos seus hóspedes de varios xeitos e todos os órganos e tecidos son invadidos, aínda que xeralmente por diferentes especies de microsporidios. Algunhas especies son letais e unhas poucas utilízanse como un control biolóxico contra pragas de insectos. A castración parasítica, o xigantismo ou o cambio de sexo do hóspede son todos efectos posibles do parasitismo dos microsporidios nos insectos. Nos casos máis avanzados de parasitismo o microsporidio toma o mando da célula hóspede completamente e controla o seu metabolismo e reprodución, formando un complexo xenoparasítico (tamén chamado xenoma -/ksenoma/-).[11]
A replicación ten lugar dentro da célula hóspede, que é infectada por medio de esporas unicelulares. Os microsporidios que infectan mamíferos miden de 1,0–4,0 μm.[12] Ademais do seu pequeno tamaño, tamén teñen os tamaños xenómicos eucarióticos máis pequenos.
O termo "microsporidio" é o nome vernáculo, mentres que Microsporidia é o nome do taxon (agora con categoría de filo). O nome Microsporidium Balbiani, 1884[13] tamén se usa ás veces como nome de xénero xeral multifuncional para os membros considerados incertae sedis.[14]

Morfoloxía
[editar | editar a fonte]
Os microsporidios son singulares porque carecen de mitocondrias e no seu lugar teñen mitosomas. Tamén carecen de estruturas móbiles, como os flaxelos.
Producen esporas moi resistentes, capaces de sobrevivir fóra do seu hóspede varios anos. A morfoloxía das esporas é útil para distinguir as diferentres especies. As esporas da maioría das especies son ovais ou piriformes, pero non son raras as esporas esféricas ou con forma bacilar. Uns poucos xéneros producen esporas cunha forma exclusiva do seu seu xénero.
A espora está protexida por unha parede que consta de tres capas:
- unha externa electrodensa ou exóspora;
- unha mediana, ancha e aparentemente sen estrtura ou endóspora, que contén quitina;
- unha delgada interna ou membrana plasmática.
Na maioría dos casos teñen dous núcleos estreitamente asociados formando un diplocarion, pero ás veces hai só un.
A metade anterior da espora contén un aparato con forma de arpón cun longo filamento polar que parece un fío, que está enroscado na metade posterior da espora. A parte anterior do filamento polar está rodeada por un polaroplasto, unha lamela de membranas. Detrás do filamento polar hai un vacúolo posterior.[11]
Infección
[editar | editar a fonte]As esporas xerminan no intestino do hóspede, acumulan presión osmótica ata que a súa parede ríxida rompe no punto máis delgado no ápice. O vacúolo posterior incha, forzando o filamento polar a exectar rapidamente o contido infeccioso ao citoplasma do potencial hóspede. Simultaneamente o material do filamento reorganízase formando un tubo que funciona como unha agulla hipodérmica e penetra no epitelio intestinal.
Unha vez dentro da célula hóspede, crece un esporoplasma, dividindo ou formando un plasmodio multinucleado, antes de producir novas esporas. O ciclo vital varía considerablemente. Algunhas especies teñen un ciclo vital simple asexual,[16] mentres que outras teñen un ciclo complexo que implica múltiples hóspedes e reprodución tanto asexual coma sexual. Poden producirse diferentes tipos de esporas en diferentes estadios, probablemente con diferentes funcións, incluíndo a autoinfección (transmisión dentro dun só hóspede).
Implicacións médicas
[editar | editar a fonte]En animais e humanos os microsporidios causan con frecuencia doenzas debilitantes crónicas en lugar de infeccións mortais. Entre os efectos sobre o hóspede están a redución da lonxevidade, fertilidade, peso e vigor xeral. Hai informacións frecuentes de transmisión vertical dos microsporidios.
No caso dos hóspedes insectos, a transmisión vertical adoita acontecer como transmisión transovárica, na cal os parasitos microsporidios pasan desde os ovarios da femia hóspede aos ovos e finalmente multiplícanse nas larvas infectadas. Amblyospora salinaria n. sp., que infecta o mosquito Culex salinarius, e Amblyospora californica, que infecta o mosquito Culex tarsalis, son os típicos exemplos de transmisión transovárica de microsporidios.[17][18][19][20] Os microsporidios e máis en concreto a especie Vavraia culicis que infecta mosquitos, están a ser investigados como posible método de control da malaria "a proba de evolución".[21] A infección por microsporidios do mosquito Anopheles gambiae (o vector principal do Plasmodium falciparum causante da malaria) reduce as infeccións de malaria dentro do mosquito e acurta a vida do mosquito.[22] Como a maioría dos mosquitos infectados polo axente da malaria morren de forma natural antes de que o parasito da malaria sexa dabondo maduro como para poder transmitirse, calquera incremento da mortalidade do mosquito por causa da infección microsporidial pode reducir a transmisión da malaria a humanos. En maio de 2020, informouse que Microsporidia MB, un simbionte do intestino medio e ovario do mosquito Anopheles arabiensis, dificultaba significativamente a transmisión de P. falciparum, non tiña "ningún efecto evidente" sobre a fitness dos mosquitos hóspede e transmitíase verticalmente (por herdanza).[23]
En humanos
[editar | editar a fonte]As infeccións por microsporidios en humanos ás veces causan unha doenza chamada microsporidiose. Polo menos 14 especies de microsporidios, pertencentes a oito xéneros, foron recoñecidas como patóxenos humanos. Entre estas está Trachipleistophora hominis.[24]
Como hiperparasitos
[editar | editar a fonte]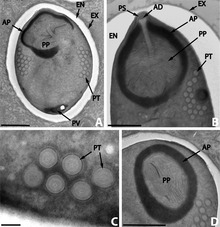
Os microsporidios poden infectar diversos hóspedes, mesmo a hóspedes que eles mesmos son parasitos. Nese caso, a especie de microsporidio dise que é un hiperparasito, é dicir, un parasito dun parasito. Como exemplo, coñécense máis de 18 especies que parasitan trematodos dixeneos (vermes planos parasitos). Estes dixeneos son á súa vez parasitos de varios vertebrados e moluscos. Oito destas especies pertencen ao xénero Nosema.[25] De xeito similar, a especie de microsporidio Toguebayea baccigeri é un parasito do dixeneo faustúlido Bacciger israelensis, que é un parasito intestinal do peixe mariño Boops boops, a boga (un teleósteo espárido).[26]
Contido xenómico
[editar | editar a fonte]Os microsporidios teñen o menor contido xenómico nuclear eucariótico. O seu estilo de vida parasito levou a unha perda de moitos xenes mitocondriais e do aparato de Golgi e incluso os seus ARN ribosómicos son de tamaño reducido comparados cos da maioría dos eucariotas. Como consecuencia, os xenomas dos microsporidios son moito menores que os dos outros eucariotas. Os xenomas microsporidiais actualemtne coñecidos son dun tamaño de 2,5 a 11,6 Mb, e codifican de 1.848 a 3.266 proteínas, o cal é o mesmo rango que teñen moitas bacterias.[27]
A transferencia horizontal de xenes parece ter ocorrido moitas veces nos microsporidios. Por exemplo, os xenomas de Encephalitozoon romaleae e Trachipleistophora hominis conteñen xenes que derivan de animais e bacterias e algúns mesmo de fungos.[27]
Clasificación
[editar | editar a fonte]O primeiro xénero de microsporidio descrito, Nosema, foi colocado inicialmente por Nägeli no grupo fúnxico dos Schizomycetes, xunto con algunhas bacterias e lévedos.[28][29] Durante algún tempo os microsporidios consideráronse eucariotas moi primitivos pertencentes ao grupo de protozoos dos Cnidospora.[4] Posteriormente, especialmente debido á ausencia neles de mitocondrias, foron situados xunto con outros Protozoa como os diplomónadas, parabasálidos e arqueamebas no grupo protozoario dos Archezoa.[30] Investigacións máis recentes refutaron esta teoría da orixe temperá de todos estes. Ao contrario, propúxose que os microsporidios son organismos moi desenvolvidos e especializados, que, por seren parasitos, se desfixeron de funcións que xa non precisaban porque lles eran proporcionadas polo hóspede.[31] Ademais, os organismos formadores de esporas en xeral teñen un sistema de reprodución complexo, tanto sexual coma asexual, que está lonxe de ser primitivo.
Desde a metade da década do 2000 os microsporidios son situados dentro dos Fungi ou como un grupo irmán dos Fungi cun antepasado común.[32][33][34][35]
Os traballos para identificar clados están baseados en gran medida no hábitat e no hóspede. Vossbrinck e Debrunner-Vossbrinck propuxeron tres clases de Microsporidia, baseándose no hábitat: Aquasporidia, Marinosporidia e Terresporidia.[36]
Unha segunda clasificación de Cavalier-Smith 1993 é:[37]
- Subfilo Rudimicrospora Cavalier-Smith 1993
- Clase Minisporea Cavalier-Smith 1993
- Orde Minisporida Sprague, 1972
- Clase Metchnikovellea Weiser, 1977
- Orde Metchnikovellida Vivier, 1975
- Clase Minisporea Cavalier-Smith 1993
- Subfilo Polaroplasta Cavalier-Smith 1993
- Clase Pleistophoridea Cavalier-Smith 1993
- Orde Pleistophorida Stempell 1906
- Clase Disporea Cavalier-Smith 1993
- Subclase Unikaryotia Cavalier-Smith 1993
- Subclase Diplokaryotia Cavalier-Smith 1993
- Clase Pleistophoridea Cavalier-Smith 1993
Notas[editar | editar a fonte]
Véxase tamén[editar | editar a fonte]Ligazóns externas[editar | editar a fonte]
|
