Criptocromo
| |
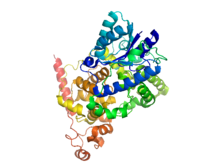
| Estrutura cristalográfica do criptocromo-1 | |
Criptocromo
| |
| Identificadores | |
| Símbolo | CRY1 |
| Entrez | 1407 |
| HUGO | 2384 |
| OMIM | |
| PDB | 5T5X |
| RefSeq | NP_004066 |
| UniProt | Q16526 |
| Outros datos | |
| Locus | Cr. 12 q23.3 |
Criptocromo
| |
| Identificadores | |
| Símbolo | CRY2 |
| Entrez | 1408 |
| HUGO | 2385 |
| OMIM | |
| PDB | 4MLP |
| RefSeq | NP_066940 |
| UniProt | Q49AN0 |
| Outros datos | |
| Locus | Cr. 11 p11.2 |
Os criptocromos son unha clase de flavoproteínas sensibles á luz azul, que se encontran en plantas e animais. Os criptocromos están implicados nos ritmos circadianos das plantas e animais e posiblemente tamén na percepción dos campos magnéticos en varias especies. O nome criptocromo (do grego κρυπτός χρώμα, 'cor oculta') foi proposto como unha palabra composta que combinaba a natureza críptica do fotorreceptor, e o nome dos organismos criptogámicos nos cales se están realizando moitos estudos sobre a luz azul.[1]
Os xenes Cry1 e Cry2 codifican as dúas proteínas criptocromos CRY1 e CRY2.[2] En insectos e plantas, CRY1 regula o reloxo circadiano de maneira dependente da luz, mentres que, en mamíferos, CRY1 e CRY2 actúan como inhibidores independentes da luz dos compoñentes CLOCK-BMAL1 do reloxo circadiano.[3] En plantas, a fotorrecepción de luz azul pode utilizarse como indicador de sinais de desenvolvemento.[4] Ademais das clorofilas, os criptocromos son as únicas proteínas coñecidas que forman pres radicais fotoinducidos in vivo.[5]
Descubrimento
[editar | editar a fonte]Aínda que Charles Darwin foi o primeiro que documentou a resposta das plantas á luz azul na década de 1880, ata cen anos máis tarde non se conseguiu empezar a identificar o pigmento responsable.[6] En 1980, descubriuse que o xene HY4 da planta Arabidopsis thaliana era necesario para que dita planta tivese sensibilidade á luz azul e, cando o xene foi secuenciado en 1993, viuse que tiña unha alta homoloxía de secuencia coa fotoliase, un encima reparador do ADN activado pola luz azul.[7] En 1995, estaba claro que os produtos do xene HY4 e os seus dous homólogos humanos non presentaban actividade de fotoliase e, ao contrario, eran unha nova clase de fotorreceptores da luz azul que se hipotetizaba que eran fotopigmentos circadianos.[8] En 1996 identificáronse homólogos de Cry en Drosophila e en 1998 no rato.[9][10]
Historia evolutiva e estrutura
[editar | editar a fonte]Os criptocromos (CRY1, CRY2) son proteínas antigas evolutivamente e están moi conservadas. Pertencen á superfamilia das flavoproteínas, que existe en todos os reinos de seres vivos.[4] Todos os membros desta superfamilia teñen un característico dominio de homoloxía coa fotoliase (PHR) N-terminal. O dominio PHR pode unirse ao cofactor flavín adenín dinucleótido (FAD) e a un cromóforo que capta a luz.[4] Os criptocromos derivan de fotoliases estreitamente relacionadas, que son encimas bacterianos que son activados pola luz e están implicados na reparación de danos no ADN inducidos pola luz ultravioleta (UV). En eucariotas, os criptocromos xa non manteñen esta actividade encimática orixinal.[11] A estrutura do criptocromo consiste nun pregamento moi similar ao da fotoliase, cunha soa molécula de FAD unida non covalentemente coa proteína.[4] Estas proteíns teñen lonxitude e superficie variables no extremo C-terminal, debido aos cambios no xenoma e aspecto que son resultado da falta de encimas de reparación do ADN. O gráfico de Ramachandran[12] mostra que a estrutura secvundaria da proteína CRY1 é principalmente unha hélice alfa dextroxira con pouco ou ningún solapamento estérico.[13] A estrutura do CRY1 está constituída case enteiramente por hélices alfa, con varios bucles e poucas follas beta. A molécula está disposta como un feixe ortogonal.[4]
Función
[editar | editar a fonte]Fototropismo
[editar | editar a fonte]En plantas, os criptocromos son mediadores do fototropismo (crecemento direccional cara á luz) en resposta á luz azul. Agora sábese que esta resposta ten o seu propio conxunto de fotorreceptores, as fototropinas.
A diferenza dos fitocromos e fototropinas, os criptocromos non son quinases. O seu cromóforo de flavina é reducido pola luz e transportado ao núcleo celular, onde afecta á presión de turxencia e causa un alongamento do talo. En concreto, Cry2 é responsable da expansión mediada pola luz do cotiledón e a folla. A sobreexpresión de Cry2 en plantas transxénicas incrementa a expansión do cotiledón estimulada pola luz azul, que ten como resultado a formación de follas máis anchas e ningunha flor en lugar dunhas poucas follas primarias e unha flor.[14] Unha mutación de dobre perda de función en Arabidopsis thaliana chamada elf3 (Early Flowering 3, ou Floración Temperán 3) e nos xenes Cry2 retarda a floración baixo luz continua e aceléraa durante os días longos e curtos, o que suxire que o CRY2 de Arabidopsis pode exercer unha función na aceleración do tempo da floración durante condicións de luz continua.[15]
Fotomorfoxénese
[editar | editar a fonte]Os receptores dos criptocromos causan a resposta das plantas á luz azul por fotomorfoxénese. Os criptocromos axudan a controlar o desenvolvemento das sementes e das plantiñas de sementeiro, así como o cambio desde o estadio de desenvolvemento vexetativo ao de floración. En Arabidopsis, os criptocromos controlan o crecemento da planta durante as condicións con luz azul subóptima.[16]
Captación da luz
[editar | editar a fonte]Malia o moito que se ten investigado sobre a cuestión da fotorrecepción e fototransdución dos criptocromos en Drosophila e Arabidopsis thaliana os coñecementos que se teñen dela aínda son incompletos. Os criptocromos posúen dous cromóforos: pterina (en forma de ácido 5,10-meteniltetrahidrofólico (MTHF)) e flavina (en forma de FAD).[17] Ambos os dous poden absorber un fotón, e en Arabidopsis, a pterina parece absorber a unha lonxitude de onda de 380 nm e a flavina a 450 nm. Estudos pasados apoiaron un modelo polo cal a enerxía capturada pola pterina se transfería á flavina.[18] Con este modelo de fototransdución, o FAD sería entón reducido a FADH, o cal probablemente media a fosforilación dun certo dominio nos criptocromos. Isto podería desencadear unha cadea de transdución de sinais, que posiblemente afecta á regulación xénica no núcleo celular.
Unha nova hipótese[19] propón que nos criptocromos de plantas a transdución do sinal luminoso nun sinal químico que poida ser percibido por moléculas asociadas poderia ser desencadeada por unha carga negativa fotoinducida dentro da proteína, quer no cofactor FAD quer no ácido aspártico veciño.[20][21] Esta carga negativa repelería electrostaticamente a molécula de ATP unida á proteína e, por tanto, tamén o dominio C-terminal da proteína, o cal cobre o peto de unión ao ATP antes da absorciónn de fotóns. O cambio resultante na conformación da proteína podería levar á fosforilación de sitios de fosforilación antes inaccesibles no C-terminal e o segmento fosforilado podería despois liberar o factor de transcrición HY5 ao competir polo mesmo sitio de unión no regulador negativo da fotomorfoxénese COP1.
En Drosophila pode funcionar un mecanismo diferente. O verdadeiro estado fundamental do cofactor de flavina no CRY de Drosophila aínda se está a discutir, e algúns modelos indican que o FAD está en forma oxidada,[22] mentres que outros apoian un modelo no cal o cofactor flavina existe en forma de rdical anión, FAD−
•. Recentemente, observouse que o FAD oxidado é doadamente reducido a FAD−
• pola luz. Ademais, as mutacións que bloquean a fotorredución non teñen efecto sobre a degradación inducida pola luz de CRY, mentres que as mutacións que alteraron a estabilidade de FAD−
• destruían a función fotorreceptora de CRY.[23][24] Estas observacións proporcionan apoio ao estado fundamental de FAD−
•. Tamén se propuxo recdentemente un modelo no cal FAD−
é excitado ao seu estado de dobrete ou cuarteto pola absorción dun fotón, o cal despois orixina un cambio conformacional na proteína CRY.[25]
Nas esponxas, os citocromos receptores de luz azul tamén se expresan. A maioría dos ollos dos animais utilizan proteínas opsinas fotosensibles expresadas en neuronas para comunicar información do ambiente luminoso ao sistema nervioso, mentres que as larvas de esponxa usan unha especie de ollos simples anulares pigmentados para orientar a súa natación fototáctica. Porén, a pesar de posuír moitos outros receptores acoplados á proteína G (GPCRs), o xenoma completamente secuenciado de Amphimedon queenslandica, unha demosponxa, aparentemente carece dun xene para un pigmento opsina sensible á luz, o que suxire que nos ollos exclusivos da larva desta esponxa podería ter evolucionado un novo mecanismo de detección da luz. As investigacións realizadas utilizando sondas de ARN indicaron que un dos dous criptocromos, o Aq-Cry2, producíase preto das células do ollo simple da larva da esponxa. O Aq-Cry2 carece de actividade de fotoliase e contén un cofactor baseado na flavina que é responsable das lonxitudes de onda de luz que tamén son as mediadoras do comportamento fótico larvario. Definido como un clado de opsina de GPCR, posúe unha lisina conservada que é esencial para a función da opsina. Igual que outras esponxas, A. queenslandica carece de sistema nervioso. Isto indica que os ollos da esponxa sen opsina utilizan o criptocromo, xunto con outras proteínas, para dirixiren ou actuaren no comportamento fototáctico mediado polo ollo.[26]
Ritmos circadianos
[editar | editar a fonte]Estudos feitos en animais e plantas suxiren que os criptocromos xogan un papel central na xeración e mantemento dos ritmos circadianos.[27] De xeito similar, os criptocromos exercen un importante papel na sincronización dos ritmos circadianos en plantas.[28] En Drosophila, o criptocromo (dCRY) actúa como un receptor da luz azul que modula directamente a entrada de luz no reloxo circadiano,[29] mentres que en mamíferos os criptocromos (CRY1 e CRY2) actúan como represores de transcrición dentro do reloxo circadiano.[30] Algúns insectos, como a bolboreta monarca, teñen versións dos citocromos tanto similares ás de Drosophila coma similares ás de mamíferos, o que proporciona unha proba do mecanismo de reloxo ancestral implicado tanto nas funcións de sensibilidade á luz coma nas de represión transcricional exercidas polos criptocromos.[31][32]
Os mutantes Cry teñen os seus ritmos circadianos alterados, o que mostra que Cry afecta ao marcapasos circadiano. As Drosophila co Cry mutado presentan poucos ou ningúns ciclos (de aumento ou diminución) do ARNm.[33] Unha mutación puntual en cryb, que é necesaria paa a asociación coa flavina na proteína CRY, ten como resultado a falta dos ciclos das proteínas PER ou TIM en escuridade constante ou en probas con luz-escuridade.[34] Ademais, os ratos que carecen dos xenes Cry1 ou Cry2 mostran os períodos e que corren libremente alterados diferencialmente, pero aínda son quen de [[fotosincronización|fotosincronizarse]. Porén, os ratos que carecen tanto de Cry1 como Cry2 son arrítmicos en condicións de luz-escuridade como en escuridade constante e sempre teñen niveis altos de ARNm de Per1. Estes resultados indican que os crfispocromos xogan un papel fotorreceptivo, así como actúan como reguladores negativos da expresión do xene Per en ratos.[35]
En Drosophila
[editar | editar a fonte]En Drosophila, o criptocromo funciona como un fotorreceptor de luz azul. A exposición á luz azul induce unha conformación similar á dos sempre activos mutantes CRY cunha deleción C-terminal (CRYΔ).[25] A vida media desta conformación é de 15 minutos na escuridade e facilita a unión de CRY a outros produtos xénicos do reloxo, PER e TIM, de maneira dependente da luz.[3][25][29][36] Unha vez que dTIM se uniu a dCRY, queda destinado á degradación polo sistema da ubiquitina-proteasoma.[25][36]
Aínda que os pulsos de luz non sincronizan, o fotoperíodo completo de ciclos de luz/escuridade aínda pode impulsar ciclos nas neuronas ventrais-laterais no cerebro de Drosophila. Estes datos, xunto con outros resultados suxiren que CRY é o fotorreceptor autónomo da célula para os reloxos corporais en Drosophila e pode desempeñar unha función na sincronización non paramétrica (sincronizsción por pulsos de luz discretos curtos). Porén, as neuronas laterais reciben información luminosa a través da vía CRY de luz azul e da vía da rodopsina. Por tanto, CRY está implicado na percepción da luz e é unha entrada de datos ao reloxo circadiano, aínda que non é a única entrada sobre información luminosa, xa que se observou un ritmo sostido en ausencia da vía CRY, no cal se cre que a vía da rodopsina proporciona algunha entrada de información sobre a luz.[37] Recentemente, demostrouse que hai unha resposta á luz mediada por CRY que é independente da interacción CRY-TIM circadiana clásica. Este mecanismo crese que require un mecanismo baseado no redox da flavina que é dependente da condutancia dunha canle de potasio. Esta resposta á luz mediada por CRY incrementa os disparos de potenciais de acción en cuestión de segundos dunha resposta á luz en Drosophila con knockout para a opsina.[38]
O criptocromo, como moitos xenes implicados nos ritmos ciradianos, mostra ciclos circadianos nos niveis de ARNm e proteínas. En Drosophila, o ciclo de concentracións do ARNm de Cry nun ciclo de luz-escuridade (LD ou light-dark) ten un alto nivel na luz e baixos niveis na escuridade.[33] Este ciclo persiste en escuridade constante (DD), pero cunha amplitude menor.[33] A transcrición do xene Cry tamén presenta ciclos cunha tendencia similar.[33] Porén, os niveis da proteína CRY ciclan de diferente maneira que na transcrición de Cry e nos niveis de ARNm. En luz-escuridade, a proteína CRY presenta baixos niveis na luz e altos niveis na escuridade, e, na escuridade permanente, os niveis de CRY increméntanse continuamente durante o día e a noite subxectivos.[33] Así, a expresión de CRY está regulada polo reloxo a nivel transcricional e pola luz a nivel traducional e postraducional.[33]
A sobreexpresión de Cry tamén afecta ás respostas circadianas á luz. En Drosophila, a sobreexpresión de Cry incementa a sensibilidade das moscas á luz de baixa intensidade.[33] Este regulación á luz dos niveis de proteínas CRY suxire que CRY ten un papel circadiano augas arriba dos outros xenes e compoñentes do reloxo.[33]
En mamíferos
[editar | editar a fonte]O criptocromo é un dos catro grupos de proteínas/xenes reloxo en mamíferos que xera un bucle de retroalimentación negativa de transcrición-tradución (TTFL), xunto cons xenes Period (PER), CLOCK e BMAL1.[39] Neste bucle, as proteínas CLOCK e BMAL1 son activadores transcricionais, que xuntos se unen aos promotores dos xenes Cry e Per e activan a súa transcrición.[39] As proteínas CRY e PER únense despois entre si, entran no núcleo e inhiben a transcrición activada por CLOCK e BMAL1.[39]
En ratos, a expresión de Cry1 mostra ritmos circadianos no núcleo supraquiasmático, unha rexión do cerebro implicada na xeración dos ritmos circadianos, nos que os niveis de ARNm chegan a un pico durante a fase de luz e alcanzan un mínimo na escuridade.[40] Estas oscilacións diarias na expresión mantéñense en escuridade constante.[40]
Aínda que é seguro que CRY é un homólogo de TIM en mamíferos, o papel de CRY como fotorreceptor en mamíferos estivo suxieto a discusións. Os primeiros artigos indicaban que CRY tiña funcións tanto dependentes coma independentes da luz. Un estudo de 2000 indicou que os ratos sen rodopsina pero con criptocromo aínda podían responder á luz; porén, en ratos sen rodopsina nin criptocromo, a transcrición de c-Fos, un mediador da sensibilidade á luz, cae significativamente.[41] En anos recentes, os datos apoian que a melanopsina é o principal fotorreceptor circadiano, en especial as células da melanopsina que median a sincronización e comunicación entre o [[ollo] e o núcleo supraquiasmático.[42] Unha das principais dificultades para confirmar ou denegar que CRY é un fotorreceptor en mamíferos é que cando o xene é sometido a knockout o animal vólvese arrítmico, polo que é difícil medir a súa capacidade simplemente como receptor. Porén, algúns estudos recentes indican que os CRY humanos poden mediar as respostas á luz en tecidos periféricos.[43]
Os ritmos circadianos normais dependen criticamente do retardo da expresión de Cry1 despois da activación do promotor Cry1. Mentres que os ritmos na activación do promotor de Per2 e os niveis de ARNm de Per2 teñen case a mesma fase, a produción de ARNm de Cry1 está retardada aproximadamente catro horas en relación coa activación do promotor de Cry1.[44] Este retardo é independente dos niveis de CRY1 ou CRY2 e está mediado por unha combinación de elementos E/E'-box e D-box no promotor e elementos de unión a RevErbA/ROR (RREs) no primeiro intrón do xene.[45] A transfección de células con dobre knockout Cry1−/− Cry2−/− arrítmicas con só o promotor de Cry1 (causando a expresión constitutiva de Cry1) non é suficiente para recuperar a ritmicidade. Nestas células cómpre a súa transfección tanto co promotor coma co primeiro intrón para a restauración dos ritmos circadianos.[45]
Magnetorrecepción
[editar | editar a fonte]- Artigo principal: Magnetorrecepción.
Os datos experimentais indican que os criptocromos das neuronas fotorreceptoras dos ollos das aves están implicados na orientación magnética durante a migración.[46] Tamén se pensa que os criptocromos son esenciais para a habilidade dependente da luz de Drosophila de percibir os campos magnéticos.[47] Antes informárase tamén que os campos magnéticos afectaban aos criptocromos na planta Arabidopsis thaliana: o comportamento de crecemento parecía ser afectado polos campos magnéticos en presenza de luz azul (pero non de vermella).[48] Non obstante, estes resultados viuse posteriormente que non se podían reproducir en condicións estritamente controladas noutro laboratorio,[49] o que suxire que os criptocromos das plantas non responden aos campos magnéticos.
Cando se expoñen os criptocromos á luz azul forman un par de radicais con spins correlacionados.[50][51] Os pares radicais poden xerarse tamén pola reoxidación na escuridade independente da luz do cofactor flavina polo oxíxeno molecular por medio da formación de pares de radicais FADH-superóxido de spins correlacionados.[52] Hipotetízase que a magnetorrecepción funciona por medio do efecto dos campos magnéticos que os rodean sobre a correlación (paralela ou antiparalela) destes radicais, o cal afecta ao tempo de vida da forma activada dos criptocromos. A activación do criptocromo pode afectar á sensibilidade á luz das neuronas da retina, co resultado global de que o animal pode percibir os campos magnéticos.[53] Os criptocromos animais e as estreitamente relacionadas (6-4) fotoliases animais conteñen unha cadea máis longa de triptófanos transferidores de electróns que outras proteínas da superfamilia criptocromo-fotoliase (unha tétrade de triptófanos en vez dunha tríade).[54][55] A cadea máis longa orixina unha mellor separación e un tempo de vida aproximadamente mil veces máis longo dos pares radicais falvina-triptófano fotoinducidos que nas proteínas que teñen unha tríade de triptófanos.[54][55] A ausencia de recombinación selectiva de spin destes pares radicais a escalas de tempo de nanosegundos a microsegundos parece ser incompatible coa suxestión de que a magnetorrecepción polos criptocromos está baseada na reacción da luz cara a adiante.
Notas
[editar | editar a fonte]- ↑ Gressel, J. (1979). "Blue Light Photoreception". Photochemistry and Photobiology (en inglés) 30 (6): 749–754. ISSN 1751-1097. doi:10.1111/j.1751-1097.1979.tb07209.x.
- ↑ van der Spek PJ, Kobayashi K, Bootsma D, Takao M, Eker AP, Yasui A (October 1996). "Cloning, tissue expression, and mapping of a human photolyase homolog with similarity to plant blue-light receptors". Genomics 37 (2): 177–82. PMID 8921389. doi:10.1006/geno.1996.0539. hdl:1765/55742.
- ↑ 3,0 3,1 Griffin EA, Staknis D, Weitz CJ (October 1999). "Light-independent role of CRY1 and CRY2 in the mammalian circadian clock". Science 286 (5440): 768–71. PMID 10531061. doi:10.1126/science.286.5440.768.
- ↑ 4,0 4,1 4,2 4,3 4,4 PDB 1u3c; Brautigam CA, Smith BS, Ma Z, Palnitkar M, Tomchick DR, Machius M, Deisenhofer J (August 2004). "Structure of the photolyase-like domain of cryptochrome 1 from Arabidopsis thaliana". Proceedings of the National Academy of Sciences of the United States of America 101 (33): 12142–7. Bibcode:2004PNAS..10112142B. PMC 514401. PMID 15299148. doi:10.1073/pnas.0404851101.
- ↑ Hore PJ, Mouritsen H (July 2016). "The Radical-Pair Mechanism of Magnetoreception". Annual Review of Biophysics 45 (1): 299–344. PMID 27216936. doi:10.1146/annurev-biophys-032116-094545.
- ↑ Darwin C (1881). The Power of Movement in Plants. New York: D. Appleton and Company.
- ↑ Ahmad M, Cashmore AR (November 1993). "HY4 gene of A. thaliana encodes a protein with characteristics of a blue-light photoreceptor". Nature 366 (6451): 162–6. Bibcode:1993Natur.366..162A. PMID 8232555. doi:10.1038/366162a0.
- ↑ Thompson CL, Sancar A (2004). "Cryptochrome: Discovery of a Circadian Photopigment". En Lenci F, Horspool WM. CRC handbook of organic photochemistry and photobiology. Boca Raton: CRC Press. pp. 1381–89. ISBN 978-0-8493-1348-6.
- ↑ Todo T, Ryo H, Yamamoto K, Toh H, Inui T, Ayaki H, et al. (April 1996). "Similarity among the Drosophila (6-4)photolyase, a human photolyase homolog, and the DNA photolyase-blue-light photoreceptor family". Science 272 (5258): 109–12. Bibcode:1996Sci...272..109T. PMID 8600518. doi:10.1126/science.272.5258.109.
- ↑ Kobayashi K, Kanno S, Smit B, van der Horst GT, Takao M, Yasui A (November 1998). "Characterization of photolyase/blue-light receptor homologs in mouse and human cells". Nucleic Acids Research 26 (22): 5086–92. PMC 147960. PMID 9801304. doi:10.1093/nar/26.22.5086.
- ↑ Weber S (February 2005). "Light-driven enzymatic catalysis of DNA repair: a review of recent biophysical studies on photolyase". Biochimica et Biophysica Acta (BBA) - Bioenergetics 1707 (1): 1–23. PMID 15721603. doi:10.1016/j.bbabio.2004.02.010.
- ↑ "MolProbity Ramachandran analysis,1U3C, model 1" (PDF). www.rcsb.org. Arquivado dende o orixinal (PDF) o 21 de outubro de 2012. Consultado o 2011-04-13.
- ↑ Nelson DR, Lehninger AL, Cox M (2005). Lehninger Principles of Biochemistry. New York: W.H. Freeman. ISBN 978-0-7167-4339-2.
- ↑ Hsu DS, Zhao X, Zhao S, Kazantsev A, Wang RP, Todo T, et al. (November 1996). "Putative human blue-light photoreceptors hCRY1 and hCRY2 are flavoproteins". Biochemistry 35 (44): 13871–7. PMID 8909283. doi:10.1021/bi962209o.
- ↑ Nefissi R, Natsui Y, Miyata K, Oda A, Hase Y, Nakagawa M, et al. (May 2011). "Double loss-of-function mutation in EARLY FLOWERING 3 and CRYPTOCHROME 2 genes delays flowering under continuous light but accelerates it under long days and short days: an important role for Arabidopsis CRY2 to accelerate flowering time in continuous light". Journal of Experimental Botany 62 (8): 2731–44. PMID 21296763. doi:10.1093/jxb/erq450.
- ↑ Pedmale UV, Huang SC, Zander M, Cole BJ, Hetzel J, Ljung K, et al. (January 2016). "Cryptochromes Interact Directly with PIFs to Control Plant Growth in Limiting Blue Light". Cell 164 (1–2): 233–245. PMC 4721562. PMID 26724867. doi:10.1016/j.cell.2015.12.018.
- ↑ Song SH, Dick B, Penzkofer A, Pokorny R, Batschauer A, Essen LO (October 2006). "Absorption and fluorescence spectroscopic characterization of cryptochrome 3 from Arabidopsis thaliana". Journal of Photochemistry and Photobiology. B, Biology 85 (1): 1–16. PMID 16725342. doi:10.1016/j.jphotobiol.2006.03.007.
- ↑ Hoang N, Bouly JP, Ahmad M (January 2008). "Evidence of a light-sensing role for folate in Arabidopsis cryptochrome blue-light receptors". Molecular Plant 1 (1): 68–74. PMID 20031915. doi:10.1093/mp/ssm008.
- ↑ Müller P, Bouly JP (January 2015). "Searching for the mechanism of signalling by plant photoreceptor cryptochrome". FEBS Letters 589 (2): 189–92. PMID 25500270. doi:10.1016/j.febslet.2014.12.008.
- ↑ Müller P, Bouly JP, Hitomi K, Balland V, Getzoff ED, Ritz T, Brettel K (June 2014). "ATP binding turns plant cryptochrome into an efficient natural photoswitch". Scientific Reports 4: 5175. Bibcode:2014NatSR...4E5175M. PMC 4046262. PMID 24898692. doi:10.1038/srep05175.
- ↑ Cailliez F, Müller P, Gallois M, de la Lande A (September 2014). "ATP binding and aspartate protonation enhance photoinduced electron transfer in plant cryptochrome". Journal of the American Chemical Society 136 (37): 12974–86. PMID 25157750. doi:10.1021/ja506084f.
- ↑ Berndt A, Kottke T, Breitkreuz H, Dvorsky R, Hennig S, Alexander M, Wolf E (April 2007). "A novel photoreaction mechanism for the circadian blue light photoreceptor Drosophila cryptochrome". The Journal of Biological Chemistry 282 (17): 13011–21. PMID 17298948. doi:10.1074/jbc.M608872200.
- ↑ Song SH, Oztürk N, Denaro TR, Arat NO, Kao YT, Zhu H, et al. (June 2007). "Formation and function of flavin anion radical in cryptochrome 1 blue-light photoreceptor of monarch butterfly". The Journal of Biological Chemistry 282 (24): 17608–12. PMID 17459876. doi:10.1074/jbc.M702874200.
- ↑ Oztürk N, Song SH, Selby CP, Sancar A (February 2008). "Animal type 1 cryptochromes. Analysis of the redox state of the flavin cofactor by site-directed mutagenesis". The Journal of Biological Chemistry 283 (6): 3256–63. PMID 18056988. doi:10.1074/jbc.M708612200.
- ↑ 25,0 25,1 25,2 25,3 Ozturk N, Selby CP, Annayev Y, Zhong D, Sancar A (January 2011). "Reaction mechanism of Drosophila cryptochrome". Proceedings of the National Academy of Sciences of the United States of America 108 (2): 516–21. Bibcode:2011PNAS..108..516O. PMC 3021015. PMID 21187431. doi:10.1073/pnas.1017093108.
- ↑ Rivera AS, Ozturk N, Fahey B, Plachetzki DC, Degnan BM, Sancar A, Oakley TH (April 2012). "Blue-light-receptive cryptochrome is expressed in a sponge eye lacking neurons and opsin". The Journal of Experimental Biology 215 (Pt 8): 1278–86. PMC 3309880. PMID 22442365. doi:10.1242/jeb.067140.
- ↑ Klarsfeld A, Malpel S, Michard-Vanhée C, Picot M, Chélot E, Rouyer F (February 2004). "Novel features of cryptochrome-mediated photoreception in the brain circadian clock of Drosophila". The Journal of Neuroscience 24 (6): 1468–77. PMC 6730330. PMID 14960620. doi:10.1523/JNEUROSCI.3661-03.2004.
- ↑ Somers DE, Devlin PF, Kay SA (November 1998). "Phytochromes and cryptochromes in the entrainment of the Arabidopsis circadian clock". Science 282 (5393): 1488–90. PMID 9822379. doi:10.1126/science.282.5393.1488.
- ↑ 29,0 29,1 Emery P, Stanewsky R, Helfrich-Förster C, Emery-Le M, Hall JC, Rosbash M (May 2000). "Drosophila CRY is a deep brain circadian photoreceptor". Neuron 26 (2): 493–504. PMID 10839367. doi:10.1016/S0896-6273(00)81181-2.
- ↑ Reppert SM, Weaver DR (August 2002). "Coordination of circadian timing in mammals". Nature 418 (6901): 935–41. Bibcode:2002Natur.418..935R. PMID 12198538. doi:10.1038/nature00965.
- ↑ Zhu H, Sauman I, Yuan Q, Casselman A, Emery-Le M, Emery P, Reppert SM (January 2008). "Cryptochromes define a novel circadian clock mechanism in monarch butterflies that may underlie sun compass navigation". PLOS Biology 6 (1): e4. PMC 2174970. PMID 18184036. doi:10.1371/journal.pbio.0060004.
- ↑ Zhu H, Yuan Q, Briscoe AD, Froy O, Casselman A, Reppert SM (December 2005). "The two CRYs of the butterfly". Current Biology 15 (23): R953–4. PMID 16332522. doi:10.1016/j.cub.2005.11.030.
- ↑ 33,0 33,1 33,2 33,3 33,4 33,5 33,6 33,7 Emery P, So WV, Kaneko M, Hall JC, Rosbash M (November 1998). "CRY, a Drosophila clock and light-regulated cryptochrome, is a major contributor to circadian rhythm resetting and photosensitivity". Cell 95 (5): 669–79. PMID 9845369. doi:10.1016/S0092-8674(00)81637-2.
- ↑ Stanewsky R, Kaneko M, Emery P, Beretta B, Wager-Smith K, Kay SA, et al. (November 1998). "The cryb mutation identifies cryptochrome as a circadian photoreceptor in Drosophila". Cell 95 (5): 681–92. PMID 9845370. doi:10.1016/S0092-8674(00)81638-4.
- ↑ Vitaterna MH, Selby CP, Todo T, Niwa H, Thompson C, Fruechte EM, et al. (October 1999). "Differential regulation of mammalian period genes and circadian rhythmicity by cryptochromes 1 and 2". Proceedings of the National Academy of Sciences of the United States of America 96 (21): 12114–9. Bibcode:1999PNAS...9612114V. PMC 18421. PMID 10518585. doi:10.1073/pnas.96.21.12114.
- ↑ 36,0 36,1 Busza A, Emery-Le M, Rosbash M, Emery P (June 2004). "Roles of the two Drosophila CRYPTOCHROME structural domains in circadian photoreception". Science 304 (5676): 1503–6. Bibcode:2004Sci...304.1503B. PMID 15178801. doi:10.1126/science.1096973.
- ↑ Dunlap JC (January 1999). "Molecular bases for circadian clocks". Cell 96 (2): 271–90. PMID 9988221. doi:10.1016/S0092-8674(00)80566-8.
- ↑ Fogle KJ, Parson KG, Dahm NA, Holmes TC (March 2011). "CRYPTOCHROME is a blue-light sensor that regulates neuronal firing rate". Science 331 (6023): 1409–13. Bibcode:2011Sci...331.1409F. PMC 4418525. PMID 21385718. doi:10.1126/science.1199702.
- ↑ 39,0 39,1 39,2 Sancar A, Lindsey-Boltz LA, Kang TH, Reardon JT, Lee JH, Ozturk N (June 2010). "Circadian clock control of the cellular response to DNA damage". FEBS Letters 584 (12): 2618–25. PMC 2878924. PMID 20227409. doi:10.1016/j.febslet.2010.03.017.
- ↑ 40,0 40,1 Miyamoto Y, Sancar A (May 1998). "Vitamin B2-based blue-light photoreceptors in the retinohypothalamic tract as the photoactive pigments for setting the circadian clock in mammals". Proceedings of the National Academy of Sciences of the United States of America 95 (11): 6097–102. Bibcode:1998PNAS...95.6097M. PMC 27591. PMID 9600923. doi:10.1073/pnas.95.11.6097.
- ↑ Selby CP, Thompson C, Schmitz TM, Van Gelder RN, Sancar A (December 2000). "Functional redundancy of cryptochromes and classical photoreceptors for nonvisual ocular photoreception in mice". Proceedings of the National Academy of Sciences of the United States of America 97 (26): 14697–702. Bibcode:2000PNAS...9714697S. PMC 18981. PMID 11114194. doi:10.1073/pnas.260498597.
- ↑ Hattar S, Liao HW, Takao M, Berson DM, Yau KW (February 2002). "Melanopsin-containing retinal ganglion cells: architecture, projections, and intrinsic photosensitivity". Science 295 (5557): 1065–70. Bibcode:2002Sci...295.1065H. PMC 2885915. PMID 11834834. doi:10.1126/science.1069609.
- ↑ Hoang N, Schleicher E, Kacprzak S, Bouly JP, Picot M, Wu W, et al. (July 2008). Schibler U, ed. "Human and Drosophila cryptochromes are light activated by flavin photoreduction in living cells". PLOS Biology 6 (7): e160. PMC 2443192. PMID 18597555. doi:10.1371/journal.pbio.0060160.
- ↑ Sato TK, Yamada RG, Ukai H, Baggs JE, Miraglia LJ, Kobayashi TJ, et al. (March 2006). "Feedback repression is required for mammalian circadian clock function". Nature Genetics 38 (3): 312–9. PMC 1994933. PMID 16474406. doi:10.1038/ng1745.
- ↑ 45,0 45,1 Ukai-Tadenuma M, Yamada RG, Xu H, Ripperger JA, Liu AC, Ueda HR (January 2011). "Delay in feedback repression by cryptochrome 1 is required for circadian clock function". Cell 144 (2): 268–81. PMID 21236481. doi:10.1016/j.cell.2010.12.019.
- ↑ Heyers D, Manns M, Luksch H, Güntürkün O, Mouritsen H (September 2007). Iwaniuk A, ed. "A visual pathway links brain structures active during magnetic compass orientation in migratory birds". PLOS ONE 2 (9): e937. Bibcode:2007PLoSO...2..937H. PMC 1976598. PMID 17895978. doi:10.1371/journal.pone.0000937.
- ↑ Gegear RJ, Casselman A, Waddell S, Reppert SM (August 2008). "Cryptochrome mediates light-dependent magnetosensitivity in Drosophila". Nature 454 (7207): 1014–8. Bibcode:2008Natur.454.1014G. PMC 2559964. PMID 18641630. doi:10.1038/nature07183.
- ↑ Ahmad M, Galland P, Ritz T, Wiltschko R, Wiltschko W (February 2007). "Magnetic intensity affects cryptochrome-dependent responses in Arabidopsis thaliana". Planta 225 (3): 615–24. PMID 16955271. doi:10.1007/s00425-006-0383-0. Resumo divulgativo – Centre national de la recherche scientifique.
- ↑ Harris SR, Henbest KB, Maeda K, Pannell JR, Timmel CR, Hore PJ, Okamoto H (December 2009). "Effect of magnetic fields on cryptochrome-dependent responses in Arabidopsis thaliana". Journal of the Royal Society, Interface 6 (41): 1193–205. PMC 2817153. PMID 19324677. doi:10.1098/rsif.2008.0519.
- ↑ Rodgers CT, Hore PJ (January 2009). "Chemical magnetoreception in birds: the radical pair mechanism". Proceedings of the National Academy of Sciences of the United States of America 106 (2): 353–60. Bibcode:2009PNAS..106..353R. PMC 2626707. PMID 19129499. doi:10.1073/pnas.0711968106.
- ↑ Biskup T, Schleicher E, Okafuji A, Link G, Hitomi K, Getzoff ED, Weber S (2009). "Direct observation of a photoinduced radical pair in a cryptochrome blue-light photoreceptor". Angewandte Chemie 48 (2): 404–7. PMC 4329312. PMID 19058271. doi:10.1002/anie.200803102.
- ↑ Müller P, Ahmad M (June 2011). "Light-activated cryptochrome reacts with molecular oxygen to form a flavin-superoxide radical pair consistent with magnetoreception". The Journal of Biological Chemistry 286 (24): 21033–40. PMC 3122164. PMID 21467031. doi:10.1074/jbc.M111.228940.
- ↑ Chandler D, Ilia Solov'yov I, Schulten K. "Cryptochrome and Magnetic Sensing". Beckman Institute for Advanced Science and Technology, University of Illinois Urbana–Champaign. Consultado o 2011-04-14.
- ↑ 54,0 54,1 Müller P, Yamamoto J, Martin R, Iwai S, Brettel K (November 2015). "Discovery and functional analysis of a 4th electron-transferring tryptophan conserved exclusively in animal cryptochromes and (6-4) photolyases". Chemical Communications 51 (85): 15502–5. PMID 26355419. doi:10.1039/C5CC06276D.
- ↑ 55,0 55,1 Cailliez F, Müller P, Firmino T, Pernot P, de la Lande A (February 2016). "Energetics of Photoinduced Charge Migration within the Tryptophan Tetrad of an Animal (6-4) Photolyase". Journal of the American Chemical Society 138 (6): 1904–15. PMID 26765169. doi:10.1021/jacs.5b10938.
Ligazóns externas
[editar | editar a fonte]- cryptochrome Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- Cryptochrome circadian clock in Monarch Butterflies Arquivado 21 de novembro de 2011 en Wayback Machine., de Steven M. Reppert, Departamento de Neurobioloxía, Universidade de Massachusetts
- Cryptochrome and Magnetic Sensing, Theoretical and Computational Biophysics Group na Universidade de Illinois en Urbana-Champaign
- 2IJG no Protein Data Bank; estrutura en 3-D do criptocromo 3 de Arabidopsis, obtida por cristalografía de raios X.
- Modelo animado da vía circadiana murina, incluíndo o papel de Cry
