Cromóforo
Un cromóforo é a parte dunha molécula responsable da súa cor.[1] A cor orixínase cando unha molécula absorbe certas lonxitudes de onda da luz visible e transmite ou reflicte outras. O cromóforo é unha rexión da molécula no que a diferenza de enerxía entre dous orbitais moleculares distintos cae dentro do rango do espectro visible. A luz visible que incide no cromóforo pode así ser absorbida ao excitar un electrón desde o seu estado fundamental ao seu estado excitado.
Nas moléculas biolóxicas que serven para capturar a luz ou detectar a enerxía luminosa, o cromóforo é o residuo que causa un cambio conformacional na molécula cando lle dá a luz.

Cromóforos de sistemas de enlaces pi conxugados[editar | editar a fonte]

Nos cromóforos conxugados, os electróns saltan entre niveis enerxéticos que son orbitais pi estendidos, creados por unha serie de enlaces simples e dobres alternados (conxugados), que a miúdo forman parte de sistemas aromáticos. Exemplos comúns son o retinal (composto que utiliza o ollo para detectar a luz), varios colorantes alimentarios, tinturas téxtiles (compostos azo), indicadores de pH, o licopeno, o β-caroteno, e as antocianinas. Hai varios factores na estrutura dun cromóforo que determinan as lonxitudes de onda do espectro de luz que absorberá o cromóforo. Ampliar os sistemas conxugados de enlaces con máis enlaces insaturados tende a facer que a absorción cambie a lonxitudes de onda máis longas. Poden utilizarse as regras de Woodward-Fieser para estimar aproximadamente a lonxitude de onda de absorción máxima ultravioleta-visible nos compostos orgánicos que teñen sistemas de enlaces pi conxugados.
Algúns destes cromóforos de compostos orgánicos son cromóforos de complexos metálicos, que conteñen un metal nun complexo de coordinación con ligandos. Exemplos son as clorofilas, que utilizan as plantas para a fotosíntese, e a hemoglobina, que transporta o oxíxeno no sangue dos vertebrados. Nestes dous exemplos, un metal está en complexo no centro dun anel macrocíclico tetrapirrol: o metal é o ferro nun grupo hemo (ferro dentro dun anel de porfirina) no caso da hemoglobina, ou un magnesio en complexo nun anel de tipo clorina no caso da clorofila. O sistema de enlaces pi moi conxugado do anel macrocíclico absorbe a luz visible. A natureza do metal central pode tamén influír na absorción do espectro do complexo metal-macrociclo ou en propiedades como o tempo de duración do estado excitado.[2][3][4] Os residuos tetrapirrólicos de compostos orgánicos que non son macrocíclicos pero que teñen sistemas de enlaces pi conxugados poden tamén actuar como cromóforo. Exemplos destes compostos son a bilirrubina e a urobilina, que mostran cor amarela.
Auxocromo[editar | editar a fonte]
Un auxocromo é un grupo funcional de átomos que se unen ao cromóforo, que modifica a capacidade do cromóforo de absorber luz, alterando a lonxitude de onda ou a intensidade da absorción.
Halocromismo en cromóforos[editar | editar a fonte]
Prodúcese halocromismo cando unha substancia cambia de cor cos cambios de pH. Esta é unha propiedade que teñen os indicadores de pH, cuxa estrutura molecular cambia ao producírense certas variacións no pH do medio que os rodea. Este cambio na estrutura afecta ao cromóforo da molécula indicadora de pH. Por exemplo, a fenolftaleína é un indicador de pH cuxa estrutura cambia cos cambios de pH da maneira que se mostra na seguinte táboa:
| Estrutura | 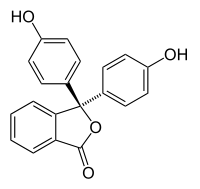 |
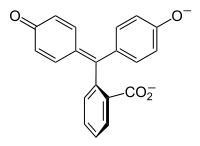
|
|---|---|---|
| pH | 0-8,2 | 8,2-12 |
| Condicións | ácido ou case neutro | básico |
| Nome da cor | de rosa a fucsia | |
| Cor |
Nun intervalo de pH de 0 a 8, a molécula ten tres aneis aromáticos unidos a un átomo de carbono con hibridación sp3 tetraédrica situado no centro, que non establece enlaces π nos aneis aromáticos conxugados. Debido á súa limitada extensión, os aneis aromáticos só absorben luz na rexión ultravioleta, e deste xeito o composto aparece incoloro no intervalo de pH 0-8. Porén, a medida que se incrementa o pH alén de 8,2, o carbono central pasa a formar parte dun dobre enlace con hibridación sp2 e cun orbital p que se solapa cos enlaces π nos aneis. Isto fai que os tres aneis se conxuguen conxuntamente para formar un cromóforo ampliado que absorbe maiores lonxitudes de onda na luz visible e mostra cor fucsia.[5] A intervalos de pH de 0-12, outros cambios de estrutura molecular dan lugar a outros cambios de cor (ver fenolftaleína).
Notas[editar | editar a fonte]
- ↑ IUPAC Gold Book Chromophore
- ↑ Gouterman, M. (1978) Optical spectra and electronic structure of porphyrins and related rings. In Dolphin, D. (ed.) The porphyrins. Academic Press, New York. Volume III, Part A, pp 1-165
- ↑ Scheer, H. (2006) An overview of chlorophylls and bacteriochlorophylls: biochemistry, biophysics, functions and applications. Advances in Photosynthesis and Respiration, vol 25, pp 1-26
- ↑ Shapley, P. (2012) Absorbing light with organic molecules. http://butane.chem.uiuc.edu/pshapley/GenChem2/B2/1.html Arquivado 21 de xuño de 2013 en Wayback Machine.
- ↑ UV-Visible Absorption Spectra
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Causa da cor Arquivado 17 de abril de 2021 en Wayback Machine.: mecanismos físicos polos cales se xera a cor.(en inglés)
- A nanoelectrónica de alta velocidade feita posible polos cromóforos - Azonano.com (en inglés)
