Clostridium difficile
| Clostridium difficile | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Colonias de C. difficile crecendo nunha placa de ágar sangue. | |||||||||||||||
| Clasificación científica | |||||||||||||||
| |||||||||||||||
| Nome binomial | |||||||||||||||
| Clostridium difficile Hall & O'Toole, 1935 | |||||||||||||||
| Sinonimia | |||||||||||||||
| |||||||||||||||
Clostridium difficile (sinónimo Clostridioides difficile) é unha especie bacteriana formada por bacilos grampositivos formadores de esporas, anaerobios estritos. Forma parte da microbiota intestinal normal nunha pequena proporción (2-5 %) de individuos sans e de pacientes hospitalizados.[1] C. difficile é a causa máis importante de colite pseudomembranosa,[2] unha infección do colon, que con frecuencia é secundaria á erradicación da flora saprófita polo uso intenso de antibióticos. O tratamento xeralmente consiste en suspender a administración de antibióticos con excepción de anticlostridiais, como o metronidazol.
Taxonomía[editar | editar a fonte]
Recentemente propuxéronse cambios taxonómicos no xénero Clostridium. Concretamente, esta especie foi transferida do xénero Clostridium ao Clostridioides en 2016, polo que o seu nome bnomial pasou a ser Clostridioides difficile.[3][4][5] Este novo nome reflicte as diferenzas taxonómicas entre esta especie e os membros do xénero Clostridium, aínda que o nome abreviado é o mesmo C. difficile.[6] En 2018, a única especie dentro do xénero Clostrioides ademais desta era Clostridioides mangenotii (antes chamada Clostridium mangenotii).[7]
Características[editar | editar a fonte]

Os clostridios son bacterias móbiles que se encontran universalmente na natureza, especialmente na terra. Co microscopio vense con forma de paus de tambor ou mixtos co avultamento localizado no extremo. As células de C. difficile son grampositivas e as colonias mostran un crecemento óptimo en placas de ágar sangue a temperaturas corporais humanas. Cando o medio que a rodea se volve estresante, a bacteria produce endósporas que toleran condiciós extremas que doutro modo destruirían o microorganismo. Descritas por primeira vez por Hail e O'Toole en 1935, entón foi chamado clostridio difícil pola súa gran resistencia aos intentos iniciais de cultivar esta esixente especie, que crecía moi lentamente nos cultivos.[8]
C. difficile é unha bacteria comensal do intestino humano nunha minoría da poboación. Os pacientes que estiveron longo tempo hospitalizados ou en residencias de coidados especiais teñen unha maior probabilidade de ser colonizadas por este organismo. En pequeno número, non adoita causar danos de importancia clínica. Os antibióticos, en especial os que teñen actividade de amplo espectro, causan un desequilibrio na flora intestinal, o que orixina unha sobrepoboación de C. difficile, e leva á aparición da colite pseudomembranosa.
Xenoma[editar | editar a fonte]
A primeira xecuencia xenómica completa dunha cepa de C. difficile publicouna en 2005 o Sanger Institute en Reino Unido. Tratábase da cepa 630, unha cepa virulenta e resistente a moitos fármacos illada en Suíza en 1982. Os científicos do Sanger Institute secuenciaran xenomas duns 30 illados de C. difficile utilizando tecnoloxías de secuenciación de nova xeración de 454 Life Sciences e Illumina.[9] O tamaño do seu xenoma é de 4,3 Mb.
Os investigadores da Universidade McGill de Montreal, Canadá secuenciaron o xenoma da cepa Quebec, moi virulenta, en 2005 utilizando tecnoloxías de secuenciación de ultra alto rendemento. As probas supuxeron facer 400.000 reaccións de secuenciación en paralelo de ADN do xenoma da bacteria, que fora previamente fragmentado para a súa secuenciación. Estas secuencias foron ensambladas por computadora para formar a secuencia xenómica completa.[10][11]
En 2012, os científicos da Universidade de Oxford secuenciaron os xenomas de C. difficile de 486 casos de infeccións ocorridas durante catro anos en Oxfordshire utilizando tecnoloxías de secuenciación de seguinte xeración de Illumina.[12]
Factores de virulencia[editar | editar a fonte]
Os mellor coñecidos son as toxinas A e B, que producen diarreas e inflamacións. En total presenta os seguintes factores de virulencia:
- Enterotoxina (toxina A): Produce quimiotaxe; induce a produción de citocinas con hipersecreción de fluído; produce necrose hemorráxica. É unha glicosiltransferase que ten como diana e inactiva GTPases da familia Rho.[1]
- Citotoxina (toxina B): Induce a despolimerización da actina con perda do citoesqueleto celular. Igual que a toxina A é unha glicosiltransferase que inactiva GTPases da familia Rho, producindo un descenso da súa ADP-ribosilación.[13]
- Toxina binaria: É outra toxina descrita nesta bacteria cuxo papel nas doenzas non se coñece ben.[14]
- Factor de adhesión: Intervén na unión ás células do colon humanas.
- Hialuronidase: Produce actividade hidrolítica.
- Formación de endósporas: Permite a supervivencia do microorganismo durante meses no medio hospitalario.
Desde 2001 describíronse cepas que causan gromos con maior gravidade e con máis frecuencia. Pertencen a un só tipo de cepas con estas características: cepa de campo pulsante tipo NAP-1 (North America pulsed-field type 1), ribotipo 027, endonuclease de restrición tipo B1, toxinotipo III.
O que fai que estas cepas se propaguen con máis rapidez e sexan máis virulenta é que posúen:
- mutación no xene regulador da toxina tcdC (deleción parcial no xene regulador negativo da toxina)
- xenes de toxina binaria
- mutacións de resistencia ás fluoroquinolonas.
Epidemioloxía[editar | editar a fonte]
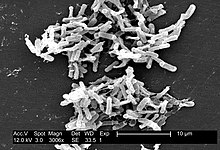
O microorganismo é ubicuo. Coloniza o intestino dunha pequena proporción de individuos sans (menor do 5%). A exposición a antibióticos asóciase co sobrecrecemento e posterior enfermidade (infección endóxena). C. difficile é resistente á maioría dos antibióticos, e mesmo pode crecer nesas condicións. Transmítese de persoa a persoa pola ruta fecal-oral. Debido a que o organismo forma esporas resistentes á calor (termorresistentes), pode permanecer nun hospital ou residencia durante longos períodos de tempo. Pode desenvolverse en case calquera superficie do hospital. Por exemplo, as esporas poden detectarse nas habitacións do hospital con pacientes infectados (fundamentalmente arredor das camas e baños), e pode ser unha fonte exóxena de infección (enfermidade nosocomial). Unha vez que se inxiren as esporas, pasan polo estómago indemnes por ser resistentes aos ácidos. Transfórmanse na súa forma vexetativa no colon, onde se multiplican.
Varios desinfectantes de uso común en hospitais non serven para matar esta bacteria, e mesmo poden promover a formación de esporas. Porén, os desinfectantes con cloro son eficaces destruíndo os organismos.[15] As cepas multirresistentes a antibióticos poden converterse nun problema sanitario emerxente.[16]
Doenzas e diagnóstico[editar | editar a fonte]
As toxinas producidas por C. difficile son as responsables de enfermidades gastrointestinais asociadas a antibióticos, que van desde unha diarrea relativamente benigna e autolimitada, ata unha colite pseudomembranosa grave que pon en risco a vida. Por tanto, as enfermidades causadas por C. difficile son:
- Colonización asintomática.
- Diarrea asociada a antibióticos.
- Colite pseudomembranosa.
A enfermidade por C. difficile confírmase co illamento do microorganismo ou coa detección da citotoxina ou a enterotoxina nas feces do paciente.
O cultivo de C. difficile pode ser útil en certas circunstancias: cando a sospeita clínica permanece alta a pesar de obter un ensaio de citotoxicidade negativo, e cando o tipado da cepa e o estudo de susceptibilidade é necesario para estudos epidemiolóxicos.
O estudo da citotoxicidade en cultivo celular, con ou sen neutralización é considerado con frecuencia o test diagnóstico estándar para a colite por Clostridium. Porén, o método de dous pasos que combina o cultivo coa citotoxicidade compite coa proba de citotoxicidade soa como mellor método, porque detecta do 15 ao 23 % máis de illamentos de C. difficile toxixénico. O estudo de citotoxicidade permite a detección dos dous tipos de cepas: toxixénica A+/B+ e A-/B+.
A técnica ELISA é doada de utilizar, de resultado moi rápido, e con capacidade de producir resultados de lotes de mostras, aínda que o custo de cada proba pode ser algo elevado cando se procesan moitas mostras. Moitos kits comerciais posúen baixa sensibilidade de detección aínda que os protocolos que usan EIA dirixidos a toxinas como un método confirmatorio despois da proba de screening dirixido a antíxeno de C. difficile, máis sensible, poden resolver este inconveniente. A detección de toxina A soa pode que non detecte as cepas A-/B+ que causaron doenza grave en varios gromos. A detección da glutamato deshidroxenase soa non pode discriminar entre illamentos toxixénicos e non toxixénicos.
Tratamento, prevención e control[editar | editar a fonte]
Na doenza grave utilízase un tratamento con metronidazol e vancomicina.
A recaída é frecuente, debido a que as esporas non se ven afectadas polos antibióticos; un segundo ciclo de antibióticos co mesmo antibiótico adoita ter éxito. Débese limpar a fondo a habitación do hospital despois de dar de alta ao paciente.
O transplante de microbiota fecal (desde feces dun suxeito san a outro doente) pode ser moi eficaz no tratamento da recorrencia da infección por este clostridio. [17][18]
Bacteriófagos[editar | editar a fonte]
De C. difficile illáronse polo menos oito virus bacteriófagos principalmente temperados, con tamaños xenómicos que van de 30 a 60 kb.[19] Tanto as cepas de C. difficile obtidas de fontes ambientais coma clínicas levan diversos profagos.[19]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 Ryan KJ; Ray CG (editors) (2004). McGraw Hill, ed. Sherris Medical Microbiology (4th ed. ed.). pp. 322–4. ISBN 0-8385-8529-9.
- ↑ WebMD, ed. (1 de xullo de 2005). "Pseudomembranous Colitis". eMedicine. Consultado o 11-01-2007.
- ↑ Oren, Aharon; Garrity, George M. (2017). "List of new names and new combinations previously effectively, but not validly, published". International Journal of Systematic and Evolutionary Microbiology 67 (9): 3140–3143. PMC 5817221. PMID 28891789. doi:10.1099/ijsem.0.002278.
- ↑ Lawson, Paul A.; Citron, Diane M.; Tyrrell, Kerin L.; Finegold, Sydney M. (agosto de 2016). "Reclassification of Clostridium difficile as Clostridioides difficile (Hall and O'Toole 1935) Prévot 1938". Anaerobe 40: 95–99. ISSN 1095-8274. PMID 27370902. doi:10.1016/j.anaerobe.2016.06.008.
- ↑ Zhu, Duolong; Sorg, Joseph A.; Sun, Xingmin (2018). "Clostridioides difficile Biology: Sporulation, Germination, and Corresponding Therapies for C. difficile Infection". Frontiers in Cellular and Infection Microbiology (en inglés) 8: 29. ISSN 2235-2988. PMC 5809512. PMID 29473021. doi:10.3389/fcimb.2018.00029.
- ↑ Lawson, Paul A.; Citron, Diane M.; Tyrrell, Kerin L.; Finegold, Sydney M. (agosto de 2016). "Reclassification of Clostridium difficile as Clostridioides difficile (Hall and O'Toole 1935) Prévot 1938". Anaerobe 40: 95–99. ISSN 1075-9964. PMID 27370902. doi:10.1016/j.anaerobe.2016.06.008.
- ↑ Galperin, Michael Y.; Brover, Vyacheslav; Tolstoy, Igor; Yutin, Natalya (2016). "Phylogenomic analysis of the family Peptostreptococcaceae (Clostridium cluster XI) and proposal for reclassification of Clostridium litorale (Fendrich et al. 1991) and Eubacterium acidaminophilum (Zindel et al. 1989) as Peptoclostridium litorale gen. nov. comb. nov. and Peptoclostridium acidaminophilum comb. nov.". International Journal of Systematic and Evolutionary Microbiology 66 (12): 5506–5513. PMC 5244501. PMID 27902180. doi:10.1099/ijsem.0.001548.
- ↑ Hall I, O'Toole E (1935). "Intestinal flora in newborn infants with a description of a new pathogenic anaerobe, Bacillus difficilis". Am J Dis Child 49: 390.
- ↑ He M, Sebaihia M, Lawley TD, Stabler RA, Dawson LF, Martin MJ, Holt KE, Seth-Smith HM, Quail MA, Rance R, Brooks K, Churcher C, Harris D, Bentley SD, Burrows C, Clark L, Corton C, Murray V, Rose G, Thurston S, van Tonder A, Walker D, Wren BW, Dougan G, Parkhill J; Sebaihia; Lawley; Stabler; Dawson; Martin; Holt; Seth-Smith; Quail; Rance; Brooks; Churcher; Harris; Bentley; Burrows; Clark; Corton; Murray; Rose; Thurston; Van Tonder; Walker; Wren; Dougan; Parkhill (abril de 2010). "Evolutionary dynamics of Clostridium difficile over short and long time scales" (PDF). Proceedings of the National Academy of Sciences of the United States of America 107 (16): 7527–32. Bibcode:2010PNAS..107.7527H. PMC 2867753. PMID 20368420. doi:10.1073/pnas.0914322107.
- ↑ Loo VG, Poirier L, Miller MA, Oughton M, Libman MD, Michaud S, Bourgault AM, Nguyen T, Frenette C, Kelly M, Vibien A, Brassard P, Fenn S, Dewar K, Hudson TJ, Horn R, René P, Monczak Y, Dascal A; Poirier; Miller; Oughton; Libman; Michaud; Bourgault; Nguyen; Frenette; Kelly; Vibien; Brassard; Fenn; Dewar; Hudson; Horn; René; Monczak; Dascal (2005 month = December). "A predominantly clonal multi-institutional outbreak of Clostridium difficile-associated diarrhea with high morbidity and mortality". The New England Journal of Medicine 353 (23): 2442–9. doi:10.1056/NEJMoa051639. PMID 16322602.
- ↑ Scientists map C. difficile strain - Institute of Public Affairs, Montreal
- ↑ Didelot X, Eyre DW, Cule M, Ip CL, Ansari MA, Griffiths D, Vaughan A, O'Connor L, Golubchik T, Batty EM, Piazza P, Wilson DJ, Bowden R, Donnelly PJ, Dingle KE, Wilcox M, Walker AS, Crook DW, A Peto TE, Harding RM; Eyre; Cule; Ip; Ansari; Griffiths; Vaughan; O'Connor; Golubchik; Batty; Piazza; Wilson; Bowden; Donnelly; Dingle; Wilcox; Walker; Crook; Peto; Harding (decembro de 2012). "Microevolutionary analysis of Clostridium difficile genomes to investigate transmission" (PDF). Genome Biology 13 (12): R118. PMC 4056369. PMID 23259504. doi:10.1186/gb-2012-13-12-r118. Arquivado dende o orixinal (PDF) o 21 de setembro de 2013. Consultado o 12 de marzo de 2015.
- ↑ Just I, Selzer J, von Eichel-Streiber C, Aktories K; Selzer; von Eichel-Streiber; Aktories (1995). "The low molecular mass GTP-binding protein Rh is affected by toxin a from Clostridium difficile". The Journal of Clinical Investigation 95 (3): 1026–31. PMC 441436. PMID 7883950. doi:10.1172/JCI117747.
- ↑ Barth H, Aktories K, Popoff MR, Stiles BG; Aktories; Popoff; Stiles (2004). "Binary Bacterial Toxins: Biochemistry, Biology, and Applications of Common Clostridium and Bacillus Proteins". Microbiology and Molecular Biology Reviews : MMBR 68 (3): 373–402, table of contents. PMC 515256. PMID 15353562. doi:10.1128/MMBR.68.3.373-402.2004.
- ↑ "Cleaning agents 'make bug strong'". BBC News Online. 3 de abril de 2006. Consultado o 11-01-2007.
- ↑ McDonald LC (agosto de 2005). "Clostridium difficile: responding to a new threat from an old enemy". Infection Control and Hospital Epidemiology : The Official Journal of the Society of Hospital Epidemiologists of America 26 (8): 672–5. doi:10.1086/502600. PMID 16156321.
- ↑ Systematic Review of Intestinal Microbiota Transplantation (Fecal Bacteriotherapy) for Recurrent Clostridium difficile Infection Ethan Gough,1 Henna Shaikh,2 and Amee R. Manges1,3 Infectious Diseases 2011;53(10):994–1002
- ↑ "Deadly superbug Clostridium difficile beaten using poo transplants from healthy people". Herald Sun Australia. 12 de xullo de 2011. Consultado o 11-08-2011.
- ↑ 19,0 19,1 Hargreaves KR, Clokie MR; Clokie (2014). "Clostridium difficile phages: Still difficult?". Frontiers in Microbiology 5: 184. PMC 4009436. PMID 24808893. doi:10.3389/fmicb.2014.00184.
Véxase tamén[editar | editar a fonte]
| Wikispecies posúe unha páxina sobre: Clostridium difficile |
| Wikimedia Commons ten máis contidos multimedia na categoría: Clostridium difficile |
Bibliografía[editar | editar a fonte]
- Murray P, Rosenthal K, Kobayashi G, Pfaller M. (2002). "Microbiología Médica". Cuarta Edición, páxinas 344, 345, 346.
