Antibiótico beta-lactámico

Os antibióticos β-lactámicos son unha clase de antibióticos de amplo espectro, que comprenden todos os axentes antibióticos que conteñen un anel beta-lactámico na súa estrutura molecular. Isto inclúe a penicilina e os seus derivados (penams), cefalosporinas (cefems), monobactams e carbapenems.[1] A maioría dos antibióticos β-lactámicos funcionan inhibindo a biosíntese da parede celular no organismo bacteriano e son o grupo máis amplamente utilizado de antibióticos. Ata 2003, cando se cuantificaron polas súas vendas, máis da metade de todos os antibióticos comerciais dispoñibles en uso eran compostos β-lactámicos.[2]
As bacterias a miúdo desenvolven resistencia a antibióticos β-lactámicos porque producen un encima β-lactamase, o cal ataca o anel β-lactámico do antibiótico. Para superar esta resistencia, os antibióticos β-lactámicos adminístranse a miúdo xunto cun inhibidor da β-lactamase, como o ácido clavulánico.
Uso médico[editar | editar a fonte]
Os antibióticos β-lactámicos están indicados para a prevención e o tratamento das infeccións bacterianas causadas por microorganismos susceptibles a eles. Ao primeiro, os antibióticos β-lactámicos eran activos esencialmente só contra bacterias grampositivas, aínda que o desenvolvemento recente de antibióticos β-lactámicos de espectrro estendido activos contra varios organismos gramnegativos incrementou a súa utilidade.
Efectos adversos[editar | editar a fonte]
Reaccións adversas[editar | editar a fonte]
Reaccións adversas comúns aos antibióticos β-lactámicos inclúen a diarrea, náusea, erupcións cutáneas, urticaria, superinfección (como a candidíase).[3]
Entre os efectos adversos infrecuentes están a febre, vómitos, eritema, dermatite, anxioedema, colite pseudomembranosa.[3]
A dor e a inflamación no lugar de inxección son tamén comúns cando os antibióticos β-lactámicos se administran por vía parenteral.
Alerxia/hipersensibilidade[editar | editar a fonte]
As reaccións adversas mediadas inmunoloxicamente ante calquera antibiótico β-lactámico poden ocorrer en ata o 10% dos pacientes que reciben ese axente, unha pequena fracción das cales son verdadeiras reaccións alérxicas mediadas por IgE (erupción por amoxicilina). A anafilaxe ocorrerá en aproximadamente o 0,01% dos pacientes.[3][4] Estimouse que hai dun 5% a un 10% de sensibilidade cruzada entre derivados da penicilina, cefalosporinas e carbapenems; pero esta cifra foi discutida por varios investigadores.
Non obstante, o risco de reactividade cruzada é suficiente para contraindicar o uso de todos os antibióticos β-lactámicos en pacientes cunha historia de reaccións alérxicas graves (urticaria, anafilaxe, nefrite intersticial) a calquera antibiótico β-lactámico.
Pode ocorrer unha reacción de Jarisch–Herxheimer despois do tratamento inicial dunha infección por espiroquetas como a sífilis cun antibiótico β-lactámico.
Modo de acción[editar | editar a fonte]



Os antibióticos β-lactámicos son bactericidas, e actúan inhibindo a síntese da capa de peptidoglicano da parede celular bacteriana. A capa de peptidoglicano é importante para a integridade estrutural da parede celular, especialmente en organismos grampositivos, nos que é o compoñente máis externo e principal da parede. O paso de transpeptidación final na síntese do peptidoglicano é facilitado polas DD-transpeptidases, que son proteínas que se unen á penicilina (PBP, penicillin binding proteins). As PBP varían na súa afinidade pola penicilina coa que se unen ou outros antibióticos β-lactámicos. A cantidade de PBP varía nas distintas especies bacterianas.
Os antibióticos β-lactámicos son análogos da d-alanil-d-alanina, que son os residuos de aminoácidos terminais nas subunidades NAM/NAG-péptido precursoras da capa nacente de peptidoglicano. A semellanza estrutural entre os antibióticos β-lactámicos e a d-alanil-d-alanina facilita asúa unión ao sitio activo das PBP. O núcleo β-lactámico da molécula únese irreversiblemente para (acilar) o residuo Ser403 do sitio activo da PBP. Esta inhibición irreversible das PBP impide os enlaces cruzados finais (transpeptidación) da capa de peptidoglicano nacente, o que distorsiona a síntese da parede celular.[5]
Os antibióticos β-lactámicos bloquean non só a división das bacterias, incluíndo as cianobacterias, pero tamén a división de cianelas, os orgánulos fotosintéticos das glaucófitas, e a división dos cloroplastos das briófitas. En contraste, non teñen efecto sobre os plastidios de plantas vasculares moi desenvolvidas. Isto apoia a teoría endosimbiótica e indica unha evolución da división dos plastidios nas plantas terrestres.[6]
En circunstancias normais os precursores dos peptidoglicano sinalizan unha reorganización da parede bacteriana e, como consecuencia, desencadean a activación de hidrolases da parede celular autolíticas. A inhibición dos enlaces cruzados feito polas β-lactamas causa unha acumulación de precursores do peptidoglicano, que desencadea a dixestión do peptidoglicano existente polas hidrolases autolíticas sen a produción de novos peptidoglicanos. Como resultado, a acción bactericida dos antibióticos β-lactámicos aínda se potencia máis.
Potencia[editar | editar a fonte]
- Véxase tamén: Beta-lactama#Reactividade.
Dúas das características dos antibióticos β-lactámicos foron correlacionadas coas súas potencias como antibióticos.[7] A primeira denomínase "parámetro de Woodward", h, e é a altura (en ángstroms) da pirámide formada polo átomo de nitróxeno da β-lactama do ápice e os tres átomos de carbono adxacentes da base.[8] O segundo chámase "parámetro de Cohen", c, e é a distancia entre o átomo de carbono do carboxilato e o átomo de oxíxeno do carbonilo da β-lactama.[9] Esta distancia crese que corresponde coa distancia entre o sitio de unión do carboxilato e o burato de oxianión do encima PBP. Os mellores antibióticos son aqueles con valores de h máis altos (máis reactivos á hidrólise) e valores de c máis baixos (mellor unión ás PBP).[7]
Modos de resistencia[editar | editar a fonte]
Por definición, todos os antibióticos β-lactámicos teñen un anel β-lactámico na súa estrutura. A efectividade destes antibióticos depende da súa capacidade de chegar intactos ao PBP e a súa capacidade de unirse á PBP. Por tanto, hai dous xeitos principais de resistencia bacteriana aos β-lactámicos:
Hidrólise encimática do anel β-lactámico[editar | editar a fonte]
Se a bacteria produce o encima β-lactamase ou a penicilinase, o encima hidrolizará o anel β-lactámico do antibiótico, facendo que o antibiótico xa non sexa efectivo.[10] (Un exemplo dun destes encimas é a metalo-beta-lactamase 1 Nova Delhi, descuberta en 2009.) Os xenes que codifican estes encimas poden estar presentes inherentemente no cromosoma bacteriano ou poden adquirirse por transferencia dun plásmido (resistencia mediada por plásmidos), e a expresión xéniica da β-lactamase pode ser inducida por exposición a β-lactamas.

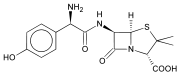
A produción de β-lactamase por unha bacteria non necesariamente descarta todos os tratamentos con antibióticos β-lactámicos. Nalgúns casos, os antibióticos β-lactámicos poden ser coadministrados xunto cun inhibidor de β-lactamase. Por exemplo, a Augmentin (FGP) está composta de amoxicilina (un antibiótico β-lactámico) e ácido clavulánico (un inhibidor da β-lactamase). O ácido clavulánico está deseñado para superar todos os encimas β-lactamases, e serve como un efectivo antagonista para que a amoxicilina non sexa afectada polos encimas β-lactamases.
Estanse estudando outros inhibidores de β-lactamases como os ácidos borónicos, os cales se unen irreversiblemente ao sitio activo das β-lactamases. Isto é unha vantaxe en comparación co ácido clavulánico e competidores beta-lactámicos similares, porque non poden ser hidrolizados, e por tanto, non quedan inutilizados. Actualmente estase facendo un grande esforzo investigador para desenvolver ácidos borónicos deseñados para unirse a diferentes isocimas de β-lactamases.[11]
Porén, en todos os casos nos que se sospeita que hai unha infección por bacterias produtoras de β-lactamase, a elección dun antibiótico β-lactámico axeitado debería considerarse coidadosamente antes do tratamento. En especial, a elección da terapia co β-lactámico apropiado é da maior importancia contra organismos que xa se sabe que teñen algún nivel de expresión de β-lactamase. Nese caso, o fracaso no uso da terapia co β-lactámico máis apropiado ao inicio do tratamento podería ter como resultado que se produza a selección de bacterias cun maior nivel de expresión de β-lactamase, facendo máis difíciles posteriores intentos con outros antibióticos β-lactámicos.[12]
Posesión de proteínas que se unen á penicilina alteradas[editar | editar a fonte]
Como resposta ao uso de β-lactámicos para controlar infeccións bacterianas, nalgunhas bacterias evolucionaron proteínas que se unen á penicilina (PBP) con novas estruturas. Os antibióticos β-lactámicos non poden unirse tan eficazmente a estas PBP alteradas, e, como resultado, os β-lactámicos son menos efectivos á hora de alterar a síntese da parede celular. Exemplos notables deste modo de resistencia son o Staphylococcus aureus resistentes á meticilina (SARM) e o Streptococcus pneumoniae resistente á penicilina. A presenza de PBP alteradas non necesariamente descartan todas as opcións de tratamento con antibióticos β-lactámicos.
Nomenclatura[editar | editar a fonte]

As β-lactamas clasifícanse segundo as súas estruturas centrais.[13]
- β-Lactamas fusionadas a aneis de cinco membros saturados:
- β-Lactamas que conteñen aneis de tiazolidina, as cales se denominan penams.
- β-Lactamas que conteñen aneis de pirrolidina, as cales se denominan carbapenams.
- β-Lactamas fusionadas a aneis de oxazolidina, as cales se denominan oxapenams ou clavams.
- β-Lactamas fusionadas a aneis de cinco membros insaturados:
- β-Lactamas que conteñen aneis de 2,3-dihidrotiazol, as cales se denominan penems.
- β-Lactamas que conteñen aneis de 2,3-dihidro-1H-pirrol, as cales se denominan carbapenems.
- β-Lactamas fusionadas a aneis de seis membros insaturados:
- β-Lactamas non fusionadas a ningún outro anel, que se denominan monobactams.
Por convención, as β-lactamas bicíclicas numéranse empezando pola posición ocupada polo xofre en penams e cefems, sen importar que átomo sexa en cada clase. É dicir, a posición 1 é sempre a adxacente ao carbono β do anel β-lactámico. A numeración continúase no sentido das agullas do reloxo desde a posición 1 ata que se chega ao carbono β da β-lactama, e desde ese punto a numeración continúa en sentido contrario ás agullas do reloxo ao longo do anel lactámico para numerar o resto dos carbonos. Por exemplo, o átomo de nitróxeno de todas as β-lactamas bicíclicas fusionado con aneis de 5 membros está etiquetado na posición 4, como nos penams, mentres que nos cefems, o nitróxeno está na posición 5.
A numeración dos monolactams segue a da IUPAC; o átomo de nitróxeno corresponde coa posición 1, o carbono carbonilo é o 2, o carbono α é o 3, e o carbono β o 4.
Biosíntese[editar | editar a fonte]
Ata agora descubríronse dous métodos de biosintetizar o núcleo β-lactámico desta familia de antibióticos. A primeira vía que se descubriu foi a dos penams e cefems. Esta vía empeza cunha sintetase de péptido non ribosómico (NRPS), a ACV sintetase (ACVS), que xera un tripéptido linear δ-(L-α-aminoadipil)-L-cisteína-D-valina (chamado ACV). O ACV é ciclado oxidativamente (dúas ciclacións por un só encima) a un intermediario bicíclico isopenicilina N pola isopenicilina N sintase (IPNS) para formar a estrutura central do penam.[14] Varias transamidacións orixinan as diferentes penicilinas naturais.
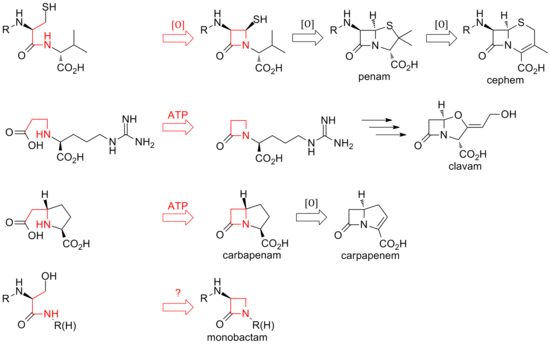
A biosíntese de cefems ramifícase ao chegar á isopenicilina N por unha expansión de anel oxidativa para dar o núcleo do cefem. Igual que nos penams, as diversas cefalosporinas e cefamicinas proceden de diferentes transamidacións, como é o caso das penicilinas.
Aínda que o peche do anel en penams e cefems se produce entre as posicións 1 e 4 da β-lactama e é oxidativo, os clavams e carbapenems pechan os seus aneis por dous procesos electrónicos entre as posicións 1 e 2 do nel. As β-lactama sintetases son responsables destas ciclacións, e o carboxilato dos substratos de anel aberto é activado polo ATP.[15] Nos clavams, a β-lactama fórmase antes que o segundo anel; en carbapenems, o anel β-lactámico péchase en segundo lugar.
A biosíntese do anel β-lactámico da tabtoxina reproduce a dos clavams e carbapenems. O peche do anel lactámico nos outros monobactams, como a sulfazecina e as nocardicinas, pode implicar un terceiro mecanismo no que se produce unha inversión de configuración no carbono β.[16]
Notas[editar | editar a fonte]
- ↑ Holten KB, Onusko EM (August 2000). "Appropriate prescribing of oral beta-lactam antibiotics". American Family Physician 62 (3): 611–20. PMID 10950216. Arquivado dende o orixinal o 06 de xuño de 2011. Consultado o 02 de decembro de 2017.
- ↑ Elander, R. P. (2003). "Industrial production of beta-lactam antibiotics". Applied microbiology and biotechnology 61 (5–6): 385–392. PMID 12679848. doi:10.1007/s00253-003-1274-y.
- ↑ 3,0 3,1 3,2 Rossi S (Ed.) (2004). Australian Medicines Handbook 2004. Adelaide: Australian Medicines Handbook. ISBN 0-9578521-4-2.
- ↑ Pichichero ME (April 2005). "A review of evidence supporting the American Academy of Pediatrics recommendation for prescribing cephalosporin antibiotics for penicillin-allergic patients". Pediatrics 115 (4): 1048–57. PMID 15805383. doi:10.1542/peds.2004-1276.
- ↑ Fisher, J. F.; Meroueh, S. O.; Mobashery, S. (2005). "Bacterial Resistance to β-Lactam Antibiotics: Compelling Opportunism, Compelling Opportunity†". Chemical Reviews 105 (2): 395–424. PMID 15700950. doi:10.1021/cr030102i.
- ↑ Kasten, B.; Reski, R. (1997-01-01). "β-Lactam antibiotics inhibit chloroplast division in a moss (Physcomitrella patens) but not in tomato (Lycopersicon esculentum)". Journal of Plant Physiology 150 (1): 137–140. doi:10.1016/S0176-1617(97)80193-9.
- ↑ 7,0 7,1 Nangia, Ashwini; Biradha, Kumar; Desiraju, Gautam R. (1996-01-01). "Correlation of biological activity in β-lactam antibiotics with Woodward and Cohen structural parameters—a Cambridge database study". J. Chem. Soc., Perkin Trans. 2 (en inglés) (5): 943–953. ISSN 1364-5471. doi:10.1039/p29960000943.
- ↑ Woodward, R. B. (1980-05-16). "Penems and Related Substances". Philosophical Transactions of the Royal Society of London B: Biological Sciences (en inglés) 289 (1036): 239–250. ISSN 0962-8436. PMID 6109320. doi:10.1098/rstb.1980.0042.
- ↑ Cohen, N. Claude (1983-02-01). ".beta.-Lactam antibiotics: geometrical requirements for antibacterial activities". Journal of Medicinal Chemistry 26 (2): 259–264. ISSN 0022-2623. doi:10.1021/jm00356a027.
- ↑ Drawz, S. M.; Bonomo, R. A. (2010). "Three Decades of β-Lactamase Inhibitors". Clinical Microbiology Reviews 23 (1): 160–201. PMC 2806661. PMID 20065329. doi:10.1128/CMR.00037-09.
- ↑ Leonard, David A.; Bonomo, Robert A.; Powers, Rachel A. (2013-11-19). "Class D β-Lactamases: A Reappraisal after Five Decades". Accounts of Chemical Research 46 (11): 2407–2415. ISSN 0001-4842. PMC 4018812. PMID 23902256. doi:10.1021/ar300327a.
- ↑ Macdougall C (2011). "Beyond Susceptible and Resistant Part I: Treatment of Infections Due to Gram-Negative Organisms with Inducible B-lactamases". Journal of Pediatric Pharmacology and Therapeutics 16 (1): 23–30. PMC 3136230. PMID 22477821.
- ↑ Dalhoff, A.; Janjic, N.; Echols, R. (2006). "Redefining penems". Biochemical Pharmacology 71 (7): 1085–1095. PMID 16413506. doi:10.1016/j.bcp.2005.12.003.
- ↑ Lundberg, M.; Siegbahn, P. E. M.; Morokuma, K. (2008). "The Mechanism for Isopenicillin N Synthase from Density-Functional Modeling Highlights the Similarities with Other Enzymes in the 2-His-1-carboxylate Family†". Biochemistry 47 (3): 1031–1042. PMID 18163649. doi:10.1021/bi701577q.
- ↑ Bachmann, B. O.; Li, R.; Townsend, C. A. (1998). "Β-Lactam synthetase: A new biosynthetic enzyme". Proceedings of the National Academy of Sciences of the United States of America 95 (16): 9082–9086. PMC 21295. PMID 9689037. doi:10.1073/pnas.95.16.9082.
- ↑ Townsend, CA; Brown, AM; Nguyen, LT (1983). "Nocardicin A: Stereochemical and biomimetic studies of monocyclic β-lactam formation". Journal of the American Society 105 (4): 919–927. doi:10.1021/ja00342a047.
