Organoclorado
 
|
| Dúas representacións dun organoclorado: cloroformo. |
Un organoclorado, composto organoclorado, hidrocarburo clorado, clorocarbono, cloroalcano ou composto orgánico clorado é un composto químico orgánico que contén un ou máis átomos de cloro unidos directamente aos átomos de carbono da molécula por enlace covalente.
A súa ampla variedade estrutural e as propiedades químicas diverxentes fan que teñan unha ampla gama de aplicacións. Moitos derivados clorados son controvertidos debido aos efectos destes compostos no medio ambiente e a saúde humana e animal, sendo en xeral daniños para os seres vivos,[1] e poden chegar a ser canceríxenos. Moitos deles empréganse pola súa acción insecticida ou pesticida;[2] outros son subprodutos da industria.
Algúns exemplos de organoclorados son: triclorometano (CHCl3), tetracloruro de carbono (CCl4), DDT e sucralosa.
Propiedades físicas[editar | editar a fonte]
Os átomos de cloro substituíntes modifican as propiedades físicas dos compostos orgánicos de diversas maneiras. Adoitan ser máis densos que a auga, debido á elevada masa atómica do cloro. Estes átomos de cloro inducen interaccións intermoleculares máis fortes que cando posúen átomos de hidróxeno no sitio dos de cloro. O efecto ilústrase pola evolución dos puntos de ebulición: metano (-161,6 °C), cloruro de metilo (-24,2 °C), diclorometano (40 °C), cloroformo (61,2 °C), e tetracloruro de carbono (76,72 °C). O aumento das interaccións intermoleculares atribúese tanto aos efectos das forzas de Van der Waals coma á maior polaridade dos enlaces.
Presenza na natureza[editar | editar a fonte]
Aínda que son máis raros que os compostos orgánicos non haloxenados, moitos compostos organoclorados foron illados de fontes naturais que van desde as bacterias ata os humanos.[3][4] Os compostos orgánicos clorados encóntranse en case todas as clases de biomoléculas, incluíndo alcaloides, terpenos, aminoácidos, flavonoides, esteroides, e ácidos graxos.[3][5] Os organoclorados, incluíndo as dioxinas, prodúcense en ambientes de alta temperatura como os incendios forestais. As dioxinas encontráronse en cinzas conservadas de incendios provocados por lóstregos anteriores á produción de dioxinas sintéticas.[6] Ademais, moitos hidrocarburos clorados simples como o diclorometano, cloroformo, e tetracloruro de carbono illáronse a partir de algas mariñas.[7] A maior parte do clorometano presente no medio ambiente prodúcese de forma natural por descomposición de restos biolóxicos, incendios forestais e volcáns.[8] O organoclorado natural epibatidina, un alcaloide illado de ras arborícolas, ten un potente efecto analxésico e estimulou a investigación de novos medicamentos para a dor.
Preparación[editar | editar a fonte]
A partir de cloro[editar | editar a fonte]
Os alcanos e arilalcanos poden ser tratados con cloro en condicións libres de radicais, con luz UV. Porén, o grao de cloración é difícil de controlar. Os cloruros de arilo poden ser preparados por haloxenación de Friedel-Crafts, usando cloro e un ácido de Lewis coma catalizador.
A reacción do haloformo, usando cloro e hidróxido de sodio, tamén pode xerar haloxenuros de alquilo a partir de metilcetonas e compostos relacionados. O cloroformo fabricouse antigamente desta maneira.
O cloro sofre reaccións de adición aos enlaces múltiples como en alquenos, alquinos e outros, dando compostos di, tri ou tetra-clorados.
Reacción con cloruro de hidróxeno[editar | editar a fonte]
Os alquenos reaccionan co cloruro de hidróxeno (HCl) para dar cloruros de alquilo. Por exemplo, a produción industrial de cloroetano procede da reacción do etileno con HCl:
- H2C=CH2 + HCl → CH3CH2Cl
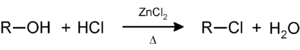
Os alcohois secundarios e terciarios reaccionan co reactivo de Lucas (cloruro de cinc) en ácido clorhídrico concentrado para obter o haluro de alquilo correspondente, polo que esta reacción serve como método para clasificar os alcohois:
Outros axentes de cloración[editar | editar a fonte]
No laboratorio, os cloruros de alquilo son máis fáciles de preparar por reacción de alcohois con cloruro de tionilo (SOCl2), tricloruro de fósforo (PCl3), ou pentacloruro de fósforo (PCl5):
- ROH + SOCl2 → RCl + SO2 + HCl
- 3 ROH + PCl3 → 3 RCl + H3PO3
- ROH + PCl5 → RCl + POCl3
No laboratorio, o uso de cloruro de tionilo é moi conveniente, xa que os subprodutos son gasosos.
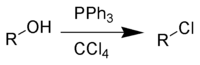
Unha alternativa é a reacción de Appel:
Reaccións[editar | editar a fonte]
Os cloruros de alquilo funcionan como bloques de construción moi versátiles en química orgánica. Aínda que os bromuros e ioduros de alquilo son máis reactivos, os cloruros de alquilo tenden a ser máis baratos e doados de obter. Os cloruros de alquilo experimentan facilmente o ataque de nucleófilos.
- Quentando haloxenuros de alquilo con hidróxido de sodio ou auga obtéñense alcohois.
- As reaccións con alcóxidos ou aróxidos producen éteres na síntese de éteres de Williamson
- A reacción con tioles da tioéteres.
- Os cloruros de alquilo reaccionan facilmente con aminas para dar aminas substituídas.
- Os cloruros de alquilo son substituídos por outros haluros máis suaves como o ioduro na reacción de Finkelstein.
- A reacción con outros pseudohaluros, como as azidas, cianuros e tiocianatos tamén son posibles.
- En presenza dunha base forte, os cloruros de alquilo sofren deshidrohaloxenación para dar alquenos ou alquinos.
- Os cloruros de alquilo reaccionan con magnesio para dar reactivos de Grignard, transformando un composto electrofílico nun composto nucleófilo.
- A reacción de Wurtz acopla redutivamente os radicais de dous haloxenuros de alquilo para que se acoplen ao sodio.
Aplicacións[editar | editar a fonte]
Cloruro de vinilo[editar | editar a fonte]
A maior aplicación dos organoclorados en química é a produción de cloruro de vinilo. A produción anual en 1985 foi de arredor de 18 millóns de toneladas e en 2005 xa pasara a máis de 32 millóns de toneladas,[9] e case todo se converteu en cloruro de polivinilo (PVC).[10]
Clorometanos[editar | editar a fonte]
A maioría dos hidrocarburos clorados de baixo peso molecular como o cloroformo, diclorometano, dicloroeteno e tricloroetano son disolventes moi útiles. Estes disolventes tenden a ser relativamente non polares, polo que son inmiscibles en auga e eficaces en aplicacións de limpeza, tales como desengraxado e limpeza en seco. Anualmente prodúcense varios miles de millóns de quilogramos de clorometanos, principalmente por medio da cloración do metano:
- CH4 + x Cl2 → CH4-xClx + x HCl
O máis importante é o diclorometano, que se utiliza principalmente como disolvente. O clorometano é un precursor dos clorosilanos e as siliconas. De importancia histórica, pero a menor escala hoxe en día, temos o cloroformo, usado sobre todo como precursor do clorodifluorometano (CHClF2) e do tetrafluoroeteno que se utiliza na fabricación de Teflón.[11]
Pesticidas[editar | editar a fonte]
Moitos pesticidas conteñen cloro. Algúns exemplos notables son: DDT, dicofol, heptacloro, endosulfán, clordano, aldrina, dieldrina, endrina, mirex e pentaclorofenol. Estes poden ser hidrofílicos ou hidrofóbicos en función da súa estrutura molecular. Moitos destes axentes foron prohibidos en varios países, por exemplo, mirex e aldrin.[12]
Illantes[editar | editar a fonte]
Os bifenilos policlorados (PCB), foron no seu momento de uso común como illantes eléctricos e axentes de transferencia de calor. O seu uso en xeral foi eliminado debido a problemas de saúde. Os PCB foron substituídos polos éteres de difenilo polibromados (PBDE), que posúen unha toxicidade e problemas de bioacumulación similares.
Toxicidade[editar | editar a fonte]
Algúns tipos de compostos organoclorados teñen unha toxicidade significativa en plantas ou animais, incluíndo os seres humanos. As dioxinas prodúcense cando a materia orgánica se queima en presenza de cloro, e algúns insecticidas como o DDT son contaminantes orgánicos persistentes (COP), que supoñen un perigo cando se liberan no medio ambiente. Por exemplo, o DDT, que foi amplamente usado para controlar pragas de insectos a mediados do século XX, tamén se acumula nas cadeas tróficas, e causa problemas reprodutivos (como adelgazamiento da casca de ovo) en determinadas especies de aves.[13]
Cando os disolventes clorados, por exemplo, o tetracloruro de carbono, non se eliminan correctamente, acumúlanse nas augas subterráneas. Algúns compostos organoclorados moi reactivos como o fosxeno foron utilizados como axentes de guerra química.
Porén, a presenza de cloro nun composto orgánico non garante a súa toxicidade. Moitos organoclorados son dabondo seguros como para o seu consumo en alimentos e medicinas. Por exemplo, os chícharos e os feixóns conteñen hormonas naturais vexetais cloradas ácido 4-cloroindol-3-acético (4-Cl-IAA);[14][15] e o edulcorante sucralosa (Splenda) é amplamente utilizado en produtos dietéticos. En 2004, había polo menos 165 compostos organoclorados aprobados no mundo para o seu uso como fármacos, entre eles o antibiótico natural vancomicina, o antihistamínico loratadina (Claritin), o antidepresivo sertralina (Zoloft), os antiepilépticos lamotrigina (Lamictal), e o anestésico por inhalación isoflurano.[16]
Rachel Carson deu a coñecer á opinión pública o problema da toxicidade do pesticida DDT coa publicación do seu libro de 1962 Silent spring (Primavera silenciosa). Aínda que moitos países eliminaron o uso dalgúns tipos de compostos organoclorados, como o DDT, que foi prohibido nos Estados Unidos, aínda se segue encontrando DDT persistente, PCBs e outros residuos de organoclorados nos seres humanos e mamíferos en todo o planeta moitos anos despois de que a súa produción e uso foran limitadas legalmente. En zonas do Ártico, os mamíferos mariños presentan altos niveis destes compostos. Estas substancias químicas concéntranse nos mamíferos, e mesmo se encontran no leite materno humano. Os machos destas especies adoitan ter niveis moito máis elevados, porque as femias reducen a súa concentración ao transferiren unha parte á súa descendencia durante a lactación.[17]
Notas[editar | editar a fonte]
- ↑ Contaminantes orgánicos persistentes (COP's). Tratamiento y valorización energética de residuos. Xavier Elías Castells. Fundación Universitaria Iberoamericana. Ediciones Díaz de Santos, 2005. ISBN 8479786949. Pág. 264
- ↑ Plaguicidas organoclorados. José Antonio Arias Verdes, Organización Mundial da Saúde, 1990. ISBN 9275370354
- ↑ 3,0 3,1 Gordon W. Gribble (1998). "Naturally Occurring Organohalogen Compounds". Acc. Chem. Res. 31 (3): 141–152. doi:10.1021/ar9701777.
- ↑ Gordon W. Gribble (1999). "The diversity of naturally occurring organobromine compounds". Chemical Society Reviews 28 (5): 335. doi:10.1039/a900201d.
- ↑ Kjeld C. Engvild (1986). "Chlorine-Containing Natural Compounds in Higher Plants". Phytochemistry 25 (4): 7891–791.
- ↑ Gribble, G.W. (1994). "The Natural production of chlorinated compounds". Environmental Science and Technology 28 (7): 310A–319A. doi:10.1021/es00056a001.
- ↑ Gribble, G. W. (1996). "Naturally occurring organohalogen compounds - A comprehensive survey". Progress in the Chemistry of Organic Natural Products 68 (10): 1–423. PMID 8795309. doi:10.1021/np50088a001.
- ↑ Public Health Statement - Chloromethane, Centers for Disease Control, Agency for Toxic Substances and Disease Registry
- ↑ What Is a Chlorinated Solvent?. Wisegeek.com
- ↑ Vinyl Chloride Monomer (VCM) Production and Manufacturing Process. Arquivado 17 de setembro de 2011 en Wayback Machine. Icis.com
- ↑ M. Rossberg et al. “Chlorinated Hydrocarbons” in Ullmann’s Encyclopedia of Industrial Chemistry 2006, Wiley-VCH, Weinheim. doi 10.1002/14356007.a06_233.pub2
- ↑ Robert L. Metcalf “Insect Control” in Ullmann’s Encyclopedia of Industrial Chemistry” Wiley-VCH, Wienheim, 2002. doi 10.1002/14356007.a14_263
- ↑ Connell, D.; et al. (1999). Introduction to Ecotoxicology. Blackwell Science. p. 68. ISBN 0-632-03852-7.
- ↑ Pless, Tanja; Boettger, Michael; Hedden, Peter; Graebe, Jan (1984). "Occurrence of 4-Cl-indoleacetic acid in broad beans and correlation of its levels with seed development". Plant Physiology 74 (2): 320–3. PMC 1066676. PMID 16663416. doi:10.1104/pp.74.2.320.
- ↑ Magnus, Volker; Ozga, Jocelyn A; Reinecke, Dennis M; Pierson, Gerald L; Larue, Thomas A; Cohen, Jerry D; Brenner, Mark L (1997). "4-chloroindole-3-acetic and indole-3-acetic acids in Pisum sativum". Phytochemistry 46 (4): 675–681. doi:10.1016/S0031-9422(97)00229-X.
- ↑ MDL Drug Data Report (MDDR), Elsevier MDL, versión 2004.2
- ↑ Marine Mammal Medicine, 2001, Dierauf & Gulland.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
| Wikimedia Commons ten máis contidos multimedia na categoría: Organoclorado |
- Organoclorados
- "Formation of Chlorinated Hydrocarbons in Weathering Plant Material". Artigo na web do SLAC (en inglés)
- "The oxidation of chlorinated hydrocarbons" Artigo de The Institute for Green Oxidation Chemistry no sitio web da Universidade Carnegie Mellon (en inglés)