Neuropéptido Y
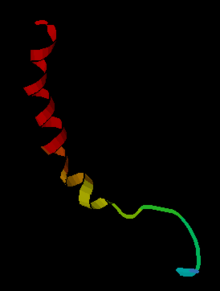
O neuropéptido Y (NPY) é un péptido de 36 aminoácidos, que funciona como neurotransmisor no cerebro e no sistema nervioso autónomo. Regula o uso de enerxía, e está implicado nos procesos de aprendizaxe, memoria e epilepsia.[1] O principal efecto do seu aumento de nivel/actividade é elevar a inxestión de alimentos e diminuír a actividade física. O neuropéptido Y é segregado polas neuronas do hipotálamo, e, ademais de incrementar o consumo de comida, incrementa a proporción de enerxía almacenada como graxa e bloquea os sinais nociceptivos (da dor) do cerebro.[2] O neuropéptido Y tamén aumenta os efectos vasoconstritores das neuronas noradrenérxicas. Está codificado nun xene do cromosoma 7 humano.
Descubrimento
[editar | editar a fonte]O neuropéptido Y foi descuberto no hipotálamo do porco en 1982, e investigáronse as súas implicacións nas funcións mediadas polo hipotálamo. Entre estes estudos, un realizado en 1983 por Allen et al.[3] descubriu a localización dos terminais axónicos NPYérxicos (lugar de liberación), que estaban situados no núcleo paraventricular do hipotálamo. Ademais, Allen et al. descubriron que os niveis maiores de inmunorreactividade ao NPY se encontraban no núcleo paraventricular do hipotálamo.[3]
Seis anos máis tarde, en 1989, Morris et al. procuraron os núcleos de produción de neuropéptido Y no cerebro, e por hibridación in situ atoparon os maiores niveis de ARNm de neuropéptido Y no núcleo arqueado do hipotálamo (lugar de produción).[4]
Porén, só dous anos antes, en 1987, Haas & George realizaron un estudo inxectando neuropéptido Y localmente no núcleo paraventricular da rata e descubriron que se producía unha liberación aguda de hormona liberadora da corticotropina (CRH), o que probaba que a actividade NPYérxica estimulaba directamente a liberación e a síntese de CRH,[5] unha hormona implicada no estrés e trastornos de alimentación como a obesidade.[6] Estes traballos marcaron o inicio do estudo do papel do neuropéptido Y na orexixénese ou inxesta de alimentos.
Papel do neuropéptido Y na inxestión de comida
[editar | editar a fonte]Ensaios de comportamento en estudos orexixénicos en ratas, feitos por medio de inmunoensaios e hibridación in situ confirmaron que a elevación da actividade NPYérxica incrementaba o consumo de comida. Nestes estudos, inxectábanse o neuropéptido Y exóxeno,[7] a dexametasona (un agonista do neuropéptido Y) [8] ou o N-acetil[Leu 28, Leu31]NPY (24-36)[9] no terceiro ventrículo encefálico [7] ou no hipotálamo cunha cánula.[8][10]
Ademais, estes estudos demostraron que a estimulación da actividade NPYérxica por medio da administración de certos agonistas do neuropéptido Y incrementa o consumo de comida nas ratas. Os efectos da actividade NPYérxica no consumo de comida tamén se demostran polo bloqueo de certos receptores do NPY (receptores Y1 e Y5), os cales, como se agardaba, inhibían a actividade NPYérxica, e facían decrecer o consumo de comida. Porén, un estudo de 1999 de King et al. demostrou os efectos da activación do autorreceptor Y2 do NPY, que inhiben a liberación de neuropéptido Y e dese xeito regulan o consumo de alimentos.[11] Neste estudo administrouse localmente no núcleo arqueado un antagonista do Y2 moi selectivo, o BIIE0246. Os datos dos radioinmunoensaios, despois da inxección do BIIE0246, mostran un incremento significativo na liberación do neuropéptido Y comparado co grupo de control. Aínda que a vida media farmacolóxica do neuropéptido Y exóxeno, e doutros agonistas e antagonistas aínda non está claro, os efectos non son moi duradeiros e o corpo da rata ten unha excelente capacidade de regular e normalizar os niveis anormais de neuropéptido Y e do consumo de comida.[7]
Papel do neuropéptido Y na obesidade
[editar | editar a fonte]Dryden et al. realizaron un estudo en 1995 utilizando ratas xeneticamente obesas para demostrar o papel do neuropéptido Y nos trastornos de alimentación como a obesidade. O estudo revelou catro factores subxacentes que contribuían á obesidade nas ratas: (1) un incremento nas concentracións de glicocorticosteroides no plasma; (2) insensibilidade ou resistencia á insulina; (3) mutación do receptor da leptina; e (4) un incremento no ARNm do neuropéptido Y e a liberación de neuropéptido Y.[12] Ademais, estes factores correlaciónanse uns con outros. O niveis elevados continuados de glicocorticosteroides estimulan a gliconeoxénese, que á súa vez causa un incremento da glicosa sanguínea que activa a liberación de insulina para regular os niveis de glicosa causando a súa recaptación e almacenamento como glicóxeno en varios tecidos do corpo. No caso da obesidade, a resistencia á insulina evita que se regulen os niveis altos de glicosa no sangue, que dan lugar a niveis mórbidos de glicosa e a diabetes mellitus.[13] Ademais, os niveis altos de glicocorticosteroides causan un incremento de neuropéptido Y pola activación directa dos receptores de glicocorticosteroides tipo II (que son activados só por niveis relativamente altos de glicocorticosteroides) e, indirectamente, pola eliminación da retroalimentación negativa do factor liberador de corticotropina (CRF) na síntese e liberación do neuropéptido Y. Mentres, a resistencia á insulina inducida pola obesidade e a mutación do receptor da leptina (ObRb) orixina a eliminación da inhibición da actividade NPYérxica e finalmente o consumo de alimento por medio doutros mecanismos de retroalimentación negativa para regulalos. Ademais, a obesidade nas ratas reducíase significativamente practicándolles unha adrenalectomía [14] ou unha hipofisectomía.[15]
Papel do neuropéptido Y na anorexia nerviosa
[editar | editar a fonte]Kaye et al. realizaron un estudo en 1990 para demostrar o papel do neuropéptido Y na anorexia nerviosa. Tratábase dun estudo post mortem no que se atoparon altos niveis de neuropéptido Y no líquido cefalorraquídeo de pacientes de anorexia nerviosa. Posteriormente, tamén se encontraron altas concentracións de hormona adrenocorticotropa (ACTH) e cortisol no plasma en pacientes de anorexia nerviosa.[16] Outros estudos realizados sete anos despois revelaron que os niveis baixos de leptina, a hormona que inhibe a liberación de neuropéptido Y a niveis relativamente altos, correlacionábanse con niveis extremadamente baixos de adipocitos neses pacientes; o que indicaba a natureza anorexixénica da leptina.[17] Ademais, mentres que os niveis altos de neuropéptido Y incrementaban o consumo de alimentos ou da fame en pacientes de anorexia nerviosa, a incomodidade emocional asociada coa comida pode explicar a resistencia aos efectos orexixénicos do neuropéptido Y, o que suxire unha forte influencia do sistema límbico sobre a inxesta de comida en trastornos de alimentación como a anorexia e a bulimia.[16]
Correlación co estrés e a dieta
[editar | editar a fonte]Estudos feitos en ratos e monos mostran que o estrés continuado e dietas ricas en graxas e azucres estimulan a liberación do neuropéptido Y, causando que se acumulen graxas no abdome. Os investigadores cren que manipulando os niveis desta substancia, poderían facer que as graxas se disolvesen nas zonas onde non se desexan e que se acumulasen nos sitios onde se necesitan.[18][19]
Os altos niveis de neuropéptido Y poden estar asociados con resiliencia (capacidade de soportar o estrés) e a recuperación do estrés postraumático [20] e co amortecemento da resposta ao medo, o que permite ás persoas desenvoverse mellor baixo un estrés extremo.[21]
Receptores
[editar | editar a fonte]A proteína receptora na que se une o neuropéptido Y é un receptor acoplado á proteína G da familia GRCR similar á rodopsina. Estes receptores son metabotrópicos, causando cambios metabólicos na célula diana en vez de abrir directamente canais iónicos. A proteína contén sete dominios que se estenden na membrana e foron identificados cinco subtipos nos mamíferos, catro dos cales son funcionais nos humanos.[22] Os subtipos Y1 e Y5 teñen papeis na estimulación da alimentación, entanto que o Y2 e Y4 parecen ter papeis na inhibición do apetito (saciedade). Algúns destes receptores están entre os receptores de neuropéptidos máis conservados.
Notas
[editar | editar a fonte]- ↑ Colmers WF, El Bahn B (2003). "Neuropeptide Y and Epilepsy". Epilepsy Currents/American Epilepsy Society 2 (3): 53–8. PMC 321170. PMID 15309085. doi:10.1046/j.1535-7597.2003.03208.x.
- ↑ Kimball JW (May 2008-05-02). "Neuropeptide Y (NPY)". Kimball's Biology Pages: Hormones of the Gut. Arquivado dende o orixinal o 05 de febreiro de 2011. Consultado o 12 de agosto de 2012.
- ↑ 3,0 3,1 Allen, YS; Adrian TE, Allen JM, Tatemoto K, Crow TJ, Bloom SR, Polak JM. (1983). "Neuropeptide Y distribution in the rat brain". Science 221 (4613): 877–879. PMID 6136091. doi:10.1126/science.6136091.
- ↑ Morris, BJ. (1989). "Neuronal localisation of neuropeptide Y gene expression in the rat brain". J Comp Neurol 290 (3): 358–368. PMID 2592617. doi:10.1002/cne.902900305.
- ↑ Haas, DA; George SR. (1989). "Neuropeptide Y-induced effects on hypothalamic corticotropin-releasing factor content and release are dependent on noradrenergic/adrenergic neurotransmission". Brain Research 498 (2): 333–338. PMID 2551461. doi:10.1016/0006-8993(89)91112-8.
- ↑ Edwardson, JA; Hough CA. (1975). "The pituitary-adrenal system of the genetically obese (ob/ob) mouse". J Endocrinol 65 (1): 99–107. PMID 167093. doi:10.1677/joe.0.0650099.
- ↑ 7,0 7,1 7,2 Hanson ES, Dallman MF (1995). "Neuropeptide Y (NPY) may integrate responses of hypothalamic feeding systems and the hypothalamo-pituitary-adrenal axis". J. Neuroendocrinol. 7 (4): 273–9. PMID 7647769. doi:10.1111/j.1365-2826.1995.tb00757.x.
- ↑ 8,0 8,1 White, B. D.; Dean, R. G.; Edwards, G. L.; Martin, R. J. (maio de 1994). "Type II corticosteroid receptor stimulation increases NPY gene expression in basomedial hypothalamus of rats". American Journal of Physiology-Regulatory, Integrative and Comparative Physiology (en inglés) 266 (5): R1523–R1529. ISSN 0363-6119. doi:10.1152/ajpregu.1994.266.5.R1523.
- ↑ King PJ, Widdowson PS, Doods HN, Williams G (1999). "Regulation of neuropeptide Y release by neuropeptide Y receptor ligands and calcium channel antagonists in hypothalamic slices". J. Neurochem. 73 (2): 641–6. PMID 10428060. doi:10.1046/j.1471-4159.1999.0730641.x.
- ↑ Pomonis JD, Levine AS, Billington CJ (1 July 1997). "Interaction of the hypothalamic paraventricular nucleus and central nucleus of the amygdala in naloxone blockade of neuropeptide Y-induced feeding revealed by c-fos expression". J. Neurosci. 17 (13): 5175–82. PMID 9185555.
- ↑ King PJ, Williams G, Doods H, Widdowson PS (2000). "Effect of a selective neuropeptide Y Y(2) receptor antagonist, BIIE0246 on neuropeptide Y release". Eur. J. Pharmacol. 396 (1): R1–3. PMID 10822055. doi:10.1016/S0014-2999(00)00230-2.
- ↑ Dryden S, Pickavance L, Frankish HM, Williams G (1995). "Increased neuropeptide Y secretion in the hypothalamic paraventricular nucleus of obese (fa/fa) Zucker rats". Brain Res. 690 (2): 185–8. PMID 8535835. doi:10.1016/0006-8993(95)00628-4.
- ↑ Wilcox G (2005). "Insulin and insulin resistance". Clin Biochem Rev 26 (2): 19–39. PMC 1204764. PMID 16278749.
- ↑ Yukimura Y, Bray GA (1978). "Effects of adrenalectomy on body weight and the size and number of fat cells in the Zucker (fatty) rat". Endocr Res Commun 5 (3): 189–98. PMID 747998. doi:10.1080/07435807809083752.
- ↑ Powley TL, Morton SA (1 April 1976). "Hypophysectomy and regulation of body weight in the genetically obese Zucker rat". Am. J. Physiol. 230 (4): 982–7. PMID 1267030. Arquivado dende o orixinal o 10 de febreiro de 2009. Consultado o 12 de agosto de 2012.
- ↑ 16,0 16,1 Kaye WH, Berrettini W, Gwirtsman H, George DT (1990). "Altered cerebrospinal fluid neuropeptide Y and peptide YY immunoreactivity in anorexia and bulimia nervosa". Arch. Gen. Psychiatry 47 (6): 548–56. PMID 2350207.
- ↑ Rohner-Jeanrenaud E, Jeanrenaud B (1997). "Central nervous system and body weight regulation". Ann. Endocrinol. (Paris) 58 (2): 137–42. PMID 9239233.
- ↑ Thomas H. Maugh II (July 2, 2007). "Research points to way to eliminate belly fat". Chicago Tribune. Consultado o 23 de abril de 2022.
- ↑ Kuo LE, Kitlinska JB, Tilan JU; et al. (2007). "Neuropeptide Y acts directly in the periphery on fat tissue and mediates stress-induced obesity and metabolic syndrome". Nat. Med. 13 (7): 803–11. PMID 17603492. doi:10.1038/nm1611.
- ↑ Yehuda, Rachel; Brand, Sarah; Yang, Ren-Kui (2006). "Plasma Neuropeptide Y Concentrations in Combat Exposed Veterans: Relationship to Trauma Exposure, Recovery from PTSD, and Coping". Biological Psychiatry 59 (7): 660–3. PMID 16325152. doi:10.1016/j.biopsych.2005.08.027.
- ↑ Julie Steenhuysen (February 16, 2009). "Research shows why some soldiers are cool under fire". Arquivado dende o orixinal o 19 de febreiro de 2009. Consultado o 12 de agosto de 2012.
- ↑ Michel MC, Beck-Sickinger A, Cox H, Doods HN, Herzog H, Larhammar D, Quirion R, Schwartz T, Westfall T (1998). "XVI. International Union of Pharmacology recommendations for the nomenclature of neuropeptide Y, peptide YY, and pancreatic polypeptide receptors". Pharmacological Reviews 50 (1): 143–50. PMID 9549761.
Véxase tamén
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- EMBL receptor database entry
- MeshName - Neuropeptide+Y|3=Neuropeptide Y [1]
