Estatina

As estatinas (ou inhibidores da HMG-CoA redutase) son unha clase de fármacos que rebaixan o nivel de colesterol no organismo e actúan inhibindo o encima HMG-CoA redutase, o cal ten un papel central na produción de colesterol. Os niveis altos de colesterol (hipercolesterolemia) foron asociados con enfermidades cardiovasculares.[1] As estatinas reducen a probabilidade de desenvolver unha enfermidade cardiovascular e a mortalidade nas persoas que están en risco. Hai fortes evidencias que indican que as estatinas son efectivas para o tratamento das enfermidades cardiovasculares nos estadios temperáns da doenza (prevención secundaria) e naquelas persoas con risco elevado pero aínda sen síntomas de doenza cardiovascular (prevención primaria).[2][3] Entre os efectos secundarios das estatinas están a dor muscular, o incremento do risco de ter diabetes mellitus, e as anormalidades nas probas de encimas hepáticos.[4] Ademais, en casos raros poden ter efectos adversos graves, especialmente danos musculares.[5]
En 2010, comercializábanse as seguintes estatinas: atorvastatina, fluvastatina, lovastatina, pitavastatina, pravastatina, rosuvastatina e simvastatina.[6] Todas elas están recoñecidas pola Axencia Europea de Medicamentos da Unión Europea e a FDA norteamericana. A cerivastatina foi retirada do mercado polo seu fabricante en 2001. Tamén se dispón de varias preparacións combinadas de estatinas e outros axentes, como ezetimibe/simvastatina. As estatinas son uns medicamentos moi vendidos; por exemplo, en 2005 e só nos Estados Unidos as vendas foron de 18,7 miles de millóns de dólares.[7] A estatina máis vendida é a atorvastatina, que en 2003 chegou a ser o fármaco máis vendido da historia.[8][9] Como algunhas das patentes xa expiraron, hoxe hai varias estatinas dispoñibles como xenéricos a un prezo menor.[10][11]
Uso en medicina
[editar | editar a fonte]Antes de tomar estatinas as recomendacións clínicas prácticas indican xeralmente que se debe intentar modificar o estilo de vida, o que inclúe seguir unha dieta que reduza o colesterol e facer exercicio físico. As estatinas e outros fármacos poden serlles recomendados ás persoas que non conseguen rebaixar o seu nivel de lípidos aos niveis axeitados facendo dietas e cambiando o estilo de vida.[12][13] As estatinas parecen funcionar igual de ben en homes que en mulleres.[14]
Prevención primaria
[editar | editar a fonte]A maioría das evidencias obtidas suxiren que as estatinas son efectivas para a prevención de doenzas cardíacas en persoas con hipercolesterolemia, pero que non teñen unha historia clínica de doenza cardíaca. Unha revisión Cochrane de 2013 encontrou un decrecemento no risco de morte e doutros malos resultados para a saúde sen que se atopasen evidencias de danos co uso de estatinas.[3][7] Outra "revisión" de 2011 chegara a conclusións similares.[15] E unha "revisión" de 2012 encontrou que eran beneficiosas tanto en homes coma en mulleres.[16] Porén, unha revisión de 2010 concluíra que o tratamento de persoas sen historia clínica de doenza cardiovascular reduce os episodios cardiovasculares en homes pero non en mulleres, e non proporciona ningún beneficio en canto á mortalidade en ningún dos sexos.[17] Outras dúas metaanálises publicadas ese ano, unha das cales usou datos obtidos exclusivamente de mulleres, non encontrou que houbese beneficios en canto á mortalidade na prevención primaria.[18][19]
A Sociedade Europea de Cardioloxía e a Sociedade da Aterosclerose Europea recomendan o uso das estatinas para a prevención primaria, dependendo da liña de referencia estimada do cómputo cardiovascular e os limiares dos niveis de LDL.[20] O National Institute for Health and Clinical Excellence (NICE) dos Estados Unidos recomenda o tratamento con estatinas de adultos cun risco estimado en 10 anos de desnvolver doenzas cardiovasculares que sexa maior do 10%.[21] As directrices do American College of Cardiology e a American Heart Association recomendan o tratamento con estatinas para a prevención primaria de doenzas cardiovasculares en adultos con colesterol LDL > 190 mg/dL.[22] Porén, hai críticos como Steven E. Nissen que dicen que as directrices da AHA/ACC non foron validadas debidamente, sobreestiman o risco polo menos nun 50%, e recomendan as estatinas a pacientes que non se beneficiarán delas, baseándose en poboacións cuxo risco observado é menor do predito polas directrices.[23]
Prevención secundaria
[editar | editar a fonte]As estatinas son efectivas para reducir a mortalidade de persoas con doenza cardiovascular preexistente. Actualmente tamén se recomendan en pacientes con alto risco de desenvolver doenzas cardíacas.[24] Como media, as estatinas poden rebaixar o colesterol LDL en 1,8 mmol/l (70 mg/dl), o que se traduce nunha diminución estimada do 60% no número de episodios cardíacos (ataques ao corazón, morte cardíaca súbita) e unha redución do 17% do risco de accidente cerebrovascular despois dun tratamento a longo prazo.[25] Teñen menos efecto que os fibratos ou a niacina á hora de reducir os triglicéridos e elevar o colesterol HDL ("colesterol bo").
As estatinas foron estudadas para mellorar o resultado de operacións en cirurxía cardíaca e vascular.[26] A mortalidade e os episodios adversos cardiovasculares reducíronse nos grupos que recibiron estatinas.[27]
Efectividade comparativa
[editar | editar a fonte]Aínda que non existen comparacións directas, todas as estatinas parecen efectivas sen ter en conta a potencia ou grao de redución do colesterol.[28] Porén, parece haber algunhas diferenzas entre elas, e a simvastatina e a pravastatina parecen superiores en canto aos menores efectos secundarios que producen.[4]
Unha comparación entre a atorvastatina, pravastatina e simvastatina baseada na súa efectividade comparadas con placebos, atopou que ás doses prescritas non había diferenzas estatisticamente significativas entre elas na redución da morbilidade e mortalidade cardiovascular.[29]
En nenos
[editar | editar a fonte]En nenos as estatinas son efectivas na redución dos niveis de colesterol en persoas con hipercolesterolemia familiar.[30] Porén, a súa seguridade a longo prazo non está clara.[30][31] Algúns recomendan que se o cambio no estilo de vida non é dabondo para producir cambios nos niveis de colesterol, a administración de estatina debería empezar aos 8 anos de idade.[32]
Hipercolesterolemia familiar
[editar | editar a fonte]As estatinas poden ser menos efectivas na redución do colesterol LDL en persoas con hipercolesterolemia familiar, especialmente os que teñen deficiencias xenéticas en homocigose.[33] Estas persoas adoitan ter defectos ou ben nos xenes do receptor de LDL ou da apolipoproteína B, que son ambos responsables da retirada ou aclaramento das LDL do sangue.[34] As estatinas seguen sendo o tratamento de primeira liña para a hipercolesterolemia familiar,[33] aínda que poden ser necesarias outras medidas de redución do colesterol.[35] En persoas con deficiencias en homocigose, as estatinas poden tamén ser útiles, aínda que a altas doses e en combinación con outros medicamentos que reducen o colesterol.[36]
Prevención da nefropatía inducida polo medio de contraste
[editar | editar a fonte]Unha metaanálise recente de ensaios controlados aleatorizados encontrou que as estatinas podían reducir o risco de nefropatía inducida polo medio contraste nun 53% en persoas que sufriron intervencións de anxiografía coronaria/percutanea (nas que se usa un medio de contraste). O efecto era máis forte entre os que tiñan unha disfunción renal preexistente ou diabetes mellitus.[37]
Efectos secundarios
[editar | editar a fonte]| Elección dunha estatina para persoas con consideracións especiais[38] | |||
|---|---|---|---|
| Condición | Estatinas normalmente recomendadas | Explicación | |
| Receptores de transplante renal que toman ciclosporina | Pravastatina ou Fluvastatina | Son posibles interaccións entre os fármacos, pero os estudos realizados non mostraron que estas estatinas incrementen a exposición á ciclosporina.[39] | |
| Persoas VIH positivas que están tomando inhibidores da protease | Atorvastatina, Pravastatina ou Fluvastatina | As interaccións negativas son máis probables con outras estatinas[40] | |
| Persoas que están tomando gemfibrozil, un fármaco que rebaixa o colesterol e non é estatina | Atorvastatina | Combinar gemfibrozil e unha estatina incrementa o risco de rabdomiólise e subseguintemente insuficiencia renal[41][42] | |
| Persoas que están tomando o anticoagulante warfarina | Calquera estatina | O uso de estatinas pode requirir que se cambie a dose de warfarina, xa que algunhas estatinas incrementan o efecto da warfarina.[43] | |
Os efectos secundarios máis importantes son o incremento de concentración de encimas hepáticos, problemas musculares, e aumento do risco de diabete.[44][45] Outros posibles efectos adversos son a perda cognitiva, neuropatía, disfunción hepática e pancreática, e disfunción sexual.[46] A taxa á que ocorren ditos eventos foi moi debatida, en parte porque a razón risco/beneficio das estatinas en poboacións de baixo risco é moi dependente da taxa de episodios adversos.[47][48][49] Unha metaanálise de grupo Cochrane de ensaios clínicos con estatinas en prevención primaria non atopou probas de que se producira un exceso de episodios adversos entre as persoas tratadas con estatinas comparadas coas tratadas con placebo.[50] Outra metaanálise encontrou un incremento do 39% nos episodios adversos nas persoas tratadas con estatinas en relación coas que recibiron placebo, pero non houbo un incremento de episodios adversos graves.[51] O autor dun estudo argumentou que os episodios adversos son máis comúns na práctica clínica que en ensaios clínicos aleatorizados.[46] Unha revisión sistemática feita pola Canadian Working Group Consensus Conference que tivo en consideración metaanálises publicadas de ensaios clínicos, informes de episodios adversos espontáneos da FDA, e estudos de cohortes publicados chegou á conclusión de que aínda que as metaanálises clínicas subestimaban a taxa de dor muscular asociada co uso de estatinas, as taxas de rabdomiólise son aínda "tranquilizadoramente baixas" e similares ás observadas en ensaios clínicos (un 1-2 por 10.000 pacientes anos).[52] Unha revisión sistemática de Ben Goldacre e outros chegou á conclusión de que só unha pequena fracción dos efectos secundarios dos que se informou en pacientes que tomaban estatinas son realmente atribuíbles ás estatinas.[53]
Efectos cognitivos
[editar | editar a fonte]Hai informes anecdóticos de declives cognitivos producidos polas estatinas.[54] Unha revisión sistemática da Canadian Working Group Consensus Conference concluíu que as evidencias dispoñibles "non apoian fortemente un efecto adverso importante das estatinas".[55] Outra metaanálise chegou á conclusión de que hai evidencias de calidade moderada de que non producen ningún aumento da demencia, trastornos cognitivos leves ou nos resultados no rendemento cognitivo, aínda que a forza das evidencias é limitada, especialmente a altas doses.[56] En 2012, recoñecendo que houbera un incremento en informes anecdóticos e un aumento da preocupación pola relación das estatinas coa perda de memoria (incluíndo informes de amnesia global transitoria), os despistes e a confusión, a FDA engadiu á etiquetaxe esixida para as estatinas unha advertencia sobre posibles impactos cognitivos.[57] Os efectos descríbense como raros, non graves, e reversibles unha vez cesa o tratamento.[58]
Músculos
[editar | editar a fonte]En estudos observacionais do 10 ao 15% das persoas que tomaron estatinas experimentou problemas musculares, que na maioría dos casos consistían en dor muscular.[5] As taxas observadas, que son moito maiores que as vistas en ensaios clínicos aleatorizados,[52] foron obxecto dun amplo debate e discusión.
As reaccións raras observadas foron miopatías como a miosite (inflamación dos músculos) ou mesmo rabdomiólise (destrución das células musculares), que pode á súa vez dar lugar a un dano renal grave que pode ser mortal. O risco da rabdomiólise inducida por estatinas increméntase a idades vellas, co uso de medicacións interaccionantes como os fibratos, e co hipotiroidismo.[59] Os niveis de coencima Q10 (ubiquinona) diminúen ao tomar estatinas;[60] ás veces utilízanse suplementos de CoQ10 para tratar a miopatía asociada coas estatinas, aínda que non hai (en 2007) evidencias da súa eficacia.[61] O xene SLCO1B1 (Solute carrier organic anion transporter family member 1B1, membro 1B1 da familia do transportador de anións orgánicos transportador de solutos) codifica un polipéptido transportador de anións orgánicos que está implicado na regulación da absorción das estatinas. En 2008 atopouse que unha variación común deste xene incrementa significativamente o risco de miopatía.[62]
Graham et al. (2004) revisaron os rexistros duns 250.000 pacientes tratados dese 1998 a 2001 coas estatinas atorvastatina, cerivastatina, fluvastatina, lovastatina, pravastatina, e simvastatina.[63] Neles a incidencia de rabdomiólise era de 0,44 por 10.000 pacientes tratados con estatinas distintas da cerivastatina. Pero o risco era unhas 10 veces maior se se utilizaba a cerivastatina, ou se as estatinas estándar (atorvastatina, fluvastatina, lovastatina, pravastatina, ou simvastatina) eran combinadas cun tratamento con fibratos (fenofibrato ou gemfibrozil). A cerivastatina foi retirada do mercado polo seu fabricante en 2001 debido aos problemas que pode producir.
Todas as estatinas usadas comunmente mostran resultados bastante similares, pero as novas estatinas, caracterizadas por ter vidas medias farmacolóxicas máis longas e máis especificidade celular, espérase que teñan menos efectos adversos. Algúns investigadores suxeriron que as estatinas hidrofílicas, como a fluvastatina, rosuvastatina, e pravastatina, son menos tóxicas que as estatinas lipófilas, como a atorvastatina, lovastatina, e simvastatina, pero outrros estudos non atoparon conexión.[64] A lovastatina induce a expresión do xene FBXO32, que se cre é o responsable de promover os danos na fibra muscular.[64]
Diabetes
[editar | editar a fonte]As estatinas están asociadas cun lixeiro incremento do risco de ter diabete (do 2 ao 17% nunha revisión).[65] As doses máis altas teñen maior efecto, pero a diminución do risco de enfermidade cardiovascular compensa o risco de desenvolver diabete.[66]
Cancro
[editar | editar a fonte]Varias metaanálises non encontraron un incremento do risco de cancro ao tomar estatinas, pero outras atoparon un pequeno risco.[67][68][69][70][71]
As estatinas poden reducir o risco de cancro esofáxico,[72] cancro colorrectal,[73] cancro gástrico,[74][75] hepatocellular carcinoma,[76] e posiblemente de cancro de próstata.[77][78] Parece que non teñen efecto sobre o risco de ter cancro de pulmón,[79] cancro renal,[80] cancro de mama,[81] cancro pancreático,[82] ou cancro de vexiga.[83]
Interaccións con outros fármacos
[editar | editar a fonte]A combinación de calquera estatina cun fibrato ou niacina, que son fármacos doutro tipo que tamén reducen o colesterol, incrementa o risco de rabdomiólise a case 6,0 por 10.000 persoas-anos.[63] É especialmente prudente monitorizar os encimas hepáticos e a creatina quinase nos pacientes que toman altas doses de estatinas ou nos que toman combinacións estatinas/fibratos, e é obrigado facelo en caso de presentarse cambras musculares ou deterioración da función renal.
O consumo de pomelos ou de zume de pomelo inhibe o metabolismo de certas estatinas. As laranxas amargas poden ter un efecto similar.[84] As furanocoumarinas do zume de pomelo (é dicir bergamotina e dihidroxibergamotina) inhiben o encima citocromo P450 CYP3A4, que está implicado no metabolismo da maioría das estatinas (porén, é un inhibidor importante só da lovastatina, simvastatina, e en menor medida da atorvastatina) e algúns outros medicamentos[85] (crese que os responsables son os flavonoides, é dicir, a narinxina). Isto incrementa os niveis de estatinas, o que aumenta o risco de efectos adversos relacionados coa dose (como a miopatía/rabdomiólise). A prohibición absoluta do consumo de zume de pomelo para os que están tomando estatinas é discutido.[86]
Os inhibidores da protease e as estatinas tomados xuntos poden incrementar os niveis sanguíneos de estatinas e incrementar o risco de danos musculares (miopatía). A forma máis grave de miopatía, a rabdomiólise, pode danar os riles e orixinar insuficiencia renal, que pode ser mortal.[87]
Mecanismo de acción
[editar | editar a fonte]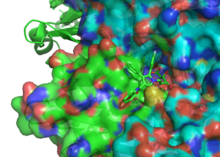
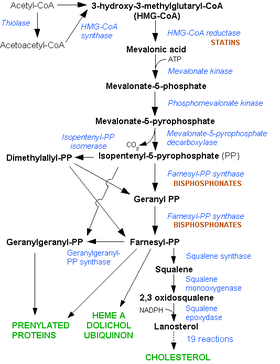
- Artigo principal: Colesterol.
As estatinas actúan inhibindo competitivamente o encima HMG-CoA redutase, o primeiro encima comprometido na vía do mevalonato, que converte o HMG-CoA en mevalonato. Como as estatinas son similares en estrutura ao HMG-CoA a nivel molecular, poden entrar no sitio activo do encima e competir co substrato nativo (HMG-CoA). Esta competición reduce a velocidade á que a HMG-CoA redutase produce mevalonato, que é a seguinte molécula da ruta que sintetiza o colesterol.
A reacción concreta inhibida é:
![]()
Os fungos Penicillium e Aspergillus producen varias estatinas naturais como metabolitos secundarios. Estas estatinas naturais probablemente funcionan no medio ambiente inhibindo os encimas HMG-CoA redutases noutras especies de bacterias e fungos que compiten coa especie que as produce.[89]
Inhibición da síntese de colesterol
[editar | editar a fonte]Ao inhibiren a HMG-CoA redutase, as estatinas bloquean a vía de síntese do colesterol no fígado. Isto é significativo porque a maioría do colesterol circulante ten oríxe endóxena (sintetízase dentro do corpo) en vez de proceder da dieta. Cando o fígado xa non pode producir colesterol, on niveis sanguíneos de colesterol baixan. A síntese de colesterol parece acontecer principalmente pola noite,[90] polo que as estatinas, que teñen unha vida media curta, adoitan tomarse pola noite para maximizar o seu efecto. Os estudos realizados indican reducións de LDL e de colesterol total maiores cando se toma a estatina de acción de curta duración simvastatina pola noita en vez de pola mañá,[91][92] pero non se observou diferenzas coa estatina de acción longa atorvastatina.[93]
Incremento da captación de LDL
[editar | editar a fonte]En experimentos con coellos demostrouse que os hepatocitos perciben os niveis reducidos de colesterol no fígado e tratan de compensalos sintetizando receptores de LDL para captar colesterol da circulación sanguínea.[94] Isto realízase por medio de proteases que clivan as proteínas que se unen ao elemento regulador de esterol unidas á membrana, as cales despois migran ao núcleo celular e únense aos elementos de resposta aos esterois. Seguidamente, os elementos de resposta aos esterois facilitan o incremento da transcrición doutras proteínas, principalmente o receptor de LDL. O recptor de LDL é transportado intracelularmente ata as membranas plasmáticas das células do fígado e alí únese a partículas circulantes de LDL e VLDL (informalmente chamadas "colesterol malo"), mediando a súa captación no fígado, onde o colesterol é reprocesado orixinando sales biliares e outros subprodutos. Os sales biliares segréganse ao duodeno durante a dixestión das graxas e despois reabsórbense no xexuno e íleo.
Decrecemento da prenilación de proteínas específicas
[editar | editar a fonte]As estatinas, ao inhibiren a vía da HMG CoA redutase, inhiben simultaneamente a produción de colesterol e tamén a prenilación de proteínas específicas. Este efecto inhibitorio sobre a prenilación de proteínas pode estar implicado, polo menos parcialmente, na mellora da función endotelial, a modulación da función inmunitaria, e noutros beneficios cardiovasculares pleiotrópicos das estatinas,[95][96][97][98][99][100] así como no feito de que outros fármacos que rebaixan o nivel de LDL non mostren nos estudos os mesmos beneficios sobre o risco cardiovascular que mostran as estatinas,[101] e pode tamén explicar certos beneficios observados na redución do cancro coas estatinas.[102] Ademais, o efecto inhibidor sobre a prenilación de proteínas pode tamén estar implicado en varios efectos secundarios non desexados asociados coas estatinas, incluíndo a dor muscular (miopatía)[103] e o nivel elevado de azucre no sangue (diabete).[104]
Outros efectos
[editar | editar a fonte]Como se indicou antes, as estatinas presentan accións que van alén da actividade de rebaixar os lípidos circulantes na prevención da aterosclerose. O ensaio ASTEROID mostrou evidencias ultrasónicas directas de regresión de ateromas durante a terapia con estatinas.[105] Os investigadores presentaron a hipótese de que as estatinas preveñen a enfermidade cardiovascular por medio de catro mecanismos que se propuxeron (todos os cales foron suxeitos de amplas investigaciós biomédicas), que son:[106]
- Mellora da función endotelial
- Modulación das respostas inflamatorias
- Mantemento da estabilidade das placas ateroscleróticas
- Prevención da formación de trombos
En 2008, o estudo JUPITER mostrou que se notaban beneficios naqueles pacientes que non tiñan unha historia clínica de colesterol alto ou enfermidade cardíaca, senón só de niveis elevados de proteína C reactiva.[107] Porén, as conclusións deste estudo foron polémicas.[108][109][110]
Formas dispoñibles
[editar | editar a fonte]As estatinas están divididas en dous grupos: as derivadas de fermentacións e as síntese. Na táboa inclúense os nomes comerciais, que poden variar dun país a outro:
| Estatina | Imaxe | Nome comercial | Obtención | Metabolismo[111] |
|---|---|---|---|---|
| Atorvastatina |  |
Lipitor, Torvast | Sintética | CYP3A4 |
| Cerivastatina |  |
Lipobay, Baycol (retirada do mercado en agosto de 2001 debido a risco de rabdomiólise grave) | Sintética | varias isoformas CYP3A[112] |
| Fluvastatina |  |
Lescol, Lescol XL | Sintética | CYP2C9 |
| Lovastatina |  |
Mevacor, Altocor, Altoprev | Este é un composto de orixe natural, que se obtén por fermentación. Encóntrase nos fungos Pleurotus ostreatus e no arroz de lévedo vermello. | CYP3A4 |
| Mevastatina |  |
Compactin | Composto de orixe natural que se encontra no arroz de lévedo vermello. | CYP3A4 |
| Pitavastatina |  |
Livalo, Pitava | Sintética | |
| Pravastatina | 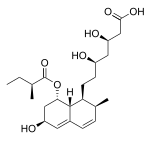 |
Pravachol, Selektine, Lipostat | Obtida por fermentación (produto de fermentación da bacteria Nocardia autotrophica). | Non CYP[113] |
| Rosuvastatina |  |
Crestor | Sintética | CYP2C9 e CYP2C19 |
| Simvastatina |  |
Zocor, Lipex | Obtida por fermentación. (é un derivado sintético dun produto de fermentación do fungo Aspergillus terreus.) | CYP3A4 |
| Simvastatina+Ezetimibe | Vytorin | Terapia de combinación | ||
| Lovastatina+Niacina de liberación prolongada | Advicor | Terapia de combinación | ||
| Atorvastatina+Amlodipine Besylate | Caduet | Terapia de combinación – Colesterol+Presión arterial | ||
| Simvastatina+Niacina de liberación prolongada | Simcor | Terapia de combinación |
A potencia para rebaixar o nivel de LDL varía entre os distintos axentes. A cerivastatina é a máis potente (pero foi retirada do mercado en 2001 polo seu risco de causar rabdomiólise grave), seguida (en orde de potencia decrecente) pola rosuvastatina, atorvastatina, simvastatina, lovastatina, pravastatina, e fluvastatina.[114] A potencia relativa da pitavastatina non se determinou.

Algúns tipos de estatinas aparecen de forma normal na natureza, e poden encontrarse en alimentos como o fungo Pleurotus ostreatus e o arroz de lévedo vermello. En ensaios clínicos controlados aleatorizados observouse que estes alimentos reducen o colesterol circulante, pero a calidade dos ensaios considérase baixa.[115] Debido á expiración dalgunhas patentes, a maioría das marcas de maior éxito de estatinas teñen xenéricos desde 2012, incluíndo a atorvastatina, que é o fármaco máis vendido.
| Doses equivalentes de estatina | ||||||
|---|---|---|---|---|---|---|
| % de redución de LDL (aprox.) | Atorvastatina | Fluvastatina | Lovastatina | Pravastatina | Rosuvastatina | Simvastatina |
| 10–20% | – | 20 mg | 10 mg | 10 mg | – | 5 mg |
| 20–30% | – | 40 mg | 20 mg | 20 mg | – | 10 mg |
| 30–40% | 10 mg | 80 mg | 40 mg | 40 mg | 5 mg | 20 mg |
| 40–45% | 20 mg | – | 80 mg | 80 mg | 5–10 mg | 40 mg |
| 46–50% | 40 mg | – | – | – | 10–20 mg | 80 mg* |
| 50–55% | 80 mg | – | – | – | 20 mg | – |
| 56–60% | – | – | – | – | 40 mg | – |
| * a dose de 80-mg xa non se recomenda debido ao incremento no risco de rabdomiólise | ||||||
| Dose de inicio | ||||||
| Dose de inicio | 10–20 mg | 20 mg | 10–20 mg | 40 mg | 10 mg; 5 mg se hai hipotiroidismo, >65 anos, Asia | 20 mg |
| Se se pretende unha maior redución de LDL | 40 mg se >45% | 40 mg se >25% | 20 mg se >20% | -- | 20 mg se LDL >190 mg/dL (4.87 mmol/L) | 40 mg se >45% |
| Momento óptimo | En calquera momento | Polo serán | Coas comidas do serán/ceas | En calquera momento | En calquera momento | Polo serán |
Historia
[editar | editar a fonte]En 1971, o bioquímico xaponés Akira Endo, que traballaba para a compañía farmacéutica Sankyo, empezou a buscar un fármaco que rebaixase os niveis de colesterol. As investigacións feitas daquela xa demostraran que o colesterol se fabricaba principalmente no corpo no fígado, utilizando o encima HMG-CoA redutase.[8] Endo e o seu equipo pensaron que certos microorganismos podían producir inhibidores deste encima para defenderse doutros organismos, xa que o mevalonato é un precursor de moitas substancias necesarias para o mantemento das paredes celulares de moitos organismos (ergosterol) ou do citoesqueleto (isoprenoides), polo que estudaron moitos organismos.[89] O primeiro axente que identificaron foi a mevastatina (ML-236B), molécula producida polo fungo Penicillium citrinum.
Un grupo británico illou o mesmo composto de Penicillium brevicompactum, e deulle o nome de compactina, e publicou o seu informe en 1976.[116] O grupo británico mencionou as propiedades antifúnxicas do produto, pero non fixo mención á inhibición da HMG-CoA redutase.
A mevastatina nunca foi comercializada debido aos seus efectos secundarios adversos sobre tumores, deterioración muscular, e ás veces a morte de cans de laboratorio. P. Roy Vagelos, científico xefe e posteriormente director executivo de Merck & Co, estaba interesado neste produto, e fixo varias viaxes ao Xapón desde 1975. En 1978, Merck illara a lovastatina (mevinolina, MK803) do fungo Aspergillus terreus, que se comercializou en 1987 como Mevacor.[8]
Xa se suxerira unha ligazón entre o colesterol e as doenzas cardiovasculares, que se chamou hipótese lipídica. O colesterol é o principal constituínte do ateroma, os nódulos de graxa que se forman nas paredes das arterias e que aparecen na aterosclerose e que, cando rompen, causan a gran maioría dos ataques ao corazón. O tratamento consistía principalmente en dietas, como as dietas baixas en graxas, e en medicinas mal toleradas polo organismo, como o clofibrato, colestiramina, e ácido nicotínico. O investigador do colesterol Daniel Steinberg escribiu que mentres que o Coronary Primary Prevention Trial de 1984 demostrara que a redución dos niveis de colesterol reducía significativamente o risco de ataques ao corazón e anxina de peito, os médicos, incluídos os cardiólogos, aínda estaban pouco convencidos.[117]
Para comercializar de forma efectiva as estatinas, Merck tivo que convencer á xente dos perigos de ter un nivel alto de colesterol, e aos doutores de que as estatinas eran seguras e prolongarían moitas vidas. Como resultado das campañas públicas, a xente nos Estados Unidos empezou a familiarizarse cos valores dos niveis normais de colesterol e a diferenza entre o colesterol "bo" e "malo", e compañías farmacéuticas rivais empezaron a producir as súas propias estatinas, como a pravastatina (Pravachol), fabricada por Sankyo e Bristol-Myers Squibb. En abril de 1994, anunciáronse os resultados dun estudo patrocinado por Merck, o Scandinavian Simvastatin Survival Study. Os investigadores probaron a simvastatina, posteriormente vendida por Merck como Zocor, en 4.444 pacientes con altos niveis de colesterol e enfermidades cardíacas. Cinco anos despois, o estudo concluíu que os pacientes mostraban unha redución do 35% no seu colesterol, e as súas posibilidades de morrer por un ataque ao corazón foran reducidas nun 42%.[8][118] En 1995, Zocor e Mevacor fixeron que Merck gañase uns mil millóns de dólares.[8] Endo foi premiado co Premio do Xapón de 2006, e co Premio de Investigación Médica Clínica Lasker-DeBakey en 2008 pola súa "investigación pioneira nunha nova clase de moléculas" para "baixar o colesterol".[119] Endo entrou no National Inventors Hall of Fame de Alexandria, Virxinia en 2012. Michael C. Brown e Joseph Goldstein, que gañaron o Premio Nobel por traballos relacionados co colesterol, dixéronlle a Endo: "Os millóns de persoas cuxas vidas serán prolongadas por medio da terapia con estatinas débeno todo a Akira Endo."[120]
Investigación
[editar | editar a fonte]Continúan as investigacións noutras áreas nas que estatinas específicas parecen ter efectos favorables, como a demencia,[121] cancro de pulmón,[122] cataratas,[123] hipertensión arterial,[124][125] e cancro de próstata.[126]
Notas
[editar | editar a fonte]- ↑ Lewington S, Whitlock G, Clarke R, Sherliker P, Emberson J, Halsey J, Qizilbash N, Peto R, Collins R (December 2007). "Blood cholesterol and vascular mortality by age, sex, and blood pressure: a meta-analysis of individual data from 61 prospective studies with 55,000 vascular deaths". Lancet 370 (9602): 1829–39. PMID 18061058. doi:10.1016/S0140-6736(07)61778-4.
- ↑ "Lipid Modification - National Library of Medicine - PubMed Health".
- ↑ 3,0 3,1 Taylor F, Huffman MD, Macedo AF, Moore TH, Burke M, Davey Smith G, Ward K, Ebrahim S (2013). "Statins for the primary prevention of cardiovascular disease". Cochrane Database Syst Rev 1: CD004816. PMID 23440795. doi:10.1002/14651858.CD004816.pub5. Arquivado dende o orixinal o 01 de marzo de 2016. Consultado o 23 de xaneiro de 2016.
- ↑ 4,0 4,1 Naci H, Brugts J, Ades T (2013). "Comparative tolerability and harms of individual statins: a study-level network meta-analysis of 246 955 participants from 135 randomized, controlled trials". Circ Cardiovasc Qual Outcomes 6 (4): 390–9. PMID 23838105. doi:10.1161/CIRCOUTCOMES.111.000071.
- ↑ 5,0 5,1 Abd TT, Jacobson TA (May 2011). "Statin-induced myopathy: a review and update.". Expert opinion on drug safety 10 (3): 373–87. PMID 21342078. doi:10.1517/14740338.2011.540568.
- ↑ Sweetman, Sean C., ed. (2009). "Cardiovascular drugs". Martindale: the complete drug reference (36th ed.). London: Pharmaceutical Press. pp. 1155–434. ISBN 978-0-85369-840-1.
- ↑ 7,0 7,1 Taylor, FC; Huffman, M; Ebrahim, S (11 December 2013). "Statin therapy for primary prevention of cardiovascular disease.". JAMA 310 (22): 2451–2. PMID 24276813. doi:10.1001/jama.2013.281348.
- ↑ 8,0 8,1 8,2 8,3 8,4 Simons, John. "The $10 billion pill", Fortune magazine, January 20, 2003.
- ↑ "Doing Things Differently" Arquivado 12 de maio de 2013 en Wayback Machine., Pfizer 2008 Annual Review, April 23, 2009, p. 15.
- ↑ "www.accessdata.fda.gov".
- ↑ "www.accessdata.fda.gov".
- ↑ National Cholesterol Education Program (2001). Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III): Executive Summary. Bethesda, MD: National Institutes of Health. National Heart, Lung, and Blood Institute. p. 40. NIH Publication No. 01-3670.
- ↑ National Collaborating Centre for Primary Care (2010). NICE clinical guideline 67: Lipid modification (PDF). London: National Institute for Health and Clinical Excellence. p. 38. Arquivado dende o orixinal (PDF) o 10 de outubro de 2010. Consultado o 23 de xaneiro de 2016.
- ↑ Cholesterol Treatment Trialists' (CTT), Collaboration; Fulcher, J; O'Connell, R; Voysey, M; Emberson, J; Blackwell, L; Mihaylova, B; Simes, J; Collins, R; Kirby, A; Colhoun, H; Braunwald, E; La Rosa, J; Pedersen, TR; Tonkin, A; Davis, B; Sleight, P; Franzosi, MG; Baigent, C; Keech, A (11 April 2015). "Efficacy and safety of LDL-lowering therapy among men and women: meta-analysis of individual data from 174,000 participants in 27 randomised trials.". Lancet (London, England) 385 (9976): 1397–405. PMID 25579834. doi:10.1016/s0140-6736(14)61368-4.
- ↑ Tonelli M, Lloyd A, Clement F, Conly J, Husereau D, Hemmelgarn B, Klarenbach S, McAlister FA, Wiebe N, Manns B (2011). "Efficacy of statins for primary prevention in people at low cardiovascular risk: a meta-analysis". CMAJ 183 (16): E1189–202. PMC 3216447. PMID 21989464. doi:10.1503/cmaj.101280.
- ↑ Kostis WJ, Cheng JQ, Dobrzynski JM, Cabrera J, Kostis JB (2012). "Meta-analysis of statin effects in women versus men". J. Am. Coll. Cardiol. 59 (6): 572–82. PMID 22300691. doi:10.1016/j.jacc.2011.09.067.
- ↑ Petretta M, Costanzo P, Perrone-Filardi P, Chiariello M (2010). "Impact of gender in primary prevention of coronary heart disease with statin therapy: a meta-analysis". Int. J. Cardiol. 138 (1): 25–31. PMID 18793814. doi:10.1016/j.ijcard.2008.08.001.
- ↑ Ray KK, Seshasai SR, Erqou S, Sever P, Jukema JW, Ford I, Sattar N (2010). "Statins and all-cause mortality in high-risk primary prevention: a meta-analysis of 11 randomized controlled trials involving 65,229 participants". Arch. Intern. Med. 170 (12): 1024–31. PMID 20585067. doi:10.1001/archinternmed.2010.182.
- ↑ Bukkapatnam RN, Gabler NB, Lewis WR (2010). "Statins for primary prevention of cardiovascular mortality in women: a systematic review and meta-analysis". Prev Cardiol 13 (2): 84–90. PMID 20377811. doi:10.1111/j.1751-7141.2009.00059.x.
- ↑ Grupo de Trabajo de la Sociedad Europea de Cardiología (ESC) y de la Sociedad Europea de Aterosclerosis, (EAS); Reiner, Z; Catapano, AL; De Backer, G; Graham, I; Taskinen, MR; Wiklund, O; Agewall, S; Alegría, E; John Chapman, M; Durrington, P; Erdine, S; Halcox, J; Hobbs, R; Kjekshus, J; Perrone Filardi, P; Riccardi, G; Storey, RF; Wood, D (Dec 2011). "ESC/EAS Guidelines for the management of dyslipidaemias." (PDF). Revista espanola de cardiologia (English ed.) 64 (12): 1168. PMID 24776417. doi:10.1016/j.rec.2011.09.015.
- ↑ "www.nice.org.uk".
- ↑ Stone, NJ; Robinson, J; Lichtenstein, AH; Merz, CN; Blum, CB; Eckel, RH; Goldberg, AC; Gordon, D; Levy, D; Lloyd-Jones, DM; McBride, P; Schwartz, JS; Shero, ST; Smith SC, Jr; Watson, K; Wilson, PW (Nov 12, 2013). "2013 ACC/AHA Guideline on the Treatment of Blood Cholesterol to Reduce Atherosclerotic Cardiovascular Risk in Adults: A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines.". Circulation 129 (25 Suppl 2): S1–S45. PMID 24222016. doi:10.1161/01.cir.0000437738.63853.7a.
- ↑ Steven E. Nissen (October 6, 2014). "Prevention Guidelines: Bad Process, Bad Outcome". JAMA Intern Med. 174: 1972. doi:10.1001/jamainternmed.2014.3278.
- ↑ National Institute for Health and Clinical Excellence (March 2010) [May 2008]. "Lipid modification – Cardiovascular risk assessment and the modification of blood lipids for the primary and secondary prevention of cardiovascular disease – Quick reference guide" (PDF). Arquivado dende o orixinal (PDF) o 08 de abril de 2011. Consultado o 2010-08-25.
- ↑ Law MR, Wald NJ, Rudnicka AR (June 2003). "Quantifying effect of statins on low density lipoprotein cholesterol, ischaemic heart disease, and stroke: systematic review and meta-analysis". BMJ 326 (7404): 1423. PMC 162260. PMID 12829554. doi:10.1136/bmj.326.7404.1423.
- ↑ de Waal BA, Buise MP, van Zundert AA (January 2015). "Perioperative statin therapy in patients at high risk for cardiovascular morbidity undergoing surgery: a review". Br J Anaesth 114 (1): 44–52. PMID 25186819. doi:10.1093/bja/aeu295.
- ↑ Antoniou GA, Hajibandeh S, Hajibandeh S, Vallabhaneni SR, Brennan JA, Torella F (December 2014). "Meta-analysis of the effects of statins on perioperative outcomes in vascular and endovascular surgery". J Vasc Surg. S0741-5214 (14): 01903–X. PMID 25498191. doi:10.1016/j.jvs.2014.10.021.
- ↑ Tonelli M, Lloyd A, Clement F, Conly J, Husereau D, Hemmelgarn B, Klarenbach S, McAlister FA, Wiebe N, Manns B (Nov 8, 2011). "Efficacy of statins for primary prevention in people at low cardiovascular risk: a meta-analysis". CMAJ : Canadian Medical Association 183 (16): E1189–E1202. PMC 3216447. PMID 21989464. doi:10.1503/cmaj.101280.
- ↑ Zhou Z, Rahme E, Pilote L (2006). "Are statins created equal? Evidence from randomized trials of pravastatin, simvastatin, and atorvastatin for cardiovascular disease prevention". Am. Heart J. 151 (2): 273–81. PMID 16442888. doi:10.1016/j.ahj.2005.04.003.
- ↑ 30,0 30,1 Vuorio, A; Kuoppala, J; Kovanen, PT; Humphries, SE; Strandberg, T; Tonstad, S; Gylling, H (Jul 7, 2010). "Statins for children with familial hypercholesterolemia.". The Cochrane database of systematic reviews (7): CD006401. PMID 20614444. doi:10.1002/14651858.CD006401.pub2.
- ↑ Lamaida, N; Capuano, E; Pinto, L; Capuano, E; Capuano, R; Capuano, V (Sep 2013). "The safety of statins in children.". Acta paediatrica (Oslo, Norway : 1992) 102 (9): 857–62. PMID 23631461. doi:10.1111/apa.12280.
- ↑ Braamskamp, MJ; Wijburg, FA; Wiegman, A (Apr 16, 2012). "Drug therapy of hypercholesterolaemia in children and adolescents.". Drugs 72 (6): 759–72. PMID 22512364. doi:10.2165/11632810-000000000-00000.
- ↑ 33,0 33,1 Repas TB, Tanner JR (February 2014). "Preventing early cardiovascular death in patients with familial hypercholesterolemia". J Am Osteopath Assoc 114 (2): 99–108. PMID 24481802. doi:10.7556/jaoa.2014.023. Arquivado dende o orixinal o 11 de marzo de 2014. Consultado o 23 de xaneiro de 2016.
- ↑ Ramasamy, I. (2015-11-04). "Update on the molecular biology of dyslipidemias". Clinica Chimica Acta; International Journal of Clinical Chemistry. ISSN 1873-3492. PMID 26546829. doi:10.1016/j.cca.2015.10.033.
- ↑ Rader DJ, Cohen J, Hobbs HH (2003). "Monogenic hypercholesterolemia: new insights in pathogenesis and treatment". J. Clin. Invest. 111 (12): 1795–803. PMC 161432. PMID 12813012. doi:10.1172/JCI18925.
- ↑ Marais AD, Blom DJ, Firth JC (January 2002). "Statins in homozygous familial hypercholesterolemia". Curr Atheroscler Rep 4 (1): 19–25. PMID 11772418. doi:10.1007/s11883-002-0058-7.
- ↑ Liu, YH; Liu, Y; Duan, CY (September 2014). "Statins for the Prevention of Contrast-Induced Nephropathy After Coronary Angiography/Percutaneous Interventions: A Meta-analysis of Randomized Controlled Trials.". J Cardiovasc Pharmacol Ther 20: 181–192. PMID 25193735. doi:10.1177/1074248414549462.
- ↑ table adapted from the following source, but check individual references for technical explanations
- Consumer Reports; Drug Effectiveness Review Project (March 2013). Evaluating statin drugs to treat High Cholesterol and Heart Disease: Comparing Effectiveness, Safety, and Price (PDF). Best Buy Drugs (Informe) (Consumer Reports). p. 9. Consultado o 27 March 2013.
- ↑ Asberg A (2003). "Interactions between cyclosporin and lipid-lowering drugs: Implications for organ transplant recipients". Drugs 63 (4): 367–378. PMID 12558459. doi:10.2165/00003495-200363040-00003.
- ↑ Food and Drug Administration (1 March 2012). "Drug Safety and Availability; FDA Drug Safety Communication: Interactions between certain HIV or hepatitis C drugs and cholesterol-lowering statin drugs can increase the risk of muscle injury". fda.gov. Consultado o 3 April 2013.
- ↑ Bellosta S, Paoletti R, Corsini A (2004). "Safety of Statins: Focus on Clinical Pharmacokinetics and Drug Interactions". Circulation 109 (23_suppl_1): III–I50. PMID 15198967. doi:10.1161/01.CIR.0000131519.15067.1f.
- ↑ Omar MA, Wilson JP (2002). "FDA Adverse Event Reports on Statin-Associated Rhabdomyolysis". The Annals of Pharmacotherapy 36 (2): 288–295. PMID 11847951. doi:10.1345/aph.1A289.
- ↑ Armitage J (2007). "The safety of statins in clinical practice". The Lancet 370 (9601): 1781–1790. PMID 17559928. doi:10.1016/S0140-6736(07)60716-8.
- ↑ Naci H, Brugts J, Ades T (July 2013). "Comparative tolerability and harms of individual statins: a study-level network meta-analysis of 246 955 participants from 135 randomized, controlled trials". Circ Cardiovasc Qual Outcomes 6 (4): 390–9. PMID 23838105. doi:10.1161/CIRCOUTCOMES.111.000071.
- ↑ Bellosta, S; Corsini, A (2012). "Statin drug interactions and related adverse reactions". Expert Opin Drug Saf 11 (6): 933–46. PMID 22866966. doi:10.1517/14740338.2012.712959.
- ↑ 46,0 46,1 Golomb BA, Evans MA (2008). "Statin Adverse Effects: A Review of the Literature and Evidence for a Mitochondrial Mechanism". Am J Cardiovasc Drugs 8 (6): 373–418. PMC 2849981. PMID 19159124. doi:10.2165/0129784-200808060-00004.
- ↑ Kmietowicz Z (2014). "New analysis fuels debate on merits of prescribing statins to low risk people". BMJ 348: g2370. PMID 24671956. doi:10.1136/bmj.g2370.
- ↑ Wise J (2014). "Open letter raises concerns about NICE guidance on statins". BMJ 348: g3937. PMID 24920699. doi:10.1136/bmj.g3937.
- ↑ Gøtzsche PC (2014). "Muscular adverse effects are common with statins". BMJ 348: g3724. PMID 24920687. doi:10.1136/bmj.g3724.
- ↑ Taylor F, Huffman MD, Macedo AF, et al. (2013). "Statins for the primary prevention of cardiovascular disease". Cochrane Database Syst Rev 1: CD004816. PMID 23440795. doi:10.1002/14651858.CD004816.pub5.
- ↑ Silva MA, Swanson AC, Gandhi PJ, Tataronis GR (January 2006). "Statin-related adverse events: a meta-analysis". Clin Ther 28 (1): 26–35. PMID 16490577. doi:10.1016/j.clinthera.2006.01.005.
- ↑ 52,0 52,1 Mancini GB, Baker S, Bergeron J, et al. (2011). "Diagnosis, prevention, and management of statin adverse effects and intolerance: proceedings of a Canadian Working Group Consensus Conference". Can J Cardiol 27 (5): 635–62. PMID 21963058. doi:10.1016/j.cjca.2011.05.007.
- ↑ Finegold JA, Manisty CH, Goldacre B, Barron AJ, Francis DP (April 2014). "What proportion of symptomatic side effects in patients taking statins are genuinely caused by the drug? Systematic review of randomized placebo-controlled trials to aid individual patient choice". Eur J Prev Cardiol 21 (4): 464–74. PMID 24623264. doi:10.1177/2047487314525531.
- ↑ Jonathan McDonagh (October 27, 2014). "Statin-Related Cognitive Impairment in the Real World: You’ll Live Longer, but You Might Not Like It". JAMA Intern Med. 174: 1889. PMID 25347692. doi:10.1001/jamainternmed.2014.5376.
- ↑ Mancini GB, Tashakkor AY, Baker S, et al. (December 2013). "Diagnosis, prevention, and management of statin adverse effects and intolerance: Canadian Working Group Consensus update". Can J Cardiol 29 (12): 1553–68. PMID 24267801. doi:10.1016/j.cjca.2013.09.023.
- ↑ Richardson K, Schoen M, French B, Umscheid CA, Mitchell MD, Arnold SE, Heidenreich PA, Rader DJ, deGoma EM. (Nov 19, 2013). "Statins and cognitive function: a systematic review.". Ann Intern Med. 159 (10): 688–97. PMID 24247674. doi:10.7326/0003-4819-159-10-201311190-00007.
- ↑ Url =http://www.fda.gov/ForConsumers/ConsumerUpdates/ucm293330.htm
- ↑ "www.accessdata.fda.gov" (PDF).
- ↑ Rull, Gurvinder; Henderson, Roger (2015-01-20). "Rhabdomyolysis and Other Causes of Myoglobinuria". Arquivado dende o orixinal o 07 de maio de 2015. Consultado o 2015-05-06.
- ↑ Ghirlanda G, Oradei A, Manto A, Lippa S, Uccioli L, Caputo S, Greco AV, Littarru GP (1993). "Evidence of plasma CoQ10-lowering effect by HMG-CoA reductase inhibitors: a double-blind, placebo-controlled study". J Clin Pharmacol 33 (3): 226–9. PMID 8463436. doi:10.1002/j.1552-4604.1993.tb03948.x.
- ↑ Marcoff L, Thompson PD (2007). "The role of coenzyme Q10 in statin-associated myopathy: a systematic review". J. Am. Coll. Cardiol. 49 (23): 2231–7. PMID 17560286. doi:10.1016/j.jacc.2007.02.049.
- ↑ Link E, Parish S, Armitage J, Bowman L, Heath S, Matsuda F, Gut I, Lathrop M, Collins R (2008). "SLCO1B1 Variants and Statin-Induced Myopathy – A Genomewide Study". NEJM 359 (8): 789–799. PMID 18650507. doi:10.1056/NEJMoa0801936.
- ↑ 63,0 63,1 Graham DJ, Staffa JA, Shatin D, Andrade SE, Schech SD, La Grenade L, Gurwitz JH, Chan KA, Goodman MJ, Platt R (2004). "Incidence of hospitalized rhabdomyolysis in patients treated with lipid-lowering drugs" (PDF). JAMA 292 (21): 2585–90. PMID 15572716. doi:10.1001/jama.292.21.2585.
- ↑ 64,0 64,1 Hanai J, Cao P, Tanksale P, Imamura S, Koshimizu E, Zhao J, Kishi S, Yamashita M, Phillips PS, Sukhatme VP, Lecker SH (2007). "The muscle-specific ubiquitin ligase atrogin-1/MAFbx mediates statin-induced muscle toxicity". J. Clin. Invest. 117 (12): 3940–51. PMC 2066198. PMID 17992259. doi:10.1172/JCI32741.
- ↑ Sattar N, Preiss D, Murray HM, Welsh P, Buckley BM, de Craen AJ, Seshasai SR, McMurray JJ, Freeman DJ, Jukema JW, Macfarlane PW, Packard CJ, Stott DJ, Westendorp RG, Shepherd J, Davis BR, Pressel SL, Marchioli R, Marfisi RM, Maggioni AP, Tavazzi L, Tognoni G, Kjekshus J, Pedersen TR, Cook TJ, Gotto AM, Clearfield MB, Downs JR, Nakamura H, Ohashi Y, Mizuno K, Ray KK, Ford I (2010). "Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials". Lancet 375 (9716): 735–42. PMID 20167359. doi:10.1016/S0140-6736(09)61965-6.
- ↑ Preiss D, Seshasai SR, Welsh P, Murphy SA, Ho JE, Waters DD, DeMicco DA, Barter P, Cannon CP, Sabatine MS, Braunwald E, Kastelein JJ, de Lemos JA, Blazing MA, Pedersen TR, Tikkanen MJ, Sattar N, Ray KK (2011). "Risk of incident diabetes with intensive-dose compared with moderate-dose statin therapy: a meta-analysis". JAMA 305 (24): 2556–64. PMID 21693744. doi:10.1001/jama.2011.860.
- ↑ Jukema JW, Cannon CP, de Craen AJ, Westendorp RG, Trompet S (Sep 4, 2012). "The controversies of statin therapy: weighing the evidence.". Journal of the American College of Cardiology 60 (10): 875–81. PMID 22902202. doi:10.1016/j.jacc.2012.07.007.
- ↑ Rutishauser J (Nov 21, 2011). "Statins in clinical medicine.". Swiss medical weekly 141: w13310. PMID 22101921. doi:10.4414/smw.2011.13310.
- ↑ Alsheikh-Ali AA, Maddukuri PV, Han H, Karas RH (2007). "Effect of the Magnitude of Lipid Lowering on Risk of Elevated Liver Enzymes, Rhabdomyolysis, and Cancer: Insights from Large Randomized Statin Trials". Journal of the American College of Cardiology 50 (5): 409–418. PMID 17662392. doi:10.1016/j.jacc.2007.02.073.
- ↑ Dale KM, Coleman CI, Henyan NN, Kluger J, White CM (2006). "Statins and cancer risk: a meta-analysis". JAMA 295 (1): 74–80. PMID 16391219. doi:10.1001/jama.295.1.74.
- ↑ Alsheikh-Ali AA, Karas RH (March 2009). "The relationship of statins to rhabdomyolysis, malignancy, and hepatic toxicity: evidence from clinical trials.". Current atherosclerosis reports 11 (2): 100–4. PMID 19228482. doi:10.1007/s11883-009-0016-8.
- ↑ Singh S, Singh AG, Singh PP, Murad MH, Iyer PG (June 2013). "Statins are associated with reduced risk of esophageal cancer, particularly in patients with Barrett's esophagus: a systematic review and meta-analysis.". Clinical gastroenterology and hepatology : the official clinical practice journal of the American Gastroenterological Association 11 (6): 620–9. PMID 23357487. doi:10.1016/j.cgh.2012.12.036.
- ↑ Liu Y, Tang W, Wang J, Xie L, Li T, He Y, Deng Y, Peng Q, Li S, Qin X (Nov 22, 2013). "Association between statin use and colorectal cancer risk: a meta-analysis of 42 studies.". Cancer causes & control : CCC 25 (2): 237–49. PMID 24265089. doi:10.1007/s10552-013-0326-6.
- ↑ Wu XD, Zeng K, Xue FQ, Chen JH, Chen YQ (October 2013). "Statins are associated with reduced risk of gastric cancer: a meta-analysis.". European journal of clinical pharmacology 69 (10): 1855–60. PMID 23748751. doi:10.1007/s00228-013-1547-z.
- ↑ Singh PP, Singh S (July 2013). "Statins are associated with reduced risk of gastric cancer: a systematic review and meta-analysis.". Annals of oncology : official journal of the European Society for Medical Oncology / ESMO 24 (7): 1721–30. PMID 23599253. doi:10.1093/annonc/mdt150.
- ↑ Pradelli D, Soranna D, Scotti L, Zambon A, Catapano A, Mancia G, La Vecchia C, Corrao G (May 2013). "Statins and primary liver cancer: a meta-analysis of observational studies.". European journal of cancer prevention : the official journal of the European Cancer Prevention Organisation (ECP) 22 (3): 229–34. PMID 23010949. doi:10.1097/cej.0b013e328358761a.
- ↑ Zhang Y, Zang T (2013). "Association between statin usage and prostate cancer prevention: a refined meta-analysis based on literature from the years 2005–2010.". Urologia internationalis 90 (3): 259–62. PMID 23052323. doi:10.1159/000341977.
- ↑ Bansal D, Undela K, D'Cruz S, Schifano F (2012). "Statin use and risk of prostate cancer: a meta-analysis of observational studies.". PLoS ONE 7 (10): e46691. PMID 23049713. doi:10.1371/journal.pone.0046691.
- ↑ Tan M, Song X, Zhang G, Peng A, Li X, Li M, Liu Y, Wang C (2013). "Statins and the risk of lung cancer: a meta-analysis.". PLoS ONE 8 (2): e57349. PMID 23468972. doi:10.1371/journal.pone.0057349.
- ↑ Zhang XL, Liu M, Qian J, Zheng JH, Zhang XP, Guo CC, Geng J, Peng B, Che JP, Wu Y (Jul 23, 2013). "Statin use and risk of kidney cancer: a meta-analysis of observational studies and randomized trials.". British Journal of Clinical Pharmacology 77 (3): 458–465. PMID 23879311. doi:10.1111/bcp.12210.
- ↑ Undela K, Srikanth V, Bansal D (August 2012). "Statin use and risk of breast cancer: a meta-analysis of observational studies.". Breast cancer research and treatment 135 (1): 261–9. PMID 22806241. doi:10.1007/s10549-012-2154-x.
- ↑ Cui X, Xie Y, Chen M, Li J, Liao X, Shen J, Shi M, Li W, Zheng H, Jiang B (July 2012). "Statin use and risk of pancreatic cancer: a meta-analysis.". Cancer causes & control : CCC 23 (7): 1099–111. PMID 22562222. doi:10.1007/s10552-012-9979-9.
- ↑ Zhang XL, Geng J, Zhang XP, Peng B, Che JP, Yan Y, Wang GC, Xia SQ, Wu Y, Zheng JH (April 2013). "Statin use and risk of bladder cancer: a meta-analysis.". Cancer causes & control : CCC 24 (4): 769–76. PMID 23361339. doi:10.1007/s10552-013-0159-3.
- ↑ Mayo clinic: article on interference between grapefruit and medication
- ↑ Kane GC, Lipsky JJ (2000). "Drug-grapefruit juice interactions". Mayo Clin. Proc. 75 (9): 933–42. PMID 10994829. doi:10.4065/75.9.933.
- ↑ Reamy BV, Stephens MB (July 2007). "The grapefruit-drug interaction debate: role of statins". Am Fam Physician 76 (2): 190, 192; author reply 192. PMID 17695563.
- ↑ FDA Website Statins and HIV or Hepatitis C Drugs: Drug Safety Communication – Interaction Increases Risk of Muscle Injury
- ↑ Istvan ES, Deisenhofer J (2001). "Structural mechanism for statin inhibition of HMG-CoA reductase". Science 292 (5519): 1160–4. PMID 11349148. doi:10.1126/science.1059344.
- ↑ 89,0 89,1 Endo A (1 November 1992). "The discovery and development of HMG-CoA reductase inhibitors". J. Lipid Res. 33 (11): 1569–82. PMID 1464741. Arquivado dende o orixinal (PDF) o 14 de febreiro de 2010. Consultado o 23 de xaneiro de 2016.
- ↑ Miettinen TA (March 1982). "Diurnal variation of cholesterol precursors squalene and methyl sterols in human plasma lipoproteins". Journal of Lipid Research 23 (3): 466–73. PMID 7200504. Arquivado dende o orixinal o 24 de xullo de 2008. Consultado o 23 de xaneiro de 2016.
- ↑ Saito Y, Yoshida S, Nakaya N, Hata Y, Goto Y (Jul–Aug 1991). "Comparison between morning and evening doses of simvastatin in hyperlipidemic subjects. A double-blind comparative study". Arterioscler Thromb 11 (4): 816–26. PMID 2065035. doi:10.1161/01.ATV.11.4.816.
- ↑ Wallace A, Chinn D, Rubin G (4 October 2003). "Taking simvastatin in the morning compared with in the evening: randomised controlled trial". British Medical Journal 327 (7418): 788. PMC 214096. PMID 14525878. doi:10.1136/bmj.327.7418.788.
- ↑ Cilla DD, Gibson DM, Whitfield LR, Sedman AJ (July 1996). "Pharmacodynamic effects and pharmacokinetics of atorvastatin after administration to normocholesterolemic subjects in the morning and evening". Journal of Clinical Pharmacology 36 (7): 604–9. PMID 8844442. doi:10.1002/j.1552-4604.1996.tb04224.x.
- ↑ Ma PT, Gil G, Südhof TC, Bilheimer DW, Goldstein JL, Brown MS (1986). "Mevinolin, an inhibitor of cholesterol synthesis, induces mRNA for low density lipoprotein receptor in livers of hamsters and rabbits" (PDF). Proc. Natl. Acad. Sci. U.S.A. 83 (21): 8370–4. Bibcode:1986PNAS...83.8370M. PMC 386930. PMID 3464957. doi:10.1073/pnas.83.21.8370.
- ↑ Laufs U , Custodis F, Böhm M (2006). "HMGCoA reductase inhibitors in chronic heart failure: potential mechanisms of benefit and risk". Drugs 66 (2): 145–154. PMID 16451090. doi:10.2165/00003495-200666020-00002.
- ↑ Greenwood J, Steinman L, Zamvil SS (May 2006). "Statin therapy and autoimmune disease: from protein prenylation to immunomodulation". Nat Rev Immunol 6 (5): 358–70. PMID 16639429. doi:10.1038/nri1839.
- ↑ Lahera V, Goicoechea M, de Vinuesa SG, Miana M, de las Heras N, Cachofeiro V, Luño J (2007). "Endothelial dysfunction, oxidative stress and inflammation in atherosclerosis: beneficial effects of statins". Curr Med Chem 14 (2): 243–8. PMID 17266583. doi:10.2174/092986707779313381.
- ↑ Blum A1, Shamburek R (April 2009). "The pleiotropic effects of statins on endothelial function, vascular inflammation, immunomodulation and thrombogenesis". Atherosclerosis 203 (2): 325–30. PMID 18834985. doi:10.1016/j.atherosclerosis.2008.08.022.
- ↑ Porter KE1, Turner NA (2011). "Statins and myocardial remodelling: cell and molecular pathways". Expert Rev Mol Med 13 (e22). PMID 21718586. doi:10.1017/S1462399411001931.
- ↑ Sawada N , Liao JK (2014). "Rho/Rho associated coiled coil forming kinase pathway as therapeutic targets for statins in atherosclerosis". Antioxid Redox Signal 20 (8): 1251–67. PMID 23919640. doi:10.1089/ars.2013.5524.
- ↑ "Questions Remain in Cholesterol Research". MedPageToday. 15 August 2014.
- ↑ Thurnher M, Nussbaumer O, Gruenbacher G (Jul 2012). "Novel aspects of mevalonate pathway inhibitors as antitumor agents". Clin Cancer Res 18 (13): 3524–31. PMID 22529099. doi:10.1158/1078-0432.CCR-12-0489.
- ↑ Norata GD1, Tibolla G2, Catapano AL3. (Oct 2014). "Statins and skeletal muscles toxicity: from clinical trials to everyday practice.". Pharmacol Res 88: 107–13. PMID 24835295. doi:10.1016/j.phrs.2014.04.012.
- ↑ Kowluru A (Jan 2008). "Protein prenylation in glucose-induced insulin secretion from the pancreatic islet beta cell: a perspective". J Cell Mol Med 12 (1): 164–73. PMID 18053094. doi:10.1111/j.1582-4934.2007.00168.x.
- ↑ Nissen SE, Nicholls SJ, Sipahi I, Libby P, Raichlen JS, Ballantyne CM, Davignon J, Erbel R, Fruchart JC, Tardif JC, Schoenhagen P, Crowe T, Cain V, Wolski K, Goormastic M, Tuzcu EM (2006). "Effect of very high-intensity statin therapy on regression of coronary atherosclerosis: the ASTEROID trial". JAMA 295 (13): 1556–65. PMID 16533939. doi:10.1001/jama.295.13.jpc60002.
- ↑ Furberg CD (19 January 1999). "Natural Statins and Stroke Risk". Circulation 99 (2): 185–188. PMID 9892578. doi:10.1161/01.CIR.99.2.185.
- ↑ Ridker PM, Danielson E, Fonseca FA, Genest J, Gotto AM, Kastelein JJ, Koenig W, Libby P, Lorenzatti AJ, MacFadyen JG, Nordestgaard BG, Shepherd J, Willerson JT, Glynn RJ (2008). "Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein" (PDF). NEJM 359 (21): 2195–207. PMID 18997196. doi:10.1056/NEJMoa0807646. Arquivado dende o orixinal (PDF) o 17 de xaneiro de 2009. Consultado o 23 de xaneiro de 2016.
- ↑ Kones R (2010). "Rosuvastatin, inflammation, C-reactive protein, JUPITER, and primary prevention of cardiovascular disease--a perspective". Drug Des Devel Ther 4: 383–413. PMC 3023269. PMID 21267417. doi:10.2147/DDDT.S10812.
- ↑ Ferdinand KC (February 2011). "Are cardiovascular benefits in statin lipid effects dependent on baseline lipid levels?". Curr Atheroscler Rep 13 (1): 64–72. PMID 21104458. doi:10.1007/s11883-010-0149-9.
- ↑ Devaraj S, Siegel D, Jialal I (February 2011). "Statin therapy in metabolic syndrome and hypertension post-JUPITER: what is the value of CRP?". Curr Atheroscler Rep 13 (1): 31–42. PMC 3018293. PMID 21046291. doi:10.1007/s11883-010-0143-2.
- ↑ Safety of Statins: Focus on Clinical Pharmacokinetics and Drug Interactions" Circulation 2004:109:III-50-IIIi-57
- ↑ "Metabolism of cerivastatin by human liver microsomes in vitro. Characterization of primary metabolic pathways and of cytochrome P450 isozymes involved". Drug Metab Dispos 25 (3): 321–31. Mar 1997.
- ↑ "Comparison of Cytochrome P-450-Dependent Metabolism and Drug Interactions of the 3-Hydroxy-3-methylglutaryl-CoA Reductase Inhibitors Lovastatin and Pravastatin in the Liver". DMD 27 (2): 173–179. 1999.
- ↑ Shepherd J, Hunninghake DB, Barter P, McKenney JM, Hutchinson HG (2003). "Guidelines for lowering lipids to reduce coronary artery disease risk: a comparison of rosuvastatin with atorvastatin, pravastatin, and simvastatin for achieving lipid-lowering goals". Am. J. Cardiol. 91 (5A): 11C–17C; discussion 17C–19C. PMID 12646338. doi:10.1016/S0002-9149(03)00004-3.
- ↑ Liu J, Zhang J, Shi Y, Grimsgaard S, Alraek T, Fønnebø V (2006). "Chinese red yeast rice (Monascus purpureus) for primary hyperlipidemia: a meta-analysis of randomized controlled trials". Chin Med 1 (1): 4. PMC 1761143. PMID 17302963. doi:10.1186/1749-8546-1-4.
- ↑ Brown Alian G., Smale Terry C., King Trevor J., Hasenkamp Rainer, Thompson Ronald H. (1976). "Crystal and Molecular Structure of Compactin, a New Antifungal Metabolite from Penicillium brevicompactum". J. Chem. Soc., Perkin Trans. 1 1976: 1165–1170. PMID 945291. doi:10.1039/P19760001165.
- ↑ Steinberg, Daniel. The Cholesterol Wars: The Skeptics vs. The Preponderance of Evidence. Academic Press, 2007, pp. 6–9.
- ↑ "Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S)". Lancet 344 (8934): 1383–9. November 1994. PMID 7968073. doi:10.1016/S0140-6736(94)90566-5.
- ↑ "National Inventors Hall of Fame Honors 2012 Inductees". PRNewswire. Arquivado dende o orixinal o 26/04/2019. Consultado o May 11, 2014.
- ↑ "How One Scientist Intrigued by Molds Found First Statin". Wall Street Journal. Consultado o May 11, 2014.
- ↑ Wolozin B, Wang SW, Li NC, Lee A, Lee TA, Kazis LE (July 19, 2007). "Simvastatin is associated with a reduced incidence of dementia and Parkinson's disease". BMC Medicine 5 (1): 20. PMC 1955446. PMID 17640385. doi:10.1186/1741-7015-5-20.
- ↑ Khurana V, Bejjanki HR, Caldito G, Owens MW (May 2007). "Statins reduce the risk of lung cancer in humans: a large case-control study of US veterans". Chest 131 (5): 1282–1288. PMID 17494779. doi:10.1378/chest.06-0931. Arquivado dende o orixinal o 14/06/2007. Consultado o 23/01/2016.
- ↑ Klein BE, Klein R, Lee KE, Grady LM (June 2006). "Statin use and incident nuclear cataract". JAMA 295 (23): 2752–8. PMID 16788130. doi:10.1001/jama.295.23.2752.
- ↑ Golomb BA, Dimsdale JE, White HL, Ritchie JB, Criqui MH (April 2008). "Reduction in blood pressure with statins: results from the UCSD Statin Study, a randomized trial". Arch. Intern. Med. 168 (7): 721–7. PMID 18413554. doi:10.1001/archinte.168.7.721.
- ↑ Drapala, A; Sikora, M; Ufnal, M (Sep 2014). "Statins, the renin-angiotensin-aldosterone system and hypertension - a tale of another beneficial effect of statins.". Journal of the renin-angiotensin-aldosterone system : JRAAS 15 (3): 250–8. PMID 25037529. doi:10.1177/1470320314531058.
- ↑ Mondul AM, Han M, Humphreys EB, Meinhold CL, Walsh PC, Platz EA (February 2011). "Association of statin use with pathological tumor characteristics and prostate cancer recurrence after surgery". Journal of Urology 185 (4): 1268–1273. PMC 3584560. PMID 21334020. doi:10.1016/j.juro.2010.11.089.
Véxase tamén
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- Statin page en Bandolier, unha revista de medicina baseada en evidencias (pouco contido despois de 2004)
- NHS Choices: High Cholesterol Prevention (medidas dietéticas etc)
