Peptidoglicano: Diferenzas entre revisións
m Bot: Substitución automática de texto (-Gram-positiva +grampositiva) |
m Bot: Substitución automática de texto (-Gram-negativa +gramnegativa) |
||
| Liña 6: | Liña 6: | ||
O peptidoglicano exerce un papel estrutural na célula bacteriana, dándolle forza estrutural, e protexéndoa da [[presión osmótica]] exercida polo [[citoplasma]]. Aínda que o peptidoglicanolle dá forza estrutural á parede, para a determinación da súa forma necesítanse tamén as proteínas [[MreB]] e [[RodZ]].<ref name="pmid11544518">{{Cita publicación periódica| author=van den Ent F, Amos LA, Löwe J| title=Prokaryotic origin of the actin cytoskeleton. | journal=Nature | year= 2001 | volume= 413 | issue= 6851 | pages= 39–44 | pmid=11544518 | doi=10.1038/35092500 | pmc= | url=http://www.ncbi.nlm.nih.gov/entrez/eutils/elink.fcgi?dbfrom=pubmed&tool=sumsearch.org/cite&retmode=ref&cmd=prlinks&id=11544518}}</ref><ref name="pmid20168300">{{Cita publicación periódica| author=van den Ent F, Johnson CM, Persons L, de Boer P, Löwe J| title=Bacterial actin MreB assembles in complex with cell shape protein RodZ. | journal=EMBO J | year= 2010 | volume= 29 | issue= 6 | pages= 1081–90 | pmid=20168300 | doi=10.1038/emboj.2010.9 | pmc=2845281}}</ref> O peptidoglicano está tamén implicado na [[fisión binaria]] durante a división celular bacteriana. |
O peptidoglicano exerce un papel estrutural na célula bacteriana, dándolle forza estrutural, e protexéndoa da [[presión osmótica]] exercida polo [[citoplasma]]. Aínda que o peptidoglicanolle dá forza estrutural á parede, para a determinación da súa forma necesítanse tamén as proteínas [[MreB]] e [[RodZ]].<ref name="pmid11544518">{{Cita publicación periódica| author=van den Ent F, Amos LA, Löwe J| title=Prokaryotic origin of the actin cytoskeleton. | journal=Nature | year= 2001 | volume= 413 | issue= 6851 | pages= 39–44 | pmid=11544518 | doi=10.1038/35092500 | pmc= | url=http://www.ncbi.nlm.nih.gov/entrez/eutils/elink.fcgi?dbfrom=pubmed&tool=sumsearch.org/cite&retmode=ref&cmd=prlinks&id=11544518}}</ref><ref name="pmid20168300">{{Cita publicación periódica| author=van den Ent F, Johnson CM, Persons L, de Boer P, Löwe J| title=Bacterial actin MreB assembles in complex with cell shape protein RodZ. | journal=EMBO J | year= 2010 | volume= 29 | issue= 6 | pages= 1081–90 | pmid=20168300 | doi=10.1038/emboj.2010.9 | pmc=2845281}}</ref> O peptidoglicano está tamén implicado na [[fisión binaria]] durante a división celular bacteriana. |
||
A capa de peptidoglicano é moito máis grosa nas bacterias [[grampositiva]]s, nas que ten entre 20 e 80 [[nanómetro]]s de grosor, ca nas [[ |
A capa de peptidoglicano é moito máis grosa nas bacterias [[grampositiva]]s, nas que ten entre 20 e 80 [[nanómetro]]s de grosor, ca nas [[gramnegativa]]s, nas que só ten entre 7 e 8 nanómetros, coa adhesión dunha [[capa S]]. O peptidoglicano constitúe arredor do 90 % do [[peso seco]] das bacterias grampositivas, pero só o 10% das gramnegativas. Deste modo, a presenza de grandes cantidades de peptidoglicano é a característica principal para caracterizar as bacterias grampositivas.<ref>C.Michael Hogan. 2010. [http://www.eoearth.org/article/Bacteria?topic=49480 ''Bacteria''. Encyclopedia of Earth. eds. Sidney Draggan and C.J.Cleveland, National Council for Science and the Environment, Washington DC]</ref> Nas bacterias grampositivas o peptidoglicano é importante para a adhesión a superficies e para o estereotipado.<ref name=Salton1996>{{cita libro | autor = Salton MRJ, Kim KS | título = Structure. ''In:'' Baron's Medical Microbiology ''(Barron S ''et al.'', eds.)| edición = 4th | editor = Univ of Texas Medical Branch | ano = 1996 | url = http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mmed.section.289#297 | isbn=0-9631172-1-1 }}</ref> As partículas de aproximadamente 2 nanómetros poden atravesar o peptidoglicano, tanto nas grampositivas coma nas negativas.<ref>{{Cita publicación periódica | author=Demchick PH, Koch AL | title=The permeability of the wall fabric of Escherichia coli and Bacillus subtilis | journal=Journal of Bacteriology | date=1 February 1996| pages=768–73| volume=178 | issue=3 |url=http://jb.asm.org/cgi/reprint/178/3/768 | pmid=8550511 | pmc=177723}}</ref> |
||
== Estrutura == |
== Estrutura == |
||
A capa de peptidoglicano na parede celular bacteriana é unha estrutura que forma unha [[rede cristalina]] constituída por cadeas liñais paralelas de dous [[aminoazucre]]s alternantes, a [[N-acetilglicosamina|''N''-acetilglicosamina]] (GlcNAc ou NAG) e o [[ácido N-acetilmurámico|''N''-acetilmurámico]] (MurNAc ou NAM), os cales están unidos por [[enlace glicosídico]] β-(1,4). Cada residuo de MurNAc está unido a un curto [[péptido]] de 4 a 5 residuos de aminoácidos, que contén [[alanina|<small>L</small>-alanina]], [[ácido glutámico|ácido <small>D</small>-glutámico]], [[ácido meso-diaminopimélico|ácido ''meso''-diaminopimélico]], e [[alanina|<small>D</small>-alanina]] no caso de ''[[Escherichia coli]]'' (unha [[bacteria |
A capa de peptidoglicano na parede celular bacteriana é unha estrutura que forma unha [[rede cristalina]] constituída por cadeas liñais paralelas de dous [[aminoazucre]]s alternantes, a [[N-acetilglicosamina|''N''-acetilglicosamina]] (GlcNAc ou NAG) e o [[ácido N-acetilmurámico|''N''-acetilmurámico]] (MurNAc ou NAM), os cales están unidos por [[enlace glicosídico]] β-(1,4). Cada residuo de MurNAc está unido a un curto [[péptido]] de 4 a 5 residuos de aminoácidos, que contén [[alanina|<small>L</small>-alanina]], [[ácido glutámico|ácido <small>D</small>-glutámico]], [[ácido meso-diaminopimélico|ácido ''meso''-diaminopimélico]], e [[alanina|<small>D</small>-alanina]] no caso de ''[[Escherichia coli]]'' (unha [[bacteria gramnegativa]]) ou [[alanina|<small>L</small>-alanina]], [[glutamina|<small>D</small>-glutamina]], [[lisina|<small>L</small>-lisina]], e <small>D</small>-alanina cunha ponte peptídica de 5 [[glicina]]s que une os tetrapéptidos no caso de ''[[Staphylococcus aureus]]'' (unha [[bacteria grampositiva]]). Estes aminoácidos, excepto os <small>L</small>-aminoácidos, non aparecen en proteínas, polo que poderían ser unha protección contra o ataque da maioría das [[peptidase]]s. |
||
Os enlaces cruzados entre os aminoácidos de diferentes cadeas de aminoazucres establécense pola acción do encima [[transpeptidase]] e orixinan unha estrutura tridimensional forte e ríxida. A secuencia específica de aminoácidos e a estrutura molecular varía coa especie bacteriana considerada.<ref>{{cita libro | autor = Ryan KJ, Ray CG (editors) | título = Sherris Medical Microbiology | edición = 4th | editor = McGraw Hill | ano = 2004 | isbn = 0-8385-8529-9 }}</ref> |
Os enlaces cruzados entre os aminoácidos de diferentes cadeas de aminoazucres establécense pola acción do encima [[transpeptidase]] e orixinan unha estrutura tridimensional forte e ríxida. A secuencia específica de aminoácidos e a estrutura molecular varía coa especie bacteriana considerada.<ref>{{cita libro | autor = Ryan KJ, Ray CG (editors) | título = Sherris Medical Microbiology | edición = 4th | editor = McGraw Hill | ano = 2004 | isbn = 0-8385-8529-9 }}</ref> |
||
Revisión como estaba o 30 de agosto de 2016 ás 17:57

O peptidoglicano, tamén chamado mureína, é un polímero formado por azucres e aminoácidos que forma unha capa que rodea a membrana plasmática da maioría das bacterias (pero non das arqueas) e que constitúe a súa parede celular. O compoñente carbohidrato do peptidoglicano é un heteropolisacárido formado por residuos alternantes dos monosacáridos N-acetilglicosamina e ácido N-acetilmurámico, unidos entre si por enlace glicosídico β-(1,4). As cadeas deste heteropolisacárido dispóñense paralelamente. Unido ao ácido N-acetilmurámico está o compoñente aminoacídico, que é un péptido de tres a cinco aminoácidos. Esta cadea peptídica pode establecer enlaces cruzados cos péptidos doutras cadeas do heteropolisacárido, formando unha capa reticular tridimensional.[1]
Algunhas Archaea teñen unha capa bastante similar pero de pseudopeptidoglicano ou pseudomureína, na que os residuos de azucres están unidos por enlaces glicosídicos β-(1,3) e os azucres que a forman son a N-acetilglicosamina e a ácido N-acetiltalosaminurónico. Isto explica que a parede das arqueas sexa insensible á lisocima, que ataca ao peptidoglicano.[2]
O peptidoglicano exerce un papel estrutural na célula bacteriana, dándolle forza estrutural, e protexéndoa da presión osmótica exercida polo citoplasma. Aínda que o peptidoglicanolle dá forza estrutural á parede, para a determinación da súa forma necesítanse tamén as proteínas MreB e RodZ.[3][4] O peptidoglicano está tamén implicado na fisión binaria durante a división celular bacteriana.
A capa de peptidoglicano é moito máis grosa nas bacterias grampositivas, nas que ten entre 20 e 80 nanómetros de grosor, ca nas gramnegativas, nas que só ten entre 7 e 8 nanómetros, coa adhesión dunha capa S. O peptidoglicano constitúe arredor do 90 % do peso seco das bacterias grampositivas, pero só o 10% das gramnegativas. Deste modo, a presenza de grandes cantidades de peptidoglicano é a característica principal para caracterizar as bacterias grampositivas.[5] Nas bacterias grampositivas o peptidoglicano é importante para a adhesión a superficies e para o estereotipado.[6] As partículas de aproximadamente 2 nanómetros poden atravesar o peptidoglicano, tanto nas grampositivas coma nas negativas.[7]
Estrutura
A capa de peptidoglicano na parede celular bacteriana é unha estrutura que forma unha rede cristalina constituída por cadeas liñais paralelas de dous aminoazucres alternantes, a N-acetilglicosamina (GlcNAc ou NAG) e o N-acetilmurámico (MurNAc ou NAM), os cales están unidos por enlace glicosídico β-(1,4). Cada residuo de MurNAc está unido a un curto péptido de 4 a 5 residuos de aminoácidos, que contén L-alanina, ácido D-glutámico, ácido meso-diaminopimélico, e D-alanina no caso de Escherichia coli (unha bacteria gramnegativa) ou L-alanina, D-glutamina, L-lisina, e D-alanina cunha ponte peptídica de 5 glicinas que une os tetrapéptidos no caso de Staphylococcus aureus (unha bacteria grampositiva). Estes aminoácidos, excepto os L-aminoácidos, non aparecen en proteínas, polo que poderían ser unha protección contra o ataque da maioría das peptidases.
Os enlaces cruzados entre os aminoácidos de diferentes cadeas de aminoazucres establécense pola acción do encima transpeptidase e orixinan unha estrutura tridimensional forte e ríxida. A secuencia específica de aminoácidos e a estrutura molecular varía coa especie bacteriana considerada.[8]
-
Estrutura do peptidoglicano.
-
Parede celular grampositiva.
-
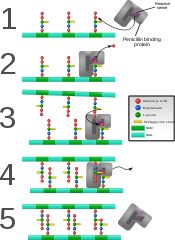
Proteína de unión á penicilina formando enlaces cruzados nunha parede bacteriana acabada de formar.
Inhibición por antibióticos
Algúns fármacos antibacterianos como a penicilina interfiren coa produción de peptidoglicano ao unirse aos encimas bacterianos chamados proteínas de unión á penicilina ou transpeptidases.[6] As proteínas de unión á penicilina forman os enlaces cruzados entre os oligopéptidos do peptidoglicano. Para que unha célula bacteriana se reproduza por fisión binaria, deben unirse máis dun millón de subunidades (NAM-NAG+oligopéptido) do peptidoglicano ás subunidades xa existentes.[9] As mutacións nas transpeptidases que reducen as interaccións cun antibiótico son unha fonte significativa de produción de resistencia aos antibióticos bacteriana.[10]
A lisocima das bágoas, considerado o antibiótico propio do corpo humano, funciona rompendo os enlaces glicosídicos β-(1,4) do peptidoglicano e destruíndo así moitas células bacterianas. Antibióticos como a penicilina xeralmente impiden a correcta formación da parede bacteriana, da cal o peptidoglicano é o compoñente principal, ao inhibir as transpeptidases.
Biosíntese
Os monómeros de peptidoglicano son sintetizados no citosol e líganse despois ao transportador de membrana bactoprenol. O bactoprenol transporta os monómeros de peptidoglicano a través da membrana celular, e son inseridos no peptidoglicano xa existente.[11] A síntese divídese en fase 1 e fase 2 e consta de varios pasos biosintéticos:
Fase 1
Ten lugar no citosol. No primeiro paso da síntese do peptidoglicano, o aminoácido glutamina, doa un grupo amino ao azucre, frutosa 6-fosfato. Isto transforma a frutosa 6-fosfato en glicosamina 6-fosfato. No segundo paso da síntese, transfírese un grupo acetilo desde o acetil-CoA ao grupo amino da glicosamina 6-fosfato orixinando N-acetilglicosamina 6-fosfato.[12] No terceiro paso, a N-acetilglicosamina 6-fosfato é isomerizada, ao que fai que cambie a N-acetilglicosamina 1-fosfato.[12]
No paso cuarto, a N-acetilglicosamina 1-fosfato, que é agora un monofosfato, ataca a UTP (nucleótido que actúa como fonte de enerxía). Nesta reacción, o UTP perde un pirofosfato, que é substituído polo fosfato do aminoazucre, orixinándose UDP-N-acetilglicosamina (UDP-GlcNAc), que é o precursor do NAG do peptidoglicano.
No 5º paso, parte do UDP-N-acetilglicosamina é convertido en UDP-ácido N-acetilmurámico (UDP-MurNAc) pola adición dun grupo lactilo á glicosamina. Tamén nesta reacción, o grupo C3 hidroxilo retira un fosfato do carbono alfa do fosfoenolpiruvato. Isto crea o que se denomina un enol derivado que será reducido a un “residuo lactil” polo NADPH no paso sexto da síntese.[12]
No 7º paso, o UDP–MurNAc covértese no pentapéptido UDP-MurNAC pola adición de cinco aminoácidos, normalmente incluíndo o dipéptido D-alanil-D-alanina.[12] Cada unha destas reaccións require como fonte de enrxía o ATP.[12]
Fase 2
A fase 2 ocorre na membrana plasmática. Na membrana o transportador lipídico bactoprenol leva os precursores do peptidoglicano a través da membrana. O bactoprenol ataca o UDP-MurNAc-pentapéptido, creando o PP-MurNac-pentapéptido, que é agora un lípido. O UDP-GlcNAc transpórtase despois ao residuo MurNAc da molécula anterior, orixinando o lípido-PP-MurNAc-pentapéptdido-GlcNAc, un disacárido, precursor do peptidoglicano.[12] Non se sabe como esta molécula é transportada ao outro lado da membrana. Porén, unha vez que está no periplasma, engádese a unha cadea de glicano en crecemento.[12] A seguinte reacción coñécese como transglicosilación. Nesta reacción, o grupo hidroxilo do GlcNAc únese ao MurNAc no glicano, o cal despraza o lípido-PP da cadea de glicano. O encima responsable disto é a transglicosilase.[12]
Notas
- ↑ Animation of Synthesis of Peptidoglycan Layer
- ↑ Madigan, M. T., J. M. Martinko, P. V. Dunlap, and D. P. Clark. Brock biology of microorganisms. 12th ed. San Francisco, CA: Pearson/Benjamin Cummings, 2009.
- ↑ van den Ent F, Amos LA, Löwe J (2001). "Prokaryotic origin of the actin cytoskeleton.". Nature 413 (6851): 39–44. PMID 11544518. doi:10.1038/35092500.
- ↑ van den Ent F, Johnson CM, Persons L, de Boer P, Löwe J (2010). "Bacterial actin MreB assembles in complex with cell shape protein RodZ.". EMBO J 29 (6): 1081–90. PMC 2845281. PMID 20168300. doi:10.1038/emboj.2010.9.
- ↑ C.Michael Hogan. 2010. Bacteria. Encyclopedia of Earth. eds. Sidney Draggan and C.J.Cleveland, National Council for Science and the Environment, Washington DC
- ↑ 6,0 6,1 Salton MRJ, Kim KS (1996). Univ of Texas Medical Branch, ed. Structure. In: Baron's Medical Microbiology (Barron S et al., eds.) (4th ed.). ISBN 0-9631172-1-1.
- ↑ Demchick PH, Koch AL (1 February 1996). "The permeability of the wall fabric of Escherichia coli and Bacillus subtilis". Journal of Bacteriology 178 (3): 768–73. PMC 177723. PMID 8550511.
- ↑ Ryan KJ, Ray CG (editors) (2004). McGraw Hill, ed. Sherris Medical Microbiology (4th ed.). ISBN 0-8385-8529-9.
- ↑ Bauman R (2007). Benjamin Cummings, ed. Microbiology with Diseases by Taxonomy (2nd ed.). ISBN 0-8053-7679-8.
- ↑ Spratt BG (1994). "Resistance to antibiotics mediated by target alterations". Science (New York) 264 (5157): 388–93. PMID 8153626. doi:10.1126/science.8153626.
- ↑ "II. THE PROKARYOTIC CELL: BACTERIA". Consultado o 1. MAY 2011.
- ↑ 12,0 12,1 12,2 12,3 12,4 12,5 12,6 12,7 White, D. (2007). Oxford University Press Inc., ed. The physiology and biochemistry of prokaryates (3rd ed.). NY.