Indol: Diferenzas entre revisións
| Liña 127: | Liña 127: | ||
A posición máis reactiva no indol para unha [[substitución aromática electrofílica]] é C-3, a cal é 10<sup>13</sup> veces máis reactiva en certas reaccións que o [[benceno]]. Por exemplo, é alquilado por unha serina fosforilada na biosíntese do aminoácido triptófano (ver figura máis arriba). A [[reacción de formilación]] de [[reacción de Vilsmeier-Haack|Vilsmeier-Haack]] do indol<ref name="james1959">{{cite journal|author=James, P. N.; Snyder, H. R.|year=1959|title=Indole-3-aldehyde |journal=[[Organic Syntheses]]|volume=39|page=30| url=http://www.orgsyn.org/orgsyn/prep.asp?prep=cv4p0539}}</ref> ten lugar a temperaturas moderadas exclusivamente en C-3. Como o anel pirrólico é a porción máis reactiva do indol, a substitución electrofílica do anel carbocíclico (benceno) pode ter lugar só despois de que son substituídos N-1, C-2, e C-3. |
A posición máis reactiva no indol para unha [[substitución aromática electrofílica]] é C-3, a cal é 10<sup>13</sup> veces máis reactiva en certas reaccións que o [[benceno]]. Por exemplo, é alquilado por unha serina fosforilada na biosíntese do aminoácido triptófano (ver figura máis arriba). A [[reacción de formilación]] de [[reacción de Vilsmeier-Haack|Vilsmeier-Haack]] do indol<ref name="james1959">{{cite journal|author=James, P. N.; Snyder, H. R.|year=1959|title=Indole-3-aldehyde |journal=[[Organic Syntheses]]|volume=39|page=30| url=http://www.orgsyn.org/orgsyn/prep.asp?prep=cv4p0539}}</ref> ten lugar a temperaturas moderadas exclusivamente en C-3. Como o anel pirrólico é a porción máis reactiva do indol, a substitución electrofílica do anel carbocíclico (benceno) pode ter lugar só despois de que son substituídos N-1, C-2, e C-3. |
||
:[[Ficheiro:Indole Vilsmeyer-Haack Formylation.png|300px|Formilaciñon de Vilsmeyer-Haack do indol.]] |
:[[Ficheiro:Indole Vilsmeyer-Haack Formylation.png|300px|miniatura|Formilaciñon de Vilsmeyer-Haack do indol.]] |
||
A [[gramina]] é un útil intermediario sintético que se produce pola [[reacción de Mannich]] do indol con [[dimetilamina]] e [[formaldehido]]. É o precursor do ácido indol-acético e do triptófano sintético. |
A [[gramina]] é un útil intermediario sintético que se produce pola [[reacción de Mannich]] do indol con [[dimetilamina]] e [[formaldehido]]. É o precursor do ácido indol-acético e do triptófano sintético. |
||
:[[Ficheiro:Gramine From Indole Scheme.png|250px|Síntese de gramina a partir do indol.]] |
:[[Ficheiro:Gramine From Indole Scheme.png|250px|miniatura|Síntese de gramina a partir do indol.]] |
||
===Acidez nitróxeno-H e complexos anión indol organometálicos=== |
===Acidez nitróxeno-H e complexos anión indol organometálicos=== |
||
Revisión como estaba o 4 de outubro de 2014 ás 19:38
Este artigo está a ser traducido ao galego por un usuario desta Wikipedia; por favor, non o edite. O usuario Miguelferig (conversa · contribucións) realizou a última edición na páxina hai 9 anos. Se o usuario non publica a tradución nun prazo de trinta días, procederase ó seu borrado rápido. |
| Indol | |
|---|---|
 | |

|

|
Indol | |
Outros nomes 2,3-benzopirrol, ketol, | |
| Identificadores | |
| Número CAS | 120-72-9 |
| PubChem | 798 |
| ChemSpider | 776 |
| UNII | 8724FJW4M5 |
| KEGG | C00463 |
| ChEBI | CHEBI:16881 |
| ChEMBL | CHEMBL15844 |
| Número RTECS | NL2450000 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C8H7N |
| Masa molecular | 117,15 g/mol |
| Aspecto | Sólido branco |
| Densidade | 1,1747 g/cm3, sólido |
| Punto de fusión | 52–54 °C |
| Punto de ebulición | 253–254°C (526 K) |
| Solubilidade en auga | 0,19 g/100 ml (20 °C) Soluble en auga quente |
| Acidez (pKa) | 16,2 (21,0 en DMSO) |
| Basicidade (pKb) | 17,6 |
| Estrutura | |
| Estrutura cristalina | Pna21 |
| Forma da molécula | Plana |
| Momento dipolar | 2,11 D en benceno |
| Perigosidade | |
| MSDS | [2] |
| Declaracións R/S | R: 21/22-37/38-41-50/53 S: 26-36/37/39-60-61 |
| Punto de inflamabilidade | 121 °C; 250 °F; 394 K |
| Compostos relacionados | |
| compostos aromáticos relacionados |
benceno, benzofurano, carbazol, carbolina, indeno, indolina, isatina, metilindol, oxindol, pirrol, excatol |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
O indol é un composto orgánico heterocíclico aromático. Ten unha estrutura bicíclica, constituída por un anel hexagonal de benceno fusionado cun anel pentagonal pirrol que contén nitróxeno. O indol está amplamente distribuído nos ambientes naturais, xa que poden producilo diversas bacterias. Como molécula de sinalización celular o indol regula varios aspectos a fisioloxía bacteriana, como a formación de esporas, estabilidade dos plásmidos, resistencia aos fármacos, formación de biopelículas, e a virulencia.[1] Un importante derivado do indol é o aminoácido triptófano, o cal é o precursor do neurotransmisor serotonina.[2]
Propiedades xerais e distribución
O indol é sólido a temperaturas moderadas. O indol poden producilo moitas bacterias como produto de degradación do aminoácido triptófano. Está presente de forma natural nas feces humanas e ten un intenso cheiro fecal. Porén, a concentracións moi baixas ten un aroma floral,[3] e é un constituínte de moitos recendos de flores (como o das flores de laranxeira) e perfumes. Tamén aparece no alcatrán de hulla.
Cando funciona como substituínte denomínase indolil (ou ás veces indol-).
O indol pode sufrir substitución electrofílica, principalmente na posición 3. Os indois substituídos son elementos estruturais (e para algúns compostos os precursores sintéticos) dos alcaloides derivados do triptófano triptaminas, como o neurotransmisor serotonina, e a melatonina. Outros compostos indólicos son a hormona de plantas auxina (ácido indolil-3-acético, IAA), triptofol, o fármaco antiinflamatorio indometacina, o betabloqueante pindolol, e o alucinóxeno natural dimetiltriptamina.
O nome indol procede da fusión das palabras indigo e oleum, xa que o indol illouse primeiramente tratando a tintura índigo con aceite (oleum). A terminación ol non se refire, pois, aos alcohois.
Historia

A química do indol empezou a desenvolverse co estudo da tintura índigo. O índigo pode converterse en isatina e despois en oxindol. Máis tarde, en 1866, Adolf von Baeyer reduciu o oxindol a indol utilizando po de cinc.[4] En 1869, este investigador propuxo unha fórmula para o indol (imaxe á esquerda).[5]
Certos derivados do indol foron importantes tinturas para uso industrial ata o final do século XIX. Na década de 1930, intensificouse o interese polo indol cando se chegou a saber que o núcleo do indol está presente en moitos alcaloides importantes, e no triptófano e as auxinas, e esta segue sendo unha área de activa investigación hoxe en día.[6]
Biosíntese
O indol biosintetízase por medio do antranilato.[2] Condénsase coa serina por medio da adición de Michael do indol ao PLP-aminoacrilato.
O indol é o principal constituínte do alcatrán de hulla, e a fracción de destilación a 220–260 °C é a principal fonte industrial deste produto.
Rutas sintéticas
O indol e os seus derivados poden tamén sintetizarse por diversos métodos.[7][8][9]
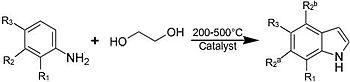
A principais rutas de síntese industrial do indol empezan a partir da anilina por medio dunha reacción en fase de vapor co etilén glicol en presenza de catalizadores:
En xeral, as reaccións realízanse entre os 200 e os 500 °C. Os rendementos poden chegar ao 60%. Outros precursores do indol son a formiltoluidina, a 2-etilanilina, e o 2-(2-nitrofenil)etanol, todos os cales sofren ciclacións.[10] Desenvolvéronse moitos outros métodos aplicables.
Síntese do indol de Leimgruber-Batcho
A síntese de indol de Leimgruber-Batcho é un método eficiente de sintetizar indol e indois substituídos. Divulgado orixinalmente nunha patente en 1976, este método ten un alto rendemento e pode xerar indois substituídos. Este método é especialmente popular na industria farmacéutica, na cal moitos fármacos están feitos de indois especificamente substituídos.
Síntese de indol de Fischer

Un dos métodos máis antigos e máis fiables para a síntese de indois substituídos é a síntese de indol de Fischer, desenvolvida en 1883 por Emil Fischer. Aínda que a síntese do propio indol é complicada utilizando o método de Fischer, este utilízase a miúdo para xerar indois substituídos nas posicións 2- e 3. Porén, o indol pode tamén sintetizarse polo método de Fischer facendo reaccionar fenilhidrazina con ácido pirúvico seguindo coa descarboxilación do ácido indol-2-carboxílico formado. Isto realizouse nunha síntese nun só recipiente utilizando irradiación con microondas.[11]
Outras reaccións formadoras de indol
- síntese de indol de Bartoli
- síntese de indol de Bischler-Möhlau
- síntese de indol de Fukuyama
- síntese de indol de Gassman
- síntese de indol de Hemetsberger
- síntese de indol de Larock
- síntese de Madelung
- síntese de indol de Nenitzescu
- síntese de indol de Reissert
- síntese de indol de Baeyer-Emmerling
- Na reacción de Diels-Reese [12][13] o dimetil acetilenodicarboxilato reacciona coa difenilhidrazina a un aducto, que en xileno dá dimetil indol-2,3-dicarboxilato e anilina. Con outros solventes, fórmanse outros produtos: con ácido acético glacial unha pirazolona, e con piridina unha quinolina.
Reaccións químicas do indol
Basicidade
A diferenza da maioría das aminas, o indol non é básico. A situación dos enlaces é completamente análoga á do pirrol. Cómpren ácidos moi fortes como o ácido clorhídrico para protonar o indol. A forma protonada ten unha pKa de −3,6. A sensibilidade de moitos compostos indólicos (por exemplo, as triptaminas) en condicións ácidas débese a esta protonación.
Substitución electrofílica
A posición máis reactiva no indol para unha substitución aromática electrofílica é C-3, a cal é 1013 veces máis reactiva en certas reaccións que o benceno. Por exemplo, é alquilado por unha serina fosforilada na biosíntese do aminoácido triptófano (ver figura máis arriba). A reacción de formilación de Vilsmeier-Haack do indol[14] ten lugar a temperaturas moderadas exclusivamente en C-3. Como o anel pirrólico é a porción máis reactiva do indol, a substitución electrofílica do anel carbocíclico (benceno) pode ter lugar só despois de que son substituídos N-1, C-2, e C-3.
A gramina é un útil intermediario sintético que se produce pola reacción de Mannich do indol con dimetilamina e formaldehido. É o precursor do ácido indol-acético e do triptófano sintético.
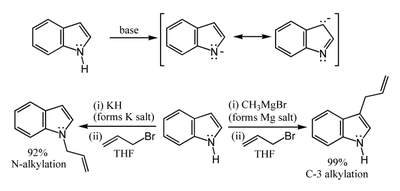
Acidez nitróxeno-H e complexos anión indol organometálicos
The N-H center has a pKa of 21 in DMSO, so that very strong bases such as sodium hydride or butyl lithium and water-free conditions are required for complete deprotonation. The resulting alkali metal derivatives can react in two ways. The more ionic salts such as the sodium or potassium compounds tend to react with electrophiles at nitrogen-1, whereas the more covalent magnesium compounds (indole Grignard reagents) and (especially) zinc complexes tend to react at carbon-3 (see figure below). In analogous fashion, polar aprotic solvents such as DMF and DMSO tend to favour attack at the nitrogen, whereas nonpolar solvents such as toluene favour C-3 attack.[15]
Acidez do carbono e litiación C-2
After the N-H proton, the hydrogen at C-2 is the next most acidic proton on indole. Reaction of N-protected indoles with butyl lithium or lithium diisopropylamide results in lithiation exclusively at the C-2 position. This strong nucleophile can then be used as such with other electrophiles.
Bergman and Venemalm developed a technique for lithiating the 2-position of unsubstituted indole.[16]
Alan Katritzky also developed a technique for lithiating the 2-position of unsubstituted indole.[17]
Oxidación do indol
Due to the electron-rich nature of indole, it is easily oxidized. Simple oxidants such as N-bromosuccinimide will selectively oxidize indole 1 to oxindole (4 and 5).
Cycloadicións do indol
Only the C-2 to C-3 pi-bond of indole is capable of cycloaddition reactions. Intramolecular variants are often higher-yielding than intermolecular cycloadditions. For example, Padwa et al.[18] have developed this Diels-Alder reaction to form advanced strychnine intermediates. In this case, the 2-aminofuran is the diene, whereas the indole is the dienophile. Indoles also undergo intramolecular [2+3] and [2+2] cycloadditions.
Despite mediocre yields, intermolecular cycloadditions of indole derivatives have been well documented.[19][20][21] One example is the Pictet-Spengler reaction between tryptophan derivatives and aldehydes.[22] The Pictet-Spengler reaction of indole derivatives, such as tryptophan, leads to a mixture of diastereomers as products. The formation of multiple products reduces the chemical yield of the desired product.
Aplicacións
Natural jasmine oil, used in the perfume industry, contains around 2.5% of indole. Since 1 kilogram of the natural oil requires processing several million jasmine blossoms and costs around $10,000, indole (among other things) is used in the manufacture of synthetic jasmine oil (which costs around $10/kg).
Notas
- ↑ Lee, Jin-Hyung; Lee, Jintae (2010). "Indole as an intercellular signal in microbial communities". FEMS Microbiology Reviews. ISSN 0168-6445. doi:10.1111/j.1574-6976.2009.00204.x.
- ↑ 2,0 2,1 Modelo:Lehninger4th
- ↑ http://www.leffingwell.com/olfact5.htm
- ↑ Baeyer, A. (1866). "Ueber die Reduction aromatischer Verbindungen mittelst Zinkstaub". Ann. 140 (3): 295. doi:10.1002/jlac.18661400306.
- ↑ Baeyer, A.; Emmerling, A. (1869). "Synthese des Indols". Chemische Berichte 2: 679. doi:10.1002/cber.186900201268.
- ↑ R. B. Van Order, H. G. Lindwall (1942). "Indole". Chem. Rev. 30: 69–96. doi:10.1021/cr60095a004.
- ↑ Gribble G. W. (2000). "Recent developments in indole ring synthesis—methodology and applications". J. Chem. Soc. Perkin Trans. 1 (7): 1045. doi:10.1039/a909834h.
- ↑ Cacchi, S.; Fabrizi, G. (2005). "Synthesis and Functionalization of Indoles Through Palladium-catalyzed Reactions". Chem. Rev. 105 (7): 2873. PMID 16011327. doi:10.1021/cr040639b.
- ↑ Humphrey, G. R.; Kuethe, J. T. (2006). "Practical Methodologies for the Synthesis of Indoles". Chem. Rev. 106 (7): 2875. PMID 16836303. doi:10.1021/cr0505270.
- ↑ Gerd Collin and Hartmut Höke “Indole” Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI 10.1002/14356007.a14_167 [1].
- ↑ Bratulescu, George (2008). "A new and efficient one-pot synthesis of indoles". Tetrahedron Letters 49 (6): 984. doi:10.1016/j.tetlet.2007.12.015.
- ↑ Diels, Otto; Reese, Johannes (1934). "Synthesen in der hydroaromatischen Reihe. XX. Über die Anlagerung von Acetylen-dicarbonsäureester an Hydrazobenzol". Ann. 511: 168. doi:10.1002/jlac.19345110114.
- ↑ Ernest H. Huntress, Joseph Bornstein, and William M. Hearon (1956). "An Extension of the Diels-Reese Reaction". J. Am. Chem. Soc. 78 (10): 2225. doi:10.1021/ja01591a055.
- ↑ James, P. N.; Snyder, H. R. (1959). "Indole-3-aldehyde". Organic Syntheses 39: 30.
- ↑ Heaney, H.; Ley, S. V. (1974). "1-Benzylindole". Organic Syntheses 54: 58.
- ↑ Bergman, J.; Venemalm, L. (1992). "Efficient synthesis of 2-chloro-, 2-bromo-, and 2-iodoindole". J. Org. Chem. 57 (8): 2495. doi:10.1021/jo00034a058.
- ↑ Alan R. Katritzky, Jianqing Li, Christian V. Stevens (1995). "Facile Synthesis of 2-Substituted Indoles and Indolo[3,2-b]carbazoles from 2-(Benzotriazol-1-ylmethyl)indole". J. Org. Chem. 60 (11): 3401–3404. doi:10.1021/jo00116a026.
- ↑ Lynch, S. M. ; Bur, S. K.; Padwa, A. (2002). "Intramolecular Amidofuran Cycloadditions across an Indole π-Bond: An Efficient Approach to the Aspidosperma and Strychnos ABCE Core". Org. Lett. 4 (26): 4643. PMID 12489950. doi:10.1021/ol027024q.
- ↑ Use {{Cita publicación periódica}} no canto deste marcador. Pode indicar a referencia DOI no parámetro
|doi= - ↑ Gremmen, C.; Willemse, B.; Wanner, M. J.; Koomen, G.-J. (2000). "Enantiopure Tetrahydro-β-carbolines via Pictet-Spengler Reactions with N-Sulfinyl Tryptamines". Org. Lett. 2 (13): 1955–1958. doi:10.1021/ol006034t.
- ↑ a) The intermolecular Pictet-Spengler condensation with chiral carbonyl derivatives in the stereoselective syntheses of optically-active isoquinoline and indole alkaloids Enrique L. Larghi, Marcela Amongero, Andrea B. J. Bracca, and Teodoro S. Kaufman Arkivoc (RL-1554K) pp 98-153 2005 (Online Review); b) Teodoro S. Kaufman “Synthesis of Optically-Active Isoquinoline and Indole Alkaloids Employing the Pictet-Spengler Condensation with Removable Chiral Auxiliaries Bound to Nitrogen”. in “New Methods for the Asymmetric Synthesis of Nitrogen Heterocycles”; Ed.: J. L. Vicario. ISBN 81-7736-278-X. Research SignPost, Trivandrum, India. 2005. Chapter 4, pp. 99-147.
- ↑ Bonnet, D.; Ganesan, A. (2002). "Solid-Phase Synthesis of Tetrahydro-β-carbolinehydantoins via the N-Acyliminium Pictet-Spengler Reaction and Cyclative Cleavage". J. Comb. Chem. 4 (6): 546–548. doi:10.1021/cc020026h.
- Referencias xerais
- Indoles Part One, W. J. Houlihan (ed.), Wiley Interscience, New York, 1972.
- Sundberg, R. J. (1996). Indoles. San Diego: Academic Press. ISBN 0-12-676945-1.
- Joule, J. A.; Mills, K. (2000). Heterocyclic Chemistry. Oxford, UK: Blackwell Science. ISBN 0-632-05453-0.
- Joule, J., In Science of Synthesis, Thomas, E. J., Ed.; Thieme: Stuttgart, (2000); Vol. 10, p. 361. ISBN 3-13-112241-2 (GTV); ISBN 0-86577-949-X (TNY).
- Schoenherr, H.; Leighton, J. L. Direct and Highly Enantioselective Iso-Pictet-Spengler Reactions with alpha-Ketoamides: Access to Underexplored Indole Core Structures. Org. Lett. 2012, 14, 2610.
Véxase tamén
Outros artigos
- Ácido Indol-3-butírico
- Isoindol
- Escatol
- Proba do indol, proba para a identificación de especies bacterianas
- Ácido indolacético
- Triptaminas
Ligazóns externas
| Commons ten máis contidos multimedia sobre: Indol |
- Síntese de indois (panorma xeral de métodos recentes)
- Síntese e propiedades dos indois en chemsynthesis.com