Dodecil sulfato de sodio
| Lauril sulfato de sodio | |
|---|---|
 | |
 | |
Sodio dodecil sulfato | |
Outros nomes Sodio monododecil sulfato; Sodio lauril sulfato; Sodio monolauril sulfato; Sodio dodecanesulfato; Sodio coco-sulfato; dodecil alcohol; hidróxeno sulfato, sal de sodio; n-dodecil sulfato de sodio; Ácido sulfúrico monododecil éster sal de sodio; | |
| Identificadores | |
| Número CAS | 151-21-3 |
| PubChem | 3423265 |
| ChemSpider | 8677 |
| DrugBank | DB00815 |
| ChEBI | CHEBI:8984 |
| ChEMBL | CHEMBL23393 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | NaC12H25SO4 |
| Masa molecular | 288,372 g/mol |
| Aspecto | sólido branco ou cor crema |
| Olor | inodoro |
| Densidade | 1,01 g/cm3 |
| Punto de fusión | 206 °C; 403 °F; 479 K |
| Índice de refracción (nD) | 1,461 |
| Perigosidade | |
| LD50 | 1288 mg/kg (rata, oral) |
| Compostos relacionados | |
| Outros anións | Sodio lauril éter sulfato Sodio miristil éter sulfato |
| Outros catións | Amonio lauril sulfato Potasio lauril sulfato |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
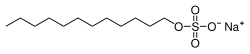
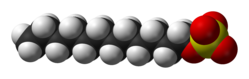
O dodecil sulfato de sodio (ou SDS, do inglés sodium dodecyl sulfate) é un composto orgánico sintético coa fórmula CH3(CH2)11SO4Na. Tamén se pode denominar dodecilsulfato sódico, sodio dodecil sulfato, lauril sulfato de sodio e outras variantes.[1] É un surfactante aniónico usado en moitos produtos de limpeza e hixiene. Esta molécula é un organosulfato e un sal. Consta dunha cola de 12 carbonos unida a un grupo sulfato, é dicir, é o sal sódico do dodecil hidróxeno sulfato, ou o éster do dodecil alcohol e o ácido sulfúrico. A súa cola hidrocarbonada combinada co seu grupo de cabeza polar danlle a este composto propiedades anfifílicas, o que fai que sexa un útil deterxente.[2] Pode ser un compoñente de mesturas producidas a partir de aceites baratos de coco e de palma. O SDS é un compoñente común de moitos limpadores domésticos, de hixiene persoal e cosméticos, así como de produtos alimenticios, e de formulacións de limpeza industriais e produtos industriais.[1]
Estrutura e propiedades[editar | editar a fonte]
Estrutura[editar | editar a fonte]
O SDS pertence á familia dos compostos organosulfatos,[3] e ten a fórmula CH3(CH2)11SO4Na. Consta dunha cola hidrocarbonada de 12 carbonos unida a un grupo sulfato, polo que é o sal sódico dun alcohol de 12 carbonos esterificado ao ácido sulfúrico. Unha descrición alternativa é que é un grupo alquilo cun grupo sulfato terminal unido. Como resultado de ter unha cola hidrocarbonada e unha "cabeza" aniónica é un composto anfipático que pode formar micelas, e así actúa como deterxente.
Propiedades fisicoquímicas[editar | editar a fonte]

A súa concentración micelar crítica (CMC) en auga pura a 25 °C é de 8,2 mM,[4] e o número de agregación a esta concentración é xeralmente considerado de aproximadamente 62.[5] A fracción de ionización de micelas (α) é de 0,3 (ou 30%).[6]
Produción[editar | editar a fonte]
O SDS é sintetizado tratando o lauril alcohol con gas trióxido de xofre, ácido sulfúrico fumante, ou ácido clorosulfúrico para producir hidróxeno lauril sulfato.[7] O produto resultante é despois neutralizado coa adición de hidróxido de sodio ou carbonato de sodio.[Cómpre referencia] O lauril alcohol pode utilizarse en forma pura ou pode derivarse a partir de aceites de coco ou aceite de palma por hidrólise (o cal libera os seus ácidos graxos), seguido de hidroxenación.[Cómpre referencia] Cando se produce a partir destas fontes, as mostras comerciais deste produto "SDS" non son realmente SDS puro, senón unha mestura de varios alquil sulfatos de sodio no que o SDS é o principal compoñente.[8] Por exemplo, o SDS é un compoñente, xunto con outros anfífilos de cadea longa, cando se produce a partir de aceite de coco e coñécese como sodio coco sulfato (SCS).[9] O SDS está dispoñible comercialmente en pos, pellets e outras formas (cada unha das cales difire nas súas taxas de disolución), e tamén en solucións acuosas de varias concentracións.[1]
Aplicacións[editar | editar a fonte]
Limpeza e hixiene[editar | editar a fonte]
O SDS utilízase principalmente en deterxentes para lavar a roupa e ten moitas aplicacións na limpeza.[2] É un surfactante moi efectivo e pode utilízarse en calquera tarefa que consista en quitar manchas e residuos de aceite; por exemplo, encóntrase en altas concentracións en produtos industriais como desengraxantes de motores, limpadores de chans, e limpadores da carrocería de coches.[1][10]
En baixas concentracións atópase en xabóns, pasta de dentes, xampús, cremas de barbear e formulacións de baños de burbullas, pola súa capacidade de crear escuma, polas súas propiedades surfactantes e en parte polo seu efecto espesante.[1][11]
Aditivo alimentario[editar | editar a fonte]
O SDS aparece co seu nome sinónimo sodio lauril sulfato (SLS) como compoñente engadido a alimentos como aditivo, que se considera seguro en países como os Estados Unidos,[12] pero o SLS non se permite na Unión Europea.[13] Utilízase como axente emulsificante e de axuda para facer batidos.[14] Informouse que o SLS fai diminuír temporalmente a percepción da dozura.[15] Como aditivo alimentario dáselle o código E487.[16]
Aplicacións nos laboratorios[editar | editar a fonte]
Aplicacións principais[editar | editar a fonte]
O lauril sulfato de sodio en ciencia adoita denominarse dodecil sulfato de sodio (SDS), e uilízase en procedementos de limpeza,[17] e como compoñente para a lise de células durante a extracción de ARN ou de ADN, así como para desnaturalizar proteínas para preparalas para unha electroforese na técnica SDS-PAGE.

No caso da aplicación na SDS-PAGE, este composto aplícase a temperatura elevada a unha concentración de 1,4 gramos de SDS por cada gramo de proteína, e o procedemento funciona alterando os enaces non covalentes das proteínas, o que causa a súa desnaturalización, é dicir, as proteínas perden a súa forma ou conformación nativa.[18][19][20] Ao unirse ás proteínas con alta afinidade e en altas concentracións, o deterxente cargado negativamente fai que todas as proteínas adquiran a mesma carga neta e que, por tanto, teñan unha proporción corga/masa similar. Deste modo, a diferenza de mobilidade das cadeas polipeptídicas no xel de poliacrilamida vai depender só do seu tamaño en vez de da súa forma ou carga.[21] Facer a separación das proteínas da mestura baseándose no tamaño da cadea polipeptídica simplifica a análise das moléculas proteicas e isto conséguese grazas á desnaturalización causada polo deterxente SDS.[21] Unha molécula de SDS ten dúas cargas negativas ao pH utilizado na electroforese, isto fai que a carga neta dos polipéptidos recubertos polo deterxente sexa moito máis negativa que na proteína nativa.[21] A proporción carga/masa é esencialmente idéntica para diferentes proteínas, porque o recubrimento de SDS é o que predomina na creación da carga.[21]
Outras aplicacións de laboratorio[editar | editar a fonte]
O SDS utilízase como unha técnica de mellora para preparar tecidos cerebrais para o seu estudo con microscopio óptico. A técnica, que se denomina comercialmente CLARITY, é resultado do traballo de Karl Deisseroth e colegas na Universidade Stanford, e implica a infusión do órgano con solución de acrilamida para que se una ás macromoléculas do órgano (proteínas, ácidos nucleicos etc.), seguido da polimerización térmica para formar un "hidroxel cerebral" (unha rede dispersa entre o tecido para fixar espacialmente as macromoléculas e outras estruturas), e despois retíranse os lípidos usando SDS para eliminar a dispersión da luz cunha mínimaperda de proteínas, facendo o tecido case transparente.[22][23][24]
Xunto co sodio dodecilbenceno sulfonato e o Triton X-100, as solucións acuosas do SDS son moi usados para dispersar ou suspender nanotubos, como os nanotubos de carbono.[25]
Outros usos[editar | editar a fonte]
Propúxose o uso do SDS como microbicida tópico efectivo para uso intravaxinal, para inhibir e posiblemente impedir as infeccións por varios virus con envoltura e sen envoltura, como o virus herpes simplex, o VIH e o virus Semliki Forest.[26][27]
Nos experimentos de formación de hidratos de gas, o SDS utilízase como un promotor do crecemento dos hidratos de gas.[28][29] Os investigadores pretenden que isto facilita a aplicación industrial dos hidratos de gas para procesos de desalinización,[30] almacenamento de gas e tecnoloxias de separación de gases.[31]
As membranas líquidas formadas con SDS en auga demostraron funcionar como separadores de partículas pouco comúns.[32] Estes dispositivos actúan como un filtro inverso, permitindo que pasen as partículas grandes, mentres que capturan as partículas máis pequenas.
Tamén se aproveitaron as propiedades do SDS para o seu uso como herbicida e praguicida de tipo "xabón".[33][1]
O SLS é un excipiente en produtos medicinais con diversos usos funcionais como axente emulsificante, axente modificador da liberación, potenciador da penetración, axente solubilizante e lubricante de tabletas e cápsulas. Os produtos medicinais autorizados conteñen SLS en concentracións que van desde o 0,2% w/w (por exemplo en cremas) ao 25% w/v (en xampús medicinais). O SLS non se usa en produtos parenterais.[13] O SLS ou os seus derivados úsanse como compoñentes dalgúns enemas laxantes.[34]
Toxicoloxía[editar | editar a fonte]
Carcinoxenicidade[editar | editar a fonte]
O SDS non é carcinóxeno cando se consome ou aplica directamente, incluso en cantidades e concentracións que exceden as cantidades usadas en produtos comerciais estándar.[35][36] Os exames iniciais do Panel de Expertos do programa Cosmetic Ingredient Review (CIR) en 1983 informaron que o SDS (aquí abreviado SLS, sodio lauril sulfato) en concentracións de ata o 2%, en estudos dietarios orais dun ano de duración en cans, non produciron evidencias de tumorixenicidade ou carcinoxenicidade, e que non se observaron aberracións cromosómicas ou efectos clastoxénicos en ratas alimentadas con 1,13% de sodio lauril sulfato nas súas dietas durante 90 días, respecto aos que estaban baixo unha dieta control.[35]:157, 175 O exame de 2005 feito polo mesmo grupo indicou que ulteriores datos dispoñibles non suxerían tampouco que o SDS ou o seu sal de amonio relacionado fosen carcinoxénicos, afirmando que "Malia as afirmacións sobre o contrario en Internet, a carcinoxenicidade destes ingredientes é só un rumor;" ambos os estudos conclúen que o SDS parece "ser seguro nas formulacións deseñadas para uso breve e descontinuo seguido do completo lavado da superficie da pel. En produtos pensados para un contacto prolongado coa pel, as concentracións non deberían exceder o 1%."[36]:89ff
Sensibilidade[editar | editar a fonte]
Como todos os deterxentes, o SDS quita os aceites da pel e pode causar irritación na pel e ollos.[37] Pode irritar a pel da face cunha exposición prolongada e constante (máis dunha hora) en adultos xoves.[38] O SDS pode empeorar os problemas da pel en individuos con hipersensibilidade cutánea crónica, e algunhas persoas son máis afectadas que outras.[39][40][41]
Uso oral[editar | editar a fonte]
O baixo custo do SDS,[42] o feito de que non afecta ao sabor,[42] o seu impacto potencial sobre os compostos do xofre volátiles, que contribúen ao mal alento,[43] e a súa desexable acción como axente escumante levaron a que o SDS se usase nas formulacións de pastas de dentes.[42] Unha serie de pequenos estudos (de 25 a 34 pacientes) apoiaron a eficacia do SLS na redución dos compostos de xofre volátiles e o seu impacto positivo sobre o mal alento, aínda que estes estudos foron xeralmente criticados por teren defectos técnicos no control das variables deseñadas do estudo.[43] Aínda que as fontes primarias do grupo de Irma Rantanen na Universidade de Turku, Finlandia concluíron que había unha mellora sobre a sequidade de boca (xerostomia) das pastas que contiñan SLS, unha revisión Cochrane de 2011 destes estudos, e da área máis xeral, concluíron que "non hai fortes evidencias… de que ningunha terapia tópica sexa efectiva para aliviar os síntomas da boca seca."[44] Indicáronse algunhas preocupacións sobre a seguridade baseándose nalgúns estudos sobre o efecto do SDS das pastas de dentes sobre a estomatite aftosa, as coñecidas como aftas ou carouquexas.[42] En 2016 non se chegara a ningún consenso sobre esta práctica (ou a necesidade do seu cambio) como resultado destes estudos.[45] Como sinala Lippert, en 2013, "moi poucas… pastas dentíficas comercializadas conteñen un surfactante distinto do SLS [SDS]," e os principais fabricantes continúan formulando os seus produtos con SDS.[42]
Interacción cos fluoruros[editar | editar a fonte]
Algúns estudos indicaron que o SLS en pastas detíficas pode facer diminuír a efectividade do fluoruro engadido para previr a carie dental. Isto pode deberse a que o SLS interacciona coa deposición de fluoruro no esmalte dental.[46]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 PubChemSodium dodecyl sulfate (Compound)
- ↑ 2,0 2,1 Smulders, Eduard ; Rybinski, Wolfgang; Sung, Eric; Rähse, Wilfried; Steber, Josef; Wiebel, Frederike & Nordskog, Anette. (2002) "Laundry Detergents," in Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi 10.1002/14356007.a08_315.pub2
- ↑ Michael Ash; Irene Ash (2004). Handbook of Preservatives. Synapse Info Resources.
- ↑ P. Mukerjee, P. & Mysels, K. J. (1971), "Critical Micelle Concentration of Aqueous Surfactant Systems," NSRDS-NBS 36, Washington, DC: US. Government Printing Office.
- ↑ Turro, N.J.; Yekta, A. (1978). "Luminescent probes for detergent solutions. A simple procedure for determination of the mean aggregation number of micelles". J. Am. Chem. Soc. 100 (18): 5951–52. doi:10.1021/ja00486a062.
- ↑ Bales, Barney L.; Messina, Luis; Vidal, Arwen; Peric, Miroslav & Nascimento, Otaciro Rangel (1998). "Precision Relative Aggregation Number Determinations of SDS Micelles Using a Spin Probe. A Model of Micelle Surface Hydration". J. Phys. Chem. B 102 (50): 10347–58. doi:10.1021/jp983364a.
- ↑ Takei, Kensuke; Tsuto, Keiichi; Miyamoto, Shigeyuki; Wakatsuki, Junya (February 1985). "Anionic surfactants: lauric products". Journal of the American Oil Chemists' Society 62 (2): 341–347. doi:10.1007/BF02541402.
- ↑ Gloxhuber, C., & Kunster, K. (1992). Anionic Surfactants: Biochemistry, toxicology, dermatology (2nd ed.). New York.[cómpre nº de páxina]
- ↑ US 3,491,033, "Process of making solid foams from polymer emulsions", published 1970 [1]
- ↑ "WHY SODIUM LAURYL SULFATES (SLS) ARE CAUSING HAIR LOSS". June 2018.
- ↑ "Household Products Database – Health and Safety Information on Household Products". nih.gov. Arquivado dende o orixinal o 12 de xuño de 2018. Consultado o 13 March 2016.
- ↑ "21 CFR 172.822 – Sodium lauryl sulfate". gpo.gov. Consultado o 13 March 2016.
- ↑ 13,0 13,1 European Medicines Agency (EMA/CHMP/606830/2017). Sodium laurilsulfate used as an excipient. 9 de outubro de 2017.
- ↑ Igoe, R. S. (1983). Dictionary of food ingredients. New York: Van Nostrand Reinhold Co.[cómpre nº de páxina]
- ↑ Adams, Michael J. (1985). "Substances That Modify the Perception of Sweetness (Ch. 2)". En Bills, Donald D.; Mussinan, Cynthia J. Characterization and Measurement of Flavor Compounds. ACS Symposium Series 289. pp. 11–25. ISBN 9780841209442. doi:10.1021/bk-1985-0289.ch002.
- ↑ Aditivos alimentarios E487
- ↑ "Sodium Lauryl Sulfate – National Library of Medicine HSDB Database". toxnet.nlm.nih.gov. Consultado o 2017-02-16.
- ↑ Reynolds JA, Charles Tanford (1970). "Binding of dodecyl sulfate to proteins at high binding ratios. Possible implications for the state of proteins in biological membranes.". Proc Natl Acad Sci U S A 66 (3): 1002–7. PMC 283150. PMID 5269225. doi:10.1073/pnas.66.3.1002.
- ↑ Smith, B. J. (1984). "SDS Polyacrylamide Gel Electrophoresis of Proteins" 1: 41–56. doi:10.1385/0-89603-062-8:41.
- ↑ Staikos, Georgios; Dondos, Anastasios (2009). "Study of the sodium dodecyl sulphate–protein complexes: evidence of their wormlike conformation by treating them as random coil polymers". Colloid and Polymer Science 287 (8): 1001–1004. ISSN 0303-402X. doi:10.1007/s00396-009-2059-3.
- ↑ 21,0 21,1 21,2 21,3 Ninfa, Alexander; Ballou, David (1998). Fundamental Laboratory Approaches for Biochemistry and Biotechnology. Hoboken, New Jersey: John Wiley & Sons. p. 129. ISBN 978-1-891-78600-6.
- ↑ Shen, Helen (2013). "See-through brains clarify connections". Nature 496 (7444; April 10): 151. PMID 23579658. doi:10.1038/496151a.
- ↑ Advances in CLARITY-based tissue clearing and imaging. Hao Du, Peihong Hou, [...], and Qiyu Li Experimental and Therapeutic Medicine. Spandidos Publications. [https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6122402/ ]
- ↑ Chung, K.; Wallace, J.; Kim, S.-Y.; et al. (2013). "Structural and molecular interrogation of intact biological systems". Nature 497 (7449; May 16): 332–37. PMC 4092167. PMID 23575631. doi:10.1038/nature12107.
Obter información de alta reolución dun sistema complexo, pero mantendo a perspectiva global necesaria para comprender a función do sistema, representa un reto clave en bioloxía. Aquí afrontamos ese reto cun método (denominado CLARITY) para a transformación do tecido intacto nunha forma de hidroxel-hibridado nanoporoso (con enlaces cruzados cunha rede tidimensional de polímeros hidrófilos) que está totalmente ensamblada, pero opticamente transparente e permeable ás macromoléculas.
- ↑ Islam, M. F. (2003). "High Weight Fraction Surfactant Solubilization of Single-Wall Carbon Nanotubes in Water". Nano Letters 3 (2): 269–73. doi:10.1021/nl025924u.
- ↑ Piret J.; Désormeaux, A. & Bergeron, M.G. (2002). "Sodium lauryl sulfate, a microbicide effective against enveloped and nonenveloped viruses". Curr. Drug Targets 3 (1): 17–30. PMID 11899262. doi:10.2174/1389450023348037.
- ↑ Piret J.; Lamontagne, J.; Bestman-Smith, J.; Roy, S.; Gourde, P.; Désormeaux, A.; Omar, R.F.; Juhász, J. & Bergeron, M.G. (2000). "In vitro and in vivo evaluations of sodium lauryl sulfate and dextran sulfate as microbicides against herpes simplex and human immunodeficiency viruses". J. Clin. Microbiol. 38 (1): 110–19. PMC 86033. PMID 10618073.
- ↑ Choudhary, Nilesh; Hande, Vrushali R.; Roy, Sudip; Chakrabarty, Suman; Kumar, Rajnish (2018-06-08). "Effect of Sodium Dodecyl Sulfate Surfactant on Methane Hydrate Formation: A Molecular Dynamics Study". The Journal of Physical Chemistry B 122 (25): 6536–6542. ISSN 1520-6106. PMID 29882664. doi:10.1021/acs.jpcb.8b02285.
- ↑ Kumar, Asheesh; Bhattacharjee, Gaurav; Kulkarni, B. D.; Kumar, Rajnish (2015-12-03). "Role of Surfactants in Promoting Gas Hydrate Formation". Industrial & Engineering Chemistry Research 54 (49): 12217–12232. ISSN 0888-5885. doi:10.1021/acs.iecr.5b03476.
- ↑ Kang, Kyung Chan; Linga, Praveen; Park, Kyeong-nam; Choi, Sang-June; Lee, Ju Dong (November 2014). "Seawater desalination by gas hydrate process and removal characteristics of dissolved ions (Na+, K+, Mg2+, Ca2+, B3+, Cl−, SO42−)". Desalination 353: 84–90. ISSN 0011-9164. doi:10.1016/j.desal.2014.09.007.
- ↑ Babu, Ponnivalavan; Linga, Praveen; Kumar, Rajnish; Englezos, Peter (June 2015). "A review of the hydrate based gas separation (HBGS) process for carbon dioxide pre-combustion capture". Energy 85: 261–279. ISSN 0360-5442. doi:10.1016/j.energy.2015.03.103.
- ↑ Birgitt Boschitsch Stogin; et al. (August 24, 2018). "Free-standing liquid membranes as unusual particle separators". Science Advances 4 (8): eaat3276. PMC 6108570. PMID 30151426. doi:10.1126/sciadv.aat3276.
- ↑ Sodium Lauryl Sulfate - Agricultural Marketing Service - USDA [2]
- ↑ Drugbank. Sodium lauryl sulfoacetate
- ↑ 35,0 35,1 Cosmetic Ingredient Review (CIR) program Expert Panel (1983). "Final Report on the Safety Assessment of Sodium Lauryl Sulfate and Ammonium Lauryl Sulfate" (PDF). Int. J. Toxicol. 2 (7): 127–81. doi:10.3109/10915818309142005. Consultado o 13 March 2016.
[Cita:] Carcinoxénese. Un estudo oral crónico dun ano na que se usaron [cans] beagles mostrou que o sodio lauril sulfato a concentracións de ata o 2% na dieta non era tumorixénico nun carcinoxénico [p. 157] / Resumo… En estudos de mutaxénese, as ratas alimentadas cun 1,13% e 0,56% de sodio lauril sulfato na dieta durante 90 días non produciron máis aberacións cromosómicas ou efectos clastoxénicos do que os con dieta de control. [p. 175]. / Conclusión. O sodio lauril sulfato e o amonio lauril sulfato parecen ser seguros en formulacións deseñadas para un uso breve e descontinuo seguido do completo lavado da superficie da pel. En produtos pensados para un contacto prolongado coa pel, as concentracións non deberían exceder o 1%. [p. 176.]
. - ↑ 36,0 36,1 Wilma F. Bergfeld, Chair, and the Cosmetic Ingredient Review (CIR) program Expert Panel (2005). "Final report on the safety assessment of sodium lauryl sulfate and ammonium lauryl sulfate" (PDF). Int. J. Toxicol. 24 (1): 1–102, esp. 89–98. Consultado o 13 March 2016.
[Cita:] O sodio lauril sulfato e o amonio laturil slfato parecen ser seguros en formulacións deseñadas para un uso breve e descontinuo seguido do completo lavado da superficie da pel. En produtos pensados para un contacto prolongado coa pel, as concentracións non deberían exceder o 1%… Novos estudos confirmaron as propiedades irritantes destes ingredientes e reafirman a concentración límite do 1% ou usos por longo tempo establecidos polo [anterior] Panel. [p. 89] / Os estudos dispoñibles que examinaban a carcinoxénese non conseguiron atopar evidencias de que o amonio lauril sulfato é [sic.] carcinoxénico. Ningún dos datos dispoñibles suxerían que o SLS ou o amonio lauril sulfato puidesen ser carcinoxénicos. Malia afirmacións dicindo o contrario en Internet, a carcinoxenicidade destes ingredients é só un rumor. [pp. 89ff]
. - ↑ Cara AM Bondi, Julia L Marks, [...], and Kay E Gebhardt. Human and Environmental Toxicity of Sodium Lauryl Sulfate (SLS): Evidence for Safe Use in Household Cleaning Products. Environmental Health Insights. [https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4651417/ ]
- ↑ Marrakchi S, Maibach HI (2006). "Sodium lauryl sulfate-induced irritation in the human face: regional and age-related differences". Skin Pharmacol Physiol 19 (3): 177–80. PMID 16679819. doi:10.1159/000093112.
- ↑ Agner T (1991). "Susceptibility of atopic dermatitis patients to irritant dermatitis caused by sodium lauryl sulphate". Acta Derm. Venereol. 71 (4): 296–300. PMID 1681644.
- ↑ Nassif A, Chan SC, Storrs FJ, Hanifin JM (November 1994). "Abnormal skin irritancy in atopic dermatitis and in atopy without dermatitis". Arch Dermatol 130 (11): 1402–07. PMID 7979441. doi:10.1001/archderm.130.11.1402.
- ↑ Löffler H, Effendy I (May 1999). "Skin susceptibility of atopic individuals". Contact Derm. 40 (5): 239–42. PMID 10344477. doi:10.1111/j.1600-0536.1999.tb06056.x.
- ↑ 42,0 42,1 42,2 42,3 42,4 Lippert, Frank (2013). "An Introduction to Toothpaste—Its Purpose, History and Ingredients". En van Loveren, Cor. Toothpastes. Monographs in Oral Science 23. Series Eds.: Huysmans, M.C., Lussi, A. & Weber, H.-P. Basel, CHE: Karger. pp. 1–14, esp. 12. ISBN 978-3-318-02206-3. PMID 23817056. doi:10.1159/000350456.
- ↑ 43,0 43,1 Dadamio, J.; Laleman, I. & Quirynen, M. (2013). "The Role of Toothpastes in Oral Malodor Management". En van Loveren, C. Toothpastes. Monographs in Oral Science 23. Series Eds.: Huysmans, M.C., Lussi, A. & Weber, H.-P. Basel, CHE: Karger. pp. 45–60, esp. 49–52. ISBN 978-3-318-02206-3. PMID 23817059. doi:10.1159/000350472.
- ↑ Furness S.; Worthington, H.V.; Bryan, G.; Birchenough, S. & McMillan R. (2011). "Interventions for the management of dry mouth: topical therapies". Cochrane Database Syst Rev 7 (12; December): CD008934. PMID 22161442. doi:10.1002/14651858.CD008934.pub2.
[Cita resumo:] Non hai fortes evidencias nesta revisión de que ningunha terapia tópica sexa efectiva para aliviar os síntomas da sequidade de boca.
Vedr Rantanen, et al. (2003) J. Contemp. Dent. Pract. 4(2):11–23, [3], e Rantanen, et al. (2003) Swed. Dent. J. 27(1):31–34, [4], referenciada alí. - ↑ Algúns dos estudos publicados, desde o último ao primeiro, son os seguintes. (i) Un estudo de 2012 de dobre cego de 90 pacientes non atopou unha diferenza significativa no número de úlceras entre os grupos que usaban pasta de dentes que contiña SLS, fronte ao grupo que a usaba sen SLS, pero suxeriron unha redución significativa na duración das úlceras e a mellora nas cifras de pacientes con dor, ver Shim, Y. J.; Choi, J. -H.; Ahn, H. -J.; Kwon, J. -S. (2012). "Effect of sodium lauryl sulfate on recurrent aphthous stomatitis: A randomized controlled clinical trial". Oral Diseases 18 (7): 655–60. PMID 22435470. doi:10.1111/j.1601-0825.2012.01920.x., un estudo tamén citado nun capítulo do libro de Lippert (2013). (ii) un estudo cruzado de 1999 de dobre cego de 47 pacientes non atopou ningunha diferenza estatística significativa no número, episodios e duración de tales úlceras entre estes dous grupos, e das cifras de dores observados entre eles, ver Healy CM, Paterson M, Joyston-Bechal S, Williams DM, Thornhill MH (January 1999). "The effect of a sodium lauryl sulfate-free dentifrice on patients with recurrent oral ulceration". Oral Dis. 5 (1): 39–43. PMID 10218040. doi:10.1111/j.1601-0825.1999.tb00062.x. (iii) Un estudo de 1997 suxeriu que había un número significativamente máis alto de úlceras despois do uso de pastas con SDS, fronte ao seu grupo de control, ver Chahine L, Sempson N, Wagoner C (December 1997). "The effect of sodium lauryl sulfate on recurrent aphthous ulcers: a clinical study". Compend. Contin. Educ. Dent. 18 (12): 1238–40. PMID 9656847., un estudo tamén citado nun capítulo do libro de Lippert (2013). (iv) Un estudo cruzado de 1996 de dobre cego de seguimento de 30 pacientes e un estudo preliminar de 1994 de 10 pacientes feito polos mesmos autores indicou que babía cantidades significativamente maiores de aftas despois de usar pastas de dentes que contiñan SLS, comparados cos que non, ver Herlofson BB, Barkvoll P (June 1996). "The effect of two toothpaste detergents on the frequency of recurrent aphthous ulcers". Acta Odontol. Scand. 54 (3): 150–53. PMID 8811135. doi:10.3109/00016359609003515. and Herlofson BB, Barkvoll P (October 1994). "Sodium lauryl sulfate and recurrent aphthous ulcers. A preliminary study". Acta Odontol. Scand. 52 (5): 257–59. PMID 7825393. doi:10.3109/00016359409029036.
- ↑ Barkvoll, P. (1989-02-01). "Should toothpastes foam? Sodium lauryl sulfate – a toothpaste detergent in focus". Den Norske Tannlaegeforenings Tidende 99 (3): 82–84. ISSN 0029-2303. PMID 2696932.
Véxase tamén[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Josh Clark, "Why does orange juice taste bad after you brush your teeth?"
- This improbable membrane can trap flies in a jar—and odor in a toilet no YouTube publicado o 24 de agosto de 2018 Science
