Ácido sulfúrico
  | |
|---|---|
|
Xeral | |
| Nome | Ácido Sulfúrico |
| Fórmula química | H2SO4 |
| Aparencia | Líquido incoloro |
|
Físicas | |
| Peso molecular | 98.1 uma |
| Punto de fusión | 283 K (10 °C) |
| Punto de ebulición | 610 K (337 °C) |
| Densidade | 1.8 ×10³ kg/m³ |
| Solubilidade | miscible |
|
Termoquímica | |
| ΔfH0líquido | -814 kJ/mol |
| S0líquido, 1 bar | 19 J/mol·K |
|
Seguridade | |
| Inxestión | Grave e pode ocasionar dano permanente. |
| Inhalación | Moi perigosa, posiblemente fatal. Efectos a longo prazo coñecidos. |
| Pel | Causa queimaduras. |
| Ollos | Causa queimaduras. |
O ácido sulfúrico é un composto químico moi corrosivo. A súa fórmula é H2SO4. É o composto químico máis producido no mundo. Unha gran parte emprégase na obtención de fertilizantes. Tamén se usa para a síntese doutros ácidos e sulfatos, e na industria petroquímica.
Características[editar | editar a fonte]
Xeralmente obtense a partir de dióxido de xofre, por oxidación con óxidos de nitróxeno en disolución acuosa. Normalmente despois lévanse a cabo procesos para conseguir unha maior concentración do ácido.
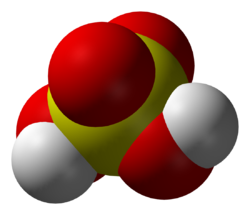
A molécula presenta unha estrutura piramidal, co átomo de xofre no centro e os catro átomos de osíxeno nos vértices. Os dous átomos de hidróxeno están unidos a cadanseu átomo de osíxeno. Dependendo da disolución, estes hidróxenos pódense disociar. Na auga compórtase como un ácido forte na súa primeira disociación, dando o anión monohidroxenosulfato, e como un ácido débil na segunda, dando o anión sulfato.
