CRISPR
| CRISPR | |
|---|---|
 Complexo de vixilancia CRISPR de Tipo-I (Cas, en azul) ligado a un ADN obxectivo (laranxa). Coñecido como Cascade en E. coli, composto por diversas proteínas Cas e un ARN cr de 61 nucleótidos. | |
| Datos clínicos | |
| Pronuncia | /crisper/ |
| Nome comercial | Varios, dependendo da aplicación |
| Sinónimos | CRISPR-Cas9, CRISPR-Cas, sistemas CRISPR |
| Grupo farmacolóxico | Sistema de defensa inmunitario / Ferramenta de edición xenética |
| Datos fisiolóxicos | |
| Metabolismo | Non aplica |
| Datos farmacocinéticos | |
| Metabolismo | Non aplica |
| Comezo de acción | Inmediato ou rápido, dependendo da célula ou organismo obxectivo |
| Excreción | Non aplica |
| Identificadores | |
| |
| Datos químicos e físicos | |
| Fórmula | Variábel (ADN/ARN e proteínas) A composición exacta pode variar |
| Solubilidade en auga | Solúbel en auga (en forma de ADN/ARN e proteínas) mg/mL (20 °C) |
Se cre que pode requirir tratamento, por favor, consúltello ao médico. | |

1. xenes cas (cas genes),
2. unha secuencia líder (leader), e
3. Unha matriz de espazadores de repetición. (Repeat-spacer array).
A disposición dos tres compoñentes non sempre é como a mostrada

CRISPR é un acrónimo na investigación do ADN que provén do inglés Clustered Regularly Interspaced Short Palindromic Repeats, traducido ao galego como repeticións palindrómicas curtas agrupadas e espazadas regularmente (a abreviatura pronúnciase crisper). [1]. Descuberta no inicio do século XXI, CRISPR é tamén unha metodoloxía en bioloxía molecular para a edición do ADN xenómico.[2] [3] [4] O sistema está composto por dous compoñentes principais: o ARN guía e a endonuclease asociada a CRISPR, como pode ser Cas9.[5]
Na natureza, a maioría das bacterias e das arqueas, que son tipos de células procariotas, incorporan o sistema CRISPR no seu xenoma e úsano como un mecanismo de defensa contra o ataque de virus.[6]
O sistema CRISPR ten múltiples secuencias de ADN repetidas e curtas. Estas secuencias son parte dun sistema inmunitario adaptativo en células procariotas, derivan de fragmentos de ADN de bacteriófagos que previamente as infectaran, e permítenlles 'lembrar' e neutralizar eses bacteriófagos se as volven atacar. Funcionan como unha especie de inmunidade adquirida para estes microorganismos.[7] [8] Na investigación, os compoñentes CRISPR son empregados como unha ferramenta de edición xenética (polas siglas en inglés, GM; véxase alimentos transxénicos) que pode modificar os xenes de case calquera organismo.[9] Actualmente, estase investigando o seu potencial uso en terapia xénica para tratar enfermidades virais en humanos.[10] [11]
Funcionamento
[editar | editar a fonte]- Véxase tamén: CRISPR (edición de xenes).
Cada secuencia repetida no sistema CRISPR é seguida por pequenos segmentos de 'ADN espazador', que se orixinan de exposicións anteriores a virus ou plásmidos.[10] Estes espazadores actúan como un sistema de recoñecemento que corta o ADN estraño, de maneira similar á forma en que o sistema de interferencia de ARN funciona en organismos eucariotas. De feito, os espazadores son fragmentos de ADN de virus que tentaron atacar a célula previamente. Este feito foi un indicio para os investigadores de que o sistema CRISPR/Cas tería un papel na inmunidade adaptativa das células procariotas.[12]
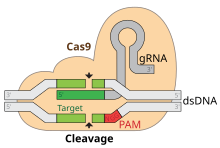
O corte do ADN é realizado por unha proteína nuclease chamada Cas9.
Cas9 posúe dous sitios de corte activos, un para cada febra ou cadea da dobre hélice de ADN. Este proceso ocorre cando Cas9 desenrola o ADN estraño e verifica se é complementario ao fragmento espazador de 20 pares de bases do ARN guía (o ARN derivado do espazador). Se hai unha concordancia, o ADN estraño é cortado.[9] [13]
Aplicacións
[editar | editar a fonte]- Véxase tamén: CRISPR (edición de xenes).
CRISPR é un sistema de defensa antiviral que se orixinou en células procariotas como bacterias e arqueas. O seu uso humano máis coñecido é na edición xenética. Esta tecnoloxía permítenos desactivar xenes específicos en células humanas, estudar organismos como Candida albicans, ou mesmo modificar lévedos utilizados na produción de biocombustíbeis. Tamén se emprega para editar xenes en diferentes tipos de cultivos con fins agrícolas.[14]
O sistema CRISPR-Cas9 non só corta o ADN; tamén ten outras utilidades. Por exemplo, pode prender ou arrancar a actividade de certos xenes e tamén pode marcar secuencias específicas para que brillen baixo unha luz especial (fluorescencia).[15] [16]
Recoñecementos
[editar | editar a fonte]En agosto de 2017, o investigador da Universidade de Alacant J. F. Martínez Mojica foi galardoado co Albany Medical Center Prize, o galardón máis importante dos Estados Unidos no ámbito da investigación médica, na categoría de Medicina e Investigación Biomédica 2017, polas súas contribucións ao desenvolvemento do sistema CRISPR/ Cas9. Compartiu este premio con Emmanuelle Charpentier, Jennifer Doudna, Luciano Marraffini e Feng Zhang.[17]A comprensión e desenvolvemento da técnica de edición do xenoma CRISPR-Cas9 gañou o Premio Nobel de Química en 2020, sendo o premio concedido conxuntamente a Charpentier e Doudna.[18][19]
Anti-CRISPR
[editar | editar a fonte]Anti-CRISPR é un grupo de proteínas nalgúns fagos (abreviatura de bacteriófagos, virus que infectan bacterias). Inhibe a actividade normal de CRISPR-Cas, o sistema inmunitario de moitas bacterias. Os fagos con anti-CRISPR evitan que os seus xenomas sexan destruídos polas células procariotas que infectan.[20]
Notas
[editar | editar a fonte]- ↑ TV3 (2020-04-19). "No pot ser! - T2xC5 - Gen-ètica?" (en catalán). Consultado o 2023-08-27.
- ↑ Gesner E.M; Schellenberg M.J; Garside E.L; George M.M. & Macmillan A.M. 2011. Recognition and maturation of effector RNAs in a CRISPR interference pathway. Nature Structural & Molecular Biology. 18 (6): 688–692.
- ↑ Véxase Premio Nobel de Química a Emmanuelle Charpentier e Jennifer Doudna, 2020.
- ↑ Wiedenheft B; Sternberg S.H; Doudna J.A. 2012. RNA-guided genetic silencing systems in bacteria and archaea. Nature. 482 (7385): 331–338.
- ↑ Zhang, Feng; Wen, Yan; Guo, Xiong (2014-09-15). "CRISPR/Cas9 for genome editing: progress, implications and challenges". Human Molecular Genetics 23 (R1): R40–46. ISSN 1460-2083. PMID 24651067. doi:10.1093/hmg/ddu125.
- ↑ Grissa I; Vergnaud G. & Pourcel C. 2007. The CRISPRdb database and tools to display CRISPRs and to generate dictionaries of spacers and repeats. BMC Bioinformatics 8: 172.
- ↑ por Jennifer Doudna
- ↑ Mojica F.J.M. et al 2000. Biological significance of regularly spaced repeats in the genomes of Archaea, Bacteria and mitochondria. Molecular Microbiology 36: 244–246.
- ↑ 9,0 9,1 Carey, Nessa 2019. Hacking the code of life: how gene editing will rewrite our futures. London: Icon Books. ISBN 978-178578-625-9
- ↑ 10,0 10,1 Marraffini L.A. & Sontheimer E.J. 2010. CRISPR interference: RNA-directed adaptive immunity in bacteria and archaea. Nature Reviews Genetics 11 (3): 181–190.
- ↑ Hille F. & Charpentier E. 2016. CRISPR-Cas: biology, mechanisms and relevance. Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 371 (1707): 20150496.
- ↑ Morange, Michel (2015-06-01). "What history tells us XXXVII. CRISPR-Cas: The discovery of an immune system in prokaryotes". Journal of Biosciences (en inglés) 40 (2): 221–223. ISSN 0973-7138. doi:10.1007/s12038-015-9532-6.
- ↑ Re-writing the Code of Life: CRISPR systems and applications of gene editing. Jennifer Doudna at the Royal Society on YouTube.
- ↑ Ledford, Heidi (2015-06-01). "CRISPR, the disruptor". Nature (en inglés) 522 (7554): 20–24. ISSN 1476-4687. doi:10.1038/522020a.
- ↑ "CRISPR: Gene editing and beyond". Consultado o 2023-08-26.
- ↑ Doudna, Jennifer & Sternberg, Samuel 2017. A crack in creation: the new power to control evolution. London: Bodley Head. ISBN 978-1-847-92382-0
- ↑ "Francisco Mojica recibe el galardón de medicina más prestigioso de EE.UU.". www.rtve.es (en castelán). 2017-08-15. Consultado o 2023-08-26.
- ↑ "The Nobel Prize in Chemistry 2020". NobelPrize.org (en inglés). Consultado o 2023-08-26.
- ↑ Wu, Katherine J.; Zimmer, Carl; Peltier, Elian (2020-10-07). "Nobel Prize in Chemistry Awarded to 2 Scientists for Work on Genome Editing". The New York Times (en inglés). ISSN 0362-4331. Consultado o 2023-08-26.
- ↑ Stanley SY, Borges AL, Chen KH, Swaney DL, Krogan NJ, Bondy-Denomy J, Davidson AR 2019. Anti-CRISPR-associated proteins are crucial repressors of Anti-CRISPR transcription. Cell 178 (6): 1452–1464.e13. doi:10.1016/j.cell.2019.07.046. PMC 6754177. PMID 31474367
Véxase tamén
[editar | editar a fonte]| Wikimedia Commons ten máis contidos multimedia na categoría: CRISPR |
Este artigo sobre bioloxía é, polo de agora, só un bosquexo. Traballa nel para axudar a contribuír a que a Galipedia mellore e medre.
Existen igualmente outros artigos relacionados con este tema nos que tamén podes contribuír. |

