Ferredoxina
As ferredoxinas (a miúdo abreviadas "fd") son proteínas ferro-sulfuradas que median na transferencia de electróns en diversas reaccións metabólicas, por exemplo na fase luminosa da fotosíntese. O termo ferredoxina (do latín ferrum + redox) foi acuñado por D.C. Wharton da Compañía DuPont e aplicado á "proteína férrica" que fora purificada en 1962 por Mortenson, Valentine, e Carnahan da bacteria anaeróbica Clostridium pasteurianum.[1][2]
Outra proteína redox, illada dos cloroplastos de espinacas por Tagawa e Arnon en 1962, foi denominada "ferredoxina cloroplástica".[3] A ferredoxina cloroplástica intervén nos transportes cíclicos e acíclicos de electróns da fase luminosa da fotosíntese implicados na fotofosforilación. Na fotofosforilación acíclica, a ferredoxina é o último aceptor de electróns e reduce ao encima ferredoxina-NADP+ redutase. Acepta os electróns liberados polas clorofilas excitadas pola luz e transfíreos ao encima ferredoxina-NADP+ redutase (con número EC 1.18.1.2).
As ferredoxinas son pequenas proteínas que conteñen átomos de ferro e xofre organizados como grupos ferro-sulfurados ou clústeres. Estes "capacitadores" biolóxicos poden aceptar ou ceder electróns, cambiando o estado de oxidación (+2 ou +3) dos seus átomos de ferro. Deste xeito, as ferredoxinas actúan como axentes de transferencias de electróns nas reaccións redox biolóxicas.
Outros sistemas de transporte de electróns bioinorgánicos son as rubredoxinas, citocromos, proteínas do cobre azuis (por exemplo plastocianina), e as proteínas de Rieske estruturalmente relacionadas.
As ferredoxinas poden clasificarse atendendo á natureza dos seus grupos ferro-sulfurados ou á semellanza da súa secuencia.
Ferredoxinas do tipo Fe2S2[editar | editar a fonte]
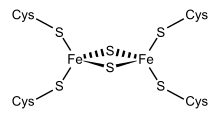
Os membros da familia de ferredoxinas 2Fe-2S teñen unha estrutura básica xeral do tipo beta(2)-alfa-beta(2), e inclúen á putidarredoxina e terpredoxina, e adrenodoxina.[4][5][6][7] Son proteínas de arredor de cen aminoácidos con catro residuos de cisteína conservados aos cales está ligado o grupo 2Fe-2S. Esta rexión conservada tamén se encontra como un dominio en varios encimas metabólicos e en proteínas multidominio, como a aldehido oxidorredutase (N-terminal), xantina oxidase (N-terminal), ftalato dioxixenase redutase (C-terminal), a proteína ferro-sulfurada succinato deshidroxenase (N-terminal), e na metano monooxixenase redutase (N-terminal).
Ferredoxinas do tipo vexetal[editar | editar a fonte]
Un grupo de ferredoxinas, atopadas orixinalmente nas membranas dos cloroplastos, foi denominado de "tipo cloroplástico" ou de "tipo planta" ou vexetal. O seu centro activo é o grupo [Fe2S2], no que os átomos de ferro están coordinados tetraedricamente tanto con átomos de xofre inorgánico coma con xofre pertencente a residuos de cisteína (Cys) conservados.
Nos cloroplastos, as ferredoxinas Fe2S2 funcionan como transportadores de electróns na cadea de transporte electrónico fotosintética e como doantes de electróns para varias proteínas celulares, como a glutamato sintase, nitrato redutase e sulfito redutase. En sistemas de dioxixenases bacterianas hidroxilantes, serven como intermediarios na transferencia de electróns entre as flavoproteínas redutases e oxixenases.
Ferredoxinas do tipo tiorredoxina[editar | editar a fonte]
As ferredoxinas Fe2S2 de Clostridium pasteurianum (Cp2FeFd) foron recoñecidas como unha familia distinta de proteínas baseándose na súa secuencia de aminoácidos, propiedades espectroscópicas dos seus grupos ferro-sulfurados e a súa capacidade de intercambiar un único ligando dos dous ligandos de cisteína co grupo [Fe2S2]. Aínda que o papel fisiolóxico desta ferredoxina non está claro, foi descuberta unha interacción específica forte de Cp2FeFd coa proteína molibdeno-ferro da nitroxenase. Foron tamén caracterizadas ferredoxinas homólogas de Azotobacter vinelandii (Av2FeFdI) e Aquifex aeolicus (AaFd). A estrutura cristalina de AaFd xa se coñece. AaFd existe como dímero. A estrutura do monómero AaFd é diferente da das outras ferredoxinas Fe2S2. O pregamento pertence á clase α+β, no que as primeiras catro cadeas β e dúas hélices α adoptan unha variante do pregamento tiorredoxina.
Ferredoxinas do tipo adrenodoxina[editar | editar a fonte]
A adrenodoxina exprésase nos mamíferos, humanos incluídos. A variante humana da adrenodoxina denomínase ferredoxina 1. A adrenodoxina, putidarredoxina, e terpredoxina son proteínas solubles Fe2S2 que actúan como transportadores dun só electrón. Nos sistemas monooxixenase mitocondriais, a adrenodoxina transfire un electrón da NADPH:adrenodoxina redutase ao citocromo P450 unido a membranas. Nas bacterias, a putidarredoxina e a terpredoxina serve como transportador de electróns entre as correspondentes ferredoxina redutases dependentes de NADH e P450s solubles. As funcións exactas doutros membros desta familia non se coñecen, aínda que a Fdx de Escherichia coli está implicada na bioxénese de grupos Fe-S. Malia a baixa similitude de secuencia entre as ferredoxinas do tipo adrenodoxina e do tipo planta, as dúas clases teñen unha topoloxía de pregamento similar.
A ferredoxina 1 (FDX-1) nos humanos participa na síntese de hormonas tiroides. Tamén transfire electróns desde a adrenodoxina redutase ao citocromo P que corta a cadea lateral do colesterol. A FDX-1 ten a capacidade de unirse a metais e proteínas. Atópase na matriz mitocondrial.
Ferredoxinas dos tipos Fe4S4 e Fe3S4[editar | editar a fonte]
As ferredoxinas [Fe4S4] poden ser subdivididas en ferredoxinas de baixo potencial (tipo bacteriano) e de alto potencial (HIPIP).
As ferredoxinas de baixo e alto potencial están relacionadas polo seguinte esquema redox:

Os números de oxidación formal dos ións ferro poden ser [2Fe3+, 2Fe2+] ou [1Fe3+, 3Fe2+] nas ferredoxinas de baixo potencial. Os números de oxidación dos ións ferro nas ferredoxinas de alto potencial poden ser [3Fe3+, 1Fe2+] ou [2Fe3+, 2Fe2+].
Ferredoxinas do tipo bacteriano[editar | editar a fonte]

Un grupo de ferredoxinas Fe4S4, atopadas inicialmente en bacterias, foron denominadas de "tipo bacteriano". As ferredoxinas de tipo bacteriano poden ser subdivididas en varios grupos segundo as propiedades da súa secuencia. A maioría conteñen polo menos un dominio conservado, que inclúe catro residuos de cisteína que se unen ao grupo [Fe4S4]. Na ferredoxina Fe4S4 de Pyrococcus furiosus, un dos residuos cisteína conservados está substituído por ácido aspártico.
No decurso da evolución das ferredoxinas de tipo bacteriano, ocorreron episodios de duplicación xénica intrasecuencia, transposición e fusión, que deron como resultado a aparición de proteínas con múltiples centros ferro-sulfurados. Nalgunhas ferredoxinas bacterianas, un dos dominios duplicados perdeu un ou máis dos catro residuos de cisteína conservados. Estes dominios perderon a súa propiedade de unión de Fe-S ou únense a grupos [Fe3S4] en vez de a grupos [Fe4S4] [9] e tipos diclúster.[10]
Coñécense as estruturas tridimensionais de varias ferredoxinas de tipo bacteriano monoclúster e diclúster. O pregamento que presentan é de clase α+β, con de 2 a 7 hélices α e catro cadeas β que forman unha estrutura con forma de barril, e un bucle que sobresae, que contén tres ligandos cisteína "proximais" do grupo ferro-sulfurado.
Proteínas ferro-sulfuradas de alto potencial[editar | editar a fonte]
As proteínas ferro-sulfuradas de alto potencial (HiPIPs) forman unha familia propia de ferredoxinas Fe4S4 que funcionan nas cadeas de transporte electrónico anaeróbicas. Algunhas HiPIPs teñen un potencial redox máis alto ca calquera outra proteína ferro-sulfurada coñecida (por exemplo, HiPIP de Rhodopila globiformis ten un potencial redox de preto de 450 mV). Foron caracterizadas estruturalmente varias HiPIPs, e os seus pregamentos pertencen á clase α+β. Como noutras ferredoxinas bacterianas, o grupo [Fe4S4] adopta unha conformación dun tipo similar á do hidrocarburo cubano e está ligado á proteína polos catro residuos de cisteína.
Proteínas humanas da familia da ferredoxina[editar | editar a fonte]
Notas[editar | editar a fonte]
- ↑ Mortenson LE, Valentine RC, Carnahan JE (1962). "An electron transport factor from Clostridium pasteurianum". Biochem. Biophys. Res. Commun. 7: 448–52. PMID 14476372. doi:10.1016/0006-291X(62)90333-9.
- ↑ Valentine RC (1964). "Bacterial ferredoxin". Bacteriol Rev 28: 497–517. PMC 441251. PMID 14244728.
- ↑ Tagawa K, Arnon DI (1962). "Ferredoxins as electron carriers in photosynthesis and in the biological production and consumption of hydrogen gas". Nature 195 (4841): 537–43. Bibcode:1962Natur.195..537T. PMID 14039612. doi:10.1038/195537a0.
- ↑ Jouanneau Y, Armengaud J, Sainz G, Sieker LC (2001). "Crystallization and preliminary X-ray diffraction analysis of a [2Fe-2S] ferredoxin (FdVI) from Rhodobacter capsulatus". Acta Crystallogr. D 57 (Pt 2): 301–303. PMID 11173487. doi:10.1107/S0907444900017832.
- ↑ Sevrioukova IF (2005). "Redox-dependent Structural Reorganization in Putidaredoxin, a Vertebrate-type [2Fe-2S] Ferredoxin from Pseudomonas putida". J. Mol. Biol. 347 (3): 607–621. PMID 15755454. doi:10.1016/j.jmb.2005.01.047.
- ↑ Pochapsky TC, Mo H, Pochapsky SS (1999). "A model for the solution structure of oxidized terpredoxin, a Fe2S2 ferredoxin from Pseudomonas". Biochemistry 38 (17): 5666–5675. PMID 10220356. doi:10.1021/bi983063r.
- ↑ Ruterjans H, Beilke D, Weiss R, Lohr F, Pristovsek P, Hannemann F, Bernhardt R (2002). "A new electron transport mechanism in mitochondrial steroid hydroxylase systems based on structural changes upon the reduction of adrenodoxin". Biochemistry 41 (25): 7969–7978. PMID 12069587. doi:10.1021/bi0160361.
- ↑ PDB 3P1M; Chaikuad A, Johansson, C, Krojer, T, Yue, WW, Phillips, C, Bray, JE, Pike, ACW, Muniz, JRC, Vollmar, M, Weigelt, J, Arrowsmith, CH, Edwards, AM, Bountra, C, Kavanagh, K, Oppermann, U (2010). "Crystal structure of human ferredoxin-1 (FDX1) in complex with iron-sulfur cluster". To be published. doi:10.2210/pdb3p1m/pdb.
- ↑ Fukuyama K, Matsubara H, Katsube Y, Tsukihara T (1989). "Structure of [4Fe-4S] ferredoxin from Bacillus thermoproteolyticus refined at 2.3 A resolution. Structural comparisons of bacterial ferredoxins". J. Mol. Biol. 210 (2): 383–398. PMID 2600971. doi:10.1016/0022-2836(89)90338-0.
- ↑ Sieker LC, Meyer J, Moulis JM, Fanchon E, Duee ED, Vicat J (1994). "Refined crystal structure of the 2[4Fe-4S] ferredoxin from Clostridium acidurici at 1.84 A resolution". J. Mol. Biol. 243 (4): 683–695. PMID 7966291. doi:10.1016/0022-2836(94)90041-8.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Bibliografía[editar | editar a fonte]
- Bruschi, M. and Guerlesquin, F. (1988). "Structure, function and evolution of bacterial ferredoxins". FEMS Microbiol. Rev. 4 (2): 155–75. PMID 3078742.
- Ciurli, S. and Musiani, F. (2005). "High potential iron-sulfur proteins and their role as soluble electron carriers in bacterial photosynthesis: tale of a discovery". Photosynth. Res. 85 (1): 115–131. PMID 15977063. doi:10.1007/s11120-004-6556-4.
- Fukuyama, K. (2004). "Structure and function of plant-type ferredoxins". Photosynth. Res. 81 (3): 289–301. PMID 16034533. doi:10.1023/B:PRES.0000036882.19322.0a.
- Grinberg, A.V., Hannemann, F., Schiffler, B., Müller, J., Heinemann, U. and Bernhardt, R. (2000). "Adrenodoxin: structure, stability, and electron transfer properties". Proteins 40 (4): 590–612. PMID 10899784. doi:10.1002/1097-0134(20000901)40:4<590::AID-PROT50>3.0.CO;2-P.
- Holden,H.M., Jacobson, B.L., Hurley, J.K., Tollin, G., Oh, B.H., Skjeldal, L., Chae, Y.K., Cheng, H., Xia, B. and Markley, J.L. (1994). "Structure-function studies of [2Fe-2S] ferredoxins". J. Bioenerg. Biomembr. 26 (1): 67–88. PMID 8027024. doi:10.1007/BF00763220.
- Meyer, J. (2001). "Ferredoxins of the third kind". FEBS Lett. 509 (1): 1–5. PMID 11734195. doi:10.1016/S0014-5793(01)03049-6.
Ligazóns externas[editar | editar a fonte]
- InterPro - IPR001055 - Adrenodoxina
- InterPro - IPR001450 - ferredoxina 4Fe-4S
- InterPro - IPR000170 - proteína de unión ao ferro de alto potencial
- PDB - 1F37 - Estrutura de raios X da ferredoxina de tipo tiorredoxina de Aquifex aeolicus (AaFd)
